Костномозговая недостаточность
Главное проявление костномозговой недостаточности – АА. Развивается при исчерпании КМ компенсаторно – приспособительных возможностей. (и дальше говорите про АА)
Костномозговая недостаточность развивается при снижении массы функционирующего КМ. Теория зерна: ключевое звено – гибель стволовых клеток. Теория почвы: различные воздействия (этиология АА) истощают клетки, составляющие микроокружение стволовых эл-тов, вследствие последние лишаются ростовых и трофических влияний.
Случаи костномозговой недостаточности делят на две категории:
1) клинически проявляющиеся как панцитопении
2) клин. проявляющиеся как дефицит клеток какого-либо одного ростка (изолированные цитопении)
Билет №181
Лейкон – совокупность всех белых клеток крови, находящихся на всех стадиях развития, а также механизмы их образования и разрушения. Это дидактическое понятие (у разных лейкоцитов (ЛЦ) разный предшественник и разные регуляторы пролиферации). В лейконе выделяют миелоидный и лимфоидный отделы, а миелоидный состоит и гранулоцитарного и моноцитарного подотделов. Лейкоциты отличны друг от друга функционально и морфологически. Регулируют лейкон факторы роста (не вызывают дифференцировку, не связываются с ДНК – работают через посредников), индукторы дифференцировки (связываются с ДНК, образуются в самих клетках под действием фактора роста). Клетки, достигшие конечной стадии дифференцировки, вырабатывают ингибиторы размножения.
|
|
|
Лейкоцитозы и лейкопении
Увеличение общего абсолютного количества лейкоцитов в единице объёма крови выше верхней границы нормы - абсолютный лейкоцитоз (крайняя степень – гиперлейкоцитоз). Уменьшение ниже ее нижней границы – абсолютная лекопения (крайняя степень – алейкия). Относительный лейкоцитоз и лейкопения - изменение процентного содержания в ту или иную сторону.
Лейкоцитоз
Истинный лейкоцитоз - из-за усиления лейкопоэза. Если он обусловлен демаргинацией ЛЦ, уже находившихся в сосудистом русле, – перераспределительный. Лейкоцитоз может быть физиологическим (у беременных, после родов).
Физиологический перераспределительный лейкоцитоз – сопровождают любой стресс после физической нагрузки (миогенный), психич. Переживаний (эмоциональный), при смене часовых поясов (акклиматизационный), после еды (пищевой). Регулируется гормонами ЖКТ, гистамином и гипоталамо-гипофизарной системой. Из них выделяют нейтрофильные (не изменяется соотношение между молодыми и зрелыми формами)
Патологические лейкоцитозы – всегда вторичны. Бывают неопластического и реактивного происхождения. Неопластические – для лейкемических форм лейкозов, моноклональны. Реактивные – изза усиления действия цитокинов, стимулирующих дифференцировку и пролиферацию ЛЦ, они поликлональны.
|
|
|
1) При инфекциях
2) При асептических воспалениях
3) При отравлениях и облучении (компенсаторно)
Также лейкоцитозы делятся поо преобладанию тех или иных ЛЦ
1) Нейтрофильно- эозинопенический (гнойные инфекции)
2) Нейтрофильно- эозинофильный (анафилаксия, паразиты)
3) Лимфоцитарно – нейтропенический (тиф, паратиф, вирусы, р-ии ГЗТ)
4) Моноцитарно – лимфоцитарный (аутоиммунные, аллергии
Лейкопения– патологическая и физиологическая (конституциональная безвредная). Физиологическая – у негров. Для них это норма
Патологическая – перераспределительная и истинная. Перераспределительная – из-за усиленной экстренной маргинации лейкоцитов (бактериемическая фаза Гр(-) инфекций, эндотоксинемия – эндотелий становится более клейким и вырабатывает молекулы клеточной адгезии, может быть при стрессе). При стрессе может быть лимфопения, связанная с хоумингом лимфоцитов под действием гормонов коры надпочеников и с разрушением их в ораганх лимфопоэза
Истинная – абсолютное уменьшение числа лейкоцитов в организме, как результат существенного и длительного преобладания скорости гибели лейкоцитов над скоростью их выхода в кровь.
|
|
|
1) При апластических состояниях
2) Смешанный механизм – ускорение гибели лейкоцитов и понижение рекрутирования
3) Тяжелые мегалобластические состояния – от снижения скорости пролиферации костномозгового пула лейкоцитов, так и от укорочения жизни зрелых белых клеток
4) Аутоиммунные - ускоренная гибель клеток предшевственников и малый выход ЛЦ в кровь, аутоиммунный цитолиз зрелых ЛЦ в крови и тканях
5) При длительном и неправильном лечении гнойно-септических процессов изза того, что они в гнойниках много гибнут, а ресурсы исчерпались
Нейтрофилы (НФ)
Нейтрофильные (полиморфноядерные лейкоциты - ПМЯЛ) гранулоциты представляют собой самую большую группу лейкоцитов.
Гранулы :
1) азурофильные первичные грунулы - богатейший источник катионных белков (миелопероксидаза, серпроцидины (азуроцидин А, эластаза, катепсин G), дефензины), ферменты: кислая фосфатаза, бета – гиалуронидаза, эстеразы, лизоцим
2) вторичные - их в 2 раза больше – не имеют пероксидазу и кислую фосфотазу. Содержат щелочную фосфотазу, коллагеназу, лактоферрин, аминопептидазу
|
|
|
3) третичные - (желатиназа – против коллагена базальных мембран), лизоцим
Дефензины – природные антибиотики – их катионный заряд позволяет им сорбироваться на микроорганизмах, оболочка которых богата анионами; проникая в мембрану, создают поры, которые выравниваютионные градиенты, нарушается работа мебарнных ферментных систем
Лизоцим деполимеризирует оболочку бактерий
Лактоферрин – связывает металлы, делает бактерии дефицитными по микроэлементам
Миелопероксидаза – маркерный фермент НФ – делает гной зеленым, главный компонент окислительной системы нейтрофила
Нейтрофилы являются микрофагами, то есть поглощают небольшие частицы. Они способны к адгезии, амебоидному движению, эмиграции за пределы сосудов и хемотаксису (направленному движению в места воспаления или повреждения тканей). После фагоцитирования нейтрофилы погибают. При фагоцитозе – каскад миграции и каскад киллинга. Миграционный каскад: маргинация-> диапедез через стенку сосуда -> хемотаксис. Каскад киллига: распознавание -> прилипание -> рецепторный эндоцитоз ->слияние гранул -> дегрануляция в фагосому -> “ метаболический взрыв”, связанный с внутриклеточным киллингом -> бактерицидный эффект - > экзоцитоз
Погибшие нейтрофилы вместе с разрушенными клетками формируют гной.
Нейтрофилы играют важную роль в защите организма от бактериальных и грибковых инфекций и сравнительно меньшую — в защите от вирусных инфекций.
Первую классификацию нейтрофилов предложил немецкий гематолог Арнет. Он разделил все нейтрофилы на 5 классов в зависимости от числа сегментов. Нейтрофилы с одним сегментом (незрелые), двумя, тремя, четырьмя и пятью сегментами (наиболее зрелые). В норме в крови преобладают нейтрофилы с двумя и тремя сегментами.
Увеличение количества незрелых 1-сегментарных клеток, расположенных в схеме слева от доминирующих в норме 2-х- и 3-х- сегментарных, Арнет назвал «сдвигом нейтрофильного ядра влево». Сдвиг влево наблюдается при многих инфекционных заболеваниях, особенно пиогенных; при радиационных поражениях, травмах, внутрисосудистом гемолизе, острых воспалительных процессах, инфаркте миокарда, кровотечениях, шоке, интоксикациях, лимфогранулематозе. Наиболее выражен сдвиг при хроническом миелолейкозе, в этом случае встречаются единичные бластные клетки.
Увеличение количества нейтрофилов с четырьмя, пятью и более сегментами Арнет назвал «сдвигом вправо». Сдвиг вправо характерен для дефицита витамина В12, витамина С, фолиевой кислоты.
Другой немецкий гематолог Шиллинг создал классификацию нейтрофилов, принятую и по сей день. Класс несегментированных нейтрофилов, по Шиллингу, включает миелоциты, юные или метамиелоциты и палочкоядерные нейтрофилы. Класс сегментированных лейкоцитов включает только зрелые формы. В современных схемах кроветворения первой морфологически распознаваемой клеткой является миелобласт, он дифференцируется в промиелоцит, далее следуют миелоцит, юный, палочкоядерный, сегментоядерный нейтрофилы.
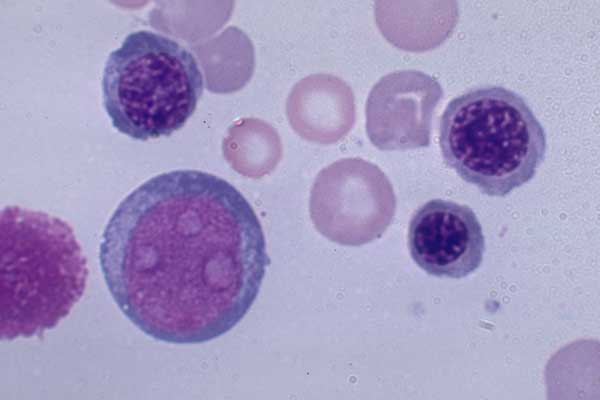




Шиллинг выделял сдвиги регенеративные и дегенеративные. Регенеративный сдвиг совпадает со сдвигом влево по Арнету и означает увеличение выработки нейтрофильных элементов. Дегенеративный сдвиг означает нарушение дифференцировки, при этом возрастает количество палочкоядерных клеток без увеличения содержания юных и миелоцитов. Пропорция сегментоядерных нейтрофилов снижается в результате блока последней стадии дифференцировки.
Повышение процента нейтрофилов в крови называется относительным нейтрофилезом (нейтрофилией). Снижение процента нейтрофилов в крови называется относительной нейтропенией. При значительных отклонениях общего числа лейкоцитов лейкоцитарная формула не дает точного представления об истинном содержании лейкоцитов в крови. В этих случаях необходимо вычислить абсолютное количество каждого отдельного лейкоцита в единице объема крови. Количество лейкоцитов, выраженное в абсолютных значениях, называется лейкоцитарным профилем. Повышение абсолютного числа нейтрофилов в крови называется абсолютным нейтрофилезом, снижение абсолютного числа нейтрофилов - абсолютной нейтропенией.
Нейтрофильный ответ (нейтрофилия, сдвиг влево) при острых воспалениях и инфекциях всегда предшествует лимфоцитарному. При хронических воспалениях и инфекциях преобладает лимфоцитарный ответ (инфильтрация очага воспаления лимфоцитами, абсолютный или относительный лимфоцитоз в крови).
Увеличение общего числа нейтрофилов (нейтрофилия, нейтрофилез):
· Острые бактериальные инфекции;
· Воспаление или некроз тканей;
· Стрессовые состояния;
· Миелопролиферативные заболевания (миелолейкоз, эритремия);
· Интоксикации.
Снижение числа нейтрофилов (нейтропения):
· Инфекции - бактериальные (тиф, паратиф, подострый эндокардит, милиарный туберкулез); вирусные (инфекционный гепатит, грипп, корь, краснуха, ветряная оспа); паразитарные - малярия;
· Хронические воспалительные заболевания;
· Почечная недостаточность;
· Тяжелые формы сепсиса с развитием септического шока;
· Гемобластозы - острый лейкоз, хронический лимфолейкоз;
· Апластическая анемия;
· Иммунные заболевания;
· Наследственные формы;
· Недостаточность витамина В12 и фолиевой кислоты;
· Приём некоторых медикаментов (производные пиразолона, нестероидные противовоспалительные препараты, антибиотики, особенно левомицетин, сульфаниламидные препараты, препараты золота);
· Прием противоопухолевых препаратов (цитостатики и иммунодепрессанты).
Агранулоцитоз – синдром, характеризующийся практически полным исчезновением из крови нейтрофильных гранулоцитов и инфекционными осложнениями. Смертность составляет от 3 до 36%. Частота встречаемости 1 на 1200 человек. Чаще болеют женщины старше 40 лет.
Этиология: в 60% случаев – медикаменты. Агранулоцитоз могут вызвать примерно 300 препаратов. Чаще всего вызвают развитие агранулоцитоза анальгетики, сульфаниламиды и антибиотики, противотуберкулезные препараты, снотворные, цитостатики. Также его вызывают некоторые химические вещества, вирусные инфекции.
Острый агранулоцитоз. Бывает двух вариантов - 1)миелотоксический (вследствие прямого действия цитостатических препаратов, ионизирующего излучения на клетки гранулопоэза и 2)аутоиммунный.
Эозинофилы содержат в цитоплазме крупные красные или розовые гранулы. В основном, располагаются в тканях. Период полужизни - 4,5 – 5 часов.
Их гранулы содержат:
1) Миелопероксидазу (не как у НФ) – повреждает паразитов
2) Катионные белки - эозинофильный катионный белок – вызывает сокращения ГМК; Главный основной белок эозинофилов – паразитоцидное действие
3) Бета- гиалуронидазу
4) Противовоспалительные медиаторы (фосфолипазы – разрушают ФАТ, гистаминаза). Эти фосфолипазы образуют кристаллы Шарко – Лейдена; гистаминаза; кининаза). Т.е. ЭФ понижают анафилактическое воспаление – фагоцитируют гранулы
Классически рассматриваются как антираразитарные клетки, могут фиксироваться на паразитах, меченых IgE и осуществлять киллинг (в качестве К-клеток в реакциях АЗКЦ). Особую роль играют ЭФ пониженной плотности, которые выделяют много ФАТ и за счет него активируют почти все проявления воспаления.

Эозинофилы участвуют в реакциях организма, которые сопровождаются гиперпродукцией Ig Е: аллергические, гельминтные и протозойные заболевания.
Эозинофилы накапливаются в тканях, контактирующих с внешней средой – в лёгких, желудочно-кишечном тракте, коже, урогенитальном тракте. При аллергических заболеваниях эозинофилы нейтрализуют образующиеся в ходе этих реакций медиаторы.
Эозинопения (снижение числа эозинофилов в крови) часто наблюдается в начале воспаления. Увеличение числа эозинофилов в крови (эозинофилия) соответствует началу выздоровления. При длительной эозинофилии, ЭФ начинают повреждать ткани орнанизма (миокардит Абрамова – Фидлера, синдром Чарга – Стросса при болезни Леффлера
Увеличение числа эозинофилов (эозинофилия) (больше 5%):
· В предприступный период при анафилаксии
· Паразитарные инвазии;
· Гемобластозы;
· Некоторые детские инфекции (скарлатина, ветряная оспа)
· При иммунопатологиях
Уменьшение числа эозинофилов и их отсутствие (эозинопения и анэозинофилия):
 Эозинопения (ниже 2%) имеет диагностическое значение при инфекциях — брюшном тифе, лептоспирозе, возвратном тифе, большинстве пиогенных инфекций; из числа прочих болезней — при эклампсии, шоке, акромегалии; эозинопению вызывают адреналин, глюкокортикоиды, никотиновая кислота, никотинамид. При агранулоцитозе, в послеприступный период при анафилаксии
Эозинопения (ниже 2%) имеет диагностическое значение при инфекциях — брюшном тифе, лептоспирозе, возвратном тифе, большинстве пиогенных инфекций; из числа прочих болезней — при эклампсии, шоке, акромегалии; эозинопению вызывают адреналин, глюкокортикоиды, никотиновая кислота, никотинамид. При агранулоцитозе, в послеприступный период при анафилаксии
Базофилы - самая малочисленная популяция лейкоцитов.
Первичные гранулы: пероксидаза, гепарин, гистамин, фактор хемотаксиса ЭФ, ФАТ, калликреин
Есть еще вторичные гранулы, они пероксидазо -неактивны
Увеличение количества базофилов (базофилия):
· Аллергические реакции на пищу, лекарства, введение чужеродного белка;
· Хронический миелолейкоз, миелофиброз, эритремия, лимфогранулематоз;
· Хронический язвенный колит;
· Аутоиммунные
Если абазофилия – заурядное явление, то даже незначителльная базофилия требует анализа
! их следует отличать от мастоцитов – у тех есть маркерные ферменты (химаза – разрушает аморфное вещество соединительной ткани, триптаза – лизирует С3 компонент комплемента. Также в мастоцитах больше гистамина и серотонина. Мастоциты ,в основном, осуществляют экзоцитоз, БФ обычно дегранулируют внутрь фаголизосомы.
Моноциты - крупные клетки с цитоплазмой серого цвета и почкообразным или складчатым ядром.

Моноциты циркулируют в крови около 20 часов, затем мигрируют в периферические ткани, превращаясь в макрофаги. Моноциты и макрофаги – представители системы мононуклеарных фагоцитов - обладают выраженной фагоцитарной активностью, участвуют в формировании и регуляции иммунного ответа, в регуляции кроветворения, участвуют в гемостазе, метаболизме липидов и железа. В очаге воспаления макрофаги фагоцитируют микробы, комплексы антиген-антитело, погибшие и поврежденные клетки, подготавливая очаг воспаления для регенерации. Секретируют более 100 биологически активных веществ. Из них наиболее значимые медиаторы – монокины.
Увеличение числа моноцитов в крови (моноцитоз – больше 8%):
· Вирусные, грибковые, протозойные инфекции;
· Период выздоровления после острых инфекций;
· Гранулематозы (туберкулез, сифилис, бруцеллез);
· Коллагенозы
· Гемобластозы
· Подострый септический эндокардит;
· Вялотекущий сепсис.
Уменьшение числа моноцитов в крови:
· Гипоплазия кроветворения;
· Роды;
· Оперативные вмешательства;
· Шоковые состояния.
Лимфоциты являются главными клеточными элементами иммунной системы; образуются в костном мозге, тимусе и периферических лифоидных органах. Главная функция лимфоцитов состоит в узнавании антигена и участии в адекватном иммунном ответе организма.

Лимфоциты представляют собой популяцию клеток, происходящих из различных предшественников и объединяемых единой морфологией. Они подразделяются на субпопуляции: Т-лимфоциты, В-лимфоциты, NK-лимфоциты (естественные или натуральные киллеры, англ. natural killer cell) —лимфоциты, обладающие цитотоксичностью против раковых клеток и клеток, зараженных вирусами. Т-лимфоциты участвуют в процессах клеточного иммунитета, а В-лимфоциты — в процессах гуморального иммунитета.
Разные субпопуляции лимфоцитов выполняют различные функции:
· обеспечение эффективного клеточного иммунитета (уничтожение опухолевых клеток и клеток, зараженных вирусами, отторжение трансплантата);
· формирование гуморального ответа (синтез антител к чужеродным белкам - иммуноглобулинов разных классов);
· регуляция иммунного ответа и координации работы всей иммунной системы в целом (выделение белковых регуляторов – цитокинов);
· обеспечение иммунологической памяти (способности организма к ускоренному и усиленному иммунному ответу при повторной встрече с антигеном).
Увеличение количества лимфоцитов (лимфоцитоз):
· Вирусная инфекция;
· Гемобластозы (острый и хронический лимфолейкоз, макроглобулинемия Вальденстрема);
· Хроническая инфекция (туберкулез, сифилис, бруцеллез);
· Интоксикация (тетрахлорэтан, свинец, мышьяк).
Уменьшение количества лимфоцитов (лимфопения):
· Голодание (квашиоркор)
· Лимфотропные вирусы – полиомиелит
· ВИЧ
· Стресс и гиперкортицизм
· Костномозговая недостаточность
· Лучевые поражения
· Иммунодепрессанты
Дата добавления: 2019-03-09; просмотров: 383; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
