Квантові числа та їх фізичний зміст
Нерелятивістська модель атома водню на основі рівняння Шредінгера визначає стаціонарні стани 3-ма квантовими числами 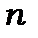 ,
,  і
і 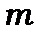 .
.
Головне квантове число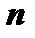 визначає енергію стаціонарного стану
визначає енергію стаціонарного стану
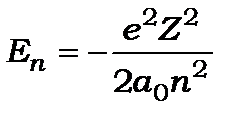 , (8.69)
, (8.69)
де 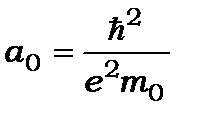 ,
,
а n набуває значень:
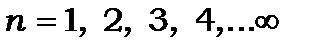 (8.70)
(8.70)
Побічне або орбітальне квантове число визначає квадрат моменту кількості руху
визначає квадрат моменту кількості руху 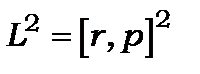
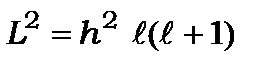 (8.71)
(8.71)
і набуває таких дискретних значень 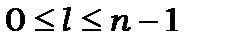
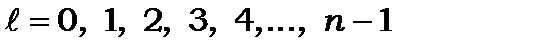 (8.72)
(8.72)
Воно подібне до числа nj в моделі Бора-Зомерфельда, проте 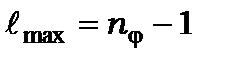 . Так як енергія стану визначається лише головним квантовим числом, то при даному
. Так як енергія стану визначається лише головним квантовим числом, то при даному 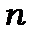 має місце n-кратневиродження - при даній енергії існує
має місце n-кратневиродження - при даній енергії існує 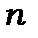 станів руху з різними
станів руху з різними  , тобто з різними моментами кількості руху
, тобто з різними моментами кількості руху 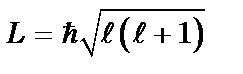 ).
).
Магнітне квантове число 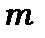 визначає проекцію моменту кількості руху на вісь
визначає проекцію моменту кількості руху на вісь 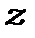
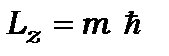 (8.73)
(8.73)
і набуває 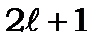 дискретних значень
дискретних значень 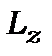 , де
, де
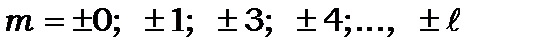 (8.74)
(8.74)
Таблиця 8.3. Кількість станів із різними значеннями квантового числа m в станах, що визначаються квантовим числом  .
.
| Стан | 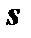
| 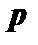
| 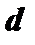
| 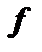
| 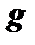
| 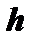
|

| 0 | 1 | 2 | 3 | 4 | 5 |
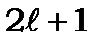
| 1 | 3 | 5 | 7 | 9 | 11 |
При заданому значенні 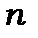 може бути
може бути 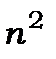 станів із різними значеннями квантових чисел
станів із різними значеннями квантових чисел  та m, тобто має місце
та m, тобто має місце 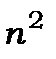 - кратне виродження. Дійсно:
- кратне виродження. Дійсно:
|
|
|
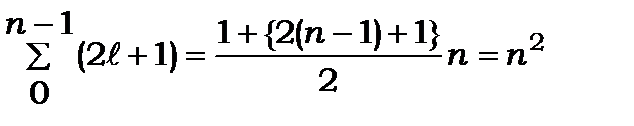 . (8.75)
. (8.75)
Таким чином, у сучасній атомній фізиці квантові числа відіграють дуже важливу роль. Вони визначають параметри стаціонарних електронних станів у атомі: енергію, момент кількості руху та зв’язаний з ним магнітний момент. Квантові числа дозволяють визначати ці величини, а також можливу кількість станів та ступінь виродження енергетичних рівнів. Виродження енергетичних рівнів можна зняти за допомогою силових полів, а саме магнітного та електричного. Зняття виродження ми розглянемо в іншому розділі. Переходи між окремими стаціонарними станами супроводжуються випромінюванням квантів електромагнітних хвиль і, щоб знайти їх, потрібно використати правила відбору.
Правила відбору квантових чисел
Розглянемо перехід з одного стаціонарного стану з 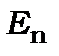 і
і 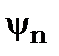 до
до
іншого з 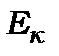 і
і 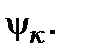 Хвильові функції цих стаціонарних станів мають
Хвильові функції цих стаціонарних станів мають
вигляд
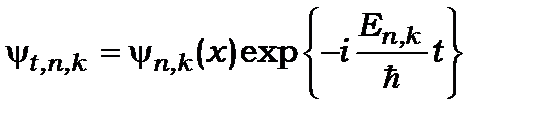 (8.76)
(8.76)
Знайдемо середнє значення 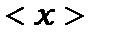 в стаціонарному стані.
в стаціонарному стані.
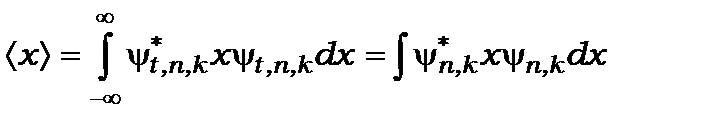 . (8.77)
. (8.77)
З формули (8.71) видно, що в стаціонарних станах середнє значення 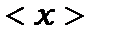 не залежить від часу. Тому й середній дипольний момент
не залежить від часу. Тому й середній дипольний момент  не залежить від часу. Незалежність дипольного моменту від часу означає, що в цьому випадку не відбувається випромінювання електромагнітних хвиль.
не залежить від часу. Незалежність дипольного моменту від часу означає, що в цьому випадку не відбувається випромінювання електромагнітних хвиль.
|
|
|
У перехідному стані від стаціонарного стану із квантовим числом 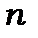 до іншого з квантовим числом
до іншого з квантовим числом 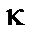 виникає змішаний стан, який є суперпозицією цих двох станів
виникає змішаний стан, який є суперпозицією цих двох станів 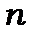 і
і 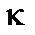 із хвильовою функцією
із хвильовою функцією 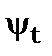
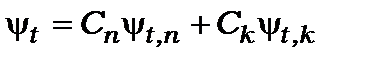 , (8.78)
, (8.78)
де 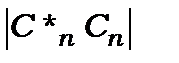 та
та 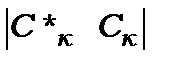 - імовірності системи знаходитись в
- імовірності системи знаходитись в 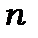 або
або  станах. Умова нормування дає
станах. Умова нормування дає
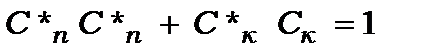 . (8.79)
. (8.79)
Обчислимо тепер середнє значення 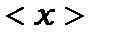 для змішаного стану
для змішаного стану
 (8.80)
(8.80)
В окремому випадку зв’язаної системи із двома станами цю задачу можна спростити, бо для такої системи
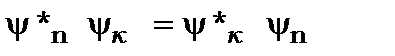 і
і 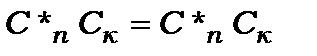
і формула (8.74) набуває вигляду
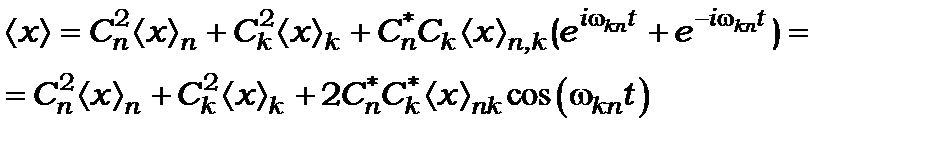 ,
,
де 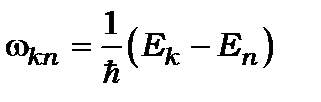
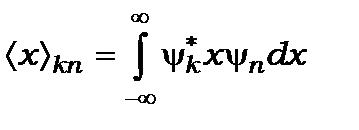 . (8.81)
. (8.81)
Вираз (8.81) називається матричним елементом переходу електрона з одного стану із квантовим числом 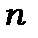 до іншого стану з квантовим числом
до іншого стану з квантовим числом 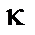 . Якщо під час цього переходу матричний елемент
. Якщо під час цього переходу матричний елемент 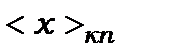 не дорівнює нулеві (
не дорівнює нулеві (  ), то й дипольний момент
), то й дипольний момент 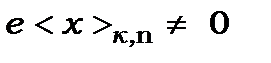 . Це означає, що при такому переході диполь випромінює електромагнітні хвилі із частотою, яка визначається за правилом частот Бора
. Це означає, що при такому переході диполь випромінює електромагнітні хвилі із частотою, яка визначається за правилом частот Бора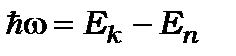 .
.
Таким чином, матричний елемент визначає дозволені й заборонені переходи, тобто правила відбору:
|
|
|
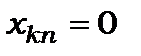 заборонені переходи;
заборонені переходи;
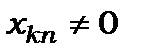 дозволені переходи . (8.82)
дозволені переходи . (8.82)
Визначимо для прикладу правило відбору для магнітного числа m для дипольних переходів (при умові 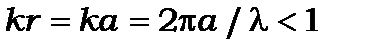 ) у випадку хвильових функцій електрона в атомі водню, для якого
) у випадку хвильових функцій електрона в атомі водню, для якого
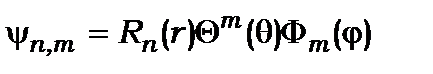 . (8.83)
. (8.83)
Знайдемо середнє значення 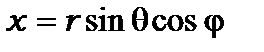
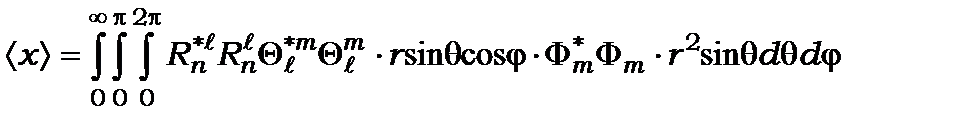 . (8.84)
. (8.84)
Інтеграли в (8.78) можна записати як добуток трьох інтегралів по 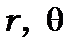 і
і 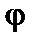 , тому що функції
, тому що функції 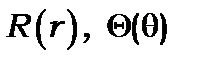 і
і 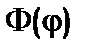 залежать лише від своєї змінної
залежать лише від своєї змінної 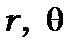 або
або 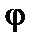 . За умовою, що
. За умовою, що 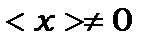 , знаходимо дозволений перехід. Це означає, що всі три інтеграли в (8.84) повинні не дорівнювати нулеві. Обмежимося розглядом інтеграла за змінною
, знаходимо дозволений перехід. Це означає, що всі три інтеграли в (8.84) повинні не дорівнювати нулеві. Обмежимося розглядом інтеграла за змінною 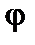 .
.
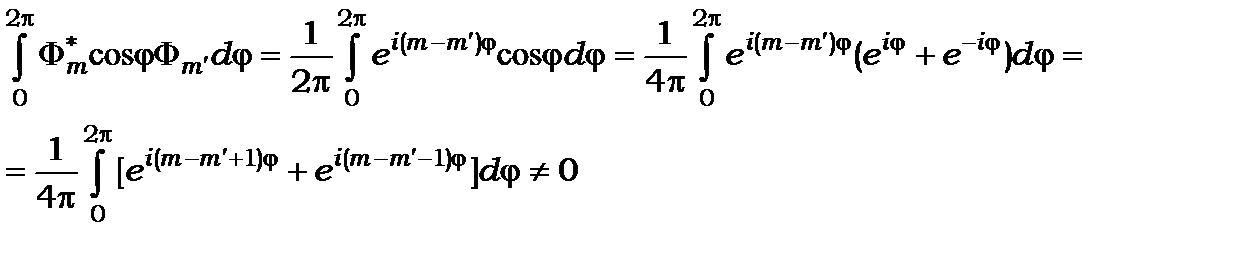 (8.85)
(8.85)
Умова (8.85) виконується лише, коли
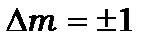 (8.86)
(8.86)
За умовою, що 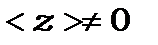 , де
, де 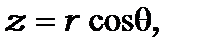 таким же способом отримаємо ще одну умову відбору
таким же способом отримаємо ще одну умову відбору
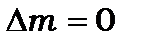 (8.86*)
(8.86*)
Томуправило відбору для магнітного квантового числа 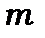 для спонтанних дипольних переходів має наступний вигляд
для спонтанних дипольних переходів має наступний вигляд
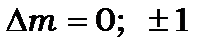 (8.87)
(8.87)
Аналогічно, аналізуючи інтеграл за 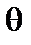 , знайдемоправила відбору для орбітального числа
, знайдемоправила відбору для орбітального числа  , яке має такий вигляд для спонтанних дипольних переходів
, яке має такий вигляд для спонтанних дипольних переходів
|
|
|
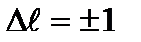 (8.88)
(8.88)
Зміна головного квантового числа 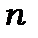 не обмежується. Воно може змінюватись на будь-яке число одиниць.
не обмежується. Воно може змінюватись на будь-яке число одиниць.
Ці правила відбору справедливі лише для спонтанних дипольних переходів. Вони іноді називаються правилами відбору Лапорта. Для інших випадків більш складних переходів, наприклад. квадрупольних та для вимушених переходів ці правила відбору ускладнюються. Квадрупольне випромінювання значно слабше дипольного (в 106 раз). Правила відбору при квадрупольних переходах змінюються: 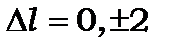 ,
, 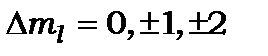 .
.
Існує ще одне правило визначення для квантових переходів з випромінюванням.
Правило Лапорта: у дипольному наближенні випромінювальний перехід дозволений між станами різної парності. Стан називається парним, якщо 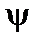 -функція не змінює знаку при інверсії системи координат. Наприклад для функцій атома водню
-функція не змінює знаку при інверсії системи координат. Наприклад для функцій атома водню 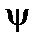 -функція є парною, якщо вона не змінює знак при заміні аргументу
-функція є парною, якщо вона не змінює знак при заміні аргументу  на
на 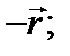 у протилежному випадку функція є непарною. З конкретного вигляду хвильових функцій для атома водню випливає, що
у протилежному випадку функція є непарною. З конкретного вигляду хвильових функцій для атома водню випливає, що 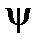 -функція парна, якщо
-функція парна, якщо 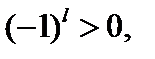 непарна — якщо
непарна — якщо 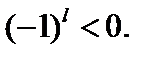 , де
, де 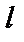 -орбітальне квантове число. Згідно формули (8.81) матричний елемент перехода
-орбітальне квантове число. Згідно формули (8.81) матричний елемент перехода 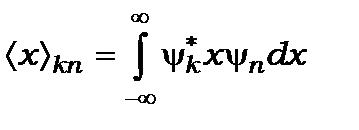 .
. 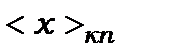 не повинен змінюватися при операціях інверсії. Але
не повинен змінюватися при операціях інверсії. Але 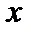 (координата) завжди змінює знак при операції інверсії системи, тому добуток хвильових функцій в інтегралі (8. 81) повинен бути відємним. Звідси випливає ,що квантовий перехід з випромінюванням можливий тільки між станами різної парності.
(координата) завжди змінює знак при операції інверсії системи, тому добуток хвильових функцій в інтегралі (8. 81) повинен бути відємним. Звідси випливає ,що квантовий перехід з випромінюванням можливий тільки між станами різної парності.
Висновки
1. Електрони в атомі водню та ізоелектронних атомах водню мають дискретні стаціонарні стани, енергія яких визначається головним квантовим числом 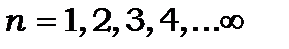
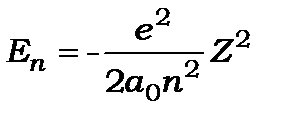 , (8.89)
, (8.89)
де 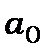 - радіус першої борівської орбіти.
- радіус першої борівської орбіти.
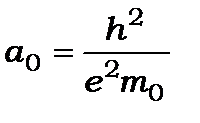 .
.
2. Для 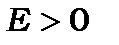 спектр енергії електронів неперервний
спектр енергії електронів неперервний
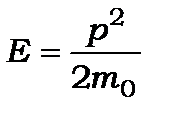 (8.90)
(8.90)
3. Скінчена маса ядра викликає ізотопічний зсув енергетичних рівнів 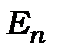 і спектральних ліній відповідно
і спектральних ліній відповідно
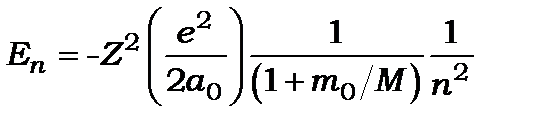 (8.91)
(8.91)
4. Електрон в атомі “розмазаний” у просторі у вигляді “електронної хмари”. Імовірність знайти електрон в елементарному об’ємі 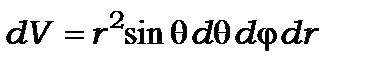 визначається
визначається
 (8.92)
(8.92)
і залежить не тільки від координат 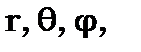 але й від квантових чисел
але й від квантових чисел 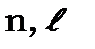 та
та 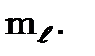 При
При 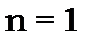 і
і 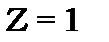 вона має максимум на відстані
вона має максимум на відстані 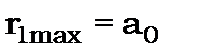 і при збільшенні
і при збільшенні 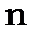
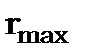 збільшується.
збільшується.
5. Стаціонарні стани визначаються трьома квантовими числами:
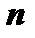 - визначає енергію і набуває таких значень:
- визначає енергію і набуває таких значень: 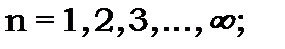
 - визначає абсолютну величину моменту кількості руху
- визначає абсолютну величину моменту кількості руху
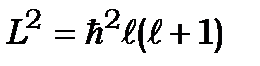 і для заданого числа
і для заданого числа 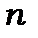 набуває таких значень:
набуває таких значень: 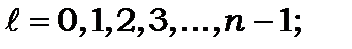
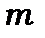 - визначає проекцію моменту кількості руху на вісь
- визначає проекцію моменту кількості руху на вісь 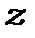
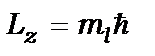 і для заданого числа
і для заданого числа  набуває таких значень:
набуває таких значень: 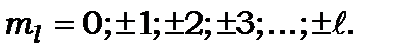
6. Для даного квантового числа  число
число 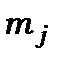 набуває
набуває 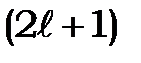 значень (див.таблицю 8.3)
значень (див.таблицю 8.3)
7. При заданому значенні 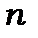 існує
існує 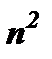 станів*
станів*
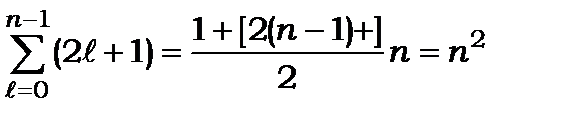 , (8.93)
, (8.93)
або 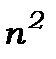 - виродження.
- виродження.
8. В атомі водню існує стан з орбітальним квантовим числом  , у якого момент кількості руху дорівнює нулеві
, у якого момент кількості руху дорівнює нулеві
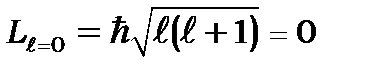 . (8.94)
. (8.94)
9. Стан з орбітальним квантовим числом 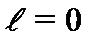 не має також орбітального магнітного моменту
не має також орбітального магнітного моменту
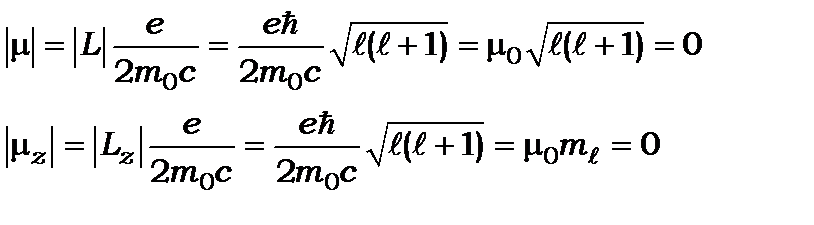 . (8.95)
. (8.95)
10. Виродження за орбітальним числом  знімається магнітним полем, бо енергія електрона в атомі, що знаходиться в магнітному полі з напруженістю
знімається магнітним полем, бо енергія електрона в атомі, що знаходиться в магнітному полі з напруженістю 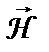 , залежить від магнітного квантового числа
, залежить від магнітного квантового числа 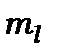

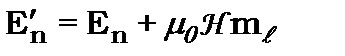 , (8.96)
, (8.96)
яке може мати 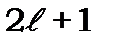 значень.
значень.
|
Рис.8.6. Схема термів і основних електронних переходів атома водню. |
11. Спектральні лінії атома водню залежать лише від головного квантового числа 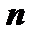 , бо енергія електрона в атомі водню не залежить від орбітального квантового числа, тобто має місце виродження по орбітальному числу
, бо енергія електрона в атомі водню не залежить від орбітального квантового числа, тобто має місце виродження по орбітальному числу  . Якщо відсутнє зовнішнє магнітне поле, то існує ще й виродження за магнітним квантовим числом
. Якщо відсутнє зовнішнє магнітне поле, то існує ще й виродження за магнітним квантовим числом  .
.
Дата добавления: 2018-05-09; просмотров: 1789; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!

