Спектральні серії атомних спектрів лужних металів
Система термів - енергій стаціонарних станів валентного електрона атомів лужних металів, що залежать від двох квантових чисел 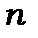 і
і  , наведена в таблиці 9.2 та на енергетичних діаграмах
, наведена в таблиці 9.2 та на енергетичних діаграмах
| Таблиця 9.2. Система термів лужних металів. | ||||||
| S | P | D | F | G | H | |
атом 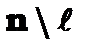
| 0 | 1 | 2 | 3 | 4 | 5 |
| Li 2 | 2S | 2P | - | - | - | - |
| Na 3 | 3S | 3P | 3D | - | - | - |
| K 4 | 4S | 4P | 4D | 4F | - | - |
| Pb 5 | 5S | 5P | 5D | 5F | 5G | - |
| Cz 6 | 6S | 6P | 6D | 6F | 6G | 6H |
(рис.9.1-9.3). Між термами можуть відбуватись дипольні переходи, коли виконуються правила відбору орбітального квантового числа  . Дипольні переходи мають місце, коли розміри атомів менші за довжину хвилі фотона, що випромінюється
. Дипольні переходи мають місце, коли розміри атомів менші за довжину хвилі фотона, що випромінюється  . У цьому разі ймовірність переходу пропорційна матричному елементу дипольного переходу
. У цьому разі ймовірність переходу пропорційна матричному елементу дипольного переходу
 , (9.13)
, (9.13)
де  - дипольний момент.
- дипольний момент.
|
Рис.9.2. Схема термів і переходів між ними для атомів водню і літію. |
Окремі лінії можна згрупувати в серії (рис.9.2).
Головна серія (principal) включає переходи між 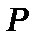 і
і  станами
станами
 ,
, 
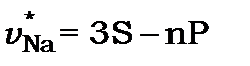




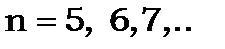


Довжини хвиль ліній випромінювального спектра цієї серії рівні довжинам хвиль відповідних ліній спектра поглинання. Такі лінії в спектроскопії називаються резонансними. Вони легко збуджуються, інтенсивні і спостерігаються навіть у спектрах поглинання холодних не збуджених додатково парах металів.
Різка серія (sharp) або друга побічна включає переходи між  і
і 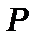 станами
станами






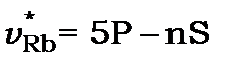

|
Рис.9.3.Схема рівнів енергії і переходів між ними для атома літію. |


|
Рис.9.4. Схема енергетичних рівнів і переходів між ними для атомів натрію. |
Лінії цієї серії різкі. Вони знаходяться в більш довгохвильовому діапазоні довжин хвиль, ніж лінії головної серії. В спектрах не збуджених „холодних” парів лужних металів не спостерігається інверсії (обертання) ліній, тобто в холодних парах не спостерігається спектрів поглинання (вбирання) цієї серії. В збуджених (нагрітих) парах з’являються лінії спектра поглинання (вбирання).
Дифузна серія (diffusion) або перша побічна виникає при переході валентного електрона із 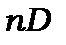 рівнів на найнижчий рівень
рівнів на найнижчий рівень 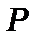 .
.


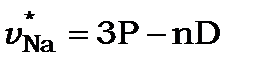


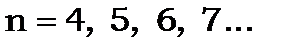




Лінії цієї серії дещо розмиті.
Фундаментальна серія(fundamental) виникає при переходах валентного електрона із  рівнів на нижчий
рівнів на нижчий  рівень.
рівень.


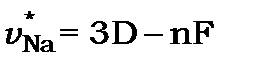





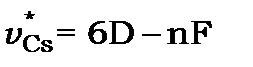

Дублетна структура термів та спектральних ліній атомів лужних металів
Дослідним шляхом було встановлено, що спектральні лінії атомних спектрів лужних металів мають складну тонку структуру. Кожна лінія головної і різкої серій – дублети, бо складається із двох близьких ліній, алінії дифузної й фундаментальної серій - триплети. Різниці частот між окремими лінями тонкої структури по різному залежать від головного квантового числа  : у дублетів головної серії вона зменшується із збільшенням квантового числа
: у дублетів головної серії вона зменшується із збільшенням квантового числа  , у ліній різкої серії
, у ліній різкої серії  не залежить від
не залежить від  , у триплетів дифузної серії різниця частот
, у триплетів дифузної серії різниця частот 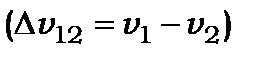 не залежить від
не залежить від  а
а  зменшується обернено пропорційно кубу головного квантового числа тощо. Наявність тонкої структури свідчить, що енергія електронів залежить не тільки від квантових чисел
зменшується обернено пропорційно кубу головного квантового числа тощо. Наявність тонкої структури свідчить, що енергія електронів залежить не тільки від квантових чисел  і
і  . Мультиплетна структура не знайшла пояснення в межах не релятивістської теорії, що базується на основі рівняння Шредінґера. Отже потрібно було шукати нові причини появи тонкої структури термів та мультиплетності спектральних ліній. Виникла необхідність припустити, що електрону притаманний внутрішній ступінь свободи.
. Мультиплетна структура не знайшла пояснення в межах не релятивістської теорії, що базується на основі рівняння Шредінґера. Отже потрібно було шукати нові причини появи тонкої структури термів та мультиплетності спектральних ліній. Виникла необхідність припустити, що електрону притаманний внутрішній ступінь свободи.
Спін електрона
В 20-х роках ХХ століття виникла гіпотеза, що електрон має власний момент кількості руху - спін. До цього спонукали такі експериментальні факти, які без уведення спіну не вдавалось пояснити:
· мультиплетна структура спектральних ліній;
· експериментальне значення гіромагнітного фактору  , замість розрахованого для орбітального моменту
, замість розрахованого для орбітального моменту 
 ,
,
де  ;
;
· наявність у незбудженого атома  в стані
в стані 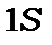 магнітного моменту
магнітного моменту  тоді як водень не повинен його мати
тоді як водень не повинен його мати 
· розщеплення атомних пучків в неоднорідному магнітному полі (досліди Штерна і Герлаха розділ 15.5) на парну кількість складових компонентів, тоді якатоми з орбітальними магнітними моментами можуть розщепитись лише на непарне число компонент.
Всі ці факти примусили припустити, що електрон має власний момент кількості руху LS, який був названий спіном. Цю гіпотезу в 1925 році висунули американські вчені Юленбек і Гаудсміт,згідно якої спін електрона за абсолютною величиною дорівнює
 , (9.14)
, (9.14)
де  - спінове квантове число, яке для електрона рівне
- спінове квантове число, яке для електрона рівне
 . (9.15)
. (9.15)
Проекція спіну на вісь  визначається за формулою
визначається за формулою
 , (9.16)
, (9.16)
де  - магнітне спінове число, яке може мати 2 значення: 1/2 і -1/2 для одного електрона.
- магнітне спінове число, яке може мати 2 значення: 1/2 і -1/2 для одного електрона.
Електронному спіну відповідає спіновий магнітний момент,
Дата добавления: 2018-05-09; просмотров: 449; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!



