Тонка структура спектрів складних атомів як наслідок спін-орбітальної взаємодії
Взаємодія спіну з орбітальним моментом електрона характеризується енергією взаємодії 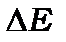 . Її можна оцінити, розглядаючи взаємодію магнітних моментів між собою або одного з магнітних моментів з магнітним полем, зв’язаним з другим магнітним моментом, наприклад, спінового магнітного моменту
. Її можна оцінити, розглядаючи взаємодію магнітних моментів між собою або одного з магнітних моментів з магнітним полем, зв’язаним з другим магнітним моментом, наприклад, спінового магнітного моменту  з магнітним полем орбітального магнітного моменту
з магнітним полем орбітального магнітного моменту  :
:
 . (9.26)
. (9.26)
Оскільки  , a
, a 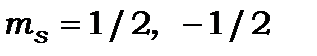 , то зміна енергії
, то зміна енергії  збільшується або зменшується в залежності від орієнтації спіну, що визначає знак квантового числа ms
збільшується або зменшується в залежності від орієнтації спіну, що визначає знак квантового числа ms 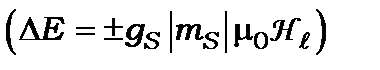 . Щоб оцінити величину цієї енергії, необхідно знати магнітне поле
. Щоб оцінити величину цієї енергії, необхідно знати магнітне поле  . Для його визначення розглянемо орбітальний рух електрона навколо атомного ядра в системі координат, зв’язаній з електроном (рис.9.6.б). У цій системі координат електрон знаходиться у спокої, а атомне ядро рухається навколо нерухомого електрона. Рух позитивно зарядженого ядра створює магнітне поле з напруженістю
. Для його визначення розглянемо орбітальний рух електрона навколо атомного ядра в системі координат, зв’язаній з електроном (рис.9.6.б). У цій системі координат електрон знаходиться у спокої, а атомне ядро рухається навколо нерухомого електрона. Рух позитивно зарядженого ядра створює магнітне поле з напруженістю  або для випадку атома водню
або для випадку атома водню  і
і  . Позначимо швидкість електрона у
. Позначимо швидкість електрона у
| Рис.9.6. Схема спін-орбітального зв’язку: а) – початок координат на ядрі, б) – початок координат на електроні, в) – розщеплення рівнів. |
стані 1s через aс = v і підставивши її у вираз  , отримаємо
, отримаємо 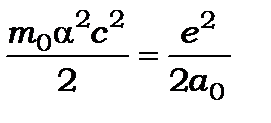 . Із цього співвідношення отримаємо вираз для сталої тонкої структури
. Із цього співвідношення отримаємо вираз для сталої тонкої структури 
 . (9.27)
. (9.27)
Стала тонкої структури - фундаментальна фізична стала, яка визначає величину розщеплення спектральний ліній. У рамках напівквантової теорії Бора для атома водню вона характеризує швидкість електрона на першій борівській орбіті  .
.
Визначимо абсолютну величину напруженості магнітного поля 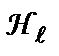 , що створюється рухом ядра навколо електрона, через сталу тонкої структури
, що створюється рухом ядра навколо електрона, через сталу тонкої структури
 (9.28)
(9.28)
Підставивши (9.28) у вираз для енергії спін-орбітальної взаємодії для атома водню (9.26) і враховуючи значення радіуса Бора і енергій  отримаємо:
отримаємо:
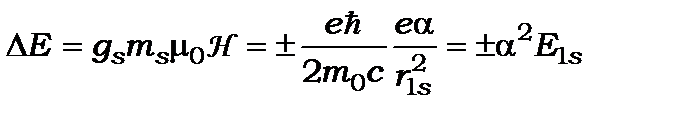 . (9.29)
. (9.29)
Енергія 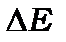 спін-орбітальної взаємодії залежить від квадрата сталої тонкої структури
спін-орбітальної взаємодії залежить від квадрата сталої тонкої структури  , яка згідно (9.27), – мала величина
, яка згідно (9.27), – мала величина  , тому спін-орбітальна взаємодія значно менша за енергію стаціонарного стану
, тому спін-орбітальна взаємодія значно менша за енергію стаціонарного стану  . Але вона збільшується у
. Але вона збільшується у 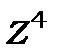 разів для воднеподібних систем із зарядом ядра
разів для воднеподібних систем із зарядом ядра  , що вже відчутно для спектрів лужних металів.
, що вже відчутно для спектрів лужних металів.
Енергія спін-орбітальної взаємодії залежить від магнітного спінового квантового числа ms, яке може мати два значення ±1/2. Це означає, що спін-орбітальна взаємодія призводить до розщеплення енергетичних рівнів стаціонарного стану на два підрівні з енергіями  і
і Ці два рівні енергії відповідають двом значенням квантового числа сумарного моменту кількості руху
Ці два рівні енергії відповідають двом значенням квантового числа сумарного моменту кількості руху  ,
,

або

Для кожного числа  одноелектронного атома є два значення числа
одноелектронного атома є два значення числа  :
:
 (9.30)
(9.30)
В окремому випадку, коли  (
(  - стан)
- стан)
 (9.31)
(9.31)
Таким чином, стаціонарні стани водневоподібних атомів лужних металів з одним валентним електроном визначаютьсятрьома квантовими числами ,
,  і
і 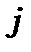 . Їх терми прийнято позначати:
. Їх терми прийнято позначати:
 ,
,
де -називаєтьсямультиплетністю термів,
-називаєтьсямультиплетністю термів,  - головне квантове число. (Стани електронів в атомі позначаються
- головне квантове число. (Стани електронів в атомі позначаються 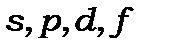 , а терми
, а терми  ).
).
Дата добавления: 2018-05-09; просмотров: 403; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
