Асфиксия, как фактор перинатальных церебральных расстройств
Среди многих факторов, повреждающих головной мозг новорожденных, особо следует выделять гипоксию, которая может быть отнесена к универсальным повреждающим агентам. Асфиксия, регистрируемая у новорожденных, очень часто является лишь продолжением гипоксии, начавшейся еще во внутриутробном периоде. Статистика репродуктивных потерь весьма убедительно свидетельствует об этом. Беременности, возникающие и протекающие на фоне острых и хронических заболеваний (болезни сердечно-сосудистой и респираторной систем и др.), сопровождаются гестозом и эпизодами внутриутробной гипоксии [1, 2). Внутриматочная гипоксия и гипоксия в родах, обусловленная нарушениями маточно-плацентарного кровообращения, в 38,45% случаев является причиной перинатальной смертности, а в 59,04%—причиной мертворожден и и. В 72,4% гипоксия и асфиксия становится одной из главных причин гибели плода в родах или в ранний неонатальный период (3).
Хорошо известно, что асфиксия, перенесенная в родах и в периоде новорож-денности, не проходит бесследно и оказывает негативное воздействие на развивающийся мозг (4, 5). В работах до 70-х годовXX столетия для оценки состояния головного мозга новорожденного ребенка использовались в основном косвенные методы ( анамнез, неврологический статус и др.). Поэтому основные сведения о патогенезе асфиксических повреждений мозга, характере морфологических изменений и др. были получены в результате экспериментальных исследований на животных (Б.Н.Клосовский, Т.П.Жукова, П.К.Анохин, А.П.Дыбан и др.). В 80-е годы в связи с появлением новой технологии по выхаживанию новорожденных и обследованию головного мозга возник «неврологический бум", в результате которого была получена новая информация о структуре и функции мозга новорожденного ребенка (Са!уег. Агтз1гопд, Ртег, Меп1,1еуепе, Ро1апс) и др.), особенностях мозгового кро-вотока (Рептап, БТе^аП), о реакциях мозга на повреждающие воздействия (1-епп, Регйпв), о компенсаторных возможностях мозга и др. (Уо1ре, Репюпе!, РгесМИидр.). Однако от экспериментальных исследований на животных не отказались. Они,как и прежде, были необходимы для изучения патофизиологических нарушений в мозгу при гипоксии (Оипп, Еау/ага, СПо1, У^ППатз, Вгуап, РюМагазоп и др.).
|
|
|
Клиницистам хорошо известны исходы гипоксических повреждений ЦНС, которые носят весьма разнообразный характер: от минимальных мозговых дисфункций (ММД) до грубых двигательных и интеллектуальных расстройств, объединяемых под общим названием детский церебральный паралич (6,7, 8, 9, 10). В основе психоневрологических расстройств лежат значительные нейрональные потери, дистрофические изменения нервных клеток в коре головного мозга, в подкорковых структурах, в желудочках мозга и перивентрикулярном пространстве (11).
|
|
|
При селективном нейрональном некрозе в патологический процесс вовлекается кора больших полушарий и мозжечка, таламус, двигательные ядра моз-
гового ствола. В клинической картине преобладают такие грубые симптомы как ступор/кома, судороги, гипотония, отсутствие сосательного рефлекса и др. Исходом селективного нейронального глиоза могут быть спастическая квадрипле-гия, судороги, атаксия, умственная отсталость и др.
Повреждения головного мозга, расцениваемыекак статус марморатус, обусловлены поражением базальных ганглиев и, прежде всего, таламуса. Следствием чего являются такие расстройства какхореоатетоз и спастическая квадриплегия.
При парасагиттальных церебральных повреждениях патологический процесс затрагивает в основном церебральную кору. В клинической картине в первые дни жизни превалируют общие симптомы в виде вялости, снижения церебральной активности. Тем не менее остаточные явления могут также иметь очень тяжелые последствия (спастическая квадриплегия или парез, гемипарез, умственная отсталость).
|
|
|
Ишемическая перивентрикулярная лейкомаляция связана с поражением белого вещества мозга и чаще всего наблюдается у недоношенных детей (грубо выраженный синдром угнетения ЦНС).
При фокальном ишемическом некрозе в патологический процесс вовлекается корковое и подкорковое белое вещество с образованием лорэнцефалий. Исходом этих нарушений могут быть спастический геми- или квадрипарез, судороги (12, 13, 14, 15, 16).
Принимая во внимание, что основной причиной этих тяжелых неврологических расстройств является асфиксия, эти неврологические заболевания склонны объединять общим термином «асфиксические энцефалопатии». Тем не менее в последние годы исследователи отдают предпочтение другому термину более полно отражающему суть заболевания — гипоксически-ишемическая эн-цефалопатия. В основу термина положен ведущий патогенетический признак-гипоксия, основные изменения, происходящие в мозге— ишемия (вплоть дс кровоизлияния), а объект воздействия асфиксии — головной мозг (энцефалои новорожденного ребенка.
При этом обращается внимание на существующую разницу между доношенными и недоношенными детьми по характеру возникающих нозологических форм неврологических расстройств.
|
|
|
У доношенных детей выделяют три нозологические формы:
• Гипоксически-ишемическая энцефалопатия (ГИЭ);
• Некроз стволовых ядер;
• Субарахноидальные кровоизлияния. Для недоношенных детей свойственны:
• Перивентрикулярный геморрагический инфаркт;
• Перивентрикулярно-интравентрикулярные кровоизлияния;
• Перивентрикулярная лейкомаляция.
Однако это деление следует считать весьма условным, т.к. речьможет идт.' лишь о преобладании тех или иных расстройств у доношенных или недоноше"-ных детей.
Патофизиология гипоксически-ишемической энцефалопатии
Асфиксия иее воздействиена растущий мозг находится в центре внимания исследователей в течениемногих лет. Тем неменее, до сих пор в изучен.".-
252
ведущих звеньев патогенеза существует много белых пятен. Все же представляется возможным выделить две главные гипотезы:
• В основе ГИЭ лежат метаболические расстройства — «метаболическая катастрофа", пусковым механизмом которой является дефицит Од, а непосредственно повреждающими мозг факторами — продукты извращенного метаболизма.
• В основе ГИЭ лежат церебро-васкулярные расстройства и нарушения механизма ауторегуляции мозгового кровообращения, наступающие при дефиците О
Не вызывает сомнения, что эти две гипотезы взаимосвязаны и представляют собой фрагменты одного процесса. Действительно, существуют "сцеплен-ность" мозгового кровотока с метаболизмом мозга. Схема нейрональных повреждений при дефиците Од, связанном с перинатальной гипоксией, такова: повреждение гемато-энцефалического барьера ведет к нарушениям метаболизма глюкозы (гексозомонофосфатный путь), затем к нарушению синтеза липидов и нуклеиновых кислот -^ снижению рН тканей (в периартериальном пространстве) —> накоплению молочной кислоты —» повышению РСО —> падению артериального давления и снижению скорости мозгового кровотока -» нарушению гомеостаза кальций, снижению высокоэнергетических фосфатных соединений, повышению уровня лактата в тканях мозга —» накоплению жирных кислот (арахидоновой кислоты) —> изменению проницаемости нейронов —> и к утрате церебральной ауторегуляции мозгового кровотока (17, 18, 19,20).
При этом непосредственными факторами повреждения головного мозга при гипоксии считают: ацидоз, накопление аминокислот и свободных кислородных радикалов. Ацидоз, являющийся неизбежным спутником кислородной недостаточности, проявлялся в высоких концентрациях молочной кислоты в тканях. Чем выше ее накопление, тем меньше существует возможность восстановления церебральных функций. Среди аминокислот, оказывающих токсическое воздействие на мозговую ткань, выделяют особо такие как у-аминобутировую кислоту, глутамат, аспартат, таурин, фосфоэтаноламин и этаноламин, участвующие в передаче возбуждения. Свободные кислородные радикалы оценивают как потенциально деструктивные вещества, повреждающие клеточные мембраны и митохондрии (супероксидный ион, гидроксия и др.).
На основе этих исследований и в последующем была предложена так называемая глутаматная гипотеза повреждения нейронов при ишемии/аноксии мозга и механизмы ее реализации через гиперстимуляцию глутаматных рецепторов и каскад внутриклеточных реакций (21,22, 23, 24, 25, 26).
Среди аминокислот, накапливающихся в мозгу при гипоксии выделяютособо глутамат.На долю глутаматных рецепторов (N1^/^- рецепторов) приходится около 80% синапсов и нейронов вкоре и гипокампе. Значимость глутаматных рецепторов очень высока,т.к. они являются основными возбуждающими рецепторами в мозге, участвуют в интегративных процессахЦНС, в регуляции сенсорной и моторной функций, вдыхании и кардиоваскулярной деятельности.
Считается, что повреждение или гибель нейронов при токсическом воздействии глутамата сопровождается повышением комплекса Са2* и зависимых от него процессов. Это приводит к чрезмерной активности протеаз, киназ, эндо-нуклеаз и, как следствие, к изменениям генетического аппарата, фрагментации ДНК, необратимой деструкции внутриклеточных структур мембран. В свою очередь повышенная концентрация внутриклеточного Са21" способствует усилению
свобод норади кал ьн о го оксиления. Таким образом, происходит грубое нарушение процессов внутриклеточного взаимодействия. Конечным исходом цепи патологических метаболических реакций является гибель нейронов. При этом ней-рональные потери могут быть связаны с некрозом или апоптозом. Разница между ними состоит в том, что при дегенерации нейрона вследствие некроза морфологическая картина представлена явлениями отека и набухания, вакуолизацией, распадом и лизисом внутриклеточных структур нейрона. При гибели нейронов, обусловленной апоптозом, речь идет озапрограммированной смерти нейрона («арор1оз1'з ог ргодгаттеа се11 аеа11т>), описанной еще в 1972 г. (Кег УУуШе, Сите). Гибель нейрона осуществляется под контролем системы функцг онально связанных генов. Следует заметить, что помимо генов, провоцирующг' процессы апоптоза, в нейронах функционируют и гены, предупреждающие ,' подавляющие «смертный приговор» нейронам- Программа смерти, запускаема^ «суицидными» генами реализуется через внутриклеточные белки р53, р54, получившие название «танатины». Существенным отличием гибели нейронов пр.-некрозе и апоптозе является то, что гибель нейронов путем апоптоза растянут-. во времени. Если это принять во внимание, то становится очевидным, чтогипок-сические повреждения мозга носят прогредиентный характер, а обнаружени-психоневрологических дефектов на протяжении постнатального развития следует рассматривать как феномен отсроченных страданий.
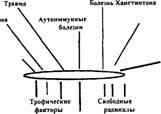
Эта сложная цепь метаболических превращений сведена в упрощенную схему (26), которая, как утверждают исследователи, является основой патогенеза многих заболеваний ЦНС, в котором принимает участие гипоксия (Рис. 4.1-1).
Для возникновения метаболической катастрофы требуется время. Обычно онс ограничивается минутами или несколькими часами после рождения ребенка.
Н.В. Использование этого краткого промежутка времени, когда наступающие изменения в мозгу еще носят обратимый характер, является залогом профилактики тяжелых церебральных расстройств. При этом первостепенное клиническое значение придается показателя?,-общей и церебральной гемодинамики. Непосредственной реакцией на гипоксию у плода и новорожденного является повышение интенсивности работы сердца, мозгового кровотока и обеспечение Од мозговой ткани (Рис. 4.1-2). До те." пор, пока содержание Од в артериальной крови успевает восстанавливаться (дс 90%) мозговых повреждений не наступает (Рис. 4.1-3}. Сниженное восстановление концентрации Од (менее 90%) способствует появлению кардиоваскулярны» расстройств (до коллапса) и возникновению поражений головного мозга.
Н.В. Очень высокая чувствительность кардиоваскулярной системык гипоксии позволяет использовать показатели деятельности сердца длямониторинга плода.Эти показатели выполняют роль «клинического гида» в оценке ситуации и определении угрозынаступления асфиксической энцефалопатии.
Действительно, новорожденные с выраженной ГИЭ почти всегда имею' нерегулярную работу сердца и измененное кровяное давление.
Следует иметь в виду, что разные структуры головного мозга обладаю" разной переносимостью кислородного голодания. Это связано с тем, что темпь созревания различных регионов мозга различны и сцепленность кровотока с интенсивностью обмена веществ варьирует в зависимости от топографической зоны мозга. Так, известно, что продолговатый мозг обладает высокой чувствительностью к РСО, и при гипоксическом воздействии происходит сразу же уве-
ИнфекцииЦНС
Болезнь Парк-ннсона
/
Боковой амиотрофический
.СЮКрОЧ
т'Са2'1' Экеайтотоксичность
111 * ^* |
Гибель нейронов: апоптоз и/илинекроз|
Ишемия
1
Энергетический
Дефицит
+
Выброс глутамата
Дата добавления: 2018-02-28; просмотров: 248; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
