Билет №136. Цирроз печени. Этиология, патогенез, виды. Исходы патогенез основных проявлений. Портальная гипертензия. Этиология, патогенез, виды.
Цирроз печени – это хроническое заболевание, характеризующееся диффузным разрастанием соединительной ткани в результате воспалительной реакции и гибели гепатоцитов, приводящей к структурной перестройке архитектоники печени и компенсаторной гиперплазии сохранившейся ткани с образованием узлов регенератов. От греч. к irrhos – «рыжий», термин, который ввел Р.Лаэннек, имея в виду особенности морфологических изменений печени (плотная, бугристая, рыжего цвета).
Чаще говорят о цирротической стадии хронического гепатита.
Этиология:
- Инфекционный (вирусный гепатит, паразитарные заболевания, инфекции желчных путей)
- Токсический и токсико-аллергический (алкоголь, промышленные и пищевые яды, лекарственные вещества, аллергены)
- Билиарный (холангит, холестаз любой природы)
- Обменно-алиментарный (недостаточность белков, витаминов, липотропных факторов, болезни накопления)
- Циркуляторный (хронический венозный застой)
- Криптогенный
Один и тот же этиологический фактор может привести к разным морфологическим вариантам цирроза, так же как и разные причины - к одному виду.
Патогенез
Воздействие этиологических факторов → некрозы гепатоцитов → коллапс стромы, образование рубцов, нарушение кровоснабжения соседних интактных участков → усиленная регенерация сохранившихся клеток → образование узлов-регенератов → сдавление окружающей ткани с проходящими в ней сосудами → сдавление печеночных вен → нарушение оттока крови → портальная гипертензия и образование анастомозов между ветвями воротной и печеночных вен → поступление крови по анастомозам в обход сохранившейся паренхимы, что нарушает ее кровоснабжение → новые ишемические некрозы и прогрессирование цирроза. Параллельно разрастается соединительная ткань: из перипортальных полей в паренхиму, фрагментируя печеночные дольки → образование «ложных долек» - источники узлов регенерации.
Виды цирроза
Различают три основных морфологических варианта:
- Портальный (септальный) – образование соединительнотканных перегородок (септ), соединяющих перипортальные поля с центральной зоной дольки и фрагментирующих ее. Мелкие узлы-регенераты, окруженные узкими прослойками соединительной ткани. Чаще следствие алиментарной недостаточности и алкоголизма.
- Постнекротический – следствие массивных и субмассивных некрозов (вирусный или токсический гепатит). Крупные узлы-регенераты неправильной формы, неодинаковой величины. Между ними широкие поля спавшейся опустошенной коллагенизированной стромы со сближенными портальными трактами.
- Билиарный – 1) первичный билиарный – хроническое аутоиммунное заболевание, деструкция мельчайших внутрипеченочных желчных ходов, внутридолевой и перипортальный холестаз. 2) вторичный билиарный – длительная закупорка внепеченочных желчных ходов приводит к их расширению, холангиту, перихолангиту.
По более современной морфологической классификации выделяют три формы цирроза: мелкоузловая, крупноузловая, смешанная.
Исход. Патогенез основных проявлений.
Течение, как правило, прогрессирующее. Терминальная стадия характеризуется желудочно-кишечными кровотечениями и развитием печеночной комы (две наиболее частые непосредственные причины смерти). ЖКТ-кровотечения возникают при разрыве варикозных узлов нижней трети пищевода, печеночная кома – следствие печеночно-клеточной недостаточности.
Основные клинические проявления цирроза печени связаны с развивающейся портальной гипертензией (следствие сдавления печеночных вен и застоя крови в печени) и печеночно-клеточной недостаточностью.
Печеночно-клеточная недостаточность:
| Расстройства обмена веществ | Нарушения функций печени |
|
|
Портальная гипертензия
Стойкое повышение давления в сосудах воротной вены (выше 7-10 мм рт.ст.). В соответствии с этиологией можно выделить следующие виды (по Литвицкому):
Внутрипеченочная – цирроз, шистосомоз, гемохроматоз, опухоль.
Предпеченочная – блокада притока крови по портальным сосудам (вследствие сдавления, окклюзии, аневризм, тромбозов ствола воротной и селезеночной вен).
Подпеченочная – блокада оттока крови от печени (застой в большом круге; тромбоз, эмболия, сдавление нижней полой вены).
При повышении портального давления нарушается отток крови от органов брюшной полости → усиливается транссудация жидкости из сосудистого русла в брюшную полость и образуется асцит. При циррозе печени важную роль в развитии асцита также играют гипоальбуминемия (снижение онкотического давления плазмы) и вторичный гиперальдостеронизм (недостаточная инактивация альдостерона и АДГ в пораженной печени).
Нарушения портального кровообращения в течение длительного времени могут быть компенсированы тем, что кровь из воротной вены по существующим анастомозам может поступать в нижнюю и верхнюю полые вены. Срок развития асцита зависит от степени развития коллатерального кровообращения – числа портокавальных анастомозов.
137. Экспериментальное моделирование патологии печени ( фистула Н. Экка и Н.Экка- И.П.Павлова, органостомия по Лондону). Стеатоз печени, этиология, патогенез. Поражение печени при алкоголизме. Этиология и патогенез ожирения печени и цирроза печени у алкоголиков.
Прямая фистула Экка (1877)
Для выяснения роли двойного кровоснабжения печени он наложил собаке анастомоз между воротной и полой венами с последующей перевязкой портальной вены выше места наложения соустья.
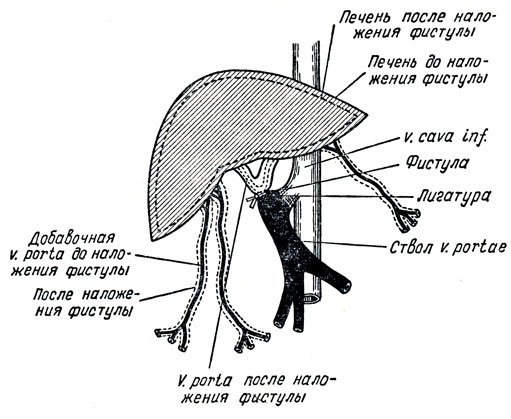
Такое изменение кровообращения у собак не было смертельным .=== кровоснабжение через воротную вену не является жизненно необходимым. ( обьем кровотока падает как минуму на ½ , но этого доствточно для печени).
В 1893 г И.П. Павлов описал феномен «мясного отравления» у собак с прямой фистулой при обильном кормлении мясом: атаксия, судороги, кома со смертельным исходом, т к в крови уровень аммиак и аминокислоты взрастает ==» «мясное отравление» (надо вспомнить пути детоксикации аммиака) в цикле мочевины(карбомоил фасфат и оттуда NH3)
Марковиц показал, что при правильной технике (отсутствие послеоперационных сращений, суживающих печеночную артерию)
Полное удаление печени ( модель острой печеночной недостаточности) Манн и МАгат
1этап – обратная фистула Павлова – Экка, анастомоз между полой и воротной веной с последующей перевязкой нижней полой вены выше места наложения соустья. Переполнение печени кровью от всей нижней половины туловища приводит к развитию мощных коллатералей, отводящих кровь, минуя печень.
2 этап – через 4-6 недель перевязывают воротную вену выше места наложения соустья.
3 этап – удаление печени.
Цель такого удаления в 3 этапа – избежать гемодинмаческие расстройства.
Через 3-8 часов после 3 этапа операции собаки впадают в гипогликемическую кому. Смерть вследствие недостаточности дыхания и кровообращения.
Частичная гепатэктомия
Можно изучить особенности регенерации печени. Даже удаление 75% массы печени не вызывает ее функциональной недостаточности. А течение 4-8 недель печень полностью восстанавливает свою массу за счет гиперплазии оставшихся частей. – в основе уникальная способность паренхиматозных и стромальных клеток органа к продукции ростовых цитокинов, например инсулиноподобный фактор роста. === но регенерация с нарушением микроархитектруры органа и биполярная ориентация гепатоцитов. Образуются узлы регенерации, нарушается внутрипеченочный желче и кровоток ==== цирроз печени.
Органостомия по Е.С. Лондону
Изучение функции печени по составу проб крови, взятых из ее крупных сосудов через специальные канюли.
Стеатоз – жировая дистрофия печени.
Мехаизмы :
- Сниженный синтез апопротеинов (при отравлении 4хлорисым углеродом и квашиоркоре (вид тяжёлой дистрофии на фоне недостатка белков в пищевом рационе))
- Нарушение экскреции ЛПОНП, усиленным притоком жирных кислот в печень( при голодании)
- увелич синтеза и ускорение этерификации ЖК и замедление их распада( при алиментарном ожирении)
Причина основанная – алкоголизм. ( все выше перечисленные механизмы в комбинации. Даже далеко зашедшая жировая трансформация полностью обратима. Накопление жирных кислот сопровождается накоплением натрия и кальция == эффект омыления. Приводит к разрушению мембран и к некрозу. ===образуют жировые клетки.
Гипоксия, классификация, этиология, виды. Нарушения обмена веществ и физиологических функций. Обратимость гипоксии. Внутриклеточные нарушения как основа необратимой стадии гипоксии. Нарушения транспорта кислорода из легких в ткани и углекислоты из тканей в легкие. Нарушения тканевого дыхания.
Гипоксия – ТПП кислородного голодания клеток, возникающего как при недостаточной поставке кислорода, так и при нарушении его использования в клетках.
Классификация по Петрову:
· Экзогенная (гипоксическая) – от недостатка кислорода в атмосферном воздухе
· Эндогенная – от нарушения процессов внешнего и внутреннего дыхания в организме
ü Дыхательная (в рез-те нарушения внешнего дыхания, т.е вентиляции, диффузии, перфузии, любых их сочетаний и равновесия между ними)
ü Гемическая – в рез-те наруш-я взаимодействия кислорода с гемоглобином, включая его дефицит (нарушается транспорт кислорода). Возможно в рез-те заболеваний.
ü Циркуляторная – в рез-ту недост-ти кровообращения или локального нарушения перфузии органа или тканей
ü Тканевая – в рез-те неиспользования кислорода митохондриями
ü Смешанная
Гипоксемия – снижения парциального напряжения кислорода в крови (оценивают по арт. крови), не всегда сопровождает гипоксию. Всегда свойственна экзогенной гипобарической и дыхательной гипоксии, но ее нет при циркуляторной и гемической. Коррелирует с ацидозом, рефлекторно возбуждают ДЦ через каротидные тела. Гиперкапния – избыточное парциальное напряжение двуокиси углерода в крови. Отс. при гипобарической, дыхательной гипоксии – при горной болезни. Явл-ся гуморальным регулятором дых. Центра. Гиперкапния способствует ацидозу. Умеренная гипоксия не отягощающий фактор. Гипокапния – недостаточное парциальное напряжение двуокиси углерода в крови, может быть следствием гипервентиляции, вызывает рефлекторное снижение мозгового кровотока, тормозит ДЦ,способствует развитию алкалоза и некоторых сердечных аритмий. Сопровождает гипобарическую гипоксию, отягащая ее течение. Асфиксия – вариант течения гипоксии, который сопровождается сочетанием гипоксемии и гиперкапнии.
При острой гипоксии мобилизируются срочные компенсаторные механизмы, основанные на гиперфункции дыхательной, сердечно-сосудистой систем и эритрона. На уровне клеток – активация гликолиза, буферные системы, реактивируемые легкими и почками, стремятся поддержать рН. При хрон-ой–долгосрочные => гипертрофия и гиперплазия.
Один вид гипоксии может переходить в другой, при длительной гипоксии обязателен переход в тканевую. Длительная гипоксия нарушает работу митохондрий:
· Начальный этап – сниж-ся скорость аэробного окисления и оксилит. Фосф-ния, возрастает кол-во АДФ и АМФ; снижаются функц. Способности клетки. Снижается соотношение АТФ/АДФ+АМФ, что акт-ет ФФК (фосфофруктокиназу) => анаэробный гликолиз => распад гликогена. На системном уровне: стресс и гормоны стресса (КА и ГКС) => накопление лактата и свободного фосфора => метаболический лактацидоз (может вызвть денатурацию некоторых белков => зернистая дистрофия; формир-ние хроматиновых глыбок) => ФФК угнетается в условиях ацидоза. У незрелых орагнизмов ФФК представлена изоферментами и кислотоустойчива – правило Сиротинина.
· Наиболее энергоемка АТФаза => наруш-ся работа => клетка теряет ионы калия, вне клеток – его избыток => ↓потенциал покоя, положит.поверхн. заряд может меняться на отрицательный (из-за этого клетки крови становятся менее устойчивы к агрегации и адгезии, на тканевом уровне – сладж ЭЦ, форм-ние белых тромбов, краевое стояние ЛЦ). => ↓возбудимость клетки. Также из-за наруш-ия работы АТФазы в клетку проникает избыток Na, возникает гипергидратация клеток => образ-ние вакуолей (мутное набухание, затем баллонная дистрофия – расширение цистерн ЭПС и т.д). Наруш-ся работа цитоскелета => гиалиноз. Белки денатурируют и т.д.
· Кальций-магниевый насос для инактивации Са не работает + Са поступает из внеклеточного пространства, из разрушенных цистерн ЭПС и митохондрий => избыток его актив-ет эндонуклеазы (ионы цинка в данном случае явл-ся антагонистами Са и блок-ют эти ферменты), наруш-ся синтез АТФ, усиливается продукция кислородных радикалов, актив-ря кальпаины (нейтр. протеазы) – их блокаторы - кальпстатины => цитоплазматический протеолиз, разрушение цитоскелета, лизис рецепторов + Са-зависимая трансглутаминаза сшивает белки цитоплазмы. При необратимом повреждении клетки митохондрии захватывают значит. кол-ва Са, что приводит к денатурации ферментов, белков, ↓синтеза АТФ => набухание митохондрий – необратимая стадия. = > нарушение тканевого дыхания
· => мтх перестают быть акцепторами кислорода и субстратов, не окисляют ЖК и их ацилы => формирование эндогенных мылов, что увел-ет детергентную спос-ть цитоплазмы, что приводит к разруш-ию мембран = > начало аутолиза клетки.
141. Дыхательная недостаточность. Виды, этиология. Показатели. Механизмы нарушения вентиляции, диффузии и перфузии. Компенсаторно-приспособительные процессы в системе внешнего дыхания при повреждении отдельных её звеньев. Особенности вентиляционной недостаточности рестриктивного и обструктивного типов.
Дыхательная недостаточность (ДН) – синдром (патологический процесс) при котором система внешнего дыхания не обеспечивает равновесия с внутренним дыханием, не покрывает потребности внутреннего дыхания нормальной ценой.
Основное условие ДН – минутный объем легочной вентиляции (МОЛВ) не достигает величины вентиляторного запроса (ВЗ)
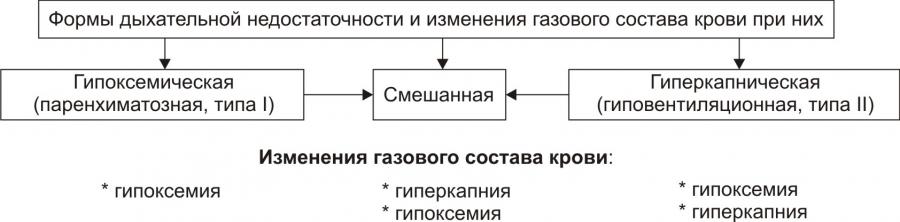
I. Вентиляционная дыхательная недостаточность характеризуется альвеолярной гиповентиляцией, развивается либо
1)из-за нарушения прохождения воздуха по дыхательным путям, тогда она называется обструктивным типом ДН; либо
2) вследствие ограничения расправления легких – в этом случае – рестриктивная ДН.
ІІ. Диффузионная дыхательная недостаточность развивается при нарушении диффузии газов через альвеоло-капиллярную мембрану, характеризуется снижением рО2 без увеличения рСО2, т.к. диффузионная способность СО2 в 20 раз выше О2.
ІІІ. Перфузионная дыхательная недотаточность
-несоответствие общего капиллярного кровотока в малом круге кровообращения объему альвеолярной вентиляции(перфузия<вентиляции).
Ингаляция О2 не повышает степень оксигенации крови при перфузионной форме ДН!
Внешнее дыхание – накачивает в кровь кислород и убирает оттуда СО2
Это тройка:
· Вентиляция (путь газов между атмосферой и альвеолами)
· Диффузия (переход газов через альвеоло-капиллярный барьер)
· Перфузия (микроциркуляция в малом круге, восстан. градиент)
Внутренее дыхание - наоборот, потребляет кислород и накачивает в кровь СО2
Это не только тканевое дыхание, но и диффузия в тканях.
Вентиляция – «коренная в тройке», остальные компоненты внешнего дыхания – пристяжные. Пристяжная может свернуть тройку в кювет. Но вывозит, если что – коренная.
Так как перфузия, а тем более – диффузия – не могут форсироваться в столь широких пределах, как вентиляция, и так как дыхательный центр управляет непосредственно вентиляцией, а не остальными компонентами внешнего дыхания – в ответ на любые нарушения внутреннего дыхания, перфузии и диффузии следует попытка компенсации путём стимуляции вентиляции.
Лимитирующей является возможность гипервентилировать в течение всего необходимого времени без утомления дыхательных мышц. Это возможно только при невысокой кислородной стоимости самой вентиляции. В норме она не превышает 2%. Если потери внутри бронхов – на трение воздушной струи, а также вне бронхов – на растяжение легких и грудной клетки, невысоки, то КПД системы внешнего дыхания велик и гипервентиляция с увеличением МОЛВ в 7-8 раз против нормального значения не сопровождается существенным ростом кислородной стоимости акта вентиляции (до 5-7% только).
Однако,
- выраженный рестриктивный синдром (ограничение растяжимости на вдохе, дыхательных объемов и/или дышащей поверхности альвеол),
- -выраженный обструктивный синдром (невозможность пассивного выдоха, ограничение скорости выдоха, уменьшение эластической тяги легких и проводимости бронхов)
- срыв диффузии и перфузии (паренхиматозная ДН)
уменьшают КПД системы, делают невозможной гипервентиляцию в оптимальном режиме и увеличивают кислородную стоимость дыхания. Это и ведет сначала к скрытой, а при утомлении мышц и установлении гипоксемии – и к явной дыхательной недостаточности.
Скрытая ДН выявляется функциональными нагрузочными пробами.
Пример: проба Траубе (задержать дыхание на 40 с.)
Степень тяжести явной ДН оценивается по глубине гипоксемии.
Критерием декомпенсации явной ДН служит декомпенсация ацидоза, т.е. сдвиг рН крови вниз.
Основной компенсаторный механизм при ДН – одышка
Одышка, её виды. Этиология и патогенез гиперпноээ, тахипноэ, стенотического дыхания. Периодическое дыхание Чейна-Стокса, его патогенез. Патологическое дыхание и его отличие от одышки. Виды патологического дыхания, их патогенез.
Одышка (dyspnoe) – основной компенсаторный механизм при дыхательной недостаточности; в субъективном смысле - тягостное, отрицательно эмоционально окрашенное вегетативное ощущение нехватки воздуха, формируемое при участии гипоталамуса и лимбической системы.
Одышка сопровождается комплексом неприятных ощущений в виде стеснения в груди и нехватки воздуха, доводящих иногда до мучительных приступов удушья. Эти ощущения формируются в лимбической области, структурах мозга, где также возникают реакции тревоги, страха и беспокойства, что придает одышке соответствующие оттенки.
К одышке не следует относить учащение и углубление дыхания, хотя в момент ощущения недостаточности дыхания человек непроизвольно и, что особенно важно, сознательно увеличивает активность дыхательных движений, направленных на преодоление дыхательного дискомфорта. При тяжелых нарушениях вентиляционной функции легких резко повышается работа дыхательной мускулатуры, что определяется визуально по ундуляции межреберных промежутков, усилению сокращения лестничных мышц, отчетливо бывают выражены и физиогномические признаки («игра» крыльев носа, страдание и утомление). Напротив, у здоровых людей при значительном повышении минутного объема вентиляции легких под влиянием физической нагрузки возникает ощущение усиленных дыхательных движений, одышка при этом не развивается. Дыхательный дискомфорт у здоровых людей может возникнуть при тяжелой физической работе на пределе их физиологических возможностей.
При патологии самые различные нарушения дыхания в целом (внешнего дыхания, транспорта газов и тканевого дыхания) могут сопровождаться чувством одышки. При этом обычно включаются различные регуляторные процессы, направленные на коррекцию патологических нарушений. При нарушении включения того или иного регуляторного механизма происходит непрекращающаяся стимуляция центра вдоха, следствием чего является возникновение одышки.
Источниками патологической стимуляции дыхательного центра могут быть:
• ирритантные рецепторы (рецепторы спадения легких) - их стимулирует снижение растяжимости легких;
• юкстакапиллярные (J-рецепторы) - реагируют на повышение содержания жидкости в интерстициальном периальвеолярном пространстве, на повышение гидростатического давления в капиллярах;
• рефлексы, поступающие с барорецепторов аорты и сонной артерии; раздражение этих барорецепторов оказывает тормо-
зящее действие на инспираторные нейроны в продолговатом мозгу; при падении артериального давления уменьшается поток импульсов, в норме тормозящих центр вдоха;
• рефлексы, поступающие от механорецепторов дыхательных мышц при их чрезмерном растяжении;
• изменения газового состава артериальной крови (падение раО2, повышение раСО2, снижение рН крови) оказывают влияние на дыхание (активируют центр вдоха) через периферические хеморецепторы аорты и сонных артерий и центральные хеморецепторы продолговатого мозга.
В зависимости от того, затруднение какой фазы дыхательного цикла испытывает человек, выделяют: инспираторную, экспираторную и смешанную одышку. По продолжительности одышки отмечают постоянную и приступообразную. Постоянную одышку обычно разделяют по степени выраженности: 1) при привычной физической нагрузке: 2) при незначительной физической нагрузке (ходьба по ровному месту); 3) в покое.
Экспираторная одышка (затруднен выдох) наблюдается при обструктивных нарушениях вентиляции легких. При хронической обструктивной эмфиземе легких одышка постоянная, при бронхообструктивном синдроме - приступообразная. При рестриктивных нарушениях вентиляции легких возникает инспираторная одышка (затруднен вдох). Сердечная астма, отек легких различной природы характеризуются приступом инспираторного удушья. При хроническом застое и диффузных грануломатозных процессах в легких, пневмофиброзе инспираторная одышка становится постоянной. Важно отметить, что не всегда при обструктивных нарушениях вентиляции легких возникает экспираторная одышка, а при рестриктивных нарушениях - инспираторная. Такое несоответствие, вероятно, связано с особенностями восприятия больным соответствующих нарушений дыхания.
В клинике весьма часто степень выраженности нарушения вентиляции легких и степень выраженности одышки неравнозначны. Более того, в ряде случаев, даже при значительно выраженных нарушениях функции внешнего дыхания, одышка вообще может отсутствовать.
Основные типа одышки при неповреждённом функционально целостном дыхательном центре:
- брадипноэ - редкое, менее 12 дыхательных движений в минуту, дыхание. Рефлекторное уменьшение частоты дыхания наблюдается при повышении артериального давления (рефлекс с барорецепторов дуги аорты), при гипероксии в результате выключения хеморецепторов, чувствительных к понижению раО2. При стенозировании крупных дыхательных путей возникает редкое и глубокое дыхание, называемое стенотическим. В этом случае рефлексы поступают только от межреберных мышц, и запаздывает действие рефлекса Геринга-Брейера (он обеспечивает переключение дыхательных фаз при возбуждении рецепторов растяжения в трахее, бронхах, бронхиолах, альвеолах, межреберных мышцах). Брадипноэ возникает при гипокапнии, развивающейся при подъеме на большую высоту (горная болезнь). Угнетение дыхательного центра и развитие брадипноэ может иметь место при длительной гипоксии (пребывание в условиях разреженной атмосферы, недостаточность кровообращения и др.), действии наркотических веществ, органических поражениях головного мозга;
- полипноэ (тахипноэ) - частое, более 24 дыхательных движений в минуту, поверхностное дыхание. Этот вид дыхания наблюдается при лихорадке, функциональных нарушениях деятельности центральной нервной системы (например, истерии), поражениях легких (пневмония, застой в легких, ателектаз), болях в грудной клетке, брюшной стенке (боль приводит к ограничению глубины дыхания и увеличению его частоты, развивается щадящее дыхание). В происхождении тахипноэ имеет значение большая, чем в норме, стимуляция дыхательного центра. При снижении растяжимости легких усиливаются импульсы от проприорецепторов дыхательных мышц. При ателектазе усиливаются импульсы с легочных альвеол, находящихся в спавшемся состоянии, и возбуждается центр вдоха. Но во время вдоха непораженные альвеолы растягиваются в большей, чем обычно, степени, что вызывает сильный поток импульсов со стороны тормозящих вдох рецепторов, которые и обрывают вдох раньше времени. Тахипноэ способствует развитию альвеолярной гиповентиляции в результате преимущественной вентиляции анатомически мертвого пространства;
- гиперпноэ - глубокое и частое дыхание. Отмечается при повышении основного обмена: при физической и эмоциональной нагрузке, тиреотоксикозе, лихорадке. Если гиперпноэ вызвано рефлекторно и не связано с повышением потребления кислорода
и выведения СО2, то гипервентиляция приводит к гипокапнии, газовому алкалозу. Это возникает вследствие интенсивной рефлекторной или гуморальной стимуляции дыхательного центра при анемиях, ацидозе, снижении содержания кислорода во вдыхаемом воздухе. Крайняя степень возбуждения дыхательного центра проявляется в виде дыхания Куссмауля;
- апноэ - отсутствие дыхания, но обычно подразумевается временная остановка дыхания. Может возникнуть рефлекторно при быстром подъеме артериального давления (рефлекс с барорецепторов), после пассивной гипервентиляции пациента под наркозом (снижение раСО2). Апноэ может быть связано с понижением возбудимости дыхательного центра (при гипоксии, интоксикациях и др.). Торможение дыхательного центра вплоть до его остановки может возникать при действии наркотических препаратов (эфир, хлороформ, барбитураты и др.), при понижении содержания кислорода во вдыхаемом воздухе.
Одним из вариантов апноэ является синдром нарушения ночного сна (или синдром ночного апноэ), проявляющийся в кратковременных остановках дыхания во сне (5 приступов и более за 1 час представляют угрозу для жизни больного). Синдром проявляется беспорядочным громким храпом, чередующимся с длительными паузами от 10 с до 2 мин. При этом развивается гипоксемия. Часто у пациентов отмечается ожирение, иногда гипотиреоз.
Нарушения ритма дыхательных движений.
Типы периодического дыхания. Периодическим дыханием называется такое нарушение ритма дыхания, при котором периоды дыхания чередуются с периодами апноэ. К нему относятся дыхание Чейна-Стокса и дыхание Биота
(рис. 1).
При дыхании Чейна- Стокса паузы (апноэ - до 5-10 с) чередуются с дыхательными движениями, которые сначала нарастают по глубине, затем убывают. При дыхании Биота паузы чередуются с дыхательными движениями нормальной частоты и глубины.
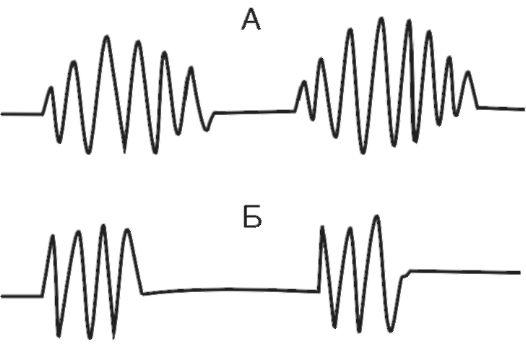
Рис. 1. A - дыхание Чейна-Стокса; Б - дыхание Биота
В основе патогенеза периодического дыхания лежит снижение возбудимости дыхательного центра (или другими словами - повышение порога возбудимости дыхательного центра). Оно может возникать при органических поражениях головного мозга - травмах, инсультах, опухолях, воспалительных процессах, при ацидозе, диабетической и уремической комах, при эндогенных и экзогенных интоксикациях. Возможен переход в терминальные типы дыхания. Предполагают, что на фоне пониженной возбудимости дыхательный центр не реагирует на нормальную концентрацию углекислого газа в крови. Для возбуждения дыхательного центра требуется большая его концентрация. Время накопления этого раздражителя до пороговой дозы определяет длительность паузы (апноэ). Дыхательные движения создают вентиляцию легких, СО2 вымывается из крови, и дыхательные движения вновь замирают. Иногда периодическое дыхание наблюдается у детей и людей старческого возраста во время сна. В этих случаях нормальное дыхание легко восстанавливается при пробуждении.
Терминальные типы дыхания. К ним относятся дыхание Куссмауля (большое дыхание), апнейстическое дыхание и гаспингдыхание. Есть основания предполагать существование определенной последовательности фатального нарушения дыхания до его полной остановки: сначала возбуждение (дыхание Куссмауля), апнейзис, гаспинг-дыхание, паралич дыхательного центра. При успешных реанимационных мероприятиях возможно обратное развитие нарушений дыхания до его полного восстановления.
Дыхание Куссмауля - большое, шумное, глубокое дыхание («дыхание загнанного зверя»), характерное для пациентов с нарушением сознания при диабетической, уремической комах, при отравлении метиловым спиртом. Дыхание Куссмауля возникает в результате нарушения возбудимости дыхательного центра на фоне гипоксии мозга, ацидоза, токсических явлений. Глубокие шумные вдохи с участием основной и вспомогательной дыхательной мускулатуры сменяются активным форсированным выдохом.
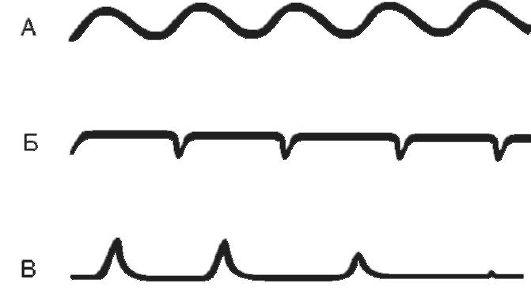
Рис. 2.А - эупноэ; Б - апнейстическое дыхание; В - гаспингдыхание
Апнейстическое дыхание (рис. 2) характеризуется продолжительным вдохом и изредка прерывающимся, форсированным коротким выдохом. Длительность вдохов многократно превышает продолжительность выдохов. Развивается при поражении пневмотаксического комплекса (передозировка барбитуратов, травмы головного мозга, инфаркт моста мозга). Такой вид дыхательных движений возникает в эксперименте после перерезки у животного обоих блуждащих нервов и ствола на границе между верхней и средней третью моста. После подобной перерезки устраняются тормозные влияния верхних отделов моста на нейроны, отвечающие за вдох.
Гаспинг-дыхание возникает в самой терминальной фазе асфиксии (т.е. при глубокой гипоксии или гиперкапнии). Оно встречается у недоношенных детей и при многих патологических состояниях (отравлениях, травмах, кровоизлияниях и тромбозах ствола головного мозга). Это единичные, редкие, убывающие по силе вдохи с длительными (по 10-20 с) задержками дыхания на выдохе. В акте дыхания при гаспинге участвуют не только диафрагма и дыхательные мышцы грудной клетки, но и мускулатура шеи и рта. Источником импульсов при данном виде дыхательных движений являются клетки каудальной части продолговатого мозга при прекращении функции вышележащих отделов мозга.
Различают еще диссоциированное дыхание - нарушение дыхания, при котором наблюдаются парадоксальные движения диафрагмы, асимметрии движения левой и правой половины грудной клетки. «Атаксическое» уродливое дыхание Грокко-Фругони характеризуется диссоциацией дыхательных движений диафрагмы и межреберных мышц. Это наблюдается при нарушениях мозгового кровообращения, опухолях мозга и других тяжелых расстройствах нервной регуляции дыхания.
143. Асфиксия. Виды, этиология, патогенез. Периоды острой асфиксии. Особенности этиологии и патогенеза. Ложная асфиксия, ее последствия.
Асфиксия - угрожающее жизни патологическое состояние, вызванное остро или подостро возникающей недостаточностью кислорода в крови и накоплением углекислоты в организме.
Виды асфиксии:
· Ненасильственная
1. Отек гортани:
- воспалительный
дифтерия, скарлатина, корь, грипп
- аллергический
сывороточная болезнь, отек Квинке
2. Спазм голосовой щели при гипопаратиреозе, рахите, спазмофилии, хорее
· Насильственная :
1) Механическая
1. Обтурационная
- Обтурация дыхательных путей инородными телами
- Сужение просвета дыхательных путей:
- Рефлекторный спазм голосовой щели:
действие химических веществ: бутан, нашатырный спирт, хлор
действие различных температур
2. Компрессионная
Сдавления грудной клетки и живота сыпучими веществами или массивными предметами.
3. Странгуляционная
Сдавливание органов шеи: повешение, удавление петлей, удавление руками; асфиксию от сдавливания груди и живота сыпучими и массивными предметами, а также в давке
2) Аноксия
Асфиксия от отсутствия кислорода (надевание на голову пакета, мешка)
3) Гемическая
Острое нарушение транспорта газов кровью
Также причинами асфиксии могут быть:
1) Нарушение регуляции дыхания и нарушения дыхательной мускулатуры
Этиология:
полиомиелит (паралич мышц), отравления снотворными, наркотическими, отравляющими веществами
2) Нарушение тканевого дыхания
Различают четыре фазы механической асфиксии:
1-я фаза
Понижение раО2 и повышение раСО2 - активация хеморецепторов, развивается гипоксимия..
Напряжение дыхательных мышц – активация проприорецепторов
=> активирование деятельности дыхательного центра:
усиливается и удлиняется вдох (фаза инспираторной одышки),
развивается общее возбуждение,
повышается симпатический тонус (расширяются зрачки, возникает тахикардия, повышается артериальное давление),
появляются судороги.
2-я фаза
Большее изменение газового состава артериальной крови (гиперкапния) - торможение дыхательного центра и центра регуляции кровообращения ( торможение экспираторного центра происходит позднее, так как при гипоксемии и гиперкапнии его возбуждение длится дольше)
=>
урежение дыхания и усиленные движения на выдохе (фаза экспираторной одышки),
начинает преобладать парасимпатический тонус (суживаются зрачки, снижается артериальное давление, возникает брадикардия).
3-я фаза (предтерминальная)
Торможение дыхательного центра =>
прекращение дыхательных движений,
потеря сознания,
падение артериального давления.
4-я фаза (терминальная)
Характеризуется глубокими вздохами типа гаспинг-дыхания.
Смерть наступает от паралича бульбарного дыхательного центра.
Сердце продолжает сокращаться после остановки дыхания 5-15 мин. В это время еще возможно оживление задохнувшегося.
Опыт « Истинная асфиксия»
Методика: полностью пережать трахею крысы
Результаты: изменения частоты, глубины дыхания в соответствии 4м стадиям асфиксии.
Ложная асфиксия
Возникает при дыхании через рот при закрытых носовых проходах.
( Опыт ложная асфиксия: ватными тампонами крысе закрывают ноздри следят за изменением спирограммы. Происходит увеличение глубины дыхания) .
Несмотря на то что газовый состав крови не меняется, создается ощущение нехватки воздуха, из-за чего происходит углубление дыхания.
Механизм действия: в носовой полости находятся барорецепторы тройничного, обонятельного, верхнего гортанного нервов. При исключении носового дыхания выключается действие рефлексов, опосредуемых этими нервами. Импульсы от этих нервов тонически влияют на дыхательный центр и ретикулярную формацию.
Последствия: нарушение когнитивных функций (концентрация, внимание, память)
Ателектаз. Виды, этиология, патогенез. Особенности механизмов образования различных видов ателектаза. Моделирование ателектаза. Сравнительная характеристика механизмов понижения воздушности лёгких при ателектазе и пневмотораксе.
Ателектаз – патологическое состояние, характеризующееся спадением альвеол, альвеолярных ходов и респираторных бронхиол и осложняющее течение легочных заболеваний.
При ателектазе нарушена вентиляция, а сохраненная перфузия ведет к всасыванию газов и достижению глубокой безвоздушности участка легкого. При пневмотораксе нарушена и вентиляция и перфузия, а остаточный объем – сохранен.
При ателектазе:
• нарушается состояние сурфактантной системы
• изменяются эластические свойства
• развивается коллатеральное кровообращение
• нарушаются вентиляция и бронхиальная проходимость в зоне ателектаза
• нарушается диффузия
При тотальных ателектазах - нарастает ослабление сердечной деятельности.
Ателектазы бывают:
1. По распространенности процесса:
• тотальные
• долевые
• сегментарные
• субсегментарные
• двухсторонние
2. По механизму развития:
• компрессионные (сдавление опухолью, кровью, травматическое смещение ткани)
• обтурационные (закупорка инородным телом, слизистыми пробками)
• врожденные (неполноценный первый вдох)
• спастичеческие (в мелких и средних бронхах)
• смешанные
3. По форме:
• конусовидные (ограниченные сегментом)
• пятнистые (ограниченные дольками, ацинусами)
• полосовидные или пластинчатые (ограниченные зонами коллатерального дыхания)
Дыхание изменяется в зависимости от распространенности ателектатического процесса.
Модель А – закупорка бронха, не затрагивая кровеносных сосудов.
Ателектаз в ранние сроки является обратимым состоянием, спустя 4—5 мес. остается стойкое снижение эластичности, уменьшение кровотока и поглощения кислорода. При инфицировании участка ателектаза развивается хронический бронхит и бронхоэктазы, при снижении защитных сил — абсцедирование.
Пневмоторакс. Виды, этиология, патогенез. Особенности механизмов различных видов пневмоторакса. Моделирование пневмоторакса. Сравнительные механизмы понижения воздушности легких при ателектазе и пневмотораксе. Механизмы саногенного действия лечебного пневмоторокса. Патофизиологические основы первой помощи при пневмотораксе.
Пневмоторакс – это патологическое состояние, характеризующееся наличием воздуха в плевральной полости.
Патогенез:
В норме в плевральной полости - отрицательное давление. При сообщении плевральной полости с окружающей средой (через просвет бронха или при нарушении целостности грудной клетки). → Поступление воздуха в плевральную полость и повышение внутриплеврального давления (в норме ниже атмосферного). →Сдавление и спадение лёгочной ткани (коллапс лёгкого) -» неэффективная вентиляция -> гипоксия. →Смещение средостения в противоположную сторону, сдавление и перегиб крупных кровеносных сосудов (верхней полой вены и других) -> уменьшение венозного возврата -» снижение сердечного выброса -» нарушение гемодинамики и усугубление гипоксии. →Через 4—6 ч развития пневмоторакса возникает воспалительная реакция плевры, через 2—5 сут плевра утолщается за счёт отёка, что затрудняет расправление лёгкого.
Виды:
· Односторонний: лево-, право-
· Двусторонний
1) Открытый - прямое сообщение между атмосферой и плевральной полостью при нарушении целостности грудной стенки при ранениях и травмах. Поступление воздуха в плевральную полость продолжается до тех пор, пока давление в ней не станет равным атмосферному или не прервется сообщение. (Накладывают окклюзионную повязку – переводят в закрытый – возможно закрытие фибрином и переход в закрытый)
2) Закрытый - прямое сообщение между альвеолами и плевральной полостью при сохраненной целости грудной стенки (в больнице зашивают и отсасывают воздух, восстанавливая отрицательное давление).
3) Клапанный (винтильный) - патологическое сообщение пропускает воздух в плевральную полость только во время вдоха, во время выдоха закрывается и препятствует эвакуации воздуха  давление в плевральной полости может значительно превышать атмосферное
давление в плевральной полости может значительно превышать атмосферное  напряженный пневмоторакс.
напряженный пневмоторакс.  смещение органов средостения, уплощение диафрагмы и компрессии непораженного легкого ( перекручивание аорты (20-30 мин на спасение пациента – перевести в открытый, путем иссечения клапана).
смещение органов средостения, уплощение диафрагмы и компрессии непораженного легкого ( перекручивание аорты (20-30 мин на спасение пациента – перевести в открытый, путем иссечения клапана).
Этиология:
1. Причинами спонтанного пневмоторакса могут быть: буллёзная болезнь лёгких; патология дыхательных путей (ХОБЛ, муковисцидоз, астматический статус); инфекционные заболевания (пневмоцистная пневмония, туберкулёз лёгких); интерстициальные болезни легких (саркоидоз, идиопатический пневмосклероз); заболевания соединительной ткани (ревматоидный артрит, дерматомиозит, склеродермия); злокачественные новообразования; грудной эндометриоз.
2. Травматический пневмоторакс: проникающие ранения грудной клетки, закрытая травма грудной клетки (повреждение отломками сломанных рёбер, травматический разрыв лёгкого).
3. Ятрогенный пневмоторакс: пункция плевральной полости, катетеризация центральной вены, биопсия плевры, трансбронхиальная эндоскопическая биопсия лёгкого, баротравма при искусственной вентиляции лёгких.
Модель – влияние пневмоторакса на внешнее дыхание: после записи исходного дыхания, крысе шприцом вводим по 5 мл воздуха в плевральную полость  закрытый пневмоторакс
закрытый пневмоторакс  давление в плевральной полости положительное, ум. транспульмонального давления
давление в плевральной полости положительное, ум. транспульмонального давления  спадение легких.
спадение легких.

При наличии воздуха в плевральной полости: тахипноэ (до 60 и более в минуту), затем брадипноэ.
Сравнительные механизмы понижения воздушности легких при ателектазе и пневмотораксе:
При пневмотораксе спавшееся легкое колабировало, НО НЕ НАХОДИТСЯ В СОСТОЯНИИ АТЕЛЕКТАЗА (абсолютная безвоздушность легкого, есть перфузия – нет вентиляции, кислород ушел в кровь). Там еще много воздуха, остаточный объем сохранен. При пневмотораксе одного легкого – ателектаз другого.
Механизм лечебного действия пневмоторакса (прорыв каверны у туберкулеза) + патогенез:
Применение закрытого пневмоторакса для лечения кавернозных форм туберкулеза:
1) Вводят воздух в плевральную полость  спадение каверн и опорожнение в бронх
спадение каверн и опорожнение в бронх  больной откашливает
больной откашливает
2) Спавшееся легкое на работает (хорошо для протекания регенераторный пр-в) - отток крови 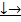 венозная гиперемия. Парциальное давление
венозная гиперемия. Парциальное давление 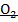
 , скорость крови ↓, снабжение тканей
, скорость крови ↓, снабжение тканей 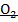 ↓
↓ 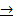 концентрация лекарственных средств
концентрация лекарственных средств  .
. 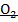
 - хорошо для фибробластов (пролиферация)
- хорошо для фибробластов (пролиферация) 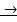 пневмосклероз легкого (плохо).
пневмосклероз легкого (плохо).
3) Диета - высокожировая: Жиры через грудной лимфатический проток идут в легкие через правое сердце – легкие орган липидиереза (место где жиры перерабатываются – до 85% липидов их ЖКТ в легкие через лимф. систему  лимф. грудной проток
лимф. грудной проток  правое сердце
правое сердце  легкие – 40% легким, а остальное дальше идет).
легкие – 40% легким, а остальное дальше идет).
Билет №146. Эмфизема. Этиология и патогенез. Характеристика дыхательной недостаточности при эмфиземе. Ключевое звено патогенеза различных видов эмфиземы. Особенности этиологии и патогенеза генуинной эмфиземы. Эмфизема как компонент хронической обструктивной болезни легких.
Дата добавления: 2019-03-09; просмотров: 780; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
