Механизмы нуклеофильного замещения в галогеналканах
Общая схема реакции:
R-X+ :Y—>R-Y+ :Х
(СН3)2СН-С1 + :ОН- —> (СН3)2СН-ОН + :С1-
Механизм(2ст)
Стадия 1.Алкилгалогенид, отщепляя галоген (электролитическая диссоциация), превращается в карбокатион:
СН3-СН-СН3<,СН3-С-СН3 + СГ
| -------------à|
Clмедленно H
Стадия 2.Кар,окатион взаимодействует с нуклеофилом (донором пары электронов) с образованием конечного продукта:
СН3
|
СНз-С + Н5+-ОН --------à СН3-СН-СН3 + H
| быстро |
HOH
Н+ + С1 ---à НС1
МЕХАНИЗМ РЕАКЦИИ НУКЛЕОФИЛЬНОГО ЗАМЕЩЕНИЯ У ТЕТРАГОНАЛЬНОГО АТОМА УГЛЕРОДА В РЯДУ СПИРТОВ КАК СЛЕДСТВИЕ ПОЛЯРИЗАЦИИ УГЛЕРОД-КИСЛОРОД СВЯЗИ (НА ПРИМЕРЕ ПОЛУЧЕНИЯ ИЗ СПИРТОВ ГАЛОГЕНАЛКАНОВ). РОЛЬ КИСЛОТНОГО КАТАЛИЗА ПРИМЕРЕ ПОЛУЧЕНИЯ ИЗ СПИРТОВ ГАЛОГЕНАЛКАНОВ). РОЛЬ КИСЛОТНОГО КАТАЛИЗА

Механизмы реакций элиминирования Е1,Е2

Реакции окисления спиртовых групп[править | править код]
Гидроксикислоты легко вступают в реакции окисления спиртовых групп, что обуславливает образование оксокислот — альдегидо- и кетокислот. Например, молочная кислота, окисляясь, превращается в пировиноградную:
|
|
|
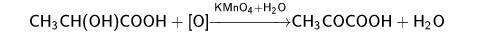
Дегидратация спиртов
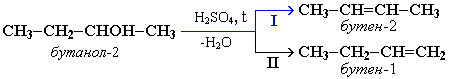
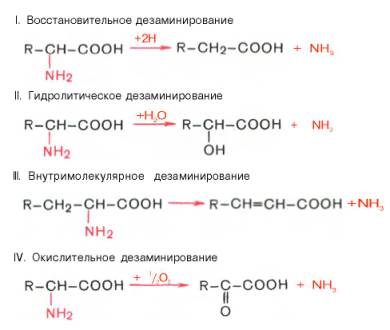
оказано существование 4 типов дезаминирования аминокислот (отщепление аминогруппы). Выделены соответствующие ферментные системы, катализирующие эти реакции, и идентифицированы продукты реакции. Во всех случаях NH2-группа аминокислоты освобождается в виде аммиака.
Реакционные центры КК. Реакции по СН-кислотному центру
Реакционные центры в молекуле карбоновых кислот
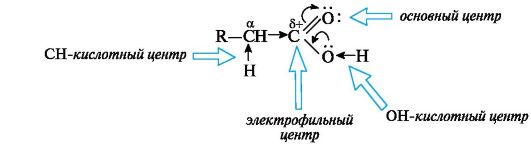
• ОН-кислотный центр, обусловленный сильной поляризацией связи О-Н;
• электрофильный центр - атом углерода карбоксильной группы;
• n- основный центр - атом кислорода карбонильной группы с неподеленной парой электронов;
• слабый СН-кислотный центр, проявляющийся только в производных кислот, так как в самих кислотах имеется несравненно более сильный ОН-кислотный центр.
Механизм реакций нуклеофильного замещения (Sп)
Реакционная способность карбоновых кислот в реакциях нуклеофильного замещения в сравнении с галогенангидридами, ангидридами, тиоэфирами понижена вследствие электронодонорных свойств ОН-группы, уменьшающей электрофильность атома углерода. Для увеличения электрофильности (эффективного положительного заряда) необходимо использовать кислотный катализ. Реакции этерификации карбоновых кислот и гидролиза сложных эфиров протекают в присутствии сильных минеральных кислот как катализаторов. В качестве катализатора часто используют серную кислоту
|
|
|
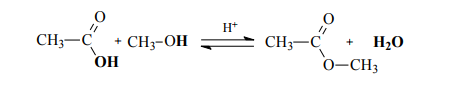
Механизм реакции:
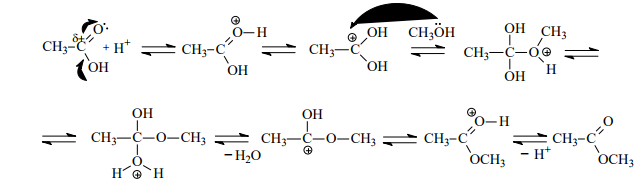
Присоединение протона к основному центру кислоты приводит к образованию карбкатиона - реакционноспособной электрофильной частицы, которая легко подвергается атаке нуклеофилом – молекулой спирта. Образовавшийся оксониевый катион, отщепляя воду, превращается в карбкатион, который регенерирует сопряженную систему путем отщепления протона, что приводит к образованию сложного эфира и возврату катализатора. Ионы водорода катализируют и прямую, и обратную реакции, равновесие реакции можно смещать, используя принцип Ле-Шателье.
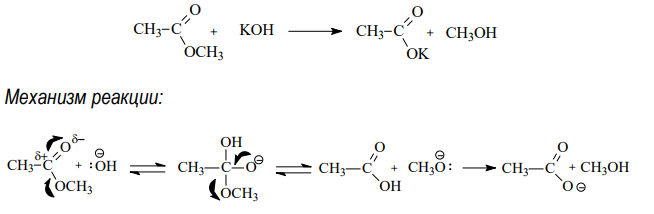
Гидролиз сложных эфиров, катализируемый основаниями, протекает необратимо
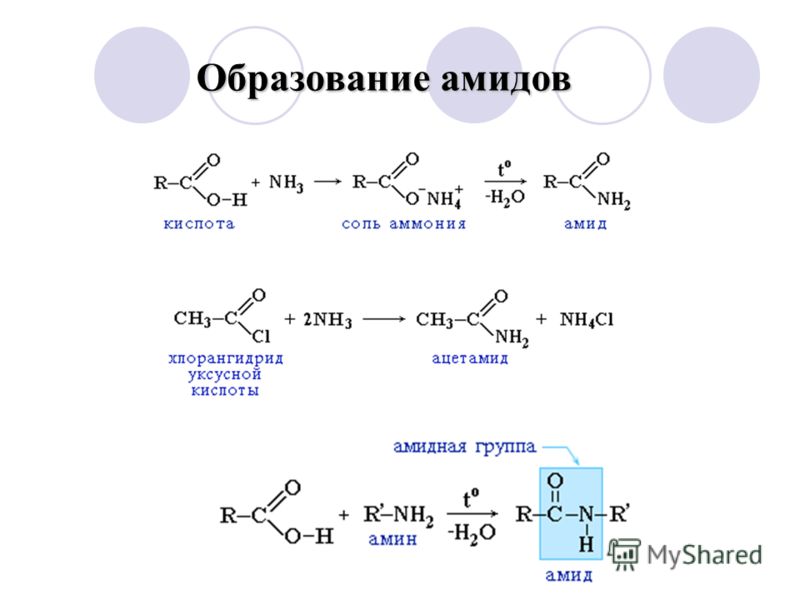
Образование ангидридов
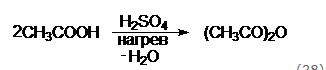
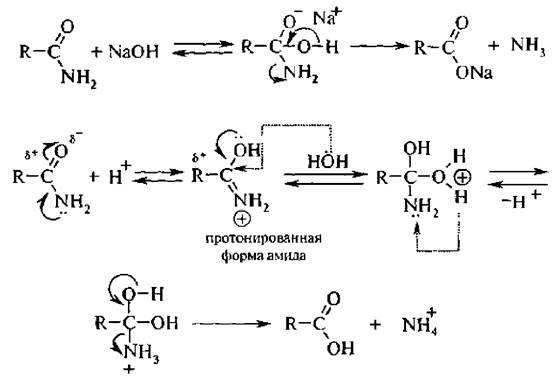
Гидролиз
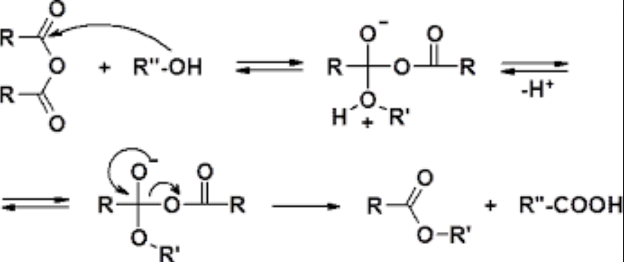
Гидролиз
Ацилирующие реагенты
Ацилирование – это введение в молекулу ацильной группы (остатка карбоновой кислоты):
Ацилирующие агенты: 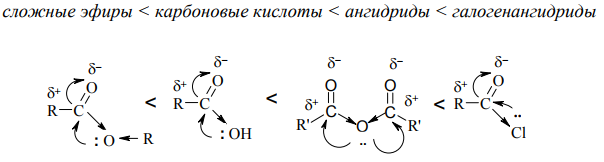
Тиоэфиры
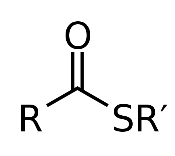
25. Механизм реакции нуклеофильного присоединения( 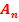 ) к тригональному атому углерода( альдегиды,кетоны) на примере получения полуацеталей, ацеталей. Сравнение реакционной способности альдегидов и кетонов. Циклические ацетали.
) к тригональному атому углерода( альдегиды,кетоны) на примере получения полуацеталей, ацеталей. Сравнение реакционной способности альдегидов и кетонов. Циклические ацетали.
|
|
|
Реакции нуклеофильного присоединения характерны для альдегидов и кетонов
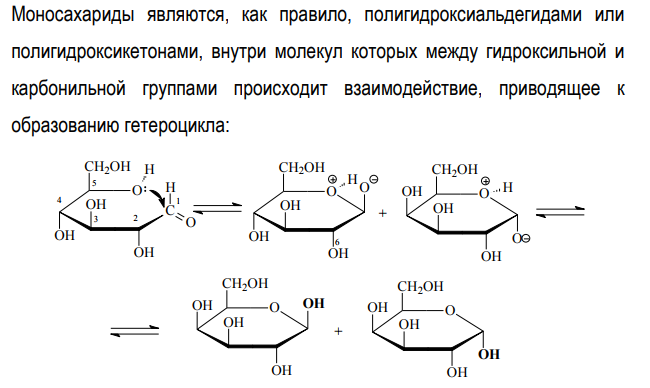
Циклические полуацетали – результат внутримолекулярной реакции АN, которая возможна у гидроксиальдегидов, если гидроксигруппа находится в положении 4 или 5 в углеродной цепи.
Дата добавления: 2018-08-06; просмотров: 1651; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
