Клиническая характеристика стадии ХБП
| Стадия ХБП | клиника | диагностика |
| 1 | нефротический и нефритический синдром, тубулоинтерстициальный синдром, асимптомный мочевой синдром, асимптомные R изменения, нефрогенная артериальная гипертензия | проба Реберга-Тареева, Зимницского, трехстаканная проба, биохимическое исследование сыворотки крови, измерения АД |
| 2 | легкие осложнения | анемия, |
| 3 | умеренные осложнения | артериальная гипертензия, анемия, нередко гиперкалиемия, гипостенурия, глюкозурия, |
| 4 | тяжелые осложнения | анемия, гиперфосфатемия, гиперкальциемия, |
| 5 | уремия, ССЗ | ГЛП, ГЛЖ, КБС, аритмии, КБС ХСН, мозговые инсульты |
Примечание: ХБП – хроническая болезнь почек; R – рентген; АД – артериальное давление; ССЗ – сердечно – сосудистые заболевания; ГЛП – гипертрофия левого предсердия; гипертрофия левого желудочка; КБС – коронарное болезнь сердца; ХСН – хроническая сердечная недостаточность.
Таблица № 16
Диагностика ХБП в зависимости от состояния функции почек и наличия маркеров повреждения
| Маркеры повреждения почек | ||
| СКФ, мл/мин/1,73 м2 | есть | нет |
| более 90 | ХБП | норма |
| 60 – 89 | ХБП | группа риска |
| менее 60 | ХБП | ХБП |
Примечание: ХБП – хроническая болезнь почек; СКФ – скорость клубочковой фильтрации.
В ходе первого обследования пациентов определяется уровень креатинина сыворотки и рассчитывается СКФ по формуле CKD-EPI. Если СКФ < 60 мл/мин/1,73 м 2 , повторить исследование через три месяца или ранее. В случайной порции мочи определяется отношение А/Кр. Если отношение А/Кр>30 мг/г (>3 мг/ммоль), повторить исследование через три месяца или ранее. Если значения СКФ < 60 мл/мин/1,73 м 2 и/или отношение А/Кр>30 мг/г (>3 мг/ммоль) сохраняются, по крайней мере, три месяца диагностируется ХБП и проводится лечение. Если оба исследования соответствуют нормальным значениям, то их следует повторять ежегодно.
|
|
|
Лабораторные маркеры повреждения почек
1.Протеинурия – появление белка в моче. Моча в норме содержит маленькое количество белка. Однако персистирующее увеличение экскреции белка обычно свидетельствует о патологии почек. Типы белка, такие как глобулины низкомолекулярного веса или альбумин, могут зависеть от характера почечного заболевания. Увеличение экскреции глобулинов низкомолекулярного веса является чувствительным маркером некоторых разновидностей тубулоинтерстициальных заболеваний. Повышенная же экскреция альбуминов свидетельствует о ХБП, связанных с СД, гломерулярными патологиями или АГ.
В руководствах НПФ термин «протеинурия» означает увеличение экскреции с мочой альбуминов и других специфических белков. Термин «альбуминурия» применяется исключительно при обнаружении альбумина в моче. Термин «микроальбуминурия» отражает экскрецию альбумина выше нормы, но ниже уровня появления других белков в моче.
|
|
|
Для выявления протеинурии или микроальбуминурии обычно не требуется сбор мочи за определенное время (ночное или за 24 часа) (НПФ шкала R и C)1. По ряду причин произвольный образец мочи (капля) используется для обнаружения протеинурии (НПФ шкала R и О)1. По стандарту на практике может быть использовано обнаружение всех экскретируемых белков и специфичные на альбумины тест полоски.
Если протеинурия при исследовании мочи тест полоской оказывается положительной (на 1+ или более), то ее следует подтвердить количественным измерением белково-креатининового или альбумин-креатининового соотношения в пределах трех месяцев. В случае если в течение недели два или более количественные тесты будут положительными, то диагноцируется персистирующая протеинурия и больной должен быть подвергнут более детальному обследованию по подозрению на ХБП. (см. рекомендацию 2 в первой части3).
У взрослых с ХБП протеинурия должна мониторироваться с помощью альбумин-креатининового соотношения (НПФ градация R и O). Использование в целом белково-креатининового соотношения предпочтительно, если величина альбумин-креатининового соотношения высокая (от 500 до 1,000 т.е. норма от 0,5 до 1 г креатинина).
|
|
|
Золотыми стандартами измерений клиренса креатинина и количества протеинурии являются соответствующие исследования, подкрепленные полноценным сбором мочи за сутки. Возможно, и измерение отношение белка или альбумина к креатинину в случайной порции мочи. Эти отношения определяются концентрацией белка в моче, связанной с гидратацией и более удобны, чем сбор мочи за определенное время. Есть доказательства, которые указывают, что отношение белка или альбумина к креатинину в произвольных образцах мочи обеспечивают аккуратную оценку скорости экскреции белка1, 2. У большинства больных произвольно собранные порции мочи могут быть использованы для обнаружения и мониторирования протеинурии. Для таких оценок излишен сбор мочи за определенное время (за ночь или за 24 часа).
| Пациенты без признаков патологии почек |
| Нет риска патологии почек |
| Есть риск патологии почек |
| Стандартная тест полоска |
| Полоска специфичная на альбумин |
| ≥ 1+ |
| Отрицательная или следы белка |
| Отрицательная |
| > 200 мг на 1 г |
| ≤ 200 мг на 1 г |
| Общее белково-креатининовое соотношение |
| Альбумин-креа-тининовое соотношение |
| Положительная |
| Повторный периодический контроль во время медосмотров |
| ≤ 30 мг на 1 г |
| > 30 мг на 1 г |
| Постановка диагноза |
| Лечение |
| Консультация |
| Рис. 1. Оценка протеинурии |
|
|
|
Измерение альбумина является достаточно дорогим и технически сложным, чем выявление общего белка. Поэтому подсчет белково-креатининового соотношения находит более широкое применение для мониторинга, особенно в случаях, где обнаруживается высокая альбумин-креатининовая пропорция.
Предлагается следующий алгоритм оценки протеинурии среди пациентов с повышенным риском заболеваний почек и относительно здоровыми людьми без такого риска (Рис. 1)1.
У взрослых пациентов, имеющих риск, анализ начинается с теста случайной капли мочи с помощью специфичной полоски на альбумин. В этих случаях можно использовать и тест на альбумин-креатининовое соотношение. Если тест положителен, то следует провести количественное определение белка в моче. Только при обнаружении персистирования протеинурии у больного диагносцируется ХБП. Данное руководство полезно для семейных врачей, поскольку исключается необходимость в количественном измерении протеинурии в суточной моче. Предложение проводить анализ скорее экскреции альбумина, чем появления в моче всех белков, отличается от общепринятой клинической практики. Кроме того, следует заметить, что оценка альбуминурии не доступна для всех клинических лабораторий.
· Высокая протеинурия потеря белка с мочой ≥ 0,5 г/сутки
- Массивная протеинурия потеря белка с мочой ≥3,5 г/сутки
Таблица № 17
Градации альбуминурии
|
Индекс |
Название | Уровень альбумина | |
| Альбумин в суточной моче, мг/сут | Альбумин/креатинин в разовой порции мочи, мг/г | ||
| А0 | Оптимальный уровень | < 10 | < 10 |
| А1 | Умеренное повышение | 10-29 | 10-29 |
| А2 | Высокая | 30-299 | 30-299 |
| А3 | Очень высокая | 300-1999 | 300-1999 |
| А4 | Нефротическая | ≥2000 | ≥2000 |
Для правильного использования анализа на протеинурию и трактовки его результатов необходимо учитывать ряд методологических условий. На сегодняшний день применяются три группы методов определения белка в моче:
- турбидиметрические методы
- метод «сухой химии»
- фотометрические методы
Определения альбуминурии в разовом анализе мочи (альбумин, мг/креатинин, г); нормальная менее 30 г; повышенная более 30 г (ADA, 2014).
Нормоальбуминурия – экскреция альбумина с мочой (утренняя) менее 20 мкг в мин.
Микроальбуминурия – экскреция альбумина с мочой (утренняя) от 19 – 199 мкг в мин.
Исследование утренней пробы мочи дает более воспроизводимые результаты, чем случайной порции, взятой в течение суток. Внепочечные факторы, влияют на уровень протеинурии/альбуминурии. Он повышается после интенсивных физических нагрузок, у лихорадящих больных, при злоупотреблении белковой пищей.
Креатинин сыворотки крови.
Креатинин представляет собой ангидрид креатина, образующийся в организме в результате отщепления остатка фосфорной кислоты от креатинфосфата; является одним из конечных продуктов азотистого обмена и постоянной составной частью мочи. Креатинина образуется в мышечной ткани. Средняя скорость образования креатинина выше у мужчин, у молодых, у лиц негроидной расы. Это приводит к различиям в концентрациях креатинина сыворотки в зависимости от возраста, пола и расы. Мышечное истощение сопровождается снижением образования креатинина, что связано с более низкой концентрацией креатинина сыворотки, чем можно было бы ожидать по уровню СКФ, у пациентов с белково-энергетической недостаточностью при ХБП. На образование креатинина влияет также употребление мяса, т. к. в процессе его приготовления доля креатина переходит в креатинина. Поэтому у пациентов на низкобелковой (вегетарианской) диете креатинина сыворотки ниже, чем можно было бы ожидать, исходя из уровня СКФ. Креатинин свободно фильтруется в клубочках, но также секретируется в проксимальных канальцах. Следовательно, количество креатинина экскретированного в мочу, является суммой профильтрованного и секретированного креатинина. Клиренс креатинина систематически завышает СКФ. Это завышение составляет ~ 10-40 % у здоровых лиц, однако выше и более непредсказуемо у пациентов с ХБП. При нормальном сывороточном креатинина возможны значительные колебания СКФ, особенно у пожилых. По мере старения уменьшаются мышечная масса и клиренс креатинина. При этом сывороточный уровень остается неизменным, что не означает неизмененную функцию почки. Таким образом, повышенный уровень креатинина сыворотки не является чувствительным показателем замедления СКФ. Только у 60 % больных ХБП со сниженной СКФ определяют повышенный креатинина сыворотки крови.
Скорость клубочковой фильтрации является лучшим общим индикатором функции почек. СКФ должна оцениваться с помощью уравнений, учитывающих концентрацию креатинина сыворотки крови и некоторых или всех следующих переменных: возраста, пола, расы, и размеров туловища. Уравнения, полученные при изучении модификации диеты при почечных заболеваниях MDRD или Cockroft-Gault, отличаются удобством для расчета СКФ у взрослых больных (табл. 1). В рекомендациях НПФ подчеркивается, что судить только по концентрации креатинина сыворотки об уровне функции почек не является оптимальной.
В дополнение к сообщению о концентрации креатинина в сыворотке клиническая лаборатория обязана дать информацию о методе оценки СКФ.
Таблица № 18
Уравнения для подсчета ожидаемой СКФ у взрослых по концентрации креатинина сыворотки крови*
Аббревиатура уравнения из MDRD изучения
СКФ (мл/мин на 1.73 м2) = 186 х (SCr)-1.154 х (возраст)-0.203 х (0.742 если женщина) х (1.210 если негр)
Уравнение Cockroft-Gault:
CCr (мл/мин) = 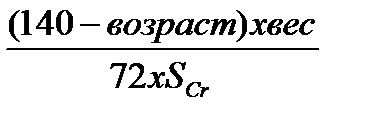 х (0.85 если женщина) х (0.85 если женщина)
|
Примечание: СКФ – скорость клубочковой фильтрации, MDRD – Modification of Diet in Renal Disease, SCr – концентрация креатинина сыворотки крови, CCr – клиренс креатинина, * - в каждом уравнении SCr выражается в мг на децилитр, возраст в годах и вес в килограммах. Информация получена из 4-6 рефератов
В большинстве случаев при измерении клиренса креатинина используется сбор мочи за определенное время (нр., 24 часа), что по надежности не превышает подсчет СКФ по уравнениям предсказания. Однако определение СКФ на базе суточного сбора мочи полезно у больных, находящихся на особой диете (вегетарианской, с добавками креатина) или с измененной мышечной массой (ампутация, потерявших мышцы и недостаток питания), при оценке диеты, состояния питания и для выяснения необходимости подключения диализа.
В клинической практике, СКФ обычно оценивается по клиренсу креатинина или концентрации креатинина в сыворотке. Для измерения клиренса креатинина требуется сбор мочи за определенное время, что является неудобным для пациента, а также часто неаккуратным. Величина концентрации креатинина сыворотки зависит от других факторов, чем показатель СКФ, а именно секреции, генерации и экстраренальной экскреции креатинина. Следовательно, возможно ее относительно широкое колебание персонально у пациента.
Оценка СКФ по концентрации креатинина сыворотки может быть улучшена при использовании уравнений предсказания, если принимать в расчет возраст, пол, расу и размеры тела (например, уравнения, представленные в табл. 18). У больных со СКФ ниже 90 мл/мин на 1,73 м², уравнение, полученное, в MDRD исследовании кажется более точным по сравнению с уравнением Cockroft – Gault, но возникает необходимость в более сложных расчетах уровня креатинина сыворотки и СКФ может снижаться почти на половину от нормального уровня даже до повышения концентрации креатинина сыворотки выше верхних границ нормы. Подобная ситуация со снижением СКФ при нормальной концентрации креатинина сыворотки крови встречается часто у пожилых больных, у которых, падение СКФ обычно обусловлено снижением продукции креатинина.
Табл. 19 показывает колебания уровня креатинина сыворотки при СКФ 60 мл/мин в зависимости от возраста, пола и расы. Здесь следует подчеркнуть, что определение ХБП НПФ включает уровень СКФ в мл/мин на 1,73 м² за три месяца и более (см табл. 2 в первой части).
Есть убедительные доказательства, что расчет клиренса креатинина после суточного сбора мочи не превосходит по информативности уравнения предсказания, которые базируются на уровне креатинина и других характеристиках больного. Следовательно, есть возможность только взятием сыворотки крови получить результат, чем подвергать больного неудобствам со сбором мочи в течение суток и ее доставкой в лабораторию. Более того, моча может быть собрана не полностью, даже если объем кажется достаточным, что приводит к некорректному подсчету клиренса креатинина и соответственно к ошибочному лечению больного. С другой стороны, если количество мочи за 24 часа будет меньше, чем есть на самом деле лабораторные данные будут искажены, а время и усилия будут затрачены впустую.
Маловероятно, что СКФ станет стандартной мерой, используемой врачами до тех пор, пока клинические лаборатории не начнут широко давать величину СКФ. Для подсчета показателя СКФ лаборатория нуждается в дополнительных данных, которые не всегда сообщаются (например, вес, раса); Поэтому если дополнительные данные не станут частью требований, врачи не смогут подсчитать СКФ. Пациенты также могут получать величину СКФ, если она станет постоянной частью лабораторной анкеты.
Кооперация с местной клинической лабораторией важна и по другим соображениям. Так, различия калибровок среди лабораторий при оценке сывороточного креатинина сопровождается ошибочными результатами по значениям СКФ более чем на 20%. Это особенно существенно у больных с близкой к норме концентрацией креатинина сыворотки. Поэтому при подсчете СКФ по уравнениям предсказания следует принимать в расчет особенности калибровки среди местных лабораторий и сопоставлять их результаты с данными референс лаборатории.
Таблица № 19
Уровни креатинина сыворотки крови по данным литературы при СКФ 60 мл/мин на 1,73 м², рассчитанные двумя уравнениями предсказания.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Примечание: СКФ = скорость клубочковой фильтрации; MDRD = Modification of Diet in Renal Disease. *-Расчет в этой таблице проведена для больного с весом 72 кг и на площадь поверхности тела of 1.73 m2. †-Сокращения уравнений MDRD исследования и Cockcroft-Gault показаны в табл. 2. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Практическое применение установленной СКФ стало достаточно удобным с появлением классификации ХБП, что позволяет регулировать дозы лекарств по уровню почечной функции.
Другие маркеры ХБП.
Помимо протеинурии, маркерами повреждения почек являются изменения в осадке мочи и в данных инструментальных исследований. При некоторых типах ХБП обнаруживаются множество маркеров. Для других форм ХБП следует искать новые маркеры для идентификации почечной патологии, которые были бы информативными еще до снижения СКФ.
Исследование осадка мочи или тест-полосками на эритроциты и лейкоциты должны проводиться у больных с ХБП и у пациентов, у которых есть факторы риска к болезни. Эти пациенты должны быть обследованы и инструментальными методами.
Многообещающими представляются некоторые новые мочевые маркеры, а именно канальцевые и низкомолекулярного веса белки, специфические моноядерные клетки. Однако в настоящее время они не должны использоваться в клинике (НПФ градация С)1,2.
Патологический альбумин мочи или экскреция общего белка являются высоко чувствительными маркерами гломерулярных заболеваний, в том числе диабетических поражений почек. Исследование мочевого осадка, инструментальное изучение почек и особенности клинических проявлений также могут выявлять характер почечной болезни.
Анализ осадка мочи, проведенный совместно с надежной оценкой протеинурии особенно полезен для обнаружения ХБП и идентификации его типа. Мочевые тест полоски содержат реагенты, которые чувствительны для обнаружения эритроцитов (гемоглобина), лейкоцитов (лейкоцитарных эстераз) и бактерий (нитритов). Полоски не могут выявлять эпителиальные клетки канальцев, жиры, цилиндры, кристаллы, грибки или паразиты. Решение о проведении исследований осадка мочи или теста с полоской зависит от рассматриваемого типа заболевания почек.
По результатам инструментальных исследований можно предположительно установить причину ХБП, таких как патология артерий или урологических нарушений. Поэтому они рекомендуются всем больным с ХБП и пациентам, у которых отмечается риск ХБП, например стеноз почечной артерии, серьезное системное осложнение инфекции мочевого тракта, мочекаменная болезнь или обструкция, везикоуретеральный рефлюкс или поликистоз почек. Ультрасонография является особенно полезной для обнаружения некоторых из них и при этом не требуется подвергать больного облучению или воздействию контрастных веществ.
В качестве альтернативного маркера функционального состояния почек и сердечно-сосудистого риска в последние годы рассматривается цистатин С, белок с низкой молекулярной массой, ингибитор протеаз. Цистатин С характеризуется свободной клубочковой фильтрацией, не подвергается канальцевой секреции. Разрабатываются формулы для расчета СКФ на основании уровня цистатина С. В ряде исследований показана эквивалентность цистатина С и креатинина в оценке функции почек. Также приводились данные, свидетельствующие о превосходстве цистатина С в отношении оценки СКФ, особенно при нормальной и незначительно сниженной СКФ. У пожилых больных цистатин С оказался лучшим предиктором развития ХБП по сравнению с уровнем креатинина. Однако образование цистатина С также не является строго постоянным, а среди факторов, влияющих на его концентрацию, указывают возраст, пол, рост, вес, курение, сывороточный уровень С-реактивного белка, терапию стероидами, ревматоидный артрит. Следовательно, в настоящее время нельзя считать доказанным преимущества определения цистатина С для оценки СКФ.
Дата добавления: 2018-05-12; просмотров: 172; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
