Вплив антисиметричності хвильових функцій на стаціонарні стани атому Не
Ще раз розглянемо вплив взаємодії електронів на енергії стаціонарних станів атому гелію з урахуванням антисиметричності хвильових функцій його електронів. Для цього один із його електронів залишимо у стані 1s, а другий може займати стани з іншими квантовими числами. Хвильові функції, у виразі (12.23), представимо у такому вигляді:
 . (12.31)
. (12.31)
Тут, як і раніше, індекси С і А означають симетричність і антисиметричність просторової частини хвильових функцій відносно перестановки1-го і 2-го електронів. Множники  і
і  характеризують спінові характеристики, використання яких робить функції
характеризують спінові характеристики, використання яких робить функції 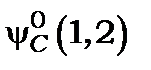 і
і  завжди антисиметричними. Після підстановки (12.31) у вираз (12.10) для внеску енергії взаємодії електронів до енергії стаціонарного стану отримаємо:
завжди антисиметричними. Після підстановки (12.31) у вираз (12.10) для внеску енергії взаємодії електронів до енергії стаціонарного стану отримаємо:
 , 12.32)
, 12.32)
де  - кулонівський інтеграл, який виникає внаслідок кулонівської взаємодії електронів між собою у незмішаному стані, і
- кулонівський інтеграл, який виникає внаслідок кулонівської взаємодії електронів між собою у незмішаному стані, і  – обмінний інтеграл, який характеризує кулонівську взаємодію електронів у змішаному стані:
– обмінний інтеграл, який характеризує кулонівську взаємодію електронів у змішаному стані:
 . (12.33)
. (12.33)
Величини  ,
,  і
і  позитивні, а інтеграл
позитивні, а інтеграл  також позитивний при використанні хвильових функцій атому водню. Отже, із виразу (12.32) видно, що
також позитивний при використанні хвильових функцій атому водню. Отже, із виразу (12.32) видно, що
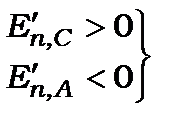 . (12.34)
. (12.34)
| Рис.12.3. Схема найнижчих термів атому гелію.
|
Вибір симетричної просторової частини хвильової функції означає, що спінова її частина повинна змінювати знак при перестановці електронів, що можливо коли спіни обох електронів антипаралельні, тобто у синглетному або парастані. Вибір антисиметричної просторової частини хвильової функції можливий при паралельних спінах, тобто у триплетному або ортостані. Отже, аналіз виразів (12.32), (12.33) і (12.34) вказує, що енергетичні рівні у парагелію мають менші енергії по відношенню до відповідних рівнів ортогелію, як це показано на схематичному рис.12.3. Найнижчим енергетичним рівнем буде синглетний стан па
|
|
|
рагелію  . Причиною появи різниці в положеннях синглетних та триплетних станів в атомі гелію є обмінна енергія
. Причиною появи різниці в положеннях синглетних та триплетних станів в атомі гелію є обмінна енергія 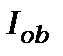 , яка не має класичного аналогу. Вона з’являється внаслідок перекриття електронних хвильових функцій, тобто начебто електрон як би одночасно знаходиться як у стані
, яка не має класичного аналогу. Вона з’являється внаслідок перекриття електронних хвильових функцій, тобто начебто електрон як би одночасно знаходиться як у стані  , так і в стані
, так і в стані  . Коли перекриття хвильових функції відсутнє, то обмінна енергія не виникає. Поява триплетних рівнів у стані
. Коли перекриття хвильових функції відсутнє, то обмінна енергія не виникає. Поява триплетних рівнів у стані  виникає внаслідок спін-орбітальної взаємодії, яка значно менша за обмінну енергію. Як видно із розгляду, схема термів збігається зі схемою термів, яку дає векторна модель атома у попередній главі. Однак, на відміну від векторної моделі, яка визначає лише структуру і систематику термів, метод збурень дозволяє отримувати значення відповідних енергій стаціонарних станів.
виникає внаслідок спін-орбітальної взаємодії, яка значно менша за обмінну енергію. Як видно із розгляду, схема термів збігається зі схемою термів, яку дає векторна модель атома у попередній главі. Однак, на відміну від векторної моделі, яка визначає лише структуру і систематику термів, метод збурень дозволяє отримувати значення відповідних енергій стаціонарних станів.
|
|
|
Висновки
1. Стаціонарні стани багатоелектронних атомів можна знаходити за допомогою теорії збурень. Вона полягає в тому, що хвильові функції складного атома можна отримувати шляхом змішування інших хвильових функцій простих атомів у відповідності до формули (12.5) і (12.12). Умовою застосовності стаціонарної теорії збурень є умова  , тобто матричні елементи оператора збурення повинні бути малими в порівнянні з різницею енергій енергетичних рівнів не збуреної задачі, коли
, тобто матричні елементи оператора збурення повинні бути малими в порівнянні з різницею енергій енергетичних рівнів не збуреної задачі, коли  , а також у випадку вироджених рівнів.
, а також у випадку вироджених рівнів.
2. Теорія збурень дає «рецепт» такого змішування, що дозволяє обчислювати додаткові члени, котрі необхідно додати до енергії п-стану одноелектронного атома, щоб отримати енергію складного атома (формула (12.10))  .
.
3. Коефіцієнт  , що відповідає кожній із орбіталей, що змішуються, визначається відношенням енергії збурення до різниці енергій (формула (12.14)). Внесок кожної із орбіталей в суміш хвильових функцій простих атомів визначається квадратом коефіцієнта змішування
, що відповідає кожній із орбіталей, що змішуються, визначається відношенням енергії збурення до різниці енергій (формула (12.14)). Внесок кожної із орбіталей в суміш хвильових функцій простих атомів визначається квадратом коефіцієнта змішування  . Тому в суміші основну роль будуть грати ті орбіталі, котрі близькі до основної орбіталі, тобто ті, у яких
. Тому в суміші основну роль будуть грати ті орбіталі, котрі близькі до основної орбіталі, тобто ті, у яких 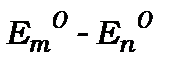 найменші. Таким чином, якщо збурення велике (
найменші. Таким чином, якщо збурення велике (  - величина не дуже мала,), то можливе сильне змішування станів і теорія збурення першого порядку стає недостатньою для отримання адекватних результатів.
- величина не дуже мала,), то можливе сильне змішування станів і теорія збурення першого порядку стає недостатньою для отримання адекватних результатів.
|
|
|
4. Обмінне виродження не узгоджується з принципом тотожності однакових частинок. Це протиріччя усувається за допомогою принципу виключення або заборони Паулі. Згідно принципу виключення частинки з напівцілим спіном - ферміони описуються антисиметричними хвильовими функціями відносно перестановки місцями ферміонів. Або два ферміони не можуть знаходитись в одному і тому ж квантовому стані, тобто не може існувати двох ферміонів (електронів), всі квантові числа яких однакові.
5. Квантовий обмін ферміонів між різними станами призводить до появи обмінної енергії, котра є кулонівською енергією в умовах квантового обміну. Знак обмінної енергії визначається орієнтацією спінів, а її величина такого порядку, як і кулонівська енергія в полі ядра, тобто вона значно більша за енергію взаємодії магнітних моментів.
Дата добавления: 2018-05-09; просмотров: 446; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
