Глава 11. ВЕКТОРНА МОДЕЛЬ АТОМА
Векторна модель атома. Типи зв’язку
Визначення електронних станів багатоелектронних атомів - дуже складна задача. Тому на практиці їх аналіз здійснюють за допомогою наближених методів, наприклад, векторної моделі атома, яка дозволяє систематизувати квантові стани. Вихідним її положенням є те, що енергія електрона в складному атомі визначається електронною конфігурацією - розподілом електронів між наявними орбіталями (наприклад, електронна конфігурація атома водню є  , гелію -
, гелію - 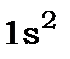 , літію -
, літію -  , тощо) і комбінацією можливих спінових і орбітальних внесків, що призводять до повного кутового моменту атома. Електронна конфігурація знаходиться за допомогою принципу Паулі, згідно якого в електронному стані з чотирма квантовими числами (наприклад,
, тощо) і комбінацією можливих спінових і орбітальних внесків, що призводять до повного кутового моменту атома. Електронна конфігурація знаходиться за допомогою принципу Паулі, згідно якого в електронному стані з чотирма квантовими числами (наприклад,  або
або  ) може знаходитись тільки один електрон (глава 12, §12.3). Терми позначають через сумарні кутові моменти, які дає векторна модель. Оскільки в основне рівняння кутових моментів не входить потенціал
) може знаходитись тільки один електрон (глава 12, §12.3). Терми позначають через сумарні кутові моменти, які дає векторна модель. Оскільки в основне рівняння кутових моментів не входить потенціал 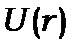 , то це значно спрощує аналіз багатоелектронних атомів. Визначення сумарного (повного) вектора кутового моменту (моменту кількості руху) зводиться у векторній моделі до алгебраїчного складання квантових чисел, що характеризують вектори кутових моментів електронів. Отже, у векторній моделі замість розв’язку складної задачі знаходження енергетичних рівнів атомів здійснюються класифікація або систематизація квантових станів. Вона полягає у знаходженні відповідних квантових чисел складної системи за допомогою комбінаторики квантових чисел більш простих (одноелектронних) систем і визначенні набору енергетичних рівнів, які належать одному терму, тобто мультиплетності термів.
, то це значно спрощує аналіз багатоелектронних атомів. Визначення сумарного (повного) вектора кутового моменту (моменту кількості руху) зводиться у векторній моделі до алгебраїчного складання квантових чисел, що характеризують вектори кутових моментів електронів. Отже, у векторній моделі замість розв’язку складної задачі знаходження енергетичних рівнів атомів здійснюються класифікація або систематизація квантових станів. Вона полягає у знаходженні відповідних квантових чисел складної системи за допомогою комбінаторики квантових чисел більш простих (одноелектронних) систем і визначенні набору енергетичних рівнів, які належать одному терму, тобто мультиплетності термів.
|
|
|
Ця задача спрощується ще й тому, що електрони всіх заповнених оболонок, крім валентної, мають нульовий кутовий момент  і, замість розгляду внесків усіх
і, замість розгляду внесків усіх  електронів, можна обмежитись розглядом лише валентних електронів. Однак залишається складність, зв’язана з вибором послідовності складання кутових моментів, яка залежить від інтенсивності взаємодії моментів між собою. Для спрощення складання кутових моментів валентних електронів прийнято розрізняти два граничних випадки моделей зв’язку: нормального (
електронів, можна обмежитись розглядом лише валентних електронів. Однак залишається складність, зв’язана з вибором послідовності складання кутових моментів, яка залежить від інтенсивності взаємодії моментів між собою. Для спрощення складання кутових моментів валентних електронів прийнято розрізняти два граничних випадки моделей зв’язку: нормального (  або Рассел-Саундеровського) та
або Рассел-Саундеровського) та  зв’язку.
зв’язку.
Нормальним називаєтьсязв’язок, коли енергії взаємодії орбітальних  і спінових моментів (
і спінових моментів (  ) кількості руху, в основі яких лежить електростатична квантова взаємодія, більші за енергію спін-орбітальної взаємодії (
) кількості руху, в основі яких лежить електростатична квантова взаємодія, більші за енергію спін-орбітальної взаємодії ( 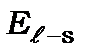 ), магнітна взаємодія якої згідно (9.31) пропорційна квадрату сталої тонкої структури,
), магнітна взаємодія якої згідно (9.31) пропорційна квадрату сталої тонкої структури,
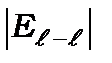 та
та  . (11.1)
. (11.1)
 зв’язком називається випадок, коли енергії орбітальної (
зв’язком називається випадок, коли енергії орбітальної (  ) та спін-спінової (
) та спін-спінової (  ) взаємодій менші за енергію спін-орбітальної взаємодії (
) взаємодій менші за енергію спін-орбітальної взаємодії (  )
)
|
|
|
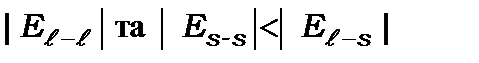 (11.2)
(11.2)
Жодна із розглянутих моделей не дає точного уявлення про справжній стан, тому що завжди існує внутрішня конкуренція між різними типами взаємодій. Навіть в одному атомі різні електрони взаємодіють за різними схемами. Але для легких атомів, у яких незначна спін-орбітальна взаємодія, нормальна (Рассел-Саундерса) модель дозволяє описувати поведінку валентних електронів. У важких атомів, здебільшого, переважає  зв¢язок, бо у них суттєво збільшується спін-орбітальна взаємодія. Взагалі векторна модель відіграє допоміжну роль мнемонічного правила.
зв¢язок, бо у них суттєво збільшується спін-орбітальна взаємодія. Взагалі векторна модель відіграє допоміжну роль мнемонічного правила.
Дата добавления: 2018-05-09; просмотров: 545; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
