Определение активности БЭТТА-амилазы солода фотоколориметрическим методом
Цель работы:освоить методику определения активности β-амилазы солода фотоколориметрически.
Общие положения
Сущность метода. В основе данного метода лежит определение скорости ферментативной реакции гидролиза крахмала по количеству образовавшихся редуцирующих углеводов, которые определяют с помощью колориметрической реакции сахаров с 3,5-динитросалициловой кислотой. Реакция протекает в щелочной среде при нагревании в кипящей водяной бане. Динитросалициловая кислота восстанавливается сахарами в 3-амино-5-нитросалициловую кислоту, которая окрашивает раствор в яркий желто-оранжевый цвет.
Реакция идет по следующему уравнению:
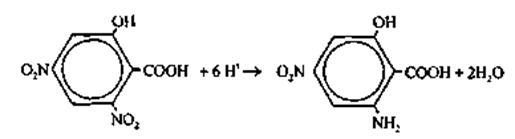
По интенсивности окраски, полученной при реакции раствора, определяют содержание углеводов. Расчет ведут по мальтозе.
Поскольку оптическая плотность раствора прямо пропорциональна количеству образовавшихся при ферментативной реакции углеводов, строят график и находят число единиц активности осахаривающих ферментов, взятых для этой реакции.
Зависимость количества образовавшихся редуцирующих углеводов в процессе гидролиза крахмала от количества введенных в реакцию единиц ферментов различна вследствие специфичности ферментного комплекса материалов различного происхождения. В связи с этим для грибных материалов и солода составлены различные специальные графики и уравнения, и этими уравнениями можно повседневно пользоваться при анализе данных продуктов.
|
|
|
За единицу осахаривающей активности ОСк.д. принимают такое количество фермента, которое катализирует превращение 1 г крахмала за 60 мин при температуре 30° С и оптимальном рН в редуцирующие углеводы, составляющие 20% от количества взятого на ферментативную реакцию крахмала. Осахаривающая активность характеризуется числом единиц фермента в 1 г или 100 см3 исследуемого материала.
Аппаратура и реактивы: Фотоэлектроколориметр; ультратермостат или водяная баня; термометр; пробирки, пипетки, стеклянные палочки; мерные цилиндры; 1 %-ный раствор ДНСК; фосфатный буферный раствор с рН 4,8-4,9; дистиллированная вода.
Приготовление фосфатного буферного раствора с рН 4,8-4,9. см. лабораторную работу № 6.
Приготовление раствора фермента. Солод измельчают, отбирают среднюю пробу. Навеску солода 5 г заливают 10 см3 фосфатного буфера с рН 4,8-4,9 и 90 см3 дистиллированной воды. Полученную суспензию для полного извлечения фермента выдерживают в течение 60 мин в термостате с температурой 30°С, периодически перемешивая стеклянной палочкой. Затем суспензию фильтруют. Для проведения ферментативной реакции используют рабочий раствор, который готовят из основного путем разбавления последнего (таблица 2).
|
|
|
Порядок выполнения работы
Для проведения реакции в две пробирки наливают по 10 см3 субстрата и ставят их в ультратермостат с постоянной температурой 30±0,2° С и выдерживают 5-10 мин. Затем в пробирки наливают по 5 см3 рабочих растворов фермента, нагретых до той же температуры (испытуемая проба). В контрольную пробу вливают инактивированный 15-минутным кипячением рабочий раствор фермента той же концентрации. Смеси быстро перемешивают и выдерживают в ультратермостате в течение 10 мин.
Затем пробирки с испытуемой и контрольной жидкостью вынимают из термостата, содержимое перемешивают, отбирают из него по 1 см3 и переносят в пробирки с предварительно налитыми туда 4,5 см3 дистиллированной воды и 2,5 см3 раствора ДНСК, которая прерывает действие фермента. Пробирки с содержимым выдерживают 10 мин в кипящей водяной бане. В это время происходит колориметрическая реакция, и растворы приобретают желто-оранжевый цвет различной интенсивности в зависимости от количества редуцирующих углеводов, образовавшихся в гидролизате. Затем растворы охлаждают и определяют их оптическую плотность на фотоэлектроколо-риметре, применяя кюветы с толщиной поглощающего слоя 5 мм и светофильтр с длиной волны 536 нм или близкой к ней. Колориметрирование проводят по инструкции, приложенной к каждому прибору.
|
|
|
Для обеспечения точности анализа необходимо, чтобы полученные значения оптических плотностей находились в пределах 0,150-0,750. Выше и ниже этих значений погрешность анализа за счет прибора увеличивается. Наиболее точные данные получаются тогда, когда значение оптической плотности составляет 0,430-0,460. Если показания оптической плотности не укладываются в пределы 0,150-0,750, анализ повторяют. Для приготовления рабочего раствора берут больше или меньше основного раствора для разбавления. Если полученные данные укладываются в указанные пределы, их используют для расчета осахаривающей активности.
Осахаривающую активность определяют по уравнениям, подставляя в них оптическую плотность раствора и количество препарата, взятого на анализ:
ОСк.д = 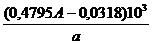 ,
,
где А - оптическая плотность раствора; а - количество солода, взятое на реакцию, мг.
Запись в лабораторном журнале производится по следующей форме:
| Наименование показателя | 1 повторность | 2 повторность | Среднее значение |
| Влажность солода, % | |||
| ОС солода предполагаемая, ед./г | |||
| Оптическая плотность раствора (А) | |||
| Осахаривающая активность солода (ОС), ед./г |
Пример. Определить ОСкд ячменного солода. Готовят вытяжку: 5 г солода на 100 см3 дистиллированной воды с фосфатным буфером. Для приготовления рабочего раствора отбирают 2 см3 основного раствора, объем которого доводят до 100 см3 дистиллированной водой. В 5 см3 такого раствора содержится 5 мг солода (а = 5 мг). После анализа получают раствор, оптическая плотность которого равна 0,420. Подставляя найденные величины в уравнение, рассчитывают осахаривающую активность солода:
|
|
|
ОСк.д = 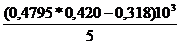 = 33,92 ед./г.
= 33,92 ед./г.
Вопросы для самоконтроля знаний
1. В чем заключается сущность метода определения осахаривающей активности солода фотоколориметрическим методом?
2. Чем характеризуется осахаривающая активность?
3. По какому продукту реакции проводят расчет осахаривающей активности ферментов солода?
Лабораторная работа №8
Дата добавления: 2018-04-05; просмотров: 1742; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
