Фишер формуласы Колли-Толленсу формуласы 19 страница
Ақуыздың екінші реттік құрылымы пептидті байланыстар тобының сутекпен өзара әрекеттесу сутектік байланыс түзу қабілетіне негізделеді: C=O….НN. Осы сәтте пептид сутекті байланыстың максималды санын түзу арқылы конформацияға ие болуға ұмтылады. Алайда пептидті байланыс қос байланысқа тән сипатқа ие болғандықтан және осы байланыстың айналасында айналу қиын болуына сәйкес, мұндай байланыстың түзілу мүмкіндігі шектеледі. Сондықтан пептидті тізбек ретсіз емес, қатаң түрде ретті конформацияға ие болады (сурет – 7.4). Полипептидті тізбектің кеңістікте орналасуының бірнеше әдісі белгілі:
1) α – оралым – бір аминқышқылы қалдығының NH – тобы және осы қалдықтан бастап рет бойынша төртінші тұрған қалдықтың СО – тобы арасында тізбек ішілік сутектік байланыс арқылы түзіледі (сурет – 7.4А);
2) β – құрылым (қатпарлы құрылым немесе жапырақ құрылымы) – полипептилті тізбектегі пептидті топтардың арасында параллель немесе антипараллель (сурет – 7.4Б) орналасқан сутектік байланыс арқылы немесе бір полипептидті тізбектің үлескілерінің арасындағы байланыстар негізінде қатпар құрап түзіледі (сурет – 7.4В);
3) ретсіз шумақтар – бұл полипептидтік тізбектегі әртүрлі бөліктердің бір – бірімен салысырмалы түрде орналасуы ретсіз (тұрақты емес) сипатта болатын аймақтар. Бірақ та бұл аймақтардың конформациясы аминқышқлыды реттілікке негізделеді.
|
|
|
Әр түрлі ақуыздарда α – оралым және β – құрылымның болуы түрліше: фибриллярлы ақуыздарда – тек оралым немесе тек қатпарлы құрылым болуы мүмкін; глобулярлы ақуыздарда – полипептидті тізбектің жекелеген фрагменттері: не оралым, не болмаса қатпарлы құрылым, не ретсіз шумақтар түрінде болады.
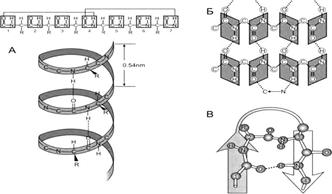 Сурет 7.4 – Полипептидті тізбектің конформациясы:
Сурет 7.4 – Полипептидті тізбектің конформациясы:
А – α – оралым;
Б – тізбек аралық β – құрылым;
В – бір полипептидті тізбек шегіндегі β – құрылым
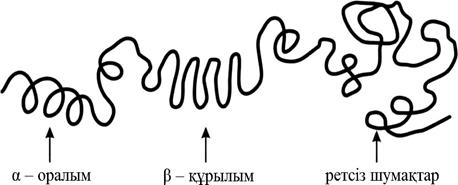
Сурет 7.5 – Пептидті тізбектің орналасу әдістері
Бір ақуызда полипептидті тізбектің орналасуының үш түрі де кездесуі мүмкін.
Глобулярлы ақуыздардың үшінші реттік құрылымы құрамында α – оралым, β – құрылым және ретсіз бөліктер (ретсіз шумақтар) бар полипептидті тізбектің кеңістігкте бағытталып орналасуын қарастырады.
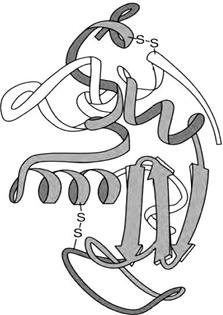 Бұралған полипептидті тізбектің қосымша қатпарлануы амин қышқылдың бүйір тізбектері арасындағы (R – топтары) байланыс негізінде қалыптасады. Бұл жинақы құрылымды түзуді қамтамасыз етеді. Мысал ретінде лизоцимнің кеңістітік құрылымы бола алады (сурет – 7.6).
Бұралған полипептидті тізбектің қосымша қатпарлануы амин қышқылдың бүйір тізбектері арасындағы (R – топтары) байланыс негізінде қалыптасады. Бұл жинақы құрылымды түзуді қамтамасыз етеді. Мысал ретінде лизоцимнің кеңістітік құрылымы бола алады (сурет – 7.6).
|
|
|
Сурет 7.6 – Лизоцимнің кеңістіктік құрылымы: нұсқарлар – қатпарлы аймақтар
R – топтары арасында негізінен ковалентсіз сипаттағы байланыстың бірнеше түрі қарасырылады (сурет – 7.7).
Үшінші реттік құрылымды ақуыздарда байланыстардың мына түрлері кездеседі:
1) қарама қарсы зарядталған ионогенді топтарды (ионды байланысты) тасымалдаушы R – топтары арасындағы тартылыстың электростатикалық күштері;
2) полюсті (гидрофильді) R – топтары арасындағы сутектік байланыс;
3) полюсті емес (гидрофобты) R – топтары арасындағы гидрофобтық әсерлесу;
4) цистеиннің екі молекуласының радикалдары арасындағы дисульфидті байланыстар. Бұл ковалентті байланыстар. Олар үшінші реттік құрылымның тұрақтылығын жоғарылатады, бірақ кеңістікте молекуланың дұрыс орналасуы үшін үнемі қажет болып табылмайды. Ақуыздардың кейбіреулерінде бұл байланыстар мүлдем болмауы да мүмкін.
|
|
|
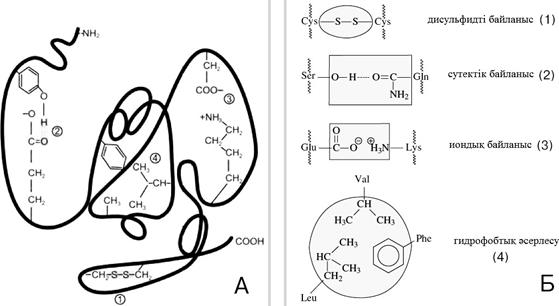
Сурет 7.7 – Үшінші реттік құрылымды тұрақтандыратын байланыстар (А). Амин қышқылдары радикалдарының арасындағы байланыстардың түзілуінің мысалдары (Б):1 – дисульфидті байланыс; 2 – сутектік байланыс;
3 – иондық байланыс; 4 – гидрофобтық әсерлесу
Төртінші реттік құрылым – кеңістікте полипептидтік тізбектердің (протомерлердің) орналасу реті және саны (сурет – 7.8 В). Протомерлер бір - бірімен ковалентті емес байланыстар (иондық, сутектік, гидрофобтық) арқылы байланысқан. Бірақ протомерлер бір - бірімен өздерінің белгілі бір беттік аймақтарымен (байланыстырғыш аймақтары) ғана әрекеттседі. Байланыстырғыш аймақтардың бір - бірін «тануы» комплементарлық принцип бойынша жүзеге асады. Әрбір промер өзге протомердің көптеген нүктелерімен өзара әрекеттеседі. Төртінші реттік құрылым екі немесе одан да көп пептидті тізбектерден құралған ақуыздарға тән. Ақуыздардың мұндай типін олигомерлік ақуыздар деп атайды.
|
|
|
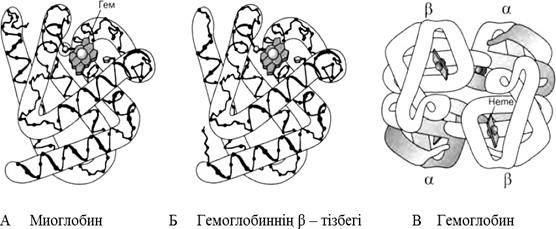 |
Сурет 7.8 – Миоглобин және гемоглобин: А – миоглобин молекуласының үлгісі; Б – гемоглобиннің β – тізбегінің үлгісі;
В – гемоглобинің төртінші реттік құрылымы, гем диск түрінде бейнеленген
Ақуыздардың біріншілік, екіншілік, үшіншілік және төртіншілік құрылымдары келтірілген (сурет – 7.9).
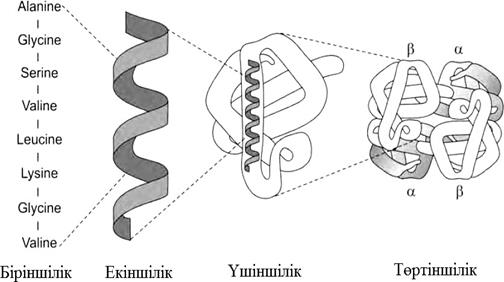 |
Сурет 7.9 – Ақуыз құрылымы бірлігінің деңгейлері
Ақуыздардың қасиеттері
1. Ақуыздың денатурациясы – оның кеңістіктік құрылымының бұзылуы. Ақуыздың молекуласы нативті (табиғи) – әлсіз байланыстар санының көптігіне байланысты энергетикалық жағынан тиімді (функциональды) конформацияға ие және ортаны өзгерткен кезде тез денатурацияға ұшырайды. Температураның өзгерісі, иондық күштің, рН, сонымен қатар органикалық және кейбір тұрақтандырғыш агенттермен өңдеу нативті конформацияның бұзылуына алып келеді. Денатурациялайтын заттар пептидті негіздің карбонилды немесе амин топтарымен, не амин қышқылдарының бүйір радикалдарымен байланыстар түзе отырып, ақуыздың молекулаішілік өзара әрекеттесуін өзінің байланстарымен алмастырады, нәтижесінде екінші және үшінші реттік құрылымдар өзгеріске ұшырайды.
2. 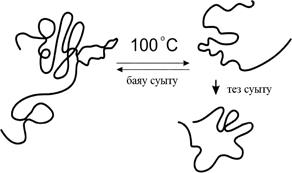 Ақуыздың ренативациясы. Белгілі бір жағдайларда денатурацияланған ақуыз ренативациялануы мүмкін. Бұл жағдай денатурациялайтын немесе детұрақтандыратын факторды жойған кезде жүреді. Мысалы, рибонуклеазаны денатурациялайтын затты - мочевинаны диализ арқылы жойған жағдайда полипептид өздігінен өзінің нативті конформациясын қайта қалпына келтіреді. Осыны қыздырылған денатурацияланған ақуызды баяу суыту арқылы да жүргізуге болады (сурет – 7.10). Бұл пептидті тізбектің орналасуы оның бірінші реттік құрылымы арқылы анықталып қойған деген тезисті дәлеледейді.
Ақуыздың ренативациясы. Белгілі бір жағдайларда денатурацияланған ақуыз ренативациялануы мүмкін. Бұл жағдай денатурациялайтын немесе детұрақтандыратын факторды жойған кезде жүреді. Мысалы, рибонуклеазаны денатурациялайтын затты - мочевинаны диализ арқылы жойған жағдайда полипептид өздігінен өзінің нативті конформациясын қайта қалпына келтіреді. Осыны қыздырылған денатурацияланған ақуызды баяу суыту арқылы да жүргізуге болады (сурет – 7.10). Бұл пептидті тізбектің орналасуы оның бірінші реттік құрылымы арқылы анықталып қойған деген тезисті дәлеледейді.
Сурет 7.10 – Қыздыру кезіндегі ақуыздың денатурациясы және баяу суыту кезіндегі ренативация
3. Гидролиз - қышқылдық, негіздік немесе ферментативті болады. Реакция нәтижесінде төмен молекулярлық пептидтер түзіледі, ең соңында ақуыз құрамына кіретін аминқышқылдары түзіледі.
альбумузалар → полипептидтер → дипептидтер → амин қышқылдары
4. Биурет реакциясы (пептидтік байланысты анықтау). Сұйылтылған ақуыз ерітіндісіне 30% натрий гидроксиді 1% мыс (ІІ) сульфаты ерітінділерін қосқанда қызыл
- күлгін түс пайда болады.
5. Ксантопротеин реакциясы. Ақуыз (фенилаланин, триптофан) құрамында ароматтық аминқышқылдарының қалдықтарының болуымен анықталады. 1 мл ақуыз ерітіндісіне концентрлі азот қышқылын ақ тұнба түзілгенше қосады, сәл қыздырғанда тұнба сарғаяды.
6. Ақуыз (цистеин, цистин) құрамында күкіртті анықтау үшін ақуыз ерітіндісіне қорғасын (ІІ) тұзын қосады, реакция нәтижесінде қара тұнба (PbS) түзіледі.
Физикалық қасиеттері
1. Агрегаттық күйі: а) сұйық; б) қатты;
2. Молекулалардың түрі:
1) глобулярлы ақуыздар – молекулалардың пішіні сферикалқы және элипсоидтық формадағы глобула түрінде болады. Суда ериді немесе коллоидты ерітінділер түзеді.
2) фибриллярлы ақуыздар – молекулалар ұзын тізбекті фибриллярлы талшық пішінді болады. Симметриясы жоғары, суда ерімейді.
7.2 Нуклеин қышқылдары
Нуклеин қышқылдары – мононуклеидтерден тұратын жоғары молекулалық қосылыстар, табиғи биополимерлер.
Нуклеотидтер құрамы мына қосылыстардан тұрады:
1. Нуклеозидтерден:
1) азотты негіздерден: пиримидин немесе пурин;
2) моносахаридтерден: рибоза немесе дезоксирибоза – оларды нуклеозидтер деп атайды.
2. Фосфор қышқылының қалдықтары: фосфаттар.
Табиғатына және атқаратын функциясына байланысты екі түрге бөлінеді:
1) құрамына рибоза кіретін рибонуклеотидтерді – рибонуклеин қышқылдары (РНҚ)
деп атайды;
2) дезоксирибоза кіретін – дезоксирибонуклеотидтерді – дезоксирибонуклеин қышқылдары (ДНҚ) деп атайды.
Рибонуклеин қышқылдар (РНҚ) құрамына мына қосылыстар кіреді:
1) көмірсулар: β – рибоза;
2) азотты негіздер: аденин (А); гуанин (Г); цитозин (Ц); урацил (У);
3) фосфаттар;
Дезоксирибонуклеин қышқылы (ДНҚ) мына қосылыстардан тұрады:
1) көмірсулар: β – дезоксирибозадан;
2) азотты негіздерден: аденин (А); гуанин (Г); цитозин (Ц); тимин (Т);
3) фосфаттар;
Нуклеотидтер РНҚ және ДНҚ молекулаларында фосфор қышқылы мен аминқышқылдар құрамындағы -ОН топтарымен күрделі эфирлі байланыстар арқылы қосылады.
РНҚ молекуласы мононуклеотидтерден құралған бір полинуклеотидті тізбектен тұрады. ДНҚ молекуласы өз осінде оралған спиральды екі параллельді полинуклеидті тізбектен тұрады. Қос спиральдың ішінде – адеин– тиминмен; гуанин – цитозинмен сутектік байланыс арқылы қосылған азотты негіздер орналасқан.
Аденин – тимин; гуанин – цитозин жұптарын комплементарлық жұптар деп атайды.
Бұл спиральды ДНҚ – ның екінші реттік құрылымы деп аталады.
ДНҚ молекуласының құрылымы күрделі болып келеді. Егер тізбекте нуклеотидтер бірінен соң бірі орналасса онда бірінші реттік құрылымы деп аталады.
Екіншілік реттік құрылымы – екі полинуклеотид тізбектен тұратын қосқабат спиральдан тұрады.
Пурин және пиридин негіздері қосқабат спиральінің ішіне бағытталып А-Г, Г-Ц сутектік байланыс нәтижесінде жұптар түзеді.
ДНҚ – ның үшінші реттік құрылымы – ақуыз комплекстерінің байланысуымен, кеңістікте орналасуымен (конфигурациясымен) анықталады. Ол суперспираль, сақина.
Нуклеин қышқылдары тұқым қуалайтын белгілерді сақтайды.
Нуклеин қышқылдарының және нуклеотидтердің биологиялық мәні
Адам организміндегі зат алмасу үдерісінде бос моно- және динуклеотидтер үлкен рөл атқарады. АТФ (аденозинтрифосфат) молекуласы – жасушада әмбебап энергия тасымалдаушы. Ол тері тіндерінің тыныс алу үдерісі барысында, АДФ (аденозиндифосфат) және Н3РО4 митохондриядан синтезделеді. Жасуша мембранасындағы АТФ-тан циклді АМФ (аденозинмонофосфат) (ц-АМФ) синтезделеді. Соңғы жылдары организмдегі ц-АМФ үлкен реттегіш әсері болатындығы анықталған:
1) гормондардың түзілуі мен синтезінде;
2) гормондардың әсерінен мембраналық өткізгіштікке әсері және жүйен импульстарының берілуі;
3) простагландин ферменттерінің секрециясына;
4) жасушадағы ақуыздар биосинтезіне;
5) көмірсу және май айналымына;
6) обыр жасушаларының көбеюіне (өсуіне) (ц-АМФ обыр жасушаларының өсуін баяулатады).
Бос моно- және динуклеотидтер ферменттердің құрылымдық бөлімі болып табылады: мысалы, никотинамидадениндинуклеотид (НАД+), флавинмононуклеотид (ФМН) тері тіндерінің тыныс алу үдерісі дегидрогеназының (тотықтырғыш фосфорлану) коферменттері болып табылады. Нуклеин қышқылдары тұқымқуалаушылық белгілердің сақталуы мен берілуіне, жасушадағы ақуыз биосинтезінде үлкен рол атқарады. ДНҚ молекуласы ядрода қос спираль түрінде орналасады және оның нуклеотидтерінің ретімен орналасуында болашақ ақуыздың шифры жазылады. ДНҚ – жасушаның негізгі генетикалық материалы.
Ақуыз биосинтезінде ДНҚ-ның қос спиралы дара екі спиральға бөлінеді.
ДНҚ атқаратын қызметі
1. ДНҚ молекуласы транскрипция үдерісінде – ақуыз молеклаларының синтезіне қажетті РНҚ молекуласының құрылымына ақпараттың қайта кодталуында матрица қызметін атқарады.
2. ДНҚ молекуласы репликация (қосарлану) процесінде – ДНҚ молекуласындағы ақпараттың көшірілуі.
3. Жасушада атқаратын фукнциясына байланысты РНҚ-ның мынандай түрлері болады: 1) ақпараттық немесе матрицалық (а-РНҚ); 2) тасымалдаушы (т-РНҚ); және 3) рибосомалық (р-РНҚ).
Ақпараттық РНҚ ядродағы бірспиральды ДНҚ - дан синтезделеді, ДНҚ-да нуклеотидтердің белгілі бір жүйесі арқылы жазылған ақпаратты қабылдап, оны рибосомаға береді. а-РНҚ - жоғары молекулярлы.
Тасымалдаушы РНҚ жасушадағы цитоплазмада болады және активтелген амин қышқылның қалдықтарын ақуыз биосинтезі жүретін орынға - рибосомаға тасымалдайды. т-РНҚ төмен молекулярлы және «үйеңкі жапырағы» пішіндес болады.
Рибосомалық РНҚ ақуыз биосинтезі жүретін рибосома құрамына кіреді
8 Жоғары молекулалық қосылыстар. Негізгі ұғымдар
Жоғары молекулалық қосылыстардың молекуласы немесе макромолекуласы өзара химиялық байланыстармен байланысқан жүздеген және мыңдаған атомдардан тұрады. Мысалы: целлюлоза молекуласы (С6Н10О5)n, табиғи көксағыз (С5Н8)n, полиэтилен (С2Н4)n т.б.
Жоғары молекулалық қосылыстар табиғи және синтетикалық болады:
1. Табиғи – целлюлоза, каучуктар, ақуыздар;
2. Синтетикалық – полиэтилен, полипропилен, тефлон т.б. жатады;
Салыстырмалы молекулярлық массасы жоғары және өздеріне тән физикалық қасиеттері бар қосылыстарды – жоғары молекулалық қосылыстар немесе полимерлер деп атайды.
Полимер деген ұғымды алғаш 1833 ж. швед ғалымы Берцелиус ұсынған. Полимерлену реакциясына қатысатын бастапқы зат – мономер деп аталады.
Мысалы, полиэтиленнің мономері – этилен.
 CH2 = CH2 →
CH2 = CH2 → [ CH2 – CH2 ]n
Дата добавления: 2021-03-18; просмотров: 232; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
