Фишер формуласы Колли-Толленсу формуласы 8 страница
Спирттермен салыстырғанда қайнау температурасы төмен, бұл эфирлер сутектік байланыс түзбейтіндігін көрсетеді.
| Метил | tқайн, C0 | Этил | tқайн, C0 |
| спирті | +65 | спирті | +78,3 |
| эфирі | –23,7 | эфирі | +34,6 |
Химиялық қасиеттері
Жай эфирлер гидролизденбейді.
1. Концентрлі күкірт қышқылымен реакция жағдайына байланысты әртүрлі жүруі мүмкін:
C2H5 – O – C2H5 + H2SO4 → C2H5 – O – SO2 – OC2H5 + H2O
диэтилсульфат
немесе
С2Н5 – О – С2Н5 + НО – SO3Н → С2Н5ОSO3Н + С2Н5ОН
этилкүкірт этил
қышқылы спирті
2. Натриймен жоғары температурада әсер еткенде ыдырайды:
𝑡
С2Н5 – О – С2Н5 + 2Na → C2H5ONa + C2H5ONa
натрий этилаты
3. Концентрлі HJ жай эфирлерді ыдыратады:
C2H5 – O – C2H5 + HJ → C2H5OH + C2H5J
Қолданылуы
Этил эфирі – еріткіш, экстракциялау үшін қолданылады; медицинада – наркоз, жүрек қызметін жоғарылату үшін, анестезияда пайдаланылады.
Диизопропил эфирі – автокөлік жанармайының антидетонациялық қасиетін жоғарылату үшін қолданылады.
Дибутил эфирі – еріткіш, көптеген органикалық заттарды ерітеді.
4.13.2 Күрделі эфирлер
Күрделі эфирлерді карбон қышқылдарының гидроксил тобындағы сутек атомы көмірсутек радикалымен орынбасқан туындысы деп қарастыруға болады.
 |
Күрделі эфирлер төмен, жоғары молекулалардың, қаныққан, қанықпаған қышқылдары мен спирттерден тұруы мүмкін.
|
|
|
Аталуы
Күрделі эфирлердің атаулары оны құрайтын қышқылдар мен спирттердің қалдықтарынан құрастырылады.
 |
Изомериясы
1. Көміртек қаңқасының изомериясымен анықталады.
 |
2. – C
O

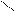 O – тобының орналасуы.
O – тобының орналасуы.

3. Класаралық изомериясы.
 |
Алынуы
1. Табиғи шикі заттардан (майлар; т.б.).
2. Этерификация реакциясы нәтижесінде. Этерификация – қышқылдар мен спирттер арасындағы реакция. Этерификация реакциясы қайтымды реакцияға жатады.
О О
 // //
// //
СН3 – С + Н – О – С2Н5 → СН3 – С + Н2О
\ \
ОН ОС2Н5
3. Хлорангидридтерді спирттермен әрекеттестіру нәтижесінде:
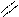
 O О
O О

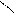 СН3 – C + HO – С2Н5 → СН3 – C + HCl Cl O – С2Н5
СН3 – C + HO – С2Н5 → СН3 – C + HCl Cl O – С2Н5
Физикалық қасиеттері
Төмен молекулалық қышқылдар мен спирттерден түзілген күрделі эфирлер ұшқыш сұйықтықтар. Суда нашар еритін сұйықтар, органикалық еріткіштерде жақсы ериді. Олар сутекті байланыс түзбейді, сондықтан қайнау температурасы төмен. Көбіне оларға жидек иіс тән. Жоғары молекулярлық қышқылдармен спирттерден түзілген күрделі эфирлер қатты заттар. Суда ерімейді, бірақ органикалық еріткіштерде ериді.
|
|
|
Химиялық қасиеттері
1. Оларға гидролиз реакциялары тән. Сілтінің әсерінен жүретін гидролизді сабындану реакциясы деп атайды. Сабындану реакциясын қайтымсыз жасау үшін қышқыл, сода, сілті қосады.
| О | О | |||
| // СН3 – С \ ОС2Н5 | + | NaOH | → | // СН3 – С + С2Н5ОН \ ОNa |
Гидролиз реакциясы қышқылдың әсерінен де жүреді (қышқылдық гидролиз).

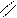 O О
O О
[Н+]

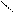 С2Н5 – C + H2О → СН3 – C + СН3ОН
С2Н5 – C + H2О → СН3 – C + СН3ОН
О – СН3 OН
Этерификация реакциясы қайтымды реакцияларға жатады. Ол қышқылдың және
спирттің құрылысына тәуелді:
1) бір қышқылмен реакцияға біріншілік, екіншілік, үшіншілік спирттер түсетін болса, онда біріншілік спирттің этерификация реакциясы жоғары болады;
|
|
|
2) спирттің бір түрімен түрлі құрылымды қышқылдар әрекеттессе, онда этерификация реакциясы мына қатарда төмендейді:
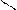
 R R
R R
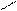
 R – CH2 – COOH > CH – COOH > R – C – COOH
R – CH2 – COOH > CH – COOH > R – C – COOH
R R
Жай эфирлер сумен әрекеттеспейді.
2. Тотықсыздану реакциялары: сутектің әсерінен спирттер түзеді:
О
//
С3Н7 – С + [Н] → С3Н7СН2ОН + С2Н5ОН
\ бутил спирті этил спирті
ОС2Н5
Қолданылуы
1) еріткіш ретінде пайдаланылады;
2) жидек эссенция даярлау үшін;
3) дәрі-дәрмек жасауда;
Минералды қышқылдардың эфирлері
Минералды қышқылдардың эфирлері қышқыл құрамындағы сутек алкил радикалына орын басу нәтижесінде түзіледі.
 CH3 – OH + H – O – NO2 → CH3 – O – NO2 + H2O
CH3 – OH + H – O – NO2 → CH3 – O – NO2 + H2O
метилнитрат
C2H5 –
– O – SO3H → C2H5 – O – SO3H + H2O
|
Бұл эфирлер қышқыл эфирлерге жатады.
Спирттің артық мөлшерімен әсер еткенде орта эфирлер түзіледі:
 |
Күрделі эфирлердің кейбір өкілдері. Олардың қолданылуы .
|
|
|
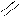 О
О
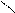 Этилацетат – СН3 – C – жағымды иісті, өндірісте көп мөлшерде
Этилацетат – СН3 – C – жағымды иісті, өндірісте көп мөлшерде
О – С2Н5
алынады. Жақсы еріткіш, дәрі – дәрмек өндірісінде қолданылады.
Үшнитроглицерин
1) қопарғыш зат;

 H2C – O – NO2 HC – O – NO2 H2C – O – NO2
H2C – O – NO2 HC – O – NO2 H2C – O – NO2
2) медицинада 1% - спирттік ерітіндісі жүрек дәрісі ретінде қолданылады. Фосфор қышқылының эфирлерінің биологиялық маңызы зор.
Күрделі эфирлердің қолдану салалары
1. Еріткіштер.
2. Жасанды талшықтар (лавсан).
3. Пластмассалар синтездеуде.
4. Жуғыш құралдар.
5. Дәрі - дәрмек өндірісінде.
6. Тағамдар эссенциялар.
7. Парфюмерия өндірісінде.
4.14 Майлар
Майлар – үшатомды спиртпен (глицерин) жоғары монокарбон қышқылдарының күрделі эфирлері. Майлардың құрамына көбіне пальмитин, стеарин (қаныққан) және олеин (қанықпаған) қышқылдары кіреді.
Оларды көбіне глицеридтер (үшглицеридтер) деп атайды. Майлардың құрамын 1811 жылы француз химигі Шеврель анықтады. 1854 жылы Бертло майлардың құрылысын дәлелдеді.
Жалпы сипаттамалары
Барлық майлардың құрамына глицерин кіреді. Сондықтан, оларды глицеридтер деп атайды. Егер глицеридтің құрамына тек қышқыл қалдықтың бір түрі кірсе оны жай глицерид деп атайды, егер құрамында қышқыл қалдықтарының бірнеше түрі болса оны аралас глицерид дейді.
Қышқылдардың ішінде жиі кездесетін: қаныққан – пальмитин С15Н31СООН және стеарин С17Н35СООН; қанықпаған – олеин С17Н33СООН, линол С17Н31СООН және линолен С17Н29СООН.
Табиғи майлардың құрамына көбіне түрлі қышқылдар кіреді. Мысалы, доңыз (шошқа) майы құрамы олеин, пальмитин және стеарин қышқылдарынан тұрады; сиыр майы құрамына олеин, пальмитин, май, стеарин, миристин (СН3(СН2)12СООН) – қаныққан) қышқылдары кіреді. Қаныққан қышқылдарының глицеридтері – қатты қосылыстар; қанықпаған – сұйықтар. Өсімдік майлары құрамына – қанықпаған қышқылдар қалдықтары кіреді. Сондықтан, олар – сұйықтар. Жануарлар майлары қатты болады. Бірақ, ерекшеліктер де кездеседі:
балық майы (жануар майы) – сұйық; кокос майы (өсімдік майы) – қатты.
Алынуы
Майларды өсімдік немесе жануарлардың табиғи өнімдерінен алады.
Аталуы
Майлар құрамына кіретін қышқылдардың радикалдары бойынша аталады Мысалы:
Н2С – О – СО – С17Н35 Н2С – О – СО – С15Н31
| |
НС – О – СО – С17Н35 НС – О – СО – С15Н31
| |
Н2С – О – СО – С17Н35 Н2С – О – СО – С17Н33
үшстеарин дипальмеостеарин
Химиялық қасиеттері
1. Гидролизденеді:
Н2С – О – СО – R Н2С – О – ОH
| |
НС – О – СО – R + 3HOH → НС – О – ОH + 3CRH35COONa
| |
Н2С – О – СО – R Н2С – О – ОH
2. Сабынданады (гидролизденеді), гидролиздің дәрежесін жоғарылату үшін NaOH қосады, спирттік ортада жүргізеді:
О
||
Н2С – О – С – С17Н35
| О Н2С – ОН
| || |
НС – О – С – С17Н35 + 3NaOH → НС – ОН + 3С17Н35СООNa
| |
Н2С – О – С – С17Н35 Н2С – ОН
||
О
Реакция нәтижесінде сабын түзіледі.
3. Гидрогендеу (гидрлеу);
О
||
Н2С – О – С – (СН2)7 – СН = СН – (СН2)7 – СН3
| О
| || + 3H2(Ni) →
НС – О – С – (СН2)7 – СН = СН – (СН2)7 – СН3
|
Н2С – О – С – (СН2)7 – СН = СН – (СН2)7 – СН3
||
О сұйық май
О
||
Н2С – О – С – (СН2)7 – СН2 – СН2 – (СН2)7 – СН3
| О
→ | ||
НС – О – С – (СН2)7 – СН2 – СН2 – (СН2)7 – СН3
|
Н2С – О – С – (СН2)7 – СН2 – СН2 – (СН2)7 – СН3
||
О қатты май
Гидрленген өнім (саламас, комбижир) маргарин алуда пайдаланылады. Бірінші маргарин зауыты 1870 жылы Францияда салынған.
4. Майлар тотығады. Құрамында қанықпаған қышқыл қалдықтары бар майлар ауадағы оттектің әсерінен оңай тотығады. Тотығу реакцияларының өнімдері адам организміне зиян келтіреді.
Майлардың қолданылу салалары
1. Майларды тағамдар өндірісінде қолданады. Себебі, олардың энергия қоры жоғары.
2. Фармацевтикада түрлі майлардың негізі болып табылады. Дәрі - дәрмектердің еріткіші ретінде қолданылады. Мысалы, балық майы.
3. Косметика өндірісінде.
4. Сабын, жуғыш заттар өндірісінде.
5. Бояу, лак өндірісінде кеңінен қолданылады.
4.15 Сабындар
Қаныққан жоғары молекулалық қышқылдардың натрий немесе калий тұздары сабындар деп аталады. Радикалдың құрамында көміртек атомы С20 жоғары болмайды, С21-ден бастап карбон қышқылдары суда ерімейді.
Сабындар көбіне пальмитин С15Н31СООNa және стеарин С17Н35СООNa қышқылдарының тұздары.
Натрий тұздары - қатты, калий тұздары - сұйық.
Алынуы
1. Майларды NaОН қатысында гидролиздеу (сабындау) арқылы алады.
С3Н5 – (О – С – С17Н35 )3 + 3NaОН → С3Н5(ОН)3 + 3С17Н35СООNa
|| глицерин нартий
О стеараты
2. Майларды сумен жоғары қысымда гидролиздейді:
а) С3Н5 – (О – С – С17Н35)3 + 3Н2О → С3Н5(ОН)3 + 3С17Н35СООН
||
О
ә) түзілген қышқылға сода қосады:
2С17Н35СООН + Na2СО3 → 2С17Н35СООNa + Н2О + СО2
кермек суда су құрамындағы Са(НСО3)2, Mg(НСО3)2 сабынмен әрекеттесіп тұнба түзеді:
2С17Н35СООNa + Са(НСО3)2 → (С17Н35СОО)2Са↓ + NaНСО3
Дата добавления: 2021-03-18; просмотров: 144; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
