Фишер формуласы Колли-Толленсу формуласы 4 страница
Жауабы: 2,5г
4. Массасы 150 г фенолдың бензол ерітіндісін бромның артық мөлшерімен өңдегенде 16,55 г фенолдың бромтуындысы алынған. Фенолдың ерітіндідегі м.ү. есептеңіз.
Жауабы: 3.1%
5. Массасы 50 г фенол ерітіндісін бромсуының артық мөлшерімен өңдегенде массасы 3,31 г тұнба түзілген. Бастапқы ерітіндідегі фенолдың м.ү. есептеңіз.
6. Массасы 4,7 г фенолмен 0,5 моль/л NaOH ерітіндісінің қандай көлемі әрекеттеседі?
Жауабы: 100 мл
7. Массасы 18,8 г фенолмен 5,1%, ρ=1,06 г/мл натрий гидроксиді ерітіндісінің қандай көлемі әрекеттеседі?
Жауабы: 148 мл
8. Мына тізбектерді іске асыру реакцияларын жазыңыз.
1) кальций карбиді→ ацетилен → бензол → бромбензол → фенол → үшбромбензол;
2) циклогексан → бензол → хлорбензол → фенол → пикрин қышқылы;
3) бензол → хлорбензол → фенол → үшнитробензол;
9. 


 Мына тізбектерді іске асыру реакцияларын жазыңыз: 1) бензол 𝐶𝑙2,𝐹𝑒𝐶𝑙2 А 𝑁𝑎𝑂𝐻,𝑡,𝑃 В 𝑁𝑎 Д 𝐶𝐻3𝐵𝑟 К
Мына тізбектерді іске асыру реакцияларын жазыңыз: 1) бензол 𝐶𝑙2,𝐹𝑒𝐶𝑙2 А 𝑁𝑎𝑂𝐻,𝑡,𝑃 В 𝑁𝑎 Д 𝐶𝐻3𝐵𝑟 К


 2) циклогексан А 𝑡,𝑘𝑎𝑡 В 𝐵𝑟2,𝐹𝑒𝐵𝑟3 Д 𝑁𝑎𝑂𝐻,𝑡,𝑃 К
2) циклогексан А 𝑡,𝑘𝑎𝑡 В 𝐵𝑟2,𝐹𝑒𝐵𝑟3 Д 𝑁𝑎𝑂𝐻,𝑡,𝑃 К
−𝐻2


 3) бензол 𝐻2𝑆𝑂4 𝑘 A 𝑁𝑎𝑂𝐻 B 𝐶𝐻2𝑂 Д
3) бензол 𝐻2𝑆𝑂4 𝑘 A 𝑁𝑎𝑂𝐻 B 𝐶𝐻2𝑂 Д
10. Көрсетілген қосылыстардың қайсысымен фенол әрекеттеседі:
1) натрий, натрий гидроксиді, тұз қышқылы, бром, сутек, темір (ІІІ) хлориді.
|
|
|
2) калий, калий гидроксиді, калий дихроматы, азот қышқылы
11. Төрт пробиркада фенол, глицерин, этил спирті және су берілген. Пробиркадағы қосылыстарды қалай ажыратуға болады?
4.6 Альдегидтер
Альдегидтер – карбонил (С = О) тобы көмірсутек радикалы және сутек атомымен байланысқан органикалық қосылыс:
 Карбонил тобын оксо – тобы деп атайды, сондықтан альдегидтер мен кетондар оксоқосылыстар деп аталады. Көміртек атомы С = О тобында sp 2 – гибридтенген, С = О байланыс ұзындығы 0,121 нм, байланыс энергиясы 708 кДж/моль.
Карбонил тобын оксо – тобы деп атайды, сондықтан альдегидтер мен кетондар оксоқосылыстар деп аталады. Көміртек атомы С = О тобында sp 2 – гибридтенген, С = О байланыс ұзындығы 0,121 нм, байланыс энергиясы 708 кДж/моль.
Карбонил тобында С атомы R, Н, О – пен 3δ және π байланысады. Тек құмырсқа альдегидінде екі сутек атомымен байланысады:
 О
О
//
Жалпы формуласы: С n Н 2n С немесе С n-1 Н 2n+1 О
\
Н
Молекулалық массасы: Мr (С n Н 2n О ) = 14n + 16
Аталуы
Көмірсутектің атауына аль- жұрнағы қосылады.
| О | О | О | О |
| // | // | // | // |
| Н – С | СН3 – С | СН3 – СН2 – С | СН3 – СН2 – СН2 – С |
| \ | \ | \ | \ |
| Н | Н | Н | Н |
| метаналь | этаналь | пропаналь | бутаналь |
| құмырсқа | сірке | пропион | май альдегиді |
| альдегиді | альдегиді | альдегиді Изомерия |
Альдегидтердің изомериясы төртінші көміртек атомынан басталады.
|
|
|
1) альдегидтердің изомериясы көмірсутек қаңқасының изомериясымен анықталады:
О О
// //
СН3 – СН2 – СН2 – С СН3 – СН – С
\ | \
Н СН3 Н
бутаналь 2-метил пропаналь
2) класаралық альдегидтер – кетондар, себебі олардың алпы формуласы бірдей (СnН2nО).
4.6.1 Формальдегид
О
//
Формальдегид – метаналь Н – С
\
Н
- ерекше иісті газ, суда жақсы ериді. Оның 40% ерітіндісі формалин деп аталады. Улы. Қайнау температурасы (-21оС) метаннан төмен.
Формальдегидті алу әдістері
1. Метанолды тотықтыру арқылы алады:
О
//
Катализатор: Сu Температура: 300оС
2. Метанды тотықтыру:
Катализатор: NO Температура: 400-600оС
2СН3ОН + О2 → 2Н – С + 2Н2О
\ Н
О
//
СН4 + О2 → Н – С + Н2О
\
Н
Химиялық қасиеттері
Химиялық қасиеттері электрондық құрылысымен түсіндіріледі. Оттектің электртерістігі жоғары болғандықтан оттек атомында теріс зарядтың тығыздығы жоғары болады, ал көміртек атомында – оң зарядтың тығыздығы жоғары болады:
|
|
|
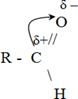 сондықтан альдегидтер оңай тотығады, екінші жақтан қос байланыс болғандықтан полимерленеді, қосылу реакцияларына қатысады.
сондықтан альдегидтер оңай тотығады, екінші жақтан қос байланыс болғандықтан полимерленеді, қосылу реакцияларына қатысады.
Тотығу реакциялары:
1) күміс (I) оксидінің аммиак ерітіндісінде тотығады, құмырсқа қышқылы не оның тұзы түзіледі:
О О
|
Н – С + Ag2O → Н – С + 2Ag
\ \
Н ОН
құмырсқа қышқылы
немесе
О О
// //
Н – С + 2[Ag (NH3)2]ОН → Н – С + 2Ag + 3NH3 + Н2О
\ /
Н ОNH4
аммоний формиаты
Бұл альдегидтердің сапалық реакциясы – күміс – айна реакциясы деп аталады.
2) мыс (II) гидроксидін мыс (I) оксидіне дейін тотықтырады:
| О | О | |
| // | // | |
| Н – С | + | 2 Cu (ОН)2 → Н – С + 2 CuОН ↓ + Н2О |
| \ | \ | |
| Н | ОН |
|
|
|
2CuОН → Cu2О↓ + Н2О
қызыл қоңыр тұнба түзіледі. Бұл реакция сапалық реакцияға жатады.
Қосып алу реакциясы:
О
//
1) Н – С + НСN → Н2С – ОН
\ циансутек |
Н СN
гидроксинитрил
аммиакты қосып алу:
 δ –
δ –
О Н – N – Н
// |
2) Н – С + N̈ Н3 → Н – С – OH → Н – СН = NН + Н2О
\ | альдимин
Н Н
3) сутекті қосып алу (гидрлеу) – тотықсыздану реакциясы:
О
//
Н – С + Н2 → СН3ОН – метанол
\
Н
Катализатор: Ni
Полимерлену реакциясы:
Н
\
nС = О → –СН2 – О – СН2 – О– → [СН2 – О]n
/ параформ
Н
 Поликонденсация реакциясы:
Поликонденсация реакциясы:
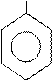 ОН ОН
ОН ОН
+ CH2O → …
+ nH2O
n
Қолданылуы
1) фенолформальдегидтер шайырын, карбамидті шайырлар;
2) бояу;
3) синтетикалық каучук;
4) дәрі – дәрмек;
5) қопарғыш заттар;
6) тері өңдеуде;
7) медицинада анатомиялық препараттарды өңдеуде кеңінен қолданылады.
4.6.2 Ацетальдегид, сірке альдегиді
Ацетальдегид, этаналь – өткір иісті, түссіз сұйықтық, суда жақсы ериді, улы.
О
// Формуласы: СН3 – С
\
Н
қайнау температурасы (21оС) этанолдан төмен.
Алу әдістері
1) Кучеров реакциясымен алады:
НС ≡ СН + Н2О → СН3 – СОН
Катализатор: HgSO4, Hg(NO3)2
2) этиленді тотықтыру арқылы:
[О]
Н2С = СН2 → СН3 – СОН
Катализатор: CuCl2, PdCl2 қоспасы Температура: 100оС
Қысым: 1мПа
3) біріншілік спирттерді тотықтыру:
СН3 – СН2ОН
СuО
→
𝑡
СН3СОН + Н2О + Cu
4) біріншілік спирттерді күшті тотықтырғыштармен (K2Cr2O7, KMnO4+ H2SO4) тотықтыру:
СН3 – СН2ОН → СН3СОН + Н2О
Химиялық қасиеттері
Оның электрондық құрылысымен түсіндіріледі.
Қосып алу реакциясы:
О ОН
// |
1) СН3 – С + Н – СN → СН3 – С – СN
\ |
Н Н
2) сутекті қосып алу (тотықсыздану, гидрлену)
О
//
СН3 – С + Н2 → СН3 – СН2 – ОН
\ этил спирті
Н
Катализатор: Ni
3) аммиакты қосып алу:
О
//
СН3 – С + N̈ Н3 → СН3 – СН = NН + Н2О
\ Н
Тотығу реакциясы:
О О
// //
1) СН3 – С + Ag2O → СН3 – С + 2Ag
\ \
Н ОН
сірке қышқылы
аммиак ортасында:
О О
// //
СН3 – С + 2 [Ag(NH3)2]ОН → СН3 – С + 2Ag + 3NH3 + Н2О
\ \
Н NН4
«Күміс айна» реакциясы – сапалық реакция.
О О
// //
2) СН3 – С + 2Cu (ОН)2 → СН3 – С + 2CuОН↓ + Н2О
\ \
Н ОН
2CuОН → Cu2О↓ + Н2О
қызыл – қоңыр тұнба – альдегидтерге сапалық реакциясы
Орынбасу реакциясына галогендендіру реакциясы жатады:
1) хлор, броммен орынбасу реакциясы α–көміртекпен байланысқан сутектің орнын басу арқылы жүреді:
О О
// //
СН3 – С + 2Br2 → Br2СН – С + 2НBr
\ \
Н Н
2) фосфор (V) хлоридімен әрекеттескенде галоген оттектің орнын басады:
О
//
СН3 – С + РСl5 → СН3 – СНСl2 + РОСl3
\ 1,1 – дихлорэтан
Н
Полимерлену реакциясы:
 О
О
//
3Н3 – С →
\ Н
паральдегид
Қолданылуы
1) сірке қышқылын, этил спиртін, этилацетатты, бутил спиртін алады;
2) С7-ден С16 - ға дейін альдегидтер парфюмерияда пайдаланылады;
3) ацетат талшығын өндіруде.
4.7 Кетондар
Кетондар – карбонил тобы екі радикалмен байланысқан органикалық қосылыстар.
Қарапайым кетон – ацетон:
R – C – R1
|| O
СН3 – С – СН3
|| О
Жалпы формуласы: СnН2nО Молекулярлық массасы: Мr (СnН2nО) = 14n + 16
Аталуы
Халықаралық атау бойынша қаныққан көмірсутекке - он жұрнағы қосылады.
СН3 – С – СН3 С2Н5 – С – СН3
|| ||
О О
пропанон бутанон
диметилкетон этилметилкетон ацетон
көбіне радикалдарына байланысты аталады.
Алыну әдістері
1. Екіншілік спирттерді K2Cr2O7, KMnO4 қышқылдық ортада СuO қатысында тотықтыру арқылы:
[О]
СН3 – СН – СН3 → СН3 – С – СН3 + Н2О
| ||
ОН О
пропанол – 2 кетон
2. Кальций ацетатын құрғақ күйде t=300оC қыздыру арқылы:
Са(СН3СОО)2 → СН3 – С – СН3 + СаСО3
|| О
3. t=3000C сірке қышқылын (Al2O3, ThО2 катализаторлар қатысында) қыздырғанда:
 СН3 – С – ОН + НО – С – СН3 → СН3 – С – СН3 + Н2СО3
СН3 – С – ОН + НО – С – СН3 → СН3 – С – СН3 + Н2СО3
|| || ||
О О О
Физикалық қасиеттері
Ацетон – ерекше иісті сұйықтық, суда жақсы ериді.
Химиялық қасиеттері
1. Сутекті қосып алады (тотықсызданады):
СН3 – С – СН3 + Н2 → СН3 – СН – СН3
|| |
О ОН – екіншілік спирт
2. HCN – циансутекті қосып алады:
СН3 Н3С ОН
\ \ /
С = О + Н – CN → С
/ / \
СН3 Н3С CN
оксинитрил, циангидрин
[О]
СН3 – С – СН3 → НСООН + СН3СООН
|| құмырсқа қышқылы сірке қышқылы
О
3. Броммен орынбасу реакциясына қатысады:
СН3 – С – СН3 + Br – Br → СН3 – С – СН2Br + НBr
|| ||
О О
бромацетон
Дата добавления: 2021-03-18; просмотров: 143; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
