Фишер формуласы Колли-Толленсу формуласы 2 страница
О
| СН2 – О – СО – СН3 | СН2 – О – СО – СН3 | ||
| | | + НООССН3 | → | | + Н2О |
| СН2 – ОН | СН2 – О – СО – СН3 |
3. Мыс (II) гидроксидімен көк түсті мыс гликолятын түзеді, яғни Cu(ОН)2 - тұнбаны ерітеді, көк түсті комплекті қосылыс түзіледі. Бұл реакция гликольдердің сапалық реакциясы болып табылады.
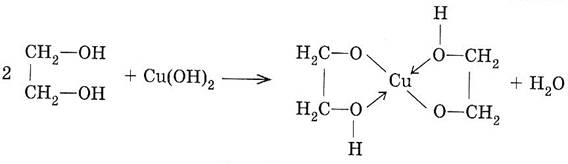
біратомды спиртерден айырмашылығы
4. Дегидратталу реакциясы тән а) молекулаішілік:
О
//
Н2С – СН – ОН → [Н2С = СН – ОН] → СН3 – С + Н2О
 │ │ винил спирті \
│ │ винил спирті \
ОН Н Н
ә) молекулааралық - екі молекула дегидратталса – диоксан түзіледі.
О
| Н2С – ОН | НО – СН2 | / Н2С | \ СН2 |
| | | + | | → | | | + 2Н2О |
| Н2С – ОН | НО – СН2 | Н2С | СН2 |
| \ | / |
О
диоксан
5. Галогенсутектермен әрекеттесіп, ОН – тобын галогендерге алмастырылады:
| Н2С – ОН | Н2С – ОН |
| |||
| | | + НCl | → | | | + | Н2О |
Н2С – ОН Н2С – Сl
Катализатор: ZnCl2
Н2С – ОН Н2С – Сl
| + НCl → | + Н2О Н2С – Сl Н2С – Сl
6. Тотығу нәтижесінде қымыздық қышқылын алуға болады:
| СН2 – ОН | [O] | СООН |
| | | → | | |
| СН2 – ОН | СООН |
Алу әдістері
1. Этиленді KMnO4 ерітіндісімен тотықтыру:
|
|
|
СН2 = СН2 + Н2О + [О] → СН2 – СН2
| |
ОН ОН
2. Алкандардың галогентуындыларынан:
| СН2 – СН2 | СН2 – СН2 |
| |
| | | | + 2NaОН → | | | + | 2NaСl |
| Сl Сl | ОН ОН | ||
Қолданылуы
1) антифриз ретінде;
2) лавсан алуда;
3) лактар, бояулар;
4) мотор майларын алуда.
4.1.3 Үшатомды спирттер. Глицерин
Глицерин – құрамында үш гидроксил тобы бар алифаттық спирттер.
Жалпы формуласы: C n Н 2n – 1 (ОН) 3
Молекулярлық массасы: Mr (СnH2n–1 (OH)3)=14n +50
Бірінші өкілі – глицерин.
СН2 – СН – СН2
| | |
ОН ОН ОН пропантриол – 1,2,3
Изомериясы
Көмірсутек қаңқасы мен гидроксил тобының орналасуына тәуелді.
Алу әдістері
1) майларды сабындау (гидролиз) реакциясы нәтижесінде:
О
||
| СН2 – О – С – С17Н35 | СН2 – ОН |
| ||||
| | | | | |||||
| СН – О – С – С17Н35 | + | 3Н2О | → | СН – ОН | + | С17Н35СООН |
| | || | | | стеарин қышқылы | ||||
| | О | СН2 – ОН | |||||
| СН2 – О – С – С17Н35 | лицерин | |||||
|| О
стеариан қышқылының үшглицериді
2) сілті (NaOH) ерітіндісінде немесе Cu2O қатысында жоғары температурада синтетикалық әдіспен пропиленнен алуға болады:
|
|
|
СН2 = СН–СН3 → СН2 = СН–СОН → СН2 = СН–СН2ОН → СН2 – СН – СН2
акролеин аллил спирті | | | ОН ОН ОН
глицерин
Физикалық қасиеттері
Түссіз, дәмді сұйық, судан ауыр. Суда, спиртте жақсы ериді, эфирде ерімейді.
Гигроскопиялық, суды жақсы сіңіреді.
Химиялық қасиеттері
1. Лакмусқа бейтарап.
2. Этиленгликольге қарағанда қышқылдық қасиеті жоғары. Cu(ОН)2 көк түсті мыс (II) глицератын түзеді:

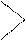 Н2С – О – Н Н – О Н2С – О
Н2С – О – Н Н – О Н2С – О
| \ | Cu
 НС – О – Н + Сu → НС – О + 2Н2О
НС – О – Н + Сu → НС – О + 2Н2О
| / |
Н2С – О – Н Н – О Н2С – О – Н
мыс глицераты
Бұл глицериннің де этиленгликольдің де сапалық реакциялары.
3. Нитрлеу реакциясы тән:
| Н2С – О – Н | НО | – NO2 | H2C – O – NO2 |
| | | H2SO4 | | ||
| HC – O – H | + HO | – NO2 | → HC – O – NO2 + 3H2O |
| | | | | ||
| H2C – O – H | HO | – NO2 | H2C – O – NO2 |
Нитроглицерин – қопарылғыш зат, ауыр сұйық, глицериннің үшнитраты.
4. Қаныққан және қанықпаған карбон қышқылдарымен күрделі эфирлер (майлар) түзеді:
|
|
|
О
\\
С – С17Н35
/ О
НО ||
Н2С – О – Н О Н2С – О – С – С17Н35
| \\ |
НС – О – Н + С – С17Н35 → НС – О – С – С17Н35
 | / ||
| / ||
Н2С – О – Н НО О
О Н2С – О – С – С17Н35
\\ ||
С – С17Н35 О
/ стеарин қышқылының глицериді
НО
стеарин қышқылы
5. Галогенсутектермен әрекеттеседі, реакция сатылап жүреді:
СН2 – СН – СН2 СН2 – СН – СН2
| | | + Н – Br → | | | ОН ОН ОН Br ОН ОН
1 – бромпропандиол
СН2 – СН – СН2 СН2 – СН – СН2
| | | + Н – Br → | | | Br ОН ОН Br Br ОН
1,2 – дибромпропанол
СН2 – СН – СН2 СН2 – СН – СН2
| | | + Н – Br → | | | Br Br ОН Br Br Br
|
|
|
1,2,3 – үшбромпропан
Қолданылуы
1) қопарылғыш зат алуда – үшнитроглицерин;
2) косметикада;
3) тері өндірісінде;
4) медицинада – нитроглицерин (жүрек дәрі–дәрмегі);
5) қағаз өндірісінде;
6) тағамдар өндірісінде.
4.2 Спирттер тақырыбына арналған есептер шығару әдістемелері
Есеп №1
Зат құрамы 52,18% – С; 13,04% – Н; 34,78% – О тұрады. Қалыпты жағдайда оның бу тығыздығы 2,05 г/л тең. Заттың молекулярлық формуласын анықтаңыз.
Шешуі:
1) заттың формуласы СХНYOZ деп белгілеп аламыз.
2) мольдік массасы:
M(CxHyOz)=ρ*V=2,05 г/л*22,4 г/л = 46 г/моль
3) элементтердің мольдік қатынасы:
n(C): n(H):n(O) = x:y:z


 52,18 : 13,04 : 34,78
52,18 : 13,04 : 34,78
= 4,35 : 13,04 :
2,17
= 2 : 6 : 1
12 1 16
4) формуласы: С2Н6О, оның молекулярлық массасы 46 г/моль.
Жауабы: С2Н6О
Есеп №2
Массасы 10,5 г этиленді көмірсутекті перманганаттың сулы ерітіндісімен өңдегенде 15,2 г екі атомды спирт түзілген. Түзілген спирт металдық натриймен әрекеттескенде 4,48 л (қ.ж.) газ бөлінеді. Спирттің құрылымымен, бірінші теңдеу бойынша шығымын анықтаңыз.
Шешуі:
1) этиленді көмірсутектің тотығуының реакциясын жазу керек:
3СnH2n + 2KMnO4 + 4H2O → 3CnH2n(OH)2 + 2MnO2 + 2KOH (1)
2) түзілген спирт натриймен келесі теңдік бойынша әрекеттеседі:
CnH2n(OH)2 + 2Na → CnH2n(ONa)2 + H2↑ (2)
3) 2-ші теңдіктен спирттің молекулярлық массасын анықтауға болады: 2-ші теңдік бойынша:
СnH2n(OH)2--------- Н2
1 моль------ 1 моль
х моль------ 0,2 моль
х = 0,2 моль
n (H2 ) =
4,48л

22,4л
= 0,2 моль ;
n (C n
H 2n
(O H )2
) = 15,2 ;
 Mr
Mr
Сонда:
0,2 = 15,2 ;
 Mr
Mr
M r (C n
H2n
(OH )2
) = 15,2 = 76 г / моль
 0,2
0,2
Mr(CnH2n(OH)2)=12n+2n+(16+1)*2=76 14n=76 – 34
14n=42
n=3 Сондықтан С3Н6(ОН)2 немесе СН2 – СН – СН3
| |
ОН ОН пропандиол – 1,2
4) өнім шығымын 1-ші теңдеу бойынша есептейді:
1- ші теңдеу бойынша:
n (C3 H6
) = 10,5 = 0,25 моль
 42
42
СnH2n-------------- СnH2n(OH)2
3 моль-------- 3 моль
0,25 моль--------- х моль
х = 0,25 моль Іс жүзінде 0,2 моль С3Н6(ОН)2 алынған.
Сондықтан: 0,25 моль------ 100 %
0,2 моль------- х
х = 80 %
Жауабы: пропандиол – 1,2; 80 %
Есеп №3
Массасы 1347,39 г құрамында 95 % таза кальций карбиді бар үлгіні сумен өңдеген. Бөлінген газды құрамында сынып (ІІ) сульфаты бар күкірт қышқылынан өткізген. Реакция нәтижесінде түзілген сұйықты никель катализаторы қатысында тотықсыздандырған. Өнім шығымы 80 % құрайды. Түзілген өнімнің массасын есептеңіз, егер оның құрамында таза қосылыстың массалық үлесі 95 % болса?
Шешуі:
1) есеп мазмұны бойынша жүйеде төмендегі реакциялар жүреді:
СаС2 + 2Н2О → Сa(OH)2 + C2H2 (1)
О
//
𝐻2𝑆𝑂4+𝐻𝑔2+
С2Н2 + H2O → СН3 – С (2)
\ Н
О
//
𝑁𝑖
СН3 – С + H2 → CH3 – CH2 – OH (3)
\ Н
Сонымен, 1 – 3 – ші теңдеулер бойынша:
1моль СаС2 – 1 моль С2Н2 – 1 моль СН3СОН – 1 моль СН3СН2ОН алынады.
2) есеп мазмұны бойынша реакцияға неше моль СаС2 қатысқанын есептеуге болады:
1347,39 г------ 100 %
х------ 95 %
 x = 1347,39 * 95 = 1280 г
x = 1347,39 * 95 = 1280 г
100
M(CaC2) = 64 г/моль
3) сонымен:
n (C aC2 )
= 1280 = 20моль
 64
64
1 моль СаС2 ----- 1 моль СН3СОН алынады 20 моль СаС2----------------------- х моль
x=n(C2H5OH)=n(C2H5OH) M(C2H5OH)=20*46 = 920 г
4) өнім шығымы 80 %, сондықтан:
100 ----- 80
920------ х
 x = 80 * 920
x = 80 * 920
100
= 736 г
5) ерітінді құрамында таза С2Н5ОН 95 %, сондықтан:
736 г----- 95 %
х----- 100 %
x = 736 * 100 = 774,7 г C H OH

Жауабы: 774,7 г
95 2 5
4.3 Өзіндік орындауға арналған есептер мен жаттығулар
1. Этанолды дегидратация нәтижесінде түзілген газ массасы 160 г 20% бром суын түзсіздендіреді. Этанолдың массасын анықтаңыз.
Жауабы: 9,2 г
2. Массасы 100 г бутил спиртін дегидраттау нәтижесінде массасы 50 г дибутилэфирі түзілген. Өнім шығымын есептеңіз.
3. Массасы 30 г органикалық зат жанғанда 33,6 л (қ.ж) көміртек (IV) оксиді және 36 г су түзілген. Осы қосылыстың буы 1,36 есе көміртек (IV) оксидінен ауыр. Қосылыстың формуласын табыңыз. Оның төрт изомерін жазып, атаңыз.
4. Массасы 60 г қанықққан спиртті тотықтырғанда 46,4 г кетон түзілген. Өнім шығымы 80%. Спирттің формуласын анықтап, құрылымдық формуласын жазып, атаңыз.
5. Массасы 45 г қаныққан спиртті сірке қышқылымен этерификациялағанда 53,55 г эфир түзілген. Өнім шығымы 70%. Бастапқы спирттің формуласын анықтап, реакция теңдеуін жазыңыз.
6. Массасы 9,6 г органикалық зат жанғанда 6,72 л (қ.ж) көміртек (IV) оксиді және 10,8 г су түзілген. Түзілген заттың буының сутек бойынша тығыздығы 16 тең. Бастапқы заттың формуласын анықтаңыз.
7. Массасы 23 г біратомды спирт молекулааралық дегидратталғанда массасы 3,6 г су түзілген. Өнім шығымы 80%. Спирттің формуласын анықтаңыз.
8. Біратомды спиртті тотықтыру нәтижесінде массасы 7,6 г түзілген қышқылды бейтараптау үшін 72 мл 10,1% тығыздығы 1,1 г/мл натрий гидроксиді ерітіндісі қажет. Осы қышқылдың формуласын анықтап, изомерлерінің құрылымдық формулаларын жазып, қайсысы қышқылға дейін тотығатынын көрсетіңіз.
9. Біріншілік біратомды спиртті натриймен өңдегенде 8,96 л (қ.ж) сутек бөлінген. Спирттің дәл осындай массасын дегидраттағанда массасы 33,6 г этиленді көмірсутек бөлінген. Спирттің формуласын анықтаңыз.
10. Массасы 76 г этанол мен пропанол-2 қоспасын натриймен өңдегенде 16,8 л (қ.ж) сутек бөлінген. Қоспа құрамындағы спирттердің м.ү. есептеңіз.
Жауабы: 45%,55%
11. Массасы 11 г этил және метил спирттері қоспасының буы құрамында 32 г мыс (ІІ) оксиді бар түтікшеден жіберілген. Түтікшедегі зат қоспасын 190,3 мл 5% тығыздығы 1,03 г/мл күкірт қышқылымен өңдеген. Қоспа құрамындағы спирттердің массалық үлестерін анықтаңыз.
Дата добавления: 2021-03-18; просмотров: 175; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
