Дифтерия уха, половых органов (анально-генитальная),кожи
Эти состояния встречают редко; обычно они развиваются в сочетании с диф терией зева или носа. Общие черты этих форм — отёк, гиперемия, инфильтра ция, фибринозный налёт в области поражения, регионарный лимфаденит.
•При дифтерии половых органов у мужчин процесс локализуется в области край ней плоти. У женщин он может стать распространённым и захватывать поло вые губы, влагалище, промежность и область заднего прохода, сопровождатьсясерозно-кровянистымивыделениями из влагалища, затруднённым и болезнен ным мочеиспусканием.
•Дифтерия кожи развивается в области ран, опрелостей, экземы, грибковых по ражений с трещинами кожи, где формируется налётгрязно-серогоцвета с се-розно-гнойнымотделяемым. Общетоксические явления при этом незначитель ны, однако местный процесс регрессирует медленно (до 1 мес и более).
Развитию этих форм способствуют травматизация участков слизистых оболо чек или кожи, занос возбудителей руками.
У лиц, перенёсших дифтерию или никогда ею не болевших, можно наблюдать бессимптомное носительство, длительность которого значительно варьирует. Фор мированию носительства способствуют сопутствующие хронические заболевания носоглотки. Антитоксический иммунитет не препятствует развитию носительства.
Дифференциальная диагностика
Локализованную и распространённую дифтерию ротоглотки дифференцируют с ангинами различной этиологии (кокковыми, ангиной Симановского—Венсана—Плаута,сифилитической, туляремийной и др.), инфекционным мононуклеозом, синдромом Бехчета, стоматитами. Её отличают умеренная интоксикация, бледность кожи, неяркая гиперемия ротоглотки, медленный регресс проявлений ангины при снижении температуры тела. При плёнчатом варианте значительно облегчает диагностику фибринозный характер налётов. Наиболее труден для дифференциальной диагностики островчатый вариант дифтерии ротоглотки, зачастую клинически не отличимый от ангин кокковой этиологии.
|
|
|
При постановке диагноза токсической дифтерии ротоглотки необходимо проводить дифференциальную диагностику с паратонзиллярным абсцессом, некротическими ангинами при заболеваниях крови, кандидозом, химическими и термическими ожогами полости рта. Для токсической дифтерии ротоглотки характерны быстро распространяющиеся фибринозные налёты, отёк слизистой оболочки ротоглотки и подкожной клетчатки шеи, выраженные и быстро прогрессирующие проявления интоксикации.
Дифтерийный круп дифференцируют от ложного крупа при кори, ОРВИ и других заболеваниях. Круп часто сочетается с дифтерией ротоглотки или носа, клинически проявляется в виде трёх последовательно развивающихся стадий: дисфонической, стенотической и асфиксической при умеренно выраженных явлениях интоксикации.
|
|
|
Лабораторная диагностика
В гемограмме при локализованной форме дифтерии отмечают умеренный, а при токсических формах — высокий лейкоцитоз, нейтрофилию со сдвигом лейкоцитарной формулы влево, нарастание СОЭ, прогрессирующую тромбоцитопению.
Основу лабораторной диагностики составляют бактериологические исследования: выделение возбудителя из очага воспаления, определение его типа и токсигенности. Материал отбирают стерильными ватными тампонами, сухими или смоченными (до стерилизации!) 5% раствором глицерина. При хранении и транспортировке тампоны предохраняют от охлаждения и высыхания. Материал дол жен быть посеян не позднее 2-4ч после взятия. У больных ангиной, бывших в контакте с больными дифтерией, а также у лиц с типичными клиническими про явлениями дифтерии диагноз ставят даже при отрицательном результате бактериологического исследования.
Вспомогательное значение имеет определение титров антитоксических AT в парных сыворотках при постановке РНГА. Токсинообразование выявляют, используя РНГА с антительным эритроцитарным диагностикумом. Для выявления дифтерийного токсина предложено использовать ПЦР.
|
|
|
Осложнения
К патогенетически обусловленным осложнениям дифтерии относят ИТШ, миокардиты, моно- и полиневриты, включая поражения черепных и периферических нервов, полирадикулоневропатию, поражения надпочечников, токсический нефроз.
Лечение
Все больные дифтерией или с подозрением на неё подлежат госпитализации. Сроки пребывания больных в стационаре и длительность постельного режима зависят от формы и тяжести заболевания. Основным в лечении дифтерии считают введение антитоксической противодифтерийной сыворотки. Она нейтрализует токсин, циркулирующий в крови, следовательно, оказывает наибольший эффект при раннем применении. При подозрении на токсическую форму дифтерии или дифтерийный круп сыворотку вводят немедленно, в остальных случаях возможно выжидание при постоянном наблюдении за больным в стационаре. У больных с локализованной формой дифтерии позже 4-годня болезни сыворотку стараются не применять, что, по современным данным, значительно сокращает возможность развития отдалённых осложнений заболевания. Положительные результаты кожной пробы (пробы Шика) — противопоказание к введению сыворотки лишь при локализованных формах, во всех остальных случаях в данной ситуации сыворотку необходимо вводить под прикрытием антигистаминных пре паратов и глюкокортикоидов.
|
|
|
Таблица 3-5.Дозы противодифтерийной сыворотки при различных клинических формах дифтерии
| Форма дифтерии | Доза сыворотки, тыс. ME | |
| Локализованная форма дифтерии | 15—30 | внутримышечно |
| ротоглотки, носа, половых органов, | ||
| глаз, кожи и др. | ||
| Распространённая дифтерия ротоглотки | 30—40 | внутримышечно |
| Субтоксическая дифтерия ротоглотки | 50—60 | внутримышечно |
| Токсическая дифтерия ротоглотки: | ||
| • I ст. тяжести | 60—80 | внутримышечно |
| • II ст. тяжести | 80—100внутримышечно и внутривенно | |
| • III ст. тяжести | 100—120внутримышечно и внутривенно | |
| • гипертоксическая | 120—150внутримышечно и внутривенно | |
| Круп локализованный | 15—20 | внутримышечно |
| Круп распространённый и нисходящий | 30—40 | внутримышечно |
Противодифтерийную сыворотку можно вводить как внутримышечно (чаще), так и внутривенно. Повторные введения сыворотки возможны при продолжающейся интоксикации. В настоящее время дозы сыворотки пересматривают как в сторону увеличения, так и в сторону уменьшения, в зависимости от формы дифтерии.
Проводят дезинтоксикационную терапию кристаллоидными и коллоидными растворами внутривенно (полиионные растворы, глюкозо-калиеваясмесь с добавлением инсулина, реополиглюкин, свежезамороженная плазма). В тяжёлых случаях к вводимым растворам добавляют глюкокортикоиды (преднизолон в дозе2-5мг/кг). Одновременно указанные капельные вливания способствуют коррекции гемодинамических нарушений. Применяют десенсибилизирующие препараты, витамины (аскорбиновую кислоту, витамины группы В и др.).
Токсическая дифтерия II и III степеней, гипертоксическая форма и тяжёлые комбинированные формы заболевания — показания к проведению плазмафереза. Разрабатывают новые эффективные пути детоксикации, такие как гемосорбция, аффинная сорбция, иммуносорбция.
При субтоксической и токсических формах рекомендовано назначение антибиотиков, оказывающих этиотропное воздействие на сопутствующую кокковую флору: пенициллина, эритромицина, а также ампициллина, ампиокса, препара тов тетрациклинового ряда и цефалоспоринов в средних терапевтических дозах.
При дифтерии гортани необходимы частые проветривания палаты, тёплое питьё, паровые ингаляции с ромашкой, содой, эвкалиптом, гидрокортизоном (125 мг на ингаляцию). Больным назначают эуфиллин, салуретики, антигиетаминные средства, при нарастании явлений стеноза — преднизолон внутривенно по 2-5мг/кг/сут. При явлениях гипоксии применяют увлажнённый кислород через носовой катетер, удаляют плёнки с помощью электроотсоса.
Грипп — острая респираторная антропонозная инфекция, вызываемая вирусами типов А, В и С, протекающая с развитием интоксикации и поражением эпителия слизистой оболочки верхних дыхательных путей, чаще трахеи. Заболевание склонно к быстрому и глобальному распространению.
Этиология
Возбудитель — РНК-геномныйвирус рода Influenzo virus семейства Orthomyxoviridae. Известно три типа вирусов — А, В, С. Тип вируса определяет набор внутренних Аг, проявляющих слабую иммуногенность. Вирусы гриппа типа А поражают человека, некоторые виды животных (лошадей, свиней и др.) и птиц. Вирусы гриппа типов В и С патогенны только для людей.
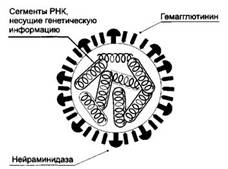
Поверхностные Аг вирусов гриппа — гемагглютинин и нейраминидаза. Они играют важную роль в формировании иммунного ответа организма при гриппе и позволяют разделить вирус гриппа типа А на подтипы H1N1, H3N2 и др. Вирус типа А обладает наиболее выраженными вирулентными свойствами и склонен к эпидемическому распространению.
Особенность вирусов гриппа — их способность к антигенной изменчивости. Она может реализовываться путём «дрейфа» (частичная изменчивость антигенных детерминант) или «шифта» (полное замещение фрагмента генома, кодирующего синтез гемагглютинина или нейраминидазы). Наиболее часто «дрейф» происходит у вируса гриппа типа А, но встречается и у типа В. Антигенный «шифт» — специфическая особенность вируса гриппа типа А, приводящая к появлению его новых подтипов. Высокая изменчивость вирусов гриппа объясняет непредсказуемость эпидемий заболевания. Вирус типа С менее изменчив и вызывает лишь небольшие эпидемические вспышки.
Вирус гриппа может сохраняться при температуре 4 °С в течение 2—3нед, прогревание при температуре50-60°С вызывает инактивацию вируса в течение не скольких минут, дезинфектанты быстро инактивируют вирус.
Эпидемиология
Резервуар и источник инфекции — человек с явными и стёртыми формами болезни. Эпидемиологическую опасность больного человека определяют количество вирусов в отделяемом верхних дыхательных путей и выраженность катарального синдрома. Контагиозность максимальна в первые5—6дней болезни. Длительное выделение вируса наблюдают у немногих больных с тяжёлым или осложнённым течением заболевания. Наличие и эпидемиологическое значение скрытого вирусоносительства при гриппе не доказаны. Вирус серотипа А выделен также от свиней, лошадей и птиц. Возможность спорадического заражения человека вирусом гриппа животных неоднократно чётко документировали в отношении вируса гриппа свиней в США и во время локальной вспышки, вызванной «куриным» вирусом гриппа A (H5NI) в Гонконге в 1997 г. В настоящее время существует предположение о роли перелётных птиц в эпидемическом процессе гриппа. Возможно, что при эпизоотии гриппа среди птиц, реже млекопитающих (свиней, лошадей и др.) формируются новые антигенные варианты вируса, поражающие затем человека.
Механизм передачи — аэрозольный, путь передачи — воздушно-капельный. Вирус выделяется с каплями слюны, слизи и мокроты при дыхании, разговоре, плаче, кашле и чихании. Сохранение вируса гриппа в воздушной среде зависит от степени дисперсности аэрозоля, содержащего вирусные частицы, а также от воздействия на него света, влаги и нагревания. Не исключена возможность инфицирования бытовым путём через инфицированные предметы обихода.
Естественная восприимчивость людей высокая, но имеет индивидуальные колебания; восприимчивость к новым серотипам возбудителя особенно выражена. Материнские противогриппозные AT выявляют у детей, находящихся на естественном вскармливании, до9-10-гмесяца, а у находящихся на искусственном — только до2—3мес. Однако они не в состоянии предохранить от заболевания. При вспышках гриппа в родильных домах новорождённые заболевают чаще и болеют тяжелее, чем их матери. Постинфекционный иммунитет при гриппе, вызванном вирусом типа А, длится 1—3года, а вирусом типа В —3—4года. Формирующаяся клеточная иммунологическая память, особенно после повторного контакта с тем или иным подтипом вируса гриппа, сохраняется длительное время.
Основные эпидемиологические признаки. Болезнь распространена повсеместно и проявляется в виде вспышек и эпидемий, охватывающих значительную часть восприимчивого населения, что представляет серьёзную социальную и медицинскую проблему. На долю гриппа и ОРВИ приходится90—95%всех заболеваний инфекционной природы. Периодически (через каждые2—3года) возникают пандемии гриппа, связанные с формированием новых антигенных вариантов вируса. Главным образом это касается вируса гриппа А. Заболевания регистрируют в течение всего года, они значительно учащаются в осенне-зимний период, чему способствуют скученность населения и влияние климатических факторов. За последнее десятилетие в Российской Федерации ежегодно регистрируют от 27,3 до 41,2 млн заболевших этими инфекциями. Смертность от самого гриппа невелика, однако смертность от гриппа, других ОРВИ и острой пневмонии, являющейся наиболее частым и опасным постгриппозным осложнением. Экономические потери от гриппа составляют миллиарды рублей только за одну эпидемию.
Быстрому распространению гриппа способствуют короткий инкубационный период, аэрогенный путь передачи, высокая восприимчивость людей к гриппу, а также социальные условия жизни населения, в первую очередь характер современных транспортных средств, обеспечивающих быстрое передвижение населения и тесный контакт не только между соседними странами, но и между континентами.
Патогенез
После аэрогенного попадания на слизистые оболочки проводящих дыхательных путей (гортани, трахеи и бронхов) вирус гриппа, отличающийся эпителиотропностью, размножается в клетках однослойного многорядного эпителия (рис. 3-11).Под действием нейраминидазы вируса оголяются базальные клеточные мембраны,

развиваются явления дегенерации в цитоплазме и ядрах поражённых эпителиоцитов, заканчивающиеся некрозом и отторжением клеток. Эти процессы облегчают накопление различных бактерий в слизистой оболочке носоглотки и бронхов и способствуют присоединению вторичных бактериальных инфекций, усиливающих воспалительные и аллергические реакции. Воспалительные изменения слизистой оболочки развиваются по типу «сухого катара» без выраженных продуктивных реакций. Воспаление активизируется вследствие макрофагальных процессов, направленных на локализацию и уничтожение вируса, но сопровождающихся гибелью макрофагов. Факторы внешней среды (например, переохлаждение) способствуют нарушению функций обкладочных (слизистых и бокаловидных) клеток.
Вирус быстро репродуцируется, что объясняет непродолжительность инкубационного периода при гриппе.
Поражение лёгочных альвеол не характерно для гриппа, чаще его наблюдают у детей вследствие возрастных особенностей строения органов дыхания (короткие гортань и трахея), пожилых людей и лиц с иммунодефицитными состояниями. Разрушение базальных мембран альвеол лежит в основе возможного развития тромбогеморрагического синдрома (геморрагического отёка лёгких).
Вместе с тем на уровне слизистой оболочки дыхательных путей включаются процессы, препятствующие дальнейшему распространению вируса: синтез ИФН инфицированными клетками, накопление секреторных IgA и неспецифических термолабильных В-ингибиторов. Борьбе макроорганизма с возбудителем способствует лихорадочная реакция, повышающая активность синтеза AT и ИФН, а так же Т-киллеров, уничтожающих поражённые вирусом клетки.
Преодолевая указанные защитные барьеры, вирус проникает в кровь. Вирусемия начинается ещё в инкубационный период и длится от нескольких дней до 2 нед. Вирус не обладает собственными токсинами, поэтому интоксикация при гриппе обусловлена в первую очередь накоплением эндогенных биологически активных веществ (ПГЕ2, серотонина, гистамина). Воздействие гемагглютинина вируса проявляется поражением эритроцитов, активизацией внутрисосудистого тромбообразования с развитием ДВС-синдрома.
Развитие синдрома интоксикации и токсико-аллергическихреакций, воздействие гемагглютинина возбудителя и накапливающихся при распаде клеток биологически активных веществ приводят к нарушениям реологических свойств крови, а в некоторых случаях — к развитию ИТШ. Возможно гематогенное проникновение вирусов в различные органы и системы: сердце, почки, мышцы, ЦНС. Расстройства микроциркуляции, а также электролитного баланса и КЩС в этих органах могут лежать в основе развития отёка мозга и лёгких, дистрофических изменений в миокарде. Нарушения церебральной гемодинамики с явлениями отёка в различных отделах ткани мозга ведут к расстройствам деятельности ЦНС, вегетативной нервной системы и опосредованным нарушениям других систем организма (сердечно-сосудистой,эндокринной и т.д.).
Клиническая картина
Инкубационный период короткий — от нескольких часов до 3 дней. Заболевание может протекать в виде лёгких, среднетяжёлых и тяжёлых вариантов неосложнённой формы либо приобретать осложнённое течение. В клинической картине неосложнённого гриппа выделяют три ведущих синдрома: интоксикационный, катаральный и геморрагический.
Интоксикационный синдром является ведущим и характеризуется острым началом заболевания, быстрым (в течение нескольких часов) повышением температуры тела от субфебрильной до 40 °С и выше, сопровождающимся ознобом. Больные жалуются на головную боль, преимущественно в лобно-орбитальной области, выраженную общую слабость, разбитость и недомогание. Нередко отмечают миалгии, развивающиеся вследствие нарушений микроциркуляции и обменных процессов в мышцах, а также артралгии и головокружение. Также возможны обморочные состояния и судорожный синдром (чаще у детей).
Интенсивность головной боли варьирует от умеренной (у пожилых лиц часто диффузной) до резкой, сочетающейся с бессонницей, галлюцинациями, много кратной рвотой. Лихорадка достигает максимума через 1 сут от начала заболевания, на 2—4-йдень болезни может снижаться, иногда она носит двухволновой характер с последующим резким повторным повышением и нормализацией на5-йдень болезни.
Развиваются гиперемия лица и конъюнктив, склерит, возможно «обмётывание» губ в результате активации герпетической инфекции. Кожные покровы горячие, сухие. В результате диффузного поражения миокарда и его гипоксии тоны сердца становятся приглушёнными, иногда прослушивается систолический шум на верхушке сердца. Возникает тахикардия или нормокардия (иногда брадикардия). Наблюдают склонность к артериальной гипотензии.
Катаральный синдром развивается несколько позже, в ряде случаев он выражен слабо или отсутствует. Присоединяются жалобы на сухость, першение в горле и болезненность в носоглотке, заложенность носа. Отмечают застойную гиперемию, сухость, набухание и отёк слизистой оболочки носоглотки. Носовое дыхание затруднено; в первые дни болезни отделяемое скудное или вообще отсутствует, в последующем появляются серозные, слизистые или сукровичные выделения из носа. Характерны ларинготрахеит и бронхит, проявляющиеся саднением и болью за грудиной, учащением дыхания, сухим кашлем, нарастающим по интенсивности. Во время кашля возможны рвота и сильные мышечные боли в верхних отделах живота и подреберьях.
Геморрагический синдром проявляется лишь в 5—10%случаев. На фоне гиперемированной, с цианотичным оттенком, зернистой слизистой оболочки ротоглотки возможны точечные кровоизлияния. В некоторых случаях отмечают носовые кровотечения.
Длительность заболевания обычно не превышает 3-5дней, хотя выраженная астения может сохраняться значительно дольше.
Лабораторная диагностика
Возможно вирусологическое выделение вируса из отделяемого носоглотки, бронхов и трахеи, однако на практике его не проводят. Экспресс-диагностику выполняют с помощью реакции непрямой иммунофлюоресценции (РНИФ), а также ИФА, выявляющего Аг вируса в мазках, взятых со слизистой оболочки нижних носовых раковин. При этом применяют диагностические сыворотки только против данного штамма вируса.
Ретроспективную серологическую диагностику проводят с помощью РТГА, РСК, РНГА, ИФА. Реакции ставят с парными сыворотками, взятыми на 4—5-йдень болезни и через5—7сут после этого. Диагностическим считается нарастание титров AT не менее чем в 4 раза.
Осложнения
Осложнения гриппа многочисленны и могут быть разделены на две категории — ранние, патогенетически обусловленные, и осложнения, вызванные вторичной бактериальной флорой. Тяжёлые и осложнённые формы могут возникать у всех людей, но особенно характерны для детей, а также пожилых лиц, страдающих хроническими заболеваниями лёгких и сердечно-сосудистойсистемы.
Лечение
Необходимо обеспечить больному постельный режим в течение всего лихорадочного периода, полноценное питание и обильное питье (чай, соки, молоко, отвары шиповника и липового цвета). Как средство этиотропной терапии назначают ремантадин: в первый день по 100 мг 3 раза в день, во 2-йи3-йдни — по 100 мг 2 раза в день. Ремантадин противопоказан детям до 14 лет, беременным, лицам с острыми или обострившимися хроническими заболеваниями печени и почек. Может быть применён озельтамивир, обладающий антинейраминидазной активностью (по 75 мг 2 раза в сутки курсом 5 дней). Оба препарата эффективны при их назначении не позднее первых 2 дней болезни.
Антибактериальные препараты (антибиотики широкого спектра действия) при гриппе назначают лицам пожилого возраста с хроническими заболеваниями дыхательной системы, а также больным с иммунодефицитами. Во всех остальных случаях лёгкого и среднетяжёлого неосложнённого гриппа они не показаны.
Патогенетическая терапия включает назначение аскорбиновой кислоты, ру тина, глюконата кальция, антигистаминных препаратов в обычных терапевти ческих дозах. Жаропонижающие средства рекомендуют лишь при повышении температуры тела более 38,5 °С, применение аспирина в этих случаях требует ос торожности из-завозможности развития астматического компонента, а также синдрома Рея у детей.
Тяжёлые формы гриппа требуют расширения патогенетической терапии. Для дезинтоксикации применяют внутривенные капельные инфузий реополиглюкина или гемодеза в дозе 200-400мл, поляризующих смесей(1-1,5л). К вводимому раствору добавляют 2,4% раствор эуфиллина(5-10мл), 5% раствор аскорбино вой кислоты(10-15мл), 1% раствор димедрола (1 мл), 40 мг фуросемида. При начинающемся отёке мозга или лёгких дозу фуросемида увеличивают до40—60мг, внутривенно вводят преднизолон (300 мг/сут и более). Дозы препаратов зависят от выраженности отёка мозга или лёгких, степени ИТШ. При сердечной недоста точности назначают 10% раствор сульфокамфокаина, панангин, кокарбоксилазу.
Инфекционный мононуклеоз — острое антропонозное вирусное инфекционное заболевание с лихорадкой, поражением ротоглотки, лимфатических узлов, печени и селезёнки и специфическими изменениями гемограммы.
Этиология
Возбудитель — ДНК-геномныйвирус рода Lymphocryptovirus подсемейства Gammaherpesvirinae семейства Herpesviridae. Вирус способен реплицироваться, в том числе в В-лимфоцитах;в отличие от других вирусов герпеса он не вызывает гибели клеток, а напротив, активирует их пролиферацию. Вирионы включают специфические Аг: капсидный (VCA), ядерный (EBNA), ранний (ЕА) и мембранный (МА) Аг. Каждый из них образуется в определённой последовательности и индуцирует синтез соответствующих AT. В крови больных инфекционным мононуклеозом сначала появляются AT к капсидному Аг, позднее вырабатываются AT к ЕА и МА. Возбудитель малоустойчив во внешней среде и быстро гибнет при высыхании, под действием высокой температуры и дезинфектантов.
Инфекционный мононуклеоз — только одна из форм инфекции вирусом Эпштайна-Барр, который также вызывает лимфому Бёркитта и носоглоточную карциному. Его роль в патогенезе ряда других патологических состояний недостаточно изучена.
Эпидемиология
Резервуар и источник инфекции — человек с манифестной или стёртой формой болезни, а также носитель возбудителя. Инфицированные лица выделяют вирус с последних дней инкубации и на протяжении 6-18мес после первичной инфекции. В смывах из ротоглотки у15-25%серопозитивных здоровых людей также обнаруживают вирус. Эпидемический процесс поддерживают лица, ранее перенёсшие инфекцию и на протяжении долгого времени выделяющие возбудитель со слюной.
Механизм передачи — аэрозольный, путь передачи —воздушно-капельный. Очень часто вирус выделяется со слюной, поэтому возможно заражение контактным путём (при поцелуях, половым путём, через руки, игрушки и предметы оби хода). Возможна передача инфекции при переливаниях крови, а также во время родов.
Естественная восприимчивость людей высокая, однако преобладают лёгкие и стёртые формы болезни. О наличии врождённого пассивного иммунитета может свидетельствовать крайне низкая заболеваемость детей первого года жизни. Иммунодефицитные состояния способствуют генерализации инфекции.
Основные эпидемиологические признаки. Заболевание распространено повсеместно; в основном регистрируют спорадические случаи, иногда — небольшие вспышки.
К30—35годам у большинства людей в крови выявляют AT к вирусу инфекционного мононуклеоза, поэтому клинически выраженные формы редко встречают среди взрослых. Заболевания регистрируют на протяжении всего года, несколько реже — в летние месяцы. Заражению способствуют скученность, пользование общим бельём, посудой, тесные бытовые контакты.
Патогенез
Проникновение вируса в верхние отделы дыхательных путей приводит к поражению эпителия и лимфоидной ткани рото- и носоглотки. Отмечают отёк слизистой оболочки, увеличение миндалин и регионарных лимфатических узлов. При последующей вирусемии возбудитель внедряется в В-лимфоциты; находясь в их цитоплазме, он диссеминирует по всему организму. Распространение вируса приводит к системной гиперплазии лимфоидной и ретикулярной тканей, в связи с чем в периферической крови появляются атипичные мононуклеары. Развиваются лимфаденопатия, отёк слизистой оболочки носовых раковин и ротоглотки, увеличиваются печень и селезёнка. Гистологически выявляют гиперплазию лимфоретикулярной ткани во всех органах, лимфоцитарную перипортальную инфильтрацию печени с незначительными дистрофическими изменениями гепатоцитов.
Репликация вируса в В-лимфоцитах стимулирует их активную пролиферацию и дифференцировку в плазмоциты. Последние секретируют иммуноглобулины низкой специфичности. Одновременно в острый период заболевания нарастают количество и активностьТ-лимфоцитов. Т-супрессоры сдерживают пролиферацию и дифференцировку В-лимфоцитов. Цитотоксические Т-лимфоциты уничтожают инфицированные вирусом клетки, распознавая мембранные вирус-индуцированные Аг. Однако вирус остаётся в организме и персистирует в нём в течение всей последующей жизни, обусловливая хроническое течение заболевания с ре активацией инфекции при снижении иммунитета.
Выраженность иммунологических реакций при инфекционном мононуклеозе позволяет считать его болезнью иммунной системы, поэтому его относят к группе заболеваний СПИД-ассоциированного комплекса.
Клиническая картина
Инкубационный период варьирует от 5 дней до 1,5 мес. Возможен продромальный период, не имеющий специфической симптоматики. В этих случаях заболевание развивается постепенно: в течение нескольких дней наблюдают субфебрильную температуру тела, недомогание, слабость, повышенную утомляемость, катаральные явления в верхних дыхательных путях — заложенность носа, гиперемию слизистой оболочки ротоглотки, увеличение и гиперемию миндалин.
При остром начале заболевания температура тела быстро поднимается до высоких цифр. Больные жалуются на головную боль, боли в горле при глотании, озноб, усиленное потоотделение, ломоту в теле. В дальнейшем температурная кривая может быть различной; длительность лихорадки варьирует от нескольких дней до 1 мес и более.
К концу первой недели заболевания развивается период разгара болезни. Характерно появление всех основных клинических синдромов: общетоксических явлений, ангины, лимфаденопатии, гепатолиенального синдрома. Самочувствие больного ухудшается, отмечают высокую температуру тела, озноб, головную боль и ломоту в теле. Могут появиться заложенность носа с затруднением носового дыхания, гнусавость голоса. Поражения зева проявляются нарастанием боли в горле, развитием ангины в катаральной, язвенно-некротической,фолликулярной или плёнчатой форме. Гиперемия слизистой оболочки выражена нерезко, на миндалинах появляются рыхлые желтоватые легко снимающиеся налёты. В некоторых случаях налёты могут напоминать дифтерийные. На слизистой оболочке мягкого нёба возможно появление геморрагических элементов, задняя стенка глотки резко гиперемированная, разрыхлённая, зернистая, с гиперплазированными фолликулами.
С первых же дней развивается лимфаденопатия. Увеличенные лимфатические узлы можно обнаружить во всех доступных пальпации областях; характерна симметричность их поражения. Наиболее часто при мононуклеозе увеличиваются затылочные, подчелюстные и особенно заднешейные лимфатические узлы с обе их сторон по ходу грудиноключично-сосцевидных мышц. Лимфатические узлы уплотнены, подвижны, при пальпации безболезненны или болезненны незначительно. Их размеры варьируют от горошины до грецкого ореха. Подкожная клетчатка вокруг лимфатических узлов в некоторых случаях может быть отёчной.
У большинства больных в период разгара заболевания отмечают увеличение печени и селезёнки. В некоторых случаях развивается желтушный синдром: усиливаются диспептические явления (снижение аппетита, тошнота), темнеет моча, появляется иктеричность склер и кожи, в сыворотке крови нарастает содержание билирубина и повышается активность аминотрансфераз.
Иногда появляется экзантема пятнисто-папулёзного характера.
Вслед за периодом разгара заболевания, продолжающимся в среднем 2—3нед, наступаетпериод реконвалесценции. Самочувствие больного улучшается, норма лизуется температура тела, постепенно исчезают ангина и гепатолиенальный син дром, В дальнейшем нормализуются размеры лимфатических узлов. Длительность периода реконвалесценции индивидуальна, иногда субфебрильная температура тела и лимфаденопатия сохраняются в течение нескольких недель.
Заболевание может протекать длительно, со сменой периодов обострений и ремиссий, из-за чего его общая продолжительность может затягиваться до 1,5 лет.
Лабораторная диагностика
Наиболее характерный признак — изменения клеточного состава крови. В гемограмме выявляют умеренный лейкоцитоз, относительную нейтропению со сдвигом лейкоцитарной формулы влево, значительное увеличение количества лимфоцитов и моноцитов (суммарно более 60%). В крови присутствуют атипичные мононуклеары — клетки с широкой базофильной цитоплазмой, имеющие различную форму. Их наличие в крови определило современное название болезни. Диагностическое значение имеет увеличение количества атипичных мононуклеаров с широкой цитоплазмой не менее чем до 10—12%,хотя число этих клеток может достигать80—90%.Следует заметить, что отсутствие атипичных мононуклеаров при характерных клинических проявлениях заболевания не противоречит предполагаемому диагнозу, поскольку их появление в периферической крови может задерживаться до конца2—3-йнедели болезни.
В период реконвалесценции количество нейтрофилов, лимфоцитов и моноцитов постепенно нормализуется, однако довольно часто длительно сохраняются атипичные мононуклеары.
Вирусологические методы диагностики (выделение вируса из ротоглотки) на практике не применяют. Методом ПЦР можно выявлять вирусную ДНК в цель ной крови и сыворотке.
Разработаны серологические методы определения AT различных классов к капсидным (VCA) Аг. Сывороточные IgM к VCA-Arможно обнаружить уже в инкубационный период; в дальнейшем их выявляют у всех больных (это служит достоверным подтверждением диагноза). Исчезают IgM кVCA-Arлишь через2-3мес после выздоровления. После перенесённого заболевания пожизненно сохраня ются IgG кVCA-Ar.
При отсутствии возможности определения анти-VCA-IgMдо сих пор применяют серологические методы обнаружения гетерофильных AT. Они образуются в результате поликлональной активацииВ-лимфоцитов. Наиболее популярны реакция Пауля—Буннеляс эритроцитами барана (диагностический титр 1:32) и более чувствительная реакция Гоффа—Бауэрас эритроцитами лошади. Недостаточная специфичность реакций снижает их диагностическую ценность.
Всем больным с инфекционным мононуклеозом или при подозрении на него нужно проводить 3-кратное(в острый период, затем через 3 и 6 мес) лаборатор ное обследование на AT к Аг ВИЧ, поскольку в стадию первичных проявлений ВИЧ-инфекции также возможен мононуклеозоподобный синдром.
Осложнения
Наиболее частое осложнение — присоединение бактериальных инфекций, вызванных золотистым стафилококком, стрептококками и др. Также возможны менингоэнцефалит, обструкция верхних отделов респираторного тракта увеличенными миндалинами. В редких случаях отмечают двустороннюю интерстициальную инфильтрацию лёгких с тяжёлой гипоксией, тяжёлый гепатит (у детей), тромбоцитопению, разрывы селезёнки. В большинстве случаев прогноз заболе вания благоприятный.
Лечение
Больных лёгкими и среднетяжёлыми формами инфекционного мононуклеоза можно лечить на дому. Необходимость постельного режима определяется выра женностью интоксикации. В случаях заболевания с проявлениями гепатита ре комендуют диету (стол №5).
Специфическая терапия не разработана. Проводят дезинтоксикационную терапию, десенсибилизирующее, симптоматическое и общеукрепляющее ле чение, полоскания ротоглотки растворами антисептиков. Антибиотики при от сутствии бактериальных осложнений не назначают. При гипертоксическом тече нии заболевания, а также при угрозе асфиксии, обусловленной отёком глотки и выраженным увеличением миндалин, назначают короткий курс лечения глюкокортикоидами (преднизолон внутрь в суточной дозе 1 — 1,5 мг/кг в течение 3-4дней).
Менингококковая инфекция
Антропонозное острое инфекционное заболевание, протекающее в виде назофарингита, менингококцемии и гнойного менингита, реже — с поражением других органов и систем.
Этиология
Возбудитель — неподвижная грамотрицательная бактерия Neisseria meningitidis. Для возбудителя характерна морфологическая изменчивость; в типичных случаях в препаратах он выглядит как диплококк, располагающийся в виде «кофейных зёрен». Менингококки растут на питательных средах, содержащих нативные белки (кровь, сыворотки и др.), склонны к образованию L-форм. На основании группоспецифических Аг бактерии разделяют на серологические группы (А, В, С, D, N, X, Y, Z,W-135и др.), но только три из них — А, В и С — ответственны за развитие более чем 90% генерализованных форм менингококковой инфекции. Штам мы серогруппы А вызывают эпидемические вспышки, В, С и Y — спорадические случаи заболевания. Однако в последние годы отмечены вспышки и эпидемии, обусловленные возбудителями этих серогрупп. Основной фактор агрессии возбудителя —ЛПС-комплекс(эндотоксин).
Возбудитель малоустойчив к воздействию факторов внешней среды: вне организма быстро погибает при высыхании, охлаждении ниже 22 °С, при 55 °С погибает через 5 мин. Под действием 0,01% раствора хлорамина, 1% раствора фенола и 0,1% раствора перекиси водорода инактивируется через 2—3мин.
Э п и д еми о л о ги я
Резервуар и источник инфекции — человек с генерализованной формой, ост рым назофарингитом, а также «здоровый» носитель. Животные не восприимчивы к менингококкам. Носительство менингококков распространено довольно широко и подвержено колебаниям. Соотношение между больными и носителями не постоянно (по разным данным, от 1:2000 до 1:50 000). В периоды спорадической заболеваемости1—3%населения бывают носителями менингококка, в эпидемических очагах — до20—30%.Длительность носительства составляет2—3нед. Более длительное носительство связано, как правило, с хроническими воспалительными поражениями носоглотки. Больные генерализованной формой менингококковой инфекции — источники заведомо вирулентных штаммов возбудителя, но в связи с их малочисленностью и быстрой госпитализацией из-за тяжёлого состояния их эпидемиологическая роль невелика. Роль «здоровых» носителей менинго кокков как источников инфекции, безусловно, меньше, чем больных, но в силуих массовости именно носители имеют большое значение в распространении заболевания и поддержании эпидемического процесса. Важную роль в качестве ис точников инфекции играют также больные менингококковым. назофарингитом.
Механизм передачи — аэрозольный. Возбудитель передаётся с капельками слизи при кашле, чихании, разговоре. Вследствие нестойкости менингококка во внешней среде и его локализации на слизистой оболочке задней стенки носоглотки он передаётся при достаточно тесном и длительном общении. В отличие от других инфекций дыхательных путей распространение эпидемии менингококковой инфекции на различные территории происходит медленно. Заражению способствуют скученность, длительное общение, особенно в спальных помещениях, нарушения режима температуры и влажности.
Естественная восприимчивость людей высокая, но исход заражения определяют как свойства возбудителя (вирулентность), так и резистентность макроорганизма. Как уже отмечалось, генерализация процесса происходит у весьма незначительного количества инфицированных лиц. Иммунологическую структуру населения формируют заболеваемость и носительство возбудителя. После перенесённой болезни сохраняется длительный иммунитет. Повторные заболевания отмечают у лиц с врождённым дефицитом компонентов комплементаС7—С9.
Основные эпидемиологические признаки. Болезнь распространена повсеместно.
Заболевание поражает преимущественно городское население. Менингококковую инфекцию регистрируют во всех возрастных группах: от первых дней жизни до преклонного возраста. Тем не менее это типичная «детская» инфекция. Дети до 5 лет составляют более 70% всех больных. Самые высокие показатели заболеваемости сохраняются у детей до 1 года.
Менингококковая инфекция имеет низкую очаговость: до 95% составляют очаги с одним заболеванием. Вспышки могут возникать в организованных коллективах детей и взрослых, что в значительной мере обусловлено социальными факторами (период обучения, проживание в общежитии, служба в армии и т.д.). Эти же обстоятельства объясняют факт преобладания среди заболевших лиц мужского пола. В странах с умеренным климатом в межэпидемический период характерна зимне-весенняя сезонность заболеваемости с максимумом в феврале марте. Во время эпидемических подъёмов пик заболеваемости смещается на март—май, причём в крупных городах в сентябре во время формирования детских коллективов наблюдают небольшой подъём заболеваемости.
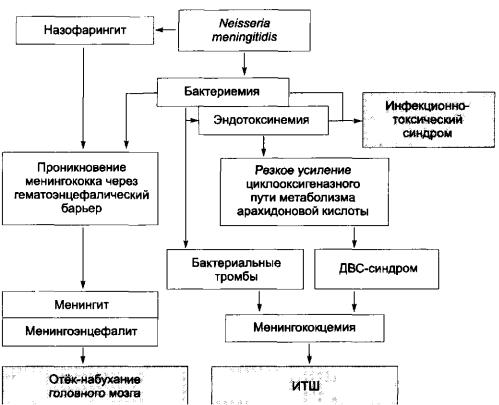
К линическая картина
В соответствии с общепринятой клинической классификацией менингококковой инфекции выделяют следующие её формы.
•Первично-локализованныеформы:
—менингококковыделительство;
—острый назофарингит;
—пневмония.
•Гематогенно-генерализованныеформы:
—менингококцемия:
•типичная;
•молниеносная;
•хроническая;
—менингит;
—менингоэнцефалит;
—смешанная форма (менингококцемия + менингит);
—редкие формы (эндокардит, артрит, иридоциклит).
Выделителей менингококка обычно обнаруживают при массовом обследовании в очаге менингококковой инфекции, а также случайно при взятии мазков со слизистой оболочки носоглотки. Клинически выявить носителей невозможно изза отсутствия каких-либосимптомов.
Острый назофарингит
Среди всех клинических форм менингококковой инфекции наиболее часто встречают острый назофарингит. Клиническая расшифровка менингококкового назофарингита чрезвычайно затруднена из-за сходства симптоматики с назофарингитами другой этиологии.
Инкубационный период при этой форме варьирует в пределах 1—10дней, но чаще составляет3—5сут. Обычно заболевание начинается достаточно остро, боль ные жалуются на кашель, першение и боли в горле, заложенность носа и насморк сослизисто-гнойнымотделяемым. Катаральные явления сопровождают голов ная боль и повышение температуры тела от субфебрильных до высоких величин. В некоторых случаях возможны боли в суставах.
Лицо больного обычно бледное, при осмотре выявляют гиперемию миндалин, мягкого нёба и дужек. Достаточно характерны гиперемия и зернистость задней стенки глотки, покрытой слизисто-гнойнымотделяемым. В некоторых случаях пальпируют несколько увеличенные и болезненные подчелюстные лимфатичес кие узлы. Характерна тахикардия.
Заболевание продолжается не более 1—3дней, хотя иногда гиперплазия фолликулов может сохраняться1—2нед. В подавляющем большинстве слу чаев заболевание заканчивается полным выздоровлением. Однако следует обратить внимание, что иногда эта форма может приобретать достаточно тя жёлое течение с развитием выраженного синдрома интоксикации: резкой головной болью, выраженной температурной реакцией, кратковременной менингеальной симптоматикой и мимолётными геморрагическими высыпаниями на коже.
Менингококковая пневмония
Менингококковую пневмонию встречают крайне редко; она может быть оча говой или долевой, обычно с тяжёлым течением. Этиологическая диагностика возможна только при обнаружении возбудителя в мокроте.
Менингококцемия (менингококковый сепсис)
В большинстве случаев менингококцемия развивается после предшествовав шего назофарингита, иногда — на фоне полного здоровья. Острое начало заболе вания проявляется ознобом и повышением температуры тела, достигающей за несколько часов 40—41°С, головной болью, неукротимой рвотой, болями в мыш цах спины и конечностей.
При осмотре больного отмечают бледность лица с цианотичным оттенком, одышку, тахикардию. Выражена склонность к значительному снижению АД; мож но наблюдать явления коллапса. Очень рано развивается олигурия или анурия, в моче повышается количество белка, лейкоцитов и эритроцитов, также появля ются цилиндры. В крови нарастают показатели креатинина и мочевины.
Опорный клинический признак, наводящий на мысль о менингококцемии, — экзантема (рис 8, см. цв. вклейку). Она обычно появляется в первые сутки забо левания (в течение 5-15ч от начала болезни), реже высыпания образуются на2-есутки. Сыпь чаще располагается на ягодицах, нижних конечностях, в подмы шечных впадинах, на верхних веках и имеет тенденцию к слиянию. Типичные геморрагические элементы различной величины имеют неправильные очертания звёздчатого характера, плотные на ощупь. Чем больше выражены бактериемия и интоксикация, тем многочисленнее и крупнее элементы сыпи. В этих случаях экзантема может принять генерализованный характер, располагаясь на любом участке тела; крупные элементы сыпи подвергаются некрозу. При их обратном развитии могут образовыватьсяязвенно-некротическиеповерхности на ушных раковинах, кончике носа, дистальных отделах конечностей.
Геморрагический синдром при менингококцемии проявляется кровоизлия ниями на конъюнктивах, склерах и слизистой оболочке ротоглотки. При более тяжёлом течении развиваются носовые, желудочные, почечные и маточные кро вотечения.
Уже на ранних сроках болезни могут появиться признаки поражения суставов; при этом в первые дни заболевания обычно возникают поражения мелких суста вов кисти, а на 2-йнеделе болезни — крупных суставов. Суставная жидкость мо жет носитьсерозно-гнойныйхарактер, однако выделить из неё возбудитель, как правило, не удаётся. В более тяжёлых и запущенных случаях экссудат носит гной ный характер, в нём обнаруживают менингококки.
Отличительная черта менингококцемии, позволяющая проводить клиничес кую дифференциальную диагностику с другими септическими состояниями, — отсутствие гепатолиенального синдрома.
Тяжёлое проявление менингококцемии, нередко с летальным исходом, — молниеносная форма, характеризующаяся развитием ИТШ уже в первые часы за болевания.
Хроническое течение менингококцемии наблюдают редко. Характерны длитель ная интермиттирующая лихорадка, полиморфные высыпания на коже, артриты и полиартриты, развитие гепатолиенального синдрома.
Менингококковый менингит
Менингококковый менингит, так же как и менингококцемия, чаще развива ется после клинических проявлений назофарингита. Заболевание начинается ос тро с подъёма температуры тела до высоких значений и развития общемозговых симптомов — резкой мучительной головной боли, часто неукротимой рвоты без тошноты, не связанной с приёмом пищи.
При осмотре больных отмечают их возбуждение, эйфорию, в части случа ев уже в первые часы заболевания наступает расстройство сознания. Харак терна гиперемия лица, нередки герпетические высыпания на губах. Отмечают гиперестезию (тактильную, слуховую и зрительную), возможны мышечные су дороги. Выражены тахикардия, артериальная гипотензия, задержка мочеот деления.
В тяжёлых случаях заболевания больной принимает характерную вынужден ную позу. Он лежит на боку с запрокинутой головой и притянутыми к животу ногами, согнутыми в тазобедренных и коленных суставах (положение «взведён ного курка»). Эту симптоматику, довольно часто встречавшуюся до эры антибиотикотерапии, в настоящее время наблюдают лишь в запущенных случаях.
Рано, уже в первые сутки болезни, появляются тоническое напряжение мышц и мышечные контрактуры — ригидность затылочных мышц и длинных мышц спины, симптомы Кернига, Брудзинского и др. Для детей грудного возраста ука занные менингеальные симптомы нетипичны; можно наблюдать лишь выбу хание и напряжение большого родничка, а также симптомы подвешивания и «треножника». Отмечают повышение сухожильных рефлексов, расширение реф лексогенных зон. Нередко менингеальные симптомы сочетаются с признаками поражения черепных нервов.
Наиболее тяжёлое течение менингококкового менингита наблюдают при мол ниеносном варианте с набуханием и отёком головного мозга, а также при синд ромах церебральной гипотензии и эпендиматита (вентрикулита).
При молниеносном течении менингита уже с первых часов заболевания можно наблюдать развитие отёка и набухания головного мозга с возможным вклинени ем головного мозга в большое затылочное отверстие. Клиническое описание это го состояния приведено в разделе «Осложнения».
У детей младшего возраста менингит может сопровождаться синдромом цереб ральной гипотензии. У взрослых состояние в очень редких случаях бывает резуль татом усиленной дегидратации при проведении лечебных мероприятий. Уже с самого начала заболевания наблюдают быстрое нарастание признаков токсикоза и эксикоза, ступора, усиление рвоты, судорог. Наблюдают снижение рефлексов, мышечную гипотонию. У детей до года можно обнаружить западение большого родничка. Трудности диагностики в этих случаях связаны с тем, что при развитии синдрома церебральной гипотензии, как правило, не выражена менингеальная симптоматика. При люмбальной пункции давление ликвора резко снижено, он вытекает редкими каплями и имеет гнойный характер.
При распространении воспалительного процесса на эпендиму может возник нуть синдром эпендиматита. Клинически он проявляется неукротимой рвотой, мышечными судорогами и тотальной ригидностью мышц. Больные принимают вынужденную позу с вытянутыми ногами, перекрещенными в стопах, и вытяну тыми, сжатыми в кулаки руками. Наблюдают расстройства психики, сонливость. Температура тела чаще нормальная. При прогрессировании эпендиматита развиваются кахексия и гидроцефалия. Больные чаще погибают на фоне расстройств дыхания и сердечно-сосудистой деятельности.
Понятие «менингококковый менингит» весьма условно, поскольку вследствие тесной анатомической связи между оболочками и веществом мозга воспали тельный процесс часто переходит на мозговую ткань. При менингоэнцефалите в клинической картине заболевания обычно отмечают быстрое нарастание психических нарушений, сонливость, развитие стойких параличей и парезов. Менингеальная симптоматика при этом может быть выражена довольно слабо. Определяют характерные для поражения вещества мозга патологические рефлексы — Бабинского, Оппенгейма, Россолимо, Гордона и др.
К генерализованным формам относится и смешанная форма (менингококцемия + менингит). Клинически она характеризуется сочетанием симптоматики этих двух состояний.
Лабораторная диагностика
Используют бактериологический (с выделением и идентификацией возбудителя) и серологический [с выявлением специфических Аг в жидкостях организма (ликворе, крови и др.) или AT в сыворотке крови] методы. Изменения гемограммы при назофарингитах незначительны. Вместе с тем при генерализованных формах менингококковой инфекции с большим постоянством наблюдают высокий лейкоцитоз, нейтрофилию с большим количеством юных форм, а также увеличение СОЭ.
Менингококковый' назофарингит подтверждают высевом и идентификацией менингококка из полости носа и ротоглотки. При генерализованных формах делают посевы крови и спинномозговой жидкости на питательные среды, содержа щие человеческий белок. Возможна прямая микроскопия спинномозговой жидкости с обнаружением в ней внутриклеточно расположенных диплококков.
При наличии менингеального синдрома основным исследованием с целью дифференциальной диагностики становится спинномозговая пункция, проводимая с согласия больного или его родственников. Данные лабораторного анализа ликвора при менингококковом менингите и сходных с ним клинических состояниях приведены в табл. 3-6.
•В случаях менингококкового (гнойного) менингита спинномозговая жидкость мутная, цитоз достигает нескольких тысяч в 1 мкл со значительным преобладанием клеток нейтрофильного ряда.
•Определяют высокое содержание белка, положительные осадочные пробы, сни женное количество глюкозы. В ряде случаев в пробирке с жидкостью образу ется грубая плёнка на поверхности жидкости или дне пробирки.
Методы иммунологической диагностики (выявление Аг менингококков в ИФА, РЛА и AT к ним с помощью РИГА) имеют вспомогательное значение: их приме няют для определения серотипа возбудителя.
Осложнения
Инфекционно-токсический шок
Лечение
При назофарингитах, подтверждённых высевом менингококка со слизистой оболочки ротоглотки, назначают пероральную терапию левомицетином или рифампицином в средних терапевтических дозах в виде 4—5-дневных курсов, а так же полоскание горла дезинфицирующими растворами. При повторном выделении возбудителя рекомендуют кварцевание(тубус-кварц).
Больные с генерализованными формами менингококковой инфекции подлежат госпитализации вследствие тяжести состояния и быстроты прогрессирования симптоматики. На догоспитальном этапе больным менингококковым менингитом рекомендовано ввести первую дозу антибиотика, анальгетики и лазикс внутривенно или внутримышечно (в случае отсутствия признаков дегидратации и частой рвоты). При состоянии, осложнённом ИТШ или отёком-набуханием мозга, во время транспортировки больного в стационар целесообразно по показаниям использовать противосудорожные средства, проводить оксигенотерапию, начать внутривенное введение реополиглюкина, инфузионных кристаллоидных растворов с добавлением преднизолона в дозе до 5 мг/кг.
Наиболее эффективным антибактериальным средством при менингококковом менингите остаётся бензилпенициллин. Для преодоления гематоэнцефалического барьера и создания достаточной концентрации антибиотика в спинномозговой жидкости назначают массивные дозы: суточное количество антибиотика назна чают из расчёта 200 000—400000 ЕД/кг при6-кратномвнутримышечном введе нии. Внутривенно антибиотик вводят каждые 2 ч, при этом его суточная доза дол жна быть увеличена на 1/3.
Эффективными этиотропными препаратами признаны ампициллин в суточ ной дозе 200-400мг/кг и цефалоспорины III поколения (цефтриаксон, цефтриаксим) в максимальных дозах. Эти антибиотики рекомендуют использовать при неясной этиологии менингита.
Растворимую форму левомицетина (левомицетин-сукцинат)в дозе 10— 50 мг/кг/сут достаточно широко применяют при менингококцемии и в случаях ИТШ в силу бактериостатического действия препарата. Однако в последнее вре мя отмечают рост резистентности возбудителя к этому лекарственному средству. Альтернативные антимикробные препараты при генерализованных формах ме нингококковой инфекции — ампициллин (по200-400мг/кг/сут) и фторхинолоны.
Показатели эффективности лечения менингококкового менингита — норма лизация температуры тела и улучшение состояния больного, наступающие через 1-4дня с момента начала терапии. На5-6-есутки лечения необходим контроль спинномозговой жидкости. Основной критерий, дающий основание для прекра щения антибиотикотерапии, — снижение цитоза до 100 в 1 мкл ликвора с преобла данием лимфоцитов (70% и более). Содержание белка в ликворе может оставаться увеличенным. При менингоэнцефалите лечение пролонгируют ещё на3—4дня.
Одновременно с этиотропной терапией проводят интенсивное патогенетичес кое лечение: внутривенные инфузий глюкозы, кристаллоидных полиионных и макромолекулярных коллоидных растворов. Регидратацию следует сопровождать форсированным диурезом, для чего применяют салуретики — фуросемид, диакарб, урегит в течение 5-6дней. По показаниям назначают анальгетики, снот ворные и седативные препараты.
В случае осложнения менингококковой инфекции ИТШ лечение больного проводят в отделении реанимации. Назначают левомицетин-сукцинат внутривенно преднизолон в дозе 5— 10мг/кг, раствор бикарбоната натрия (с целью коррекции ацидоза), свежезамороженную плазму, альбумин или реополиглюкин, а затем — внутривенные инфузии полиионных изотонических растворов и поляризующей смеси. Показана оксигенотерапия, при выраженной дыхательной недостаточности — ИВ Л. Эффективны плазмаферез и ультрафильт рация плазмы.
При остром отёке-набуханиимозга антибактериальную терапию комбиниру ют с форсированным диурезом (салуретики,10—20%раствор альбумина) с пос ледующим введением полиионных растворов. Применение гипертонических ра створов глюкозы, мочевины и маннитола противопоказано в связи с возможным развитием синдрома отдачи при диффузии этих препаратов через гематоэнцефалический барьер. Назначают глюкокортикоиды (дексаметазон в дозе 0,25- 0,5 мг/кг/сут), ингаляции 30%кислородно-воздушнойсмеси. Показания к при менению ИВЛ — коматозное состояние, судороги и дыхательная недостаточность.
Гепатиты. ВИЧ
ВИЧ-инфекция (HIV-infaction)
Антропонозное вирусное заболевание, в основе патогенеза которого лежит прогрессирующий иммунодефицит и развитие вследствие этого вторичных оппортунистических инфекций и опухолевых процессов.
Этиология
Возбудитель —вирус рода Lentivirus подсемейства Lentivirinae семейства Retroviridae. Геном свободной частицы ВИЧ образован двухнитевой РНК. В пораженных клетках ВИЧ формирует ДНК. Наличие обратной транскриптазы обесечивает обратную направленность потока генетической информации (не от ДНК к РНК, а наоборот, от РНК к ДНК), что определило название семейства. В настоящее время выделяют вирусы двух типов — ВИЧ-1 иВИЧ-2, различающиеся по своим структурным и антигенным характеристикам.
ВИЧ-1— основной возбудитель пандемии ВИЧ-инфекциии СПИДа; его выделяют в Северной и Южной Америке, Европе и Азии.
ВИЧ-2 не так широко распространен. Впервые выделен из крови выходцев из Гвинеи-Бисаус подтверждённым диагнозом СПИД, не имеющих в кровиВИЧ-1.В эволюционном плане он родствененВИЧ-1.Его выделяют преимущественно в Западной Африке.
ВИЧ чрезвычайно чувствителен к внешним воздействиям, гибнет под действием всех известных дезинфектантов. Нагревание до 56 °С резко снижает инфекционность вируса, при нагревании до 70-80°С он инактивируется через 10 мин. Вирионы чувствительны к действию 70% этилового спирта (инактивируются че рез 1 мин), 0,5% раствора гипохлорида натрия, 1% раствора глутаральдегида. Устойчив при лиофильной сушке, воздействии ультрафиолетовых лучей и ионизирующей радиации. В крови, предназначенной для переливания, вирус сохраняется годами, хорошо переносит низкие температуры.
Эпидемиология
Резервуар и источник инфекции — инфицированный ВИЧ человек, во всех стадиях инфекции, пожизненно. Природный резервуарВИЧ-2— африканские обезьяны. Природный резервуар ВИЧ-1 не выявлен, не исключается, что это могут быть дикие шимпанзе. В лабораторных условияхВИЧ-1вызывает у шимпанзе и некоторых других видов обезьян клинически не выраженную инфекцию, заканчивающуюся быстрым выздоровлением. Другие животные к ВИЧ не восприимчивы.
В большом количестве вирус содержится в крови, в сперме, менструальных выделениях и вагинальном секрете. Кроме того, вирус обнаруживают в женском молоке, слюне, слезной и спинномозговой жидкостях. Наибольшую эпидемиологическую опасность представляют кровь, сперма и вагинальный секрет.
Наличие очагов воспаления или нарушение целостности слизистых оболочсй половых органов (например, эрозия шейки матки) повышают вероятность передачи ВИЧ в обоих направлениях, становясь выходными или входными воротам для ВИЧ. Вероятность заражения при единичном половом контакте низкая, однако частота половых сношений делает этот путь наиболее активным. Бытовая передача вируса не установлена. Передача ВИЧ от матери плоду возможна nfl дефектах плаценты, приводящих к проникновению ВИЧ в кровоток плода, а так же при травматизации родовых путей и ребенка во время родов.
Парентеральный путь также реализуется при переливании крови, эритроцитарной массы, тромбоцитов, свежей и замороженной плазмы. Внутримышечные, подкожные инъекции и случайные уколы инфицированной иглой составляют в среднем 0,3% случаев (1 случай на 300 инъекций). Среди детей, родившихся от инфицированных матерей или вскармливавшихся' ими, инфицированы 25—35%.Возможно заражение ребенка во время родов и через женское молоко.
Естественная восприимчивость людей — высокая. В последнее время рассматривают возможность существования незначительных генетически отличающихся групп населения, встречающихся особенно часто среди североевропейских народов, реже заражающихся при половых контактах. Существование этих отклонений в восприимчивости связывают с геном CCR5; люди с гомозиготной формой гена устойчивы к ВИЧ. Последние данные показывают, что причиной невосприимчивости к заражению ВИЧ могут быть специфические IgA, обнаруживаемые на слизистых оболочках половых органов. Люди, заразившиеся в возрасте старше 35 лет, заболевают СПИДом в два раза быстрее, чем инфицированные в более молодом возрасте.
Средняя продолжительность жизни инфицированных ВИЧ составляет 11-12лет. Однако появление эффективных химиопрепаратов позволило значительно продлить жизнь ВИЧинфицированных. Среди заболевших преобладают лица сексуально активного возраста, главным образом мужчины, но ежегодно увеличивается процент женщин и детей. В последние годы в России доминировал парентеральный путь инфицирования (при использовании одного шприца несколькими лицами), главным образом среди наркоманов. В то же время отмечают увеличение абсолютного числа передачи при гетеросексуальных контактах, что вполне объяснимо, так как наркоманы становятся источниками инфекции для своих половых партнеров. Показатель встречаемости ВИЧ-инфекции среди доноров резко возрос (более чем в 150 раз по сравнению с периодом начала эпидемии), кроме того, очень опасны доноры, находящиеся в периоде «серонегативного окна». Выявляемость ВИЧ среди беременных в последние годы также резко возросла.
Основные эпидемиологические признаки. В настоящее время мир переживает пандемию ВИЧ-инфекции. Если в первые годы появления заболевания наибольшее число случаев было зарегистрировано в США, то теперь инфекция наиболее широко распространена среди населения стран Африки, Латинской Америки,Юго-ВосточнойАзии.
Патогенез
Основу составляет селективное поражение иммунокомпетентных клеток с развитием прогрессирующего иммунодефицита. ВИЧ способен проникать в любые клетки организма человека, несущие поверхностные CD4 рецепторы. Основной мишенью вируса становятся лимфоциты, макрофаги и клетки микроглии. При взаимодействии вируса с рецепторной системой макрофагов нарушается его «распознавание» как чужеродного антигена. Репродукция дочерней популяции ВИЧ вызывает гибель заражённой клетки. Вирусы выходят в кровь и внедряются в новые функционально активные лимфоциты. Непораженные вирусом лимфоциты «прилипают» к пораженным, образуя симпласты и синцитий, их функциональная активность снижается под воздействием токсичных веществ, образующихся при гибели клеток. Развитие иммунодефицита идет медленно и волнообразно, в течение месяцев и лет, поскольку уменьшение количества лимфоцитов сначала компенсируется продукцией новых иммунных клеток. По мере накопления вируса в организме, поражения им все более ранних популяций клеток вплоть до первичных стволовых и истощения лимфоидной ткани прогрессирует раз рушение иммунной системы, нарастает иммунодефицит с поражением всех звеньев иммунитета.
Противовирусные AT, синтезируемые неинфицированными лимфоцитами, проявляют сравнительно низкий аффинитет, что обусловлено свойствами АГ вируса, а также появлением АГ с изменёнными свойствами вследствие высокой частоты мутаций. Кроме того, AT не способны связывать вирус внутри инфицированных клеток, что делает формирующиеся гуморальные иммунные реакции заведомо малоэффективными. Вместе с тем в крови определяют высокие уровни иммуноглобулинов всех классов (полииммуноглобулинопатия) и циркулирующих иммунных комплексов.
Вследствие развивающегося иммунодефицита иммунная система теряет способность противодействовать не только патогенным микроорганизмам, но и условно-патогенной и даже сапрофитной флоре, ранее латентно персистировавшей в различных органах и тканях. Активизация условно-патогенных микроорганизмов и сапрофитов обусловливает возникновение так называемых «оппортунистических» инфекций.
При ВИЧ-инфекции происходит активное размножение бластных клеток, развитие которых остановилось на первых этапах клеточной дифференцировки. Эти клетки, не достигая полного созревания и представляя собой чужеродные для организма АГ, разрушаются при нормальном функционировании иммунной системы и безудержно размножаются в условиях иммунодефицита. Указанное лежит в основе возникновения у больного ВИЧ-инфекцией быстро прогрессирующих болезней злокачественного роста(Т-лимфомы,саркомы Капоши и др.).
Паразитирование ВИЧ в нервной ткани сопровождается развитием ауто-.иммунных реакций, приводящих к гибели клеток. Этим обусловлено развитие! неврологических нарушений, которые могут даже предшествовать иммунодефициту.
Клиническая картина
Многообразие проявлений заболевания на различных этапах его развития; вызывает необходимость применения в практической работе клинических классификаций ВИЧ-инфекции.В Российской Федерации применяли клиническую классификацию, предложенную В.И. Покровским (1989).За 10 лет после ее создания представления о течении ВИЧ-инфекции несколько изменились, в том числе за счет усовершенствования методов лечения. Эти изменения нашли отражение в классификации 2001 г., которая позволяет осуществлять клинической и диспансерное наблюдение заВИЧ-инфицированными, прогнозировать течение заболевания и определять тактику ведения больного, показания к назначению лекарственных препаратов без использования дорогостоящих лабораторнных методов.
Клиническая классификация ВИЧ-инфекции2001 г.
1.Стадия инкубации
2.Стадия первичных проявлений
Варианты течения:
A. Бессимптомная
Б. Острая ВИЧ-инфекциябез вторичных заболеваний. B. Острая инфекция с вторичными заболеваниями.
3.Латентная стадия
4.Стадия вторичных заболеваний 4А. Потеря веса менее 10%; грибковые, вирусные, бактериальные поражения кожи и слизистых оболочек; опоясывающий лишай; повторные фарингиты, синуситы, повышенная утомляемость.
Фазы. Прогрессирование (на фоне отсутствия противоретровирусной терапии, на фоне противоретровирусной терапии).
Ремиссия (спонтанная, после ранее проводимой противоретровирусной терапии, на фоне противоретровирусной терапии).
4Б. Потеря веса более 10%; необъяснимая диарея или лихорадка более од ного месяца; волосистая лейкоплакия; туберкулез легких; повторные или стойкие вирусные, бактериальные, грибковые, протозойные поражения внутренних органов; повторный или диссеминированный опоясываю щий лишай; локализованная саркома Капоши, прогрессирующая общая слабость.
Фазы. Прогрессирование (на фоне отсутствия противоретровирусной тера пии, на фоне противоретровирусной терапии).
Ремиссия (спонтанная, после ранее проводимой противоретровирусной терапии, на фоне противоретровирусной терапии).
4В. Кахексия; генерализованные бактериальные, вирусные, грибковые, про тозойные и паразитарные заболевания; пневмоцистная пневмония; кандидоз пищевода, бронхов, легких; внелегочный туберкулез; атипичные микобактериозы; диссеминированная саркома Капоши; поражения цен тральной нервной системы различной этиологии.
Фазы. Прогрессирование (на фоне отсутствия противоретровирусной тера пии, на фоне противоретровирусной терапии).
Ремиссия (спонтанная, после ранее проводимой противоретровирусной терапии, на фоне противоретровирусной терапии).
5. Терминальная стадия.
Стадия 1.«Стадия инкубации» — период от момента заражения до появления реакции организма в виде клинических проявлений «острой инфекции» и/или выработки антител. Продолжительность ее обычно составляет от 3 нед до 3 мес, но в единичных случаях может затягиваться и до года. В этот период идет актив ное размножение ВИЧ, однако клинических проявлений заболевания нет и ан титела к ВИЧ еще не выявляются. ДиагнозВИЧ-инфекциина данной стадии ставится на основании эпидемиологических данных и лабораторно должен под тверждаться обнаружением в сыворотке крови пациента вируса иммунодефицита человека, его антигенов, нуклеиновых кислот ВИЧ.
Стадия 2.«Стадия первичных проявлений». В этот период активная реплика ция ВИЧ в организме продолжается, однако проявляется уже первичный ответ организма на внедрение этого возбудителя в виде клинических проявлений и/или выработки антител. Стадия ранней ВИЧ-инфекции может протекать в нескольких формах.
2А. «Бессимптомная», когда какие-либо клинические проявления ВИЧ-инфекции или оппортунистических заболеваний, развивающихся на фоне иммунодефицита, отсутствуют. Ответ организма на внедрение ВИЧ проявляется при этом лишь выработкой антител.
2Б. «ОстраяВИЧ-инфекциябез вторичных заболеваний»может проявляться разнообразной клинической симптоматикой. Наиболее часто это — лихорадка, высыпания (уртикарные, папулезные, петехиальные) на коже и слизистых, уве личение лимфатических узлов, фарингит. Может отмечаться увеличение печени, селезенки, появление диареи. В крови больных с острой ВИЧ-инфекцией могут обнаруживаться широкоплазменные лимфоциты («мононуклеары»).
Острая клиническая инфекция отмечается у 50—90%инфицированных лиц в первые 3 мес после заражения. Начало периода острой инфекции, как правило, опережает сероконверсию, т.е. появление антител к ВИЧ. В стадии острой ин фекции часто отмечается транзиторное снижение уровняС04-лимфоцитов.
2В «ОстраяВИЧ-инфекцияс вторичными заболеваниями».В 10—15% случаев у больных острой ВИЧ-инфекциейна фоне снижения уровняСЭ4-лимфоцитов и развившегося вследствие этого иммунодефицита появляются вторичные забо левания различной этиологии (ангина, бактериальная и пневмоцистная пневмония, кандидозы, герпетическия инфекция и др.).
Продолжительность клинических проявлений острой ВИЧ-инфекцииварьи рует от нескольких дней до нескольких месяцев, однако обычно она составляет2—3нед. У подавляющего большинства пациентов стадия начальнойВИЧ-инфекции переходит в латентную стадию.
Стадия 3, «Латентная». Характеризуется медленным прогрессированием им мунодефицита, компенсируемого за счет модификации иммунного ответа и из быточного воспроизводстваС04-клеток.В крови обнаруживаются антитела к ВИЧ. Единственным клиническим проявлением заболевания является увеличе ние двух и более лимфатических узлов не менее чем в двух не связанных между собой группах (не считая паховые).
Лимфатические узлы обычно эластичные, безболезненные, не спаяны с окру жающей тканью, кожа над ними не изменена.
Длительность латентной стадии может варьироовать от 2—3до 20 и более лет, в среднем —6—7лет. В этот период отмечается постепенное снижение уровняС04-лимфоцитов,в среднем со скоростью0,05—0,07х109/лв год.
Стадия 4. «Стадия вторичных заболеваний». Продолжающаяся репликация ВИЧ, приводящая к гибели С04-клеток и истощению их популяций, приводит к развитию на фоне иммунодефицита вторичных (оппортунистических) заболева ний, инфекционных и/или онкологических.
Взависимости от тяжести вторичных заболеваний выделяют стадии 4А, 4Б, 4В.
Встадии вторичных заболеваний выделяют фазы прогресснрования (на фоне отсутствия противоретровирусной терапии или на фоне противоретровирусной терапии) иремиссии (спонтанной или на фоне противоретровирусной терапии).
Стадия 5.«Терминальная стадия». В этой стадии имеющиеся у больных вторичные заболевания приобретают необратимое течение. Даже адекватно проводимые противовирусная терапия и терапия вторичных заболеваний не эффективны, и больной погибает в течение нескольких месяцев. Для этой стадии типично снижение количества СД4-клетокниже 0,05х109/л.
Следует отметить, что клиническое течение ВИЧ-инфекции отличается большим разнообразием. Последовательность прогрессирования ВИЧ-инфекции через прохождение всех стадий болезни не обязательна. Продолжительность течения ВИЧ-инфекции колеблется в широких пределах — от нескольких месяцев до15-20лет.
Лабораторная диагностика
Выделение вируса на практике не проводят. В практической работе более популярны методы определения AT к ВИЧ. Первоначально AT выявляют методом ИФА. При положительном результате ИФА сыворотку крови исследуют методом иммунного блота (блоттинга). Он позволяет обнаружить специфические AT к частицам белковой структуры ВИЧ, имеющим строго определенную молекулярную массу.
Отрицательный результат иммуноблоттинга при наличии клинических и эпидемиологических подозрений на ВИЧ-инфекцию не отвергает возможность данного заболевания и требует повторения лабораторного исследования. Это объясняется, как уже говорилось тем, что в инкубационном периоде заболевания AT ещё нет, а в терминальной стадии, вследствие истощения иммунной системы, они уже перестают вырабатываться. В этих случаях наиболее перспективна полимеразная цепная реакция (ПЦР), позволяющая обнаружить частицы РНК вируса.
При установлении диагноза ВИЧ-инфекции проводят многократное исследование иммунного статуса в динамике для контроля за прогрессированием болезни и эффективностью лечения.
Лечение
Радикальные методы лечения ВИЧ-инфекциидо настоящего времени не разработаны. В мировой практике для подавления репродукции вируса применяют комбинации противовирусных препаратов трёх групп:
•нуклеозидные аналоги — препараты групп тимидина (тимазид, ретровир, фосфазид, зерит); цитизина (хивид, эпивир); инозина (видекс) и др;
•ненуклеозидные ингибиторы обратной транскриптазы (вирамун, невирапин, делавирдин);
•ингибиторы протеазы (инвираза, норвир, вирасепт, ритонавир, индинавир, нельфинавир) и др.
Показанием к началу противоретровирусной терапии являются ВИЧ-инфекция в стадии первичных проявлений в клинически выраженной форме (стадия 2Б, 2В) и стадия вторичных заболеваний (4Б,4В). При применении указанных препаратов необходимо учитывать степень развития их отрицательных побочных эффектов.
Кроме того, проводят интенсивное лечение имеющихся у больного оппорту нистических инфекций, что требует применения разнообразных этиотропных средств: низорала и дифлукана (диссеминированный кандидоз), бисептола (пневмоцистная пневмония), ацикловира, ганцикловира, фоскарнета (герпетические инфекции) и т.д. Назначение цитостатиков при опухолях усугубляет иммунодефицит. Иммуностимулирующая терапия не показана, так как способствует более быстрому прогрессированию заболевания. Информация о заражении ВИЧ, необратимость и фатальный прогноз вызывает у инфицированного тяжелые эмоциональные реакции, вплоть до суицида. Поэтому создание охранительного ре жима является важнейшей терапевтической мерой. Консультирование и психологическая поддержка ВИЧ-инфицированных,так же как и назначение лекарственной терапии, осуществляется с их добровольного согласия.
Вирусный гепатит В (ВГВ) — антропонозная вирусная инфекция из условной группы трансфузионных гепатитов, характеризующаяся иммунологически опос редованным поражением гепатоцитов и протекающая в различных клинических формах (от вирусоносительства до цирроза печени).
Этиология
Возбудитель — ДНК-геномный вирус рода Orthohepadnavirus семейства Hepadnaviridae. В крови больных ВГВ циркулируют частицы трёх морфологических типов. Наиболее часто обнаруживают сферические частицы, реже — нитевидные формы. Вирусные частицы этих типов не проявляют инфекционных свойств. Лишь 7% частиц представлено комплексными двухслойными сферическими образованиями с полной структурой (так называемые частицы Дейна), проявляющими выраженную инфекционность. Верхний их слой образует суперкапсид. Геном представлен неполной (одна нить короче) двухнитевой кольцевой молекулой ДНК и ассоциированной с ней ДНК-полимеразой.У вирионов выделяют четыре Аг — поверхностный (HBsAg) и три внутренних (HBeAg, HBcAg и HBxAg).
Основными Аг частиц Дейна являются поверхностный HBsAg и сердцевинный HBcAg. AT против HBsAg и HBcAg появляются в течение заболевания. Повышение титра AT против HBcAg напрямую связано с формированием противовирусных иммунных реакций.
HBcAg (сердцевинный, или коровый, Аг) играет важную роль в репродукции вируса. При инфекционном процессе он выявляется только в ядрах гепатоцитов. HBeAg локализуется не только в сердцевине вируса, он циркулирует в крови в свободном виде или связан с AT. Его определяют как Аг инфекционное™. HBgAg (поверхностный Аг) определяет способность к длительной персистенции вируса в организме; он имеет относительно низкую иммуногенность, термостабильность и устойчивость к протеазам и детергентам. Известно несколько подтипов HBsAg, отличающихся субдетерминантами:adw, adr, ayw, ауг. Общей антигенной детерминантой являетсяа детерминанта, поэтому поствакцинальный иммунитет яв ляется защитным по отношению к любому субтипу вируса. В России регистриру ют в основном субтипыayw иadw. Клинические проявления болезни не зависят от субтипа вируса.
HBxAg остаётся наименее изученным. Предположительно он опосредует зло качественную трансформацию клеток печени.
Вирус ВГВ чрезвычайно устойчив во внешней среде. В цельной крови и её препаратах сохраняется годами.. На него губительно действуют перекись водорода, хлорамин, формалин.
Эпидемиология
Источник инфекции — лица с манифестными или субклиническими формами заболевания (больные острым и хроническим гепатитами, с циррозом печени и так называемые «здоровые» вирусоносители). В крови больного вирус появляется задолго до проявления болезни (за2—8нед до повышения активности аминотрансфераз) и циркулирует в течение всего острого периода болезни, а также при хроническом носительстве, формирующемся в5—10%случаев.
Механизм передачи. Выделение вируса с различными биологическими секретами (кровь, слюна, моча, жёлчь, слёзы, грудное молоко, сперма и др.) определяет множественность путей передачи инфекции. Однако только кровь, сперма и, возможно, слюна представляют реальную эпидемиологическую опасность, так как в других жидкостях концентрация вируса очень мала. Заболевание передаётся главным образом парентеральным путём при переливаниях крови и кровезаменителей, при использовании медицинских инструментов без их достаточно эффективной стерилизации.
Из естественных механизмов передачи реализуется контактный (половой) путь, а также передача вируса через различные контаминированные предметы обихода (бритвы, зубные щётки, полотенца и т.д.) при проникновении возбудителя в организм через микротравмы на коже и слизистых оболочках. Заражение происходит также в результате нанесения татуировки, прокола мочек ушей и при других манипуляциях. Половой путь передачи ВГВ реализуется при гомо- и гетеросексуальных контактах: вирус проникает через микротравмы слизистых оболочек при половых контактах. Контактно-бытовой путь передачи инфекции — внутрисемейное инфицирование, инфицирование в организованных коллективах детей и взрослых. Главную опасность представляют носители ВГВ при тесном общении в этих коллективах.
Возможна также и вертикальная передача.возбудителя. Обычно заражение происходит во время родов, однако инфицирование плода возможно в матке при разрыве плаценты.
Доля естественных путей заражения составляет 30—35%и имеет тенденцию к увеличению. Серьёзную опасность представляет распространение ВГВ в коллективах с круглосуточным пребыванием детей: в домах ребёнка, детских домах, интернатах.
Естественная восприимчивость высокая. Известно, что переливание крови, содержащей HB^g, приводит к развитию гепатита у50-90%реципиентов в зависимости от инфицирующей дозы. Постинфекционный иммунитет длительный, возможно пожизненный. Повторные случаи заболеваний наблюдают исключи тельно редко.
Основные эпидемиологические признаки. ВГВ относят к числу повсеместно распространённых инфекционных болезней. Считается, что вирусом инфицированы около 2 млрд человек, ежегодно умирают порядка 2 млн больных
Заболеваемость ВГВ связана в основном с плохими социальными и экономическими условиями жизни. Весь мир можно разделить на регионы с высокой, промежуточной и низкой эндемичностью. В России, которую относят к регионам с относительно высоким уровнем распространённости ВГВ, наблюдают устойчивую тенденцию к росту заболеваемости
В эпидемический процесс интенсивно вовлекается молодое трудоспособное население: среди заболевших преобладают лица в возрасте от 15 до 30 лет, на долю которых приходится около 90% заболевших. Такой возрастной состав заболевших гепатитом обусловлен тем, что в структуре путей инфицирования доминиру ет «наркозависимый» и половой пути передачи инфекции.
Среди заболевших преобладают лица, подвергавшиеся гемотрансфузиям и другим медицинским парентеральным манипуляциям. Группы риска составляют медицинские работники, в процессе своей профессиональной деятельности соприкасающиеся с кровью и её препаратами (хирурги, стоматологи, работники гемодиализа, лабораторий и др.), а также наркоманы (особенно в последние годы) при пользовании единым шприцем и заражении друг от друга половым путём. Характерен семейный характер заболеваемости, где активно реализуются половой и контактный пути заражения.
Патогенез
Вирус проникает в организм человека через повреждённые кожные покровы или слизистые оболочки, затем гематогенно диссеминирует в печень, где фиксируется на гепатоцитах благодаря поверхностным рецепторам, содержащим HBjAg. Экспрессия HBjAg происходит на мембране печёночных клеток. При этом возбудитель не оказывает прямого цитопатического действия на клетки печени.
Процесс репродукции в гепатоцитах обусловлен активностью ДНК-полимеразы, активно участвующей в «достройке» неполноценной цепочки вирусной ДНК за счёт Аг гистосовместимости, общих для различных клеток организма хозяина. Дочерние популяции накапливаются в поверхностной мембране гепатоцитов.
Цитолиз печёночных клеток происходит под действием цитотоксических иммунных механизмов. Мишенями для последних являются антигенные детерминанты вируса ВГВ, ассоциированные с Аг главного комплекса гистосовместимости (HLA) на поверхности гепатоцитов.
Существенную роль в патогенезе ВГВ играют иммунные комплексы (HBsAgАТ), оседающие на эндотелии сосудов различных органов и в лимфатических уз лах, обусловливая внепечёночные поражения (например, гломерулонефрит и узел ковый периартериит).
Аутоиммунные реакции возникают также в ответ на воздействие фрагментов гепатоцитов после их гибели. Это ведёт не только к элиминации указанных фрагментов, но и к повреждению здоровых печёночных клеток.
Морфологические изменения характеризуются дистрофическими и некробиотическими процессами в центролобулярных и перипортальных зонах печёночной дольки с последующим развитием фиброза. Одновременно в процесс вовлекаются внутрипечёночные жёлчные ходы, что ведёт к формированию холестаза.
Клиническая картина
Инкубационный период. При острой циклической форме ВГВ его длительность подвержена большим колебаниям и варьирует от 30 до 180 дней и более.
Дожелтушный период. Может протекать в тех же вариантах, что и при ВГА, но чаще встречают артралгический, астеновегетативный и диспептический варианты. При диспептическом варианте выражены стойкая анорексия, постоянное чувство тошноты, периодическая рвота без каких-либо видимых причин. Следует заметить, что при гриппоподобном варианте до желтушного периода при ВГВ катаральные явления нехарактерны и только у небольшой части больных можно наблюдать повышение температуры тела. Вместе с тем больные нередко жалуются на суставные боли; при этом внешне суставы, как правило, не изменяются. Артралгии чаще бывают в ночное и утреннее время, а при движениях в суставах ненадолго исчезают. Их могут сопровождать высыпания на коже типа крапивницы. Сочетание артралгии и экзантемы обычно предвещает более тяжёлое течение заболевания. В таких случаях клиническую картину дополняет повышение температуры тела, иногда до высоких цифр.
Уже в до желтушный период можно наблюдать головокружение, упорную сон ливость и проявления геморрагического синдрома в виде кровотечений из носа и дёсен.
Желтушный период. Самочувствие больных, как правило, не улучшается, а в большинстве случаев ухудшается. Артралгии и экзантема исчезают, но нарастают диспептические симптомы.
Иктеричность кожных покровов и слизистых оболочек медленно прогресси рует, достигая своего максимума не ранее 7—10-годня с момента её появления. Желтуха обычно интенсивная, сопровождается кожным зудом. На коже нередко выявляют геморрагии в виде петехий или крупных синяков. При более тяжёлом течении отмечают носовые кровотечения, кровоточивость дёсен, а у женщин — ранний приход обильных менструаций. Моча приобретает тёмный цвет, у боль шинства больных кал ахоличен.
Печень, как правило, увеличивается в размерах; она отчётливо болезненна при пальпации, достаточно мягкая по консистенции. Необходимо обратить внима ние на то, что на фоне интенсивной желтухи нередко печень не увеличивается, что указывает на более тяжёлое течение гепатита. В 50—60%случаев наблюдают спленомегалию. Пульс урежен, однако при более тяжёлом течении можно наблю дать тахикардию. Тоны сердца приглушены, отмечают небольшую гипотонию. Больные обычно апатичны, испытывают головокружение, расстройства сна.
Течение желтушного периода длительное, затягивается до 1 мес и более. Период реконвалесценции начинается с момента уменьшения или исчезновения комплекса диспептических симптомов, после чего происходит медленное снижение билирубинемии. Что касается изменения размеров печени, то этот процесс иногда затягивается на несколько месяцев.
При присоединении холестатического компонента (5—15%больных) заболевание приобретает торпидное течение. В этих случаях характерны невыраженная интоксикация, длительные холестатические проявления (высокие «монотонные» показатели билирубинемии и ферментемии, тёмная моча, ахоличный стул, увеличенная, не сокращающаяся в размерах печень, субфебрилитет).
Помимо острой циклической формы заболевания ВГВ может проявляться в виде хронической формы (хронизация в 5—10%случаев) и циррозов вирусной этиологии.
Лабораторная диагностика
На высоте заболевания в сыворотке крови обнаруживают HBsAg, HBeAg или HBcIgM с помощью ИФА, РИА, в период ранней реконвалесценции — HBJgG, HBeIgG, на стадии выздоровления — HBJgG и HBcIgG. Для верификации возбудителя всё большее значение приобретает ПЦР, выявляющая вирусную ДНК, что определяет степень активности репликации вируса.
Биохимические исследования крови и изменения гемограммы приведены в разделе «Вирусный гепатит А». В динамике заболевания нужно достаточно часто повторять эти исследования для контроля за функциональной активностью печени. Особое значение в этом плане приобретает определение протромбинового индекса, уменьшение показателей которого ниже 40% говорит о тяжёлом, а иногда критическом состоянии больного.
Определённые данные, свидетельствующие о нарушениях структуры печени, даёт УЗ И.
Осложнения
Наиболее тяжёлое и серьёзное в плане прогноза осложнение — острая пе чёночная энцефалопатия (печёночная кома). Она развивается при массивном цитолизе гепатоцитов и характеризуется глубоким угнетением функции печени, прогрессирующей психоневрологической симптоматикой и выраженными гемор рагическими проявлениями. В своём клиническом развитии острая печёночная энцефалопатия проходит три последовательных стадии.
Лечение
Больных с острым циклическим течением ВГВ госпитализируют. В лёгких и среднетяжёлых случаях лечение аналогично таковому при ВГА. При тяжёлом течении решают вопрос о назначении преднизолона по 40—60мг/сут внутрь. Сни жение доз производят постепенно с момента купирования симптомов интокси кации. Одновременно больным интенсифицируют дезинтоксикационную тера пию (кристаллоиды и реополиглюкин в соотношении 1:3), проводят коррекцию нарушенийводно-электролитногобаланса (панангин, аспаркам при гипокалиемии), применяют лактулозу (нормазу), спазмолитические препараты(но-шпа,эуфиллин), назначают антибиотики с низкой резорбцией из кишечника (неомицин). В случаях выраженного холестаза рекомендованы препараты урсодеоксихолевой кислоты (уросан, урсофальк). При развитии острой печёночной энцефалопатии назначают глюкокортикоиды (внутривенно 240—480мг и более предни золона в сутки), хотя их эффективность сомнительна.
Вирусный гепатит А (ВГА) — доброкачественная острая циклическая вирус ная инфекция из группы фекально-оральных гепатитов, сопровождающаяся некрозом гепатоцитов. Клинически проявляется синдромом интоксикации, гепатоспленомегалией и часто желтухой. Синонимы — болезнь Боткина, вирусный гепатит типа А.
Этиология
Возбудитель — РНК-геномный вирус рода Hepatovirus семейства Picornaviridae. Вирионы мелкие, просто устроенные, лишённые суперкапсида. Геном образован односпиральной РНК. В настоящее время известен только один серовар вируса. Во внешней среде он более устойчив, чем типичные энтеровирусы. Может сохраняться во внешней среде в течение нескольких месяцев при 4 °С, несколько лет при — 200С, в течение нескольких недель — при комнатной температуре. Вирус инактивируется при кипячении через 5 мин. При ультрафиолетовом облучении возбудитель погибает через 60 с. В присутствии хлора в концентрации0,5—1мл/л, при рН 7,0 выживает 30 мин и более, что определяет его способность сохраняться определённое время в хлорированной водопроводной воде.
Эпидемиология
Резервуар и источник инфекции — человек с любыми проявлениями болезни (желтушными, безжелтушными, бессимптомными инаппарантными формами). Существенная часть заразившихся переносит болезнь в бессимптомной, а потому и нерегистрируемой форме. У детей эта величина достигает90-95%,у взрослых —25—50%.Больной человек опасен для окружающих начиная с о2-й недели инкубационного периода болезни; пик выделения вируса приходится на первую неделю болезни. Контагиозность больного с появлением желтухи значительно уменьшается: в первую неделю желтушного периода частота положительных находок составляет30-50%,во вторую —15-25%,позже выделение вируса наблюдают лишь у единичных больных. Хроническое носительство вируса не установлено. Описаны случаи заражения человека от шимпанзе и некоторых других видов обезьян.
Механизм передачи — фекально-оральный. Выделение вируса происходит с фекальными массами. В 1 мл фекалий может содержаться до 108 инфекционных вирионов. Заражение людей происходит при употреблении воды и пищи, инфицированной вирусом, иногда контактно-бытовым путём. Обсуждается возможность полового пути передачи инфекции, особенно в среде гомосексуалистов. В ряде стран (США, страны Европы) описаны случаи заболеваний, связанные с заражением при парентеральном введении психотропных веществ, переливании крови и её препаратов. Роль каждого пути передачи неодинакова в разных условиях. Водный путь, как правило, приводит к вспышкам заболевания среди лиц, пользовавшихся инфицированной водой, плававших в загрязнённых бассейнах и озёрах. Поскольку вирус ВГА может выживать в воде от 12 нед до 10 мес, инфицирование может произойти при употреблении различных сырых моллюсков, мидий, собранных в зонах, загрязнённых сточными водами.
Пищевые вспышки чаще всего связаны с контаминацией продуктов на пищевых предприятиях персоналом с лёгкой формой болезни, при несоблюдении правил личной гигиены. Возможно также заражение овощей и ягод (особенно клубники и земляники, салата) при их удобрении фекалиями человека. Контактно-бытовой путь передачи, как правило, имеет место в условиях ДЦУ, домах ребёнка и других аналогичных учреждениях, особенно в условиях их неудовлетворительного санитарного состояния.
Естественная восприимчивость человека высокая. После перенесённой инфекции вырабатывается стойкий напряжённый иммунитет. Наиболее восприимчивы дети от 2 до 14 лет. Бессимптомные формы болезни формируют менее напряжённый иммунитет.
Основные эпидемиологические признаки. ВГА отличают повсеместное распространение, неравномерная интенсивность на отдельных территориях, цикличность в многолетней динамике, выраженная осенне-зимняя сезонность, преимущественное поражение детей дошкольного возраста, подростков и лиц молодого возраста.
Для многолетней динамики характерно наличие периодических (через 4—6лет) подъёмов заболеваемости. Самые последние годы характеризует очередной подъём заболеваемости. Особенностью последнего подъёма явилось возникновение эпи демических вспышек с пищевым путём передачи.
Патогенез
Обычными входными воротами для вируса ВГА служат слизистые оболочки ротоглотки и тонкой кишки. В месте внедрения развивается воспалительный процесс, обусловливающий формирование катарального синдрома, диспептических явлений и температурной реакции. Проникновение возбудителя в кровь приводит к вирусемии, благодаря которой он достигает печени. В настоящее время предполагают, что повреждение гепатоцитов обусловлено клеточными цитотоксическими иммунными реакциями. Вместе с тем не исключают прямое цитопатическое действие вируса на гепатоциты. У больных ВГА при биопсии печени установлено значительное повреждение портальной зоны с интенсивной клеточной инфильтрацией и разрушением пограничной пластины, выраженными признаками холестаза.
Даже при небольшом поражении гепатоцитов формируется гепатолиенальный синдром, развивается дискинезия желчевыводящих путей; при более выраженном поражении печени возникает желтуха. В дальнейшем для восстановления гепатоцитов требуется несколько недель, а для восстановления полной цитоархитектоники печени — несколько месяцев,
Аг вируса ВГА проявляют высокую иммуногенность: активация иммунной системы и специфическая сенсибилизация лимфоцитов начинаются с момента внедрения возбудителя.
Аг вируса (оболочечные белки) экспрессируются на мембранах гепатоцитов в комплексе с Аг главного комплекса гистосовместимости (HLA) I типа, и инфицированные клетки уничтожаются цитотоксическими Т-лимфоцитамииТ-кил-лерами.
Сходство Аг вируса и Аг гепатоцитов определяет развитие общих аутоиммунных процессов, от интенсивности которых во многом зависит исход заболевания. У лиц с генетической предрасположенностью вследствие ВГА может развить ся хронический аутоиммунный гепатит I типа. Описаны нефротический синдром с развитием мезангиопролиферативного гломерулонефрита, артриты, васкулиты, криоглобулинемии; при этом ВГА выступал в качестве провоцирующего факто ра. В очень редких случаях (0,1%) возможно развитие фульминантных форм ВГА.
Уже в инкубационный период выявляют специфические IgM; длительность инкубации объясняют индивидуальные особенности иммунного ответа. При бы стром нарастании титров AT желтуха не развивается.
В результате иммунных реакций в большинстве случаев довольно быстро, в течение 2—3нед, наступает выздоровление с полным освобождением организма от вируса. Вирусоносительство и хронические формы при ВГА не наблюдают.
Клиническая картина
Инкубационный период продолжается 3—4нед. ВГА протекает как острое циклическое заболевание и характеризуется последовательной сменой нескольких периодов — продромального (дожелтушного), разгара (желтушного) и периода реконвалесценции.
Дожелтушный период. Характеризуется достаточно широким разнообразием симптомов, условно сгруппированных в несколько вариантов его течения.
•Гриппоподобный (лихорадочный, катаральный) вариант при ВГА встречается наи более часто. Обычно заболевание начинается достаточно остро с повышения температуры тела (от субфебрильных до высоких цифр), слабости, недомога ния, мышечных болей, развития лёгких катаральных симптомов (заложенность носа, боли или першение в горле, покашливание). Однако гриппоподобная симптоматика у большинства больных сопровождается диспептическими рас стройствами различной степени выраженности.
•Диспептический вариант. Катаральные явления отсутствуют, и на первый план выступают симптомы вовлечения ЖКТ. Больных беспокоят дискомфорт в эпигастральной области, снижение аппетита до полной анорексии, тошнота, иног да рвота, возникающая чаще после приёма пищи. Возможны тупые боли в пра вом подреберье, горечь во рту, отрыжка, запоры или послабление стула.
•Астеновегетативный вариант. Характеризуется рядом неспецифических сим птомов: развитием общей слабости, потерей работоспособности, раздражи тельностью или безразличием, стойкой бессонницей или, наоборот, сонли востью.
ВГА может клинически проявиться сразу же с развития желтухи; в этом случае продромальные признаки отсутствуют (латентный вариант начального периода).
Следует подчеркнуть, что клиническая симптоматика, отнесённая к различ ным вариантам дожелтушного периода, может сочетаться в различных комбина циях. В этих случаях говорят о смешанном варианте.
Диагностика заболевания в начальный его период крайне затруднена. Необ ходимо опираться на данные эпидемиологического анамнеза (контакт с желтуш ными больными). При осмотре больных уже в это время можно обнаружить уве личенную в размерах печень и повышение показателей аминотрансфераз.
Начальный период заболевания продолжается от 2 до 7—10дней и плавно пе реходит вжелтушный. К этому моменту нормализуется температурная реакция, исчезают катаральные явления, однако диспептические симптомы сохраняются или даже могут возрастать по интенсивности.
Начало желтушного периода необходимо считать с момента появления тём ной мочи. Вслед за этим появляется иктеричность на уздечке языка, мягком нёбе, склерах, затем на кожных покровах. Её интенсивность быстро прогрессирует, обычно через 3-4дня достигая максимума; при этом желтуха часто приобре тает шафранный оттенок. Принято считать, что интенсивность желтухи прямо пропорциональна тяжести заболевания, однако при этом необходимо боль ше ориентироваться на выраженность синдрома интоксикации: повторную рвоту, диспептические расстройства, степень снижения аппетита. При более тяжёлом течении болезни на кожных покровах можно отметить появление си няков, особенно в местах инъекций. У части больных наблюдают носовые кровотечения.
Язык, как правило, обложен. Пальпаторно определяют увеличенную в разме рах печень, чувствительную при пальпации; степень её увеличения может быть различной. В 30-40%случаев к этому времени обнаруживают спленомегалию. У части больных в разгар желтухи появляется обесцвеченный стул. Со сторонысердечно-сосудистойсистемы достаточно характерны брадикардия и тенденция к снижению АД. На фоне желтухи помимо диспептических явлений больные от мечают адинамию, головокружение, иногда расстройства сна.
Продолжительность желтушного периода при ВГА не превышает 30 дней. Чаще он длится около 2 нед и переходит в период реконвалесценции. К этому времени происходит постепенное снижение интенсивности желтушного синдрома, умень шается в размерах печень, исчезают признаки интоксикации. Период реконва лесценции значительно более длителен, чем период желтухи, и может затягиваться до 3—6мес.
У 5—10%больных ВГА может приобрести более длительное течение, характе ризующееся малыми проявлениями или отсутствием интоксикации, неболь шими цифрами билирубинемии и гиперферментемии, стойким увеличением в размерах печени. Чаще всего это объясняет развитие холестаза. Несмотря на уве личенную продолжительность заболевание заканчивается благоприятно.
ВГА обычно протекает в лёгкой или среднетяжёлой формах, но не исключены и тяжёлые варианты, и обострения.
Диагностика ВГА в основном осуществляется при выраженном желтушном синдроме, однако накопилось большое количество сообщений о том, что ВГА зачастую может протекать в безжелтушной форме, которая в большинстве случаев не диагностируется. По мнению ряда исследователей, соотношение желтушных и безжелтушных форм может достигать 3:7.
Лабораторная диагностика
Лабораторные исследования приобретают особое значение для установления этиологии гепатита и оценки его тяжести. При анализе крови необходимо учитывать наличие лейкопении, относительного лимфоцитоза и замедление СОЭ.
Интенсивность желтухи устанавливают на основании определения уровня билирубина в крови (особенно его связанной фракции). Активность аминотрансфераз [аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (ACT)] увеличивается в несколько раз, и степень её повышения свидетельствует об интенсивности цитолиза гепатоцитов. Нарушения белоксинтетической функции печени отражают изменения показателей коллоидных проб (снижение сулемовой и повышение тимоловой проб), снижение уровня альбуминов и преальбуминов в крови, а также уменьшение показателей протромбинового индекса.
Возможно выделение вируса ВГА из фекалий, однако в широкой медицинской практике вирусологические исследования не применяют. Для верификации диагноза используют серологические реакции — ИФА, РИА, выявляющие нарастание специфических IgM в желтушный период и нарастание титров IgG к периоду реконвалесценции. Наиболее достоверный метод диагностики — обнаружение в крови РНК вируса с помощью ПЦР.
Осложнения
Развиваются сравнительно редко. К ним можно отнести обострения воспалительных процессов в жёлчных путях (холециститы, холангиты, дискинезии), а также развитие вторичных инфекций (пневмонии и др.). Острая печёночная энцефалопатия при ВГА развивается крайне редко.
Лечение
После установления факта заболевания ВГА лечение больного можно проводить в амбулаторных условиях. Госпитализируют больных с тяжёлым течением заболевания, затяжными формами, при наличии тяжёлых сопутствующих заболеваний, а также лиц декретированных групп.
Больным назначают постельный режим на период выраженного интоксикационного синдрома и полноценное питание. В диете исключают тугоплавкие жиры, трудно усвояемые сорта мяса (баранина, свинина, мясо водоплавающей птицы), жареные блюда, консервы, маринады, лук, чеснок и пряности. Категорически запрещено употребление алкоголя. Рекомендована молочно-раститель-ная пища. Дополнительно в пищевые продукты добавляют витамины групп С и В.
В связи с отсутствием средств этиотропной терапии проводят патогенетическое лечение. Для снятия интоксикации в зависимости от её степени применяют обильное питьё или инфузионные растворы. Для ежедневного очищения кишечника и подавления анаэробной флоры рекомендовано назначать производные лактулозы, дозы которых подбирают индивидуально. Для купирования холестатического компонента применяют спазмолитики (но-шпа,эуфиллин) и производные урсодезоксихолевой кислоты.
После завершения заболевания больной подлежит диспансерному наблюдению в течение 3—6мес.
Вирусный гепатит С (ВГС) — антропонозная вирусная инфекция из условной группы трансфузионных гепатитов, характеризующаяся поражением печени, безжелтушным, лёгким и среднетяжёлым течением в острой фазе и час той склонностью к хронизации, развитию циррозов печени и первичных гепатокарцином.
Этиология
Возбудитель — РНК-геномный вирус, включённый в состав безымянного рода семейства Flaviviridae. Вирионы сферической формы, окружены суперкапсидом; геном содержит однонитчатую РНК. Выделяют 6 серотипов и более чем 90 субтипов вируса, каждый из которых «привязан» к определённым странам, например в США распространёнВГС-1,в Японии —ВГС-2,тогда какВГС-2и-3чаще встречают в Северной и Центральной Европе, аВГС-4— на Ближнем Востоке и в Африке. Перекрёстного иммунитета эти серотипы не дают. В ряде исследований показано, что подтип lb сочетается с более тяжёлым течением заболевания, более высоким содержанием РНК ВГС крови, большей устойчивостью к противовирусным препаратам и большей вероятностью серьёзного рецидива.
Отличительной особенностью вируса ВГС является способность к длительной персистенции в организме, что обусловливает высокий уровень хронизации инфекции. Механизмы, лежащие в основе неэффективной элиминации вируса, изучены недостаточно. Основное значение придают высокой изменчивости возбудителя. Подобно другим флавивирусам дочерние популяции ВГС образуют вазиштаммы — иммунологически различающиеся антигенные варианты, ускользающие от иммунного надзора, что усложняет разработку вакцины.
Поскольку вирус ВГС не размножается на культурах клеток, сведения о чувствительности вируса к воздействию факторов внешней среды малочисленны. Вирус устойчив к нагреванию до 50 °С, инактивируется УФО. Устойчивость возбудителя во внешней среде более выражена, чем у ВИЧ.
Эпидемиология
Резервуар и источник инфекции — больные хроническими и острыми формами болезни, протекающими как с клиническими проявлениями, так и бессимптомно. Сыворотка и плазма крови инфицированного человека заразны в течение периода, начинающегося с одной или нескольких недель до появления клинических признаков болезни, и могут содержать вирус неопределённо долгое время.
Механизм передачи. Аналогичен ВГВ, однако структура путей заражения имеет свои особенности. Это связано с относительно невысокой устойчивостью вирус* во внешней среде и довольно большой инфицирующей дозой, необходимой для заражения. Вирус ВГС передаётся прежде всего через заражённую кровь и в меньшей степени через другие биологические жидкости человека. РНК вируса обнаружена в слюне, моче, семенной и асцитической жидкостях.
К группам повышенного риска относят лиц, которым многократно переливали кровь и её препараты, а также лиц, имеющих в анамнезе массивные медицинские вмешательства, пересадку органов от доноров с ВГС-положительной реакцией и многократные парентеральные манипуляции, особенно при повторное использовании нестерильных шприцев и игл. Распространённость ВГС среди наркоманов очень высока(70—90%);этот путь передачи представляет собой наибольшую опасность в распространении заболевания. \ Риск передачи вируса повышают процедуры гемодиализа, нанесение татуировок, нарушение целостности кожи при инъекциях.
Вертикальная передача ВГС от беременной к плоду редка, но возможна Частота половой передачи возбудителя возрастает при сопутствующей ВИЧ-инф||ции, большом количестве сексуальных партнёров
Естественная восприимчивость высокая и в большой степени определяется инфицирующей дозой. Напряжённость и длительность постинфекционного иммунитета неизвестны. В экспериментах на обезьянах показана возможность повторного заболевания.
Основные эпидемиологические признаки. Инфекция распространена повсеместно.
Основную группу заболевших составляют, как и при ВГВ, подростки и лица 20-29лет. Число заразившихся в ЛПУ составляет1-2%всех случаев инфекции. ВГС является одной из основных причин развития хронических диффузных заболеваний печени и гепатоцеллюлярной карциномы (первичного рака печени). Цирроз печени, обусловленный ВГС, занимает одно из основных мест в ряду показаний к трансплантации печени.
Патогенез
Остаётся плохо изученным. Прямому цитопатическому действию вируса на гепатоциты отводится незначительная роль, причём только при первичной инфекции. Основные поражения различных органов и тканей при ВГС обусловлены иммунологическими реакциями. Доказана репликация вируса вне печени — в тканях лимфоидного и нелимфоидного происхождения. Размножение вируса в иммунокомпетентных клетках (моноцитах) приводит к нарушению их иммунологических функций.
Высокая хронизация ВГС, очевидно, в первую очередь объясняется отсутствием формирования достаточного защитного иммунного ответа, т.е. образования специфических AT, что является следствием большой частоты сбоев транскрипции РНК ВГС. У инфицированных лиц происходит постоянная быстрая мутация ВГС, особенно по поверхностным белкам вируса, что не позволяет полностью реализоваться клеточным звеньям иммунитета (антителозависимый и Т-клеточ-но-опосредованныйкиллинг инфицированных вирусом клеток).
Всё это позволяет предположить наличие двух ведущих факторов в патогенезе ВГС: 1. Постоянная неконтролируемая репликация вируса; 2. Активный, но неэффективный гуморальный иммунный ответ. Эти факторы способствуют образованию значительного количества перекрёстно реагирующих ауто-АТи поликлональной гаммаглобулинопатии, что реализуется в виде большого числа аутоиммунных заболеваний, ассоциируемых с персистенцией ВГС или запускаемых ВГС с последующей элиминацией вируса.
Клиническая картина
Инкубационный период. Составляет2—13нед, однако в зависимости от пути передачи может удлиняться до 26 нед.
Острая инфекция большей частью клинически не диагностируется, протекает преимущественно в субклинической безжелтушной форме, составляющей до 95% всех случаев острого ВГС Поздняя лабораторная диагностика острой инфекцииобусловлена существованием так называемого «антительного окна»: при исследовании тестсистемами первого и второго поколений AT к ВГС у 61% больных появляются в период до 6 мес от начальных клинических проявлений, а во многих случаях и значительно позже.
При клинически манифестной форме острого ВГС классические признаки заболевания выражены незначительно или отсутствуют. Больные отмечают слабость, вялость, быструю утомляемость, ухудшение аппетита, снижение толерантности к пищевым нагрузкам. Иногда в до желтушном периоде возникают тяжесть в правом подреберье, лихорадка, артралгии, полиневропатия, диспептические про явления. В общем анализе крови могут выявлять лейко- и тромбоцитопению. Желтуху встречают у 25% больных, в основном у лиц с посттрансфузионным заражением. Течение желтушного периода чаще всего лёгкое, иктеричность быстро исчезает. Заболевание склонно к обострениям, при которых вновь возникает желтушный синдром и повышается активность аминотрансфераз.
Вместе с тем в настоящее время описаны редко встречающиеся (не более 1% случаев) фульминантные формы ВГС.
В части случаев манифестацию острой инфекции сопровождают тяжёлые аутоиммунные реакции — апластическая анемия, агранулоцитоз, периферическая невропатия. Эти процессы связаны с внепечёночной репликацией вируса и могут завершиться гибелью больных до появления значимых титров AT.
Отличительная особенность ВГС — многолетнее латентное или малосимптомное течение по типу так называемой медленной вирусной инфекции. В таких случаях заболевание большей частью долго остаётся нераспознанным и диагностируется на далеко зашедших клинических стадиях, в том числе на фоне развития цирроза печени и первичной гепатоцеллюлярной карциномы.
Дата добавления: 2020-04-25; просмотров: 149; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
