Комплексонометрия. Комплексоны, их строение и свойства.
Комплексоны-это органические соединения, в молекулах которых содержится большое число основных донорных центров и кислых функциональных групп, расположенных так, что при их взаимодействии образуются комплексонаты.
| Нитрилотриуксусная кислота | Этилендиаминтетрауксусная кислота(ЭДТУК) | Этилендиаминтетраацетат(ЭДТА) | Диаминциклогексантетрауксусная кислота |
| N(CH2COOH)3 | (HOOCCH2)2N-CH2CH-N(CH2COOH)2 | Na2H2Y*2H2O | 
|
| Дентантность=4 | Дентантность=6 | Дентантность=6 | Дентантность=6 |
Состав и устойчивость комплексонатов.
Состав и устойчивость комплексонатов:
1.Если в растворе доминирует форма H2Y^2-,то реакции комплексообразования протек по схеме:
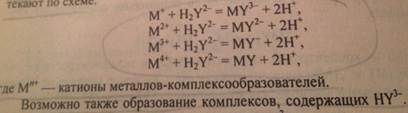
2.При образовании комплексоната металла возникают несколько хелатных циклов,поэтому комплексонаты-устойчивые соединения(устойчивость зависит от природы катиона Ме,его заряда,состав комплекса,температуры)
3.Катионы щелочных Ме образуют малостойкие эдетеаты как с Y^4- и c HY^3-
Трилонометрия. Прямая, заместительная, обратная.
Титрант – Трилон Б (Эитилендиаминтетраацетат) Реагирует с определяемым металлом 1:1
Условия: Использование буферных систем


Гексацианоферратометрия.


Меркуриметрия.
Меркуриметрия-метод анализа, основанный на образовании растворимых комплексных соединений ртути(2).
1)Титрант-стандартные растворы Hg(NO3)2 или перхлората Hg(ClO4)2
2)Условия:кислая среда.
3)Титрант-вторичный стандарт.
Стандартизация по NaCl или NH 4 SCN :
Hg(2)+2Cl=HgCl2(изменение окраски из розово-желт до светло-сиренев);Hg(2)+2SCN=Hg(SCN)2 Фиксация КТТ:по изменению окраски индикатора,либо по появлению осадка.
4)Применение:для определения анионов Cl,Br,I,CN,SCN,Hg(2)
Индикаторы:
Равновесия в водных растворах ЭДТУК.
Комплексон Н4Y-четырехосновная кислота.При pH<1.6 она протонируется:протоны присоединяются к молекуле ЭДТУК,образуя формы H5Y,H6Y.

В водных растворах существуют и находятся в равновесии все формы ЭДТУК,в зависимости от кислотности среды.
Требования, предъявляемые к реакциям в комплексиметрии.
Комплексиметрия-это группа методов анализа, основанных на использовании реакции комплексообразования между определяемым компонентом анализируемого раствора и титрантом.
Требования:
1.Стехиометричность. В реакции должен образовываться 1 продукт точно определенного вещ-ва.
2.Полнота протекания реакции. Она должна протекать не менее чем на 99,99 %.
3.Должна протекать быстро.
4.Должна обеспечивать отчетливую фиксацию КТТ.
Особенности работы металлохромных индикаторов. Примеры.
Сущность обнаружения КТТ:
1.При добавлении индикатора к исходному раствору тируем катион Ме образуя окрашиваемый растворимый комплекс.

2.В процессе титрования данного раствора в точке экв.или в близи нее комплекс Ме с индикатором разрушается.
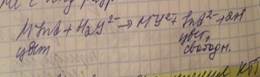
Условия:
1. Металлохромные индикаторы должны образовывать достаточно прочные, окрашенные комплексы с определяемыми катионами Ме,с тем чтобы окраска раствора была устойчивой и отчетливой.
2. Комплексы определяемых катионов с индикатором должны быть менее устойчивы, чем комплексы тех же катионов с комплексоном.
3. Изменение окраски раствора в ТЭ должно быть контрастным.
4. Комплексы Ме с индикатором должен разрушатся быстро.
Дата добавления: 2020-04-25; просмотров: 795; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
