Темы для реферативных сообщений
1. Белки — положительные реактанты острой фазы воспаления.
2. Возрастная динамика белковых фракций. Эмбриоспецифические белки и их диагностическое значение.
3. Остаточный азот: его основные компоненты. Возрастная динамика уровня фракций остаточного азота.
Лабораторная работа 1.
Определение содержания остаточного азота в сыворотке крови
Актуальность
Остаточный азот является суммарным показателем безбелкового азота крови. Он складывается из мочевины (около 50 %), аминокислот (около 25 %), эрготионеина (около 8 %), креатина и креатинина (до 7,5 %), пептидов, нуклеотидов и азотистых оснований (около 5 %), мочевой кислоты (до 4%), аммиака и индикана (0,5 %). Необходимо учитывать: поскольку показатель включает различные низкомолекулярные азотсодержащие вещества, то более информативным в клинике является определение отдельных фракций остаточного азота, а не суммарного показателя.
Принцип метода
Определение содержания остаточного азота по методу Аселя основано на сжигании безбелкового фильтрата с концентрированной серной кислотой и переходе азота органических веществ в сульфат аммония, который с реактивом Несслера образует продукты желто-оранжевого цвета. Интенсивность окраски прямо пропорциональна концентрации азота.
Реактивы
1) 10% раствор ТХУ, 2) концентрированная H2SO4, 3) 3% раствор Н2О2, 4) реактив Несслера (щелочной раствор йодистых солей ртути и калия), 5) 5% раствор NaOH, 6) 26 ммоль/л стандартный раствор (NH4)2SO4, 7) лакмусовая бумага.
|
|
|
Материал для исследования
Сыворотка крови.
Проведение анализа
Подготовительный этап выполняет лаборант: в центрифужную пробирку вносят 1,8 мл дистиллированной воды и 0,2 мл сыворотки крови, приливают 1,0 мл 10% раствора ТХУ, центрифугируют, из пробирки берут 1,0 мл надосадка и переносят в термостойкую пробирку для минерализации, приливают 3 капли концентрированной H2SO4 и 3 капли Н2О2. Осторожно упаривая жидкость, нагревают до получения бесцветного минерализата.
Цветную реакцию на остаточный азот проводят согласно таблице:
| Опыт, мл | Стандарт, мл | |
| Минерализат | 1,0 | –– |
| Стандартный раствор (NH4)2SO4 | –– | 1,0 |
| Раствор NaOH | добавляют по каплям, проверяя величину рН по лакмусовой бумажке, пока рН не станет нейтральной и лакмус не посинеет (излишек NaOH вызывает помутнение раствора) | |
| Дистил. вода Реактив Несслера | 8,0 2,0 | 8,0 2,0 |
| Измеряют оптическую плотность опыта и стандара против воды в кювете с длиной оптического пути 10 мм при длине волны 540 нм (зеленый светофильтр) | ||
Расчет
Расчёт проводят по формуле:
Содержание остаточного азота [ммоль/л] = 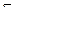 ,
,
где ЕОП и ЕСТ — оптическая плотность опытной и стандартной проб,
ССТ — концентрация стандартногораствора.
|
|
|
Клинико‑диагностическое значение
Остаточный азот — это суммарный показатель состояния обмена белков. Снижениеконцентрации остаточного азота (гипоазотемия) возникает при снижении содержания мочевины, аминокислот или других его фракций.
Увеличениефракций остаточного азота (гиперазотемия) может быть абсолютной, связанной с действительным накоплением этих компонентов в крови, и относительной, связанной с дегидратацией организма. В свою очередь, абсолютная гиперазотемия может быть ретенционная (почечного и внепочечного происхождения) и продукционная.
Ретенционная азотемия возникает в результате задержки выведения азотосодержащих веществ и бывает почечного происхождения (заболевания клубочков — нефриты, туберкулез почек, нефросклероз и др.) и внепочечного происхождения. Внепочечные гиперазотемии подразделяют на надпочечные (результат нарушения гемодинамики и падения фильтрационного давления при сердечно-сосудистой недостаточности, снижении артериального давления) и подпочечные (при гипертрофии или аденоме простаты, почечно-каменной болезни).
Продукционная азотемия выявляется при всех состояниях, связанных с увеличением распада белков, от ретенционной ее отличает повышение содержания аминокислот в крови, а также одновременное накопление азотистых компонентов в крови и моче.
|
|
|
Оформление работы
Указывают принцип метода, записывают результаты, производят расчёты, делают вывод о возможной патологии, отмечают клинико-диагностическое значение.
Лабораторная работа 2 (теоретически).
Электрофорез белков на бумаге и ацетатцеллюлозных пленках
Принцип
Белковые молекулы, отрицательно заряженные при рН 6,8, перемещаются в электрическом поле постоянного тока по направлению к аноду. Наиболее быстро перемещаются альбумины, затем по порядку a1‑, a2‑, b‑ и g‑глобулины. На ход электрофореза влияет подвижность разделяемых веществ, зависящая от следующих факторов: 1) заряд (зависит от pH), размеры и форма молекул веществ; 2) электрическое поле ‑ скорость движения ионов белка прямо пропорциональна силе тока и напряжению и обратно пропорциональна сопротивлению (зависит от типа и размеров носителя и ионной силы буфера); 3) буферный раствор ‑ состав, концентрация, pH и ионная сила (зависит от концентрации присутствующих ионов и их заряда); 4) носитель ‑ учитывается его гидрофильность и адсорбция веществ на его молекулах.
|
|
|
Материал для исследования
Сыворотка крови.
Оборудование
1) Прибор для электрофореза, 2) денситометр.
Проведение анализа (основные положения)
Образцы сыворотки равномерно наносят по линии старта на носитель (бумага, ацетатцеллюлозная пленка). Носитель помещают в прибор для электрофореза, подают электрический ток. Буферный раствор, двигаясь в электрическом поле, захватывает молекулы белка. Молекулы с наибольшим отрицательным зарядом и наименьшим размером (альбумины) двигаются быстрее остальных, последними оказываются наиболее крупные и нейтральные (g‑глобулины). Через определённое время (устанавливают для каждого прибора индивидуально) электрофорез завершают.

|
Полоски бумаги/ацетатцеллюлозной пленки отмывают от буферного раствора и окрашивают. В итоге участки, содержащие белок, прокрашиваются, причём площадь и интенсивность окраски зависят от содержания белка во фракции.
В настоящее время количественный учет окрашенных зон на электрофореграмме проводят при помощи денситометра. Работа денситометра основана на пропускании луча света через движущуюся полоску носителя. При изменении интенсивности окраски носителя происходит "всплеск" и регистрируется наличие окрашенной зоны (белковой фракции). Параллельно современные приборы автоматически рассчитывают процентное соотношение белковых фракций.
|
Клинико-диагностическое значение
Альбумины
Снижение содержания фракции альбуминов связано с пониженным синтезом альбуминов — при врожденной анальбуминемии, белковом голодании, нарушении всасывания, тяжелых поражениях печени (цирроз, дистрофии, некроз, активный гепатит, амилоидоз печени); или с повышенным катаболизмом альбуминов — при лихорадке, кахексии, тяжелых инфекциях, панкреатите, коллагенозах, тиреотоксикозе, болезни Иценко-Кушинга (гипофункция надпочечников); или с потерей альбуминов через поверхности ожогов, почки, пищеварительный тракт; или с выходом альбумина из кровотока в межклеточное пространство при воспалительных процессах.
a -Глобулины
Повышение содержания a1‑ и a2‑глобулиновой фракции происходит при острых и подострых воспалительных процессах, некоторыми злхачественных опухолях, травмах, так как эти фракции содержат большинство белков острой фазы (С‑реактивный белок, церулоплазмин, гаптоглобин, a1‑гликопротеин, a1‑анти-трипсин, a2‑макроглобулин).
b -Глобулины
Большая доля белков b‑глобулиновой фракции является b‑липопротеинами (ЛПОНП и ЛПНП), поэтому повышение этой фракции чаще всего связано с гиперлипопротеинемиями. Влияние на динамику этой фракции оказывают трансферрин, гемопексин, компоненты системы комплемента.
g -Глобулины
Содержание g‑глобулинов увеличивается при патологических состояниях, связанных с хроническими воспалительными процессами, так как класс содержит иммуноглобулины G, A, M.
Лабораторная работа 3.
Оценка альбуминовой фракции белков сыворотки крови
Реактивы
1) Рабочий раствор (бромкрезоловый зелёный в сукцинатном буфере, 2) 40 г/л стандартный раствор альбумина, 3) биуретовый реактив (раствор сульфата меди (II) и натрия гидроксида), 4) 70 г/л стандартный раствор альбумина.
Материал для исследования
Сыворотка крови.
Дата добавления: 2020-04-25; просмотров: 104; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!

