Опыт 6.2.3 Выделение жирных кислот из мыла
Реактивы, материалы, приборы: мыло, 10%-й раствор соляной кислоты, пробирки, спиртовки, мерные пробирки.
В пробирку помещают кусочек полученного мыла (опыт 4.5.9), добавляют 5 см3 10%-ной HCl и нагревают до кипения. Жировые кислоты всплывают в виде маслянистого слоя, застывающего при охлаждении.
R–COONa + HCl ¾¾ ® R–COOH↓ + NaCl
Напишите уравнение реакции стеарата натрия с хлороводородной кислотой.
Наблюдение:
Выводы:
Опыт 6.2.4 Образование кальциевых солей жирных кислот
Реактивы, материалы, приборы: мыло, 5%-й раствор хлорида кальция, пробирки.
В воде растворяют небольшой кусочек полученного мыла и добавляют 1 см3 5%-го раствора хлорида кальция. При нагревании выпадает осадок кальциевых солей высших карбоновых кислот.
2R–COONa + Са Cl2 ¾¾ ® ( R–COO)2 Са ↓ + 2NaCl
Аналогично в процессе обменных реакций осаждаются нерастворимые в воде соли свинца и меди с анионами высших карбоновых кислот.
Напишите уравнение реакции пальмитата натрия с нитратом кальция.
Наблюдение:
Выводы:
Опыт 6.2.5 Обнаружение остатков ненасыщенных
кислот в жире
Реактивы, материалы, приборы: подсолнечное масло, маргарин, хлороформ, 1%-й водный раствор крахмала, 0,05%-й раствор йода в спирте, пробирки, капельницы.
В две пробирки наливают по 1 см3 хлороформа и добавляют в одну из них 0,5 г маргарина, а в другую 0,5 г подсолнечного масла. Встряхивают до полного растворения, добавляют по 2 капли 1%-го водного раствора крахмала и приливают 0,05%-ный спиртовой раствор йода до появления синего окрашивания. На поверхности смеси появляется синее кольцо.
|
|
|
Присоединение йода (Х=I) происходит по двойным связям, которые содержатся в остатках ненасыщенных жирных кислот подсолнечного масла (олеиновая, линолевая, линоленовая):
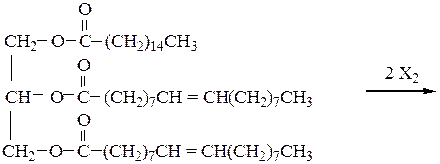
1-Пальмитоил - 2,3 - диолеилглицерин

Реакция присоединения йода по месту разрыва двойных связей в жирных кислотах является качественной пробой на свойство непредельности жира. При количественном определении степени ненасыщенности жира определяют йодное число, т.е. количество граммов йода, присоединяющееся к 100 г жира.
Рассчитайте йодное число триолеата глицерина.
Наблюдение:
Выводы:
УГЛЕВОДЫ
Сахариды – это циклические полуацетали алифатических многоатомных гидроксиальдегидов или гидроксикетонов. В растворе циклические полуацетали находятся в таутомерном равновесии с открытыми цепными формами, содержащими свободные карбонильные группы. Поэтому для сахаридов характерны реакции как по карбонильной группе (окисление, восстановление, присоединение синильной кислоты, образование оксимов, озазонов), так и по спиртовым и гликозидному гидроксилам в циклической форме с образованием сахаратов, простых, сложных эфиров и гликозидов.
|
|
|
МОНОСАХАРИДЫ
Опыт 7.1.1 Реакции карбонильной группы
Реактивы, материалы, приборы: 5%-й раствор глюкозы, аммиакат серебра, жидкость Фелинга, солянокислый фенилгидразин, ацетат натрия безводный, пробирки, капельницы, водяные бани.
а) Окисление моносахаридов аммиачным раствором оксида серебра (реакция серебряного зеркала). В чистой пробирке смешивают 1 см3 5%-го раствора глюкозы с 1 см3 аммиачного раствора оксида серебра (реактива Толенса) и нагревают на водяной бане. Металлическое серебро выделяется в виде зеркала на стенках пробирки. Глюкоза окисляется до глюконовой кислоты:

б) Окисление жидкостью Фелинга. К 1 см3 раствора глюкозы приливают равное количество раствора Фелинга и нагревают на водяной бане. Образуется желтый осадок гидроксида меди (I), переходящий в красный осадок оксида меди (I). Глюкоза при этом окисляется в глюконовую кислоту:

в) Образование фенилозазона глюкозы. В растворе смеси солянокислого фенилгидразина и ацетата натрия при обменной реакции образуется ацетат фенилгидразина, который как соль слабой кислоты и слабого основания, сильно гидролизуется. В растворе ацетат фенил-гидразина находится в равновесии со свободным фенилгидразином, который и реагирует с глюкозой:
|
|
|
С 6 H5NHNH2 ▪ HCl + CH3COONa ¾ ® С 6 H5NHNH2 ▪ CH3COOH + NaCl
С 6 H5NHNH2 ▪ CH3COOH + H2O ↔ С 6 H5NHNH2 + CH3COOH

В пробирку вносят небольшое количество кристаллов солянокислого фенилгидразина и такое же количество ацетата натрия, добавляют 3 капли раствора глюкозы и нагревают на кипящей водяной бане. Через 10-15 мин в пробирке выпадают желтые кристаллы глюкозазона, которые наблюдают под микроскопом.
Как можно отличить D-глюкозу от D-фруктозы?
Напишите уравнение реакции D-рибозы с избытком фенилгидразина. Какие еще моносахариды образуют озазон того же строения?
Наблюдение:
Выводы:
Дата добавления: 2020-04-08; просмотров: 263; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
