Атеросклероз. Эпидемиология. Факторы риска. Теории патогенеза. Первичная и вторичная профилактика.
Атеросклероз - уплотнение интимы артерий и отложение в ней липидов (atero – кашица; sclerosis -уплотнение)
Атеросклероз в развитых странах вышел на первое место как причина заболеваемости. Атеросклероз обусловливает примерно половину смертных случаев в целом по популяции и является причиной около 1/3 летальных исходов у лиц в возрасте 35–65 лет.
По оценкам Всемирной Организации Здравоохранения, ежегодно в мире от сердечно-сосудистых заболеваний погибает более 17 млн человек, причем 90% смертей приходится на эти основные осложнения атеросклероза; ишемическая болезнь сердца является основной причиной смерти в индустриально развитых странах.
В России на долю сердечно-сосудистых заболеваний приходится 53-55% общей смертности и она продолжает расти, в то время как в США и во многих западноевропейских странах (Швеции, Франции, Нидерландах) этот показатель постепенно снижается за счет эффективной борьбы с атеросклерозом и его осложнениями. Несмотря на это, к 2020 году атеросклероз может стать главной причиной смертности населения во всем мире. Наиболее часто атеросклероз наблюдается у мужчин; у женщин риск развития этого заболевания повышается после наступления менопаузы. В большинстве случаев клинические проявления атеросклероза регистрируются в возрасте 40-70 лет.
Факторы риска развития атеросклероза
В настоящее время кардиологи выделяют немодифицируемые (неизменяемые) и модифицируемые (изменяемые) факторы риска развития атеросклероза.
Немодифицируемые (неизменяемые) факторы риска
Возраст. Пол. Атеросклероз чаще наблюдается у мужчин.
Отягощенная наследственность (семейный анамнез).
Модифицируемые (изменяемые) факторы риска
Дислипидемии (нарушения жирового обмена).
В патогенезе атеросклероза имеют важное значение следующие показатели жирового обмена:
· Высокие показатели общего холестерина.
· Высокое содержание холестерина липопротеинов низкой плотности
· Низкое содержание холестерина липопротеинов высокой плотности
· Гипертриглицеридемия.
Артериальная гипертензия (АГ).
Курение.
К числу наиболее значимых и в то же время наиболее легко модифицируемых факторов риска атеросклероза и ИБС относится ожирение, в особенности – висцеральное, с «центральным» распределением жира в организме.
Нарушения углеводного обмена (сахарный диабет, гипергликемия).
Сахарный диабет I и II типа сочетается со значительным увеличением заболеваемости атеросклерозом и тяжестью течения многих его клинических проявлений.
Малоподвижный образ жизни (гиподинамия).
Нерациональное питание.
Почечная недостаточность.
Хроническое воспаление и стресс.
Патогенез. В атеросклеротическом процессе задействовано множество патологических механизмов, но наибольшее значение принадлежит повышенному уровню холестерина.
Холестерин – биомолекула, без которой невозможна жизнь. Он является составной частью клеточных мембран, предшественником желчных кислот, стероидных и половых гормонов. В то же время избыток холестерина становится причиной развития тяжелого атеросклероза.

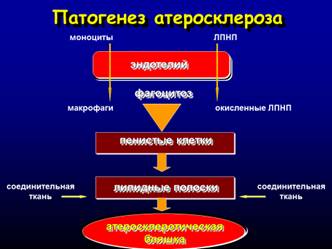
Различают три основные стадии формирования атеросклеротической бляшки (атерогенез):
1) Образование липидных пятен и полосок (стадия липоидоза).
2) Образование фиброзной бляшки (стадия липосклероза).
3) Формирование осложненной атеросклеротической бляшки.
Начальная стадия характеризуется появлением в интиме артерий пятен и полосок, содержащих липиды.
Основа патогенеза – хроническое эндотелиальное повреждение.
Артериальная стенка (коронарной артерии) представлена тремя основными слоями: интима, медия, адвентиция. Интима представляет собой монослой эндотелиальных клеток.
При нормальном содержании липидов в крови ЛПВП препятствуют проникновению ЛПНП в стенку артерии. Процесс активного удаления холестерина ЛПНП, накопленного в стенке сосуда, с помощью ЛПВП получил название обратного транспорта холестерина (обратный транспорт ХС – процесс обратного переноса ХС от тканей организма в клетки печени с последующим выведением его наружу через желч). Однако при избыточном содержании в крови ЛПНП или слишком низком уровне ЛПВП данный баланс нарушается и происходит накопление ЛПНП в артериальной стенке. Под действием эндотелиальных клеток происходит окисление ЛПНП. Появление окисленных ЛПНП запускает воспалительный процесс, в результате чего из кровотока в место повреждения начинают поступать клетки воспаления – моноциты. В эндотелии они превращаются в макрофаги. Макрофаги начинают активно поглощать и переваривать богатые холестерином окисленные ЛПНП. По мере поглощения ЛПНП макрофаги увеличиваются и превращаются в пенистые клетки.
Накопление пенистых клеток в интиме коронарной артерии приводит к формированию жировой полоски, которую принято рассматривать как первое патологическое проявление атеросклероза. Однако на этой стадии сужения просвета артерии нет.
По мере увеличения объема жировой полоски на ней появляется фиброзная покрышка и образуется атеросклеротическая бляшка.
Согласно принятой в настоящее время концепции, клиническое и прогностическое значение коронарного атеросклероза определяется стадией развития и морфологическими особенностями атеросклеротических бляшек.
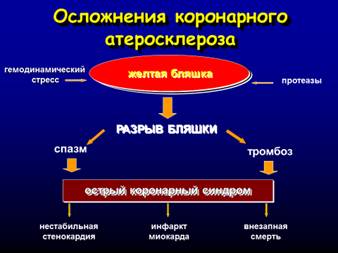
Оказалось, что инфаркт миокарда чаще возникает на месте разрыва так называемой «ранимой» (нестабильной, желтой) бляшки, которая редко вызывает значимое стенозирование просвета сосуда и часто не выявляется при коронарографии. В исследованиях было показано, что 80-90% инфарктов миокарда связано с разрывами бляшек, суживающих просвет коронарной артерии менее чем на 70%.
В дальнейших гистохимических исследованиях было установлено, что ранимые бляшки отличаются от стабильной тем, что имеют большое липидное ядро, тонкую соединительнотканную капсулу и высокое содержание воспалительных клеточных. Их еще называют желтыми (нестабильными) бляшками («желтая», т.к. через тонкую капсулу просвечиваются липиды). Благодаря своей эластичности и небольшим размерам они обычно не вызывают гемодинамически значимого сужения коронарных артерий и чаще всего не выявляются при коронарографии. На периферии желтых бляшек расположены Т-лимфоциты, секретирующие гамма-интерферон, который ингибирует синтез коллагена гладкомышечными клетками и тем самым препятствует укреплению фиброзной капсулы бляшки.
Покрышка может быть повреждена как в связи с воздействием гемодинамических факторов (например, перепады давления в сосуде), так и в результате того, что содержащиеся вблизи оболочки макрофаги и тучные клетки вырабатывают протеиназы, которые способны разрушить защитный интерстициальный матрикс.
Разрыв фиброзной капсулы приводит к контакту содержащихся в бляшке детрита и липидов с тромбоцитами и немедленному формированию тромба. В результате развивается острый коронарный синдром, проявляющийся нестабильной стенокардией, инфарктом миокарда или внезапной смертью.

Клиническая картина
Ксантелазмы на веках
Липоидная дуга роговицы
Туберозные и сухожильные ксантомы (На разгибательных поверхностях кистей, локтевых и коленных суставов, ахилловых сухожилий)
Желтоватое окрашивание ладонного рисунка
Лечение.
1. Немедикаментозные
антисклеротическая диета, физические
тренировки, устранение факторов риска, прекращение курения
2. Медикаментозные
статины, секвестранты желчных кислот, никотиновая кислота, фибраты
3. Хирургические
операция шунтирования части тонкого кишечника, плазмаферез ЛПНП
Механизм действия статинов Ингибирование ГМГ-КоА-редуктазы →
в гепатоцитах ↓ эндогенный синтез ХС → ↑ компенсаторно R на поверхности печеночной клетки→ ↑ выведение из плазмы и связывание ХС ЛПНП → ↓ в крови ХС + в печени ↓ синтез ЛПОНП
- Компактин – 1976 г., Penicillium citrinum
- Ловастатин (мевакор) – 1987 г.
- Правастатин (липостат) – 1991 г.
- Симвастатин (зокор) – 1992 г.
- Флувастатин (лескол) – 1994 г.
- Аторвастатин (липримар) – 1997 г.
- Церивастатин (липобай) – 1998 г.
Прием на ночь: Доза 5-10 мг до 20-40 мг /сут (max 80 мг/сут)
Основным механизмом действия производных фиброевой кислоты является активация плазменной и печеночной липопротеидлипазы, ферментов, регулирующих катаболизм ЛПОНП и ЛППП (богатых ТГ частиц), что приводит к снижению их уровня и существенному уменьшению концентрации ТГ в плазме. Кроме того, фибраты тормозят синтез в печени ЛПОНП.
- Клофибрат – не используется
- Гемфиброзил 600 мг 2 р/д
- Безафибрат (безалип, безамидин)
- Ципрофибрат (липанор)
- Фенофибрат (липантил 200 М) 200 мг 1 р/д
Прием утром во время еды
- Никотиновая кислота 2-4 г/сут в 2-3 приема
- Эндурацин 1,5 г/сут в 3 приема
Прием во время еды
Секвестранты желчных кислот: - Холестирамин 8-24 г/сут
- Колестипол 5-30 г/сут в виде порошка, растворенного в чае или кисиле
Прием перед едой
Дата добавления: 2019-11-25; просмотров: 458; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
