Образование микрогальванопар в кислой среде
Поместите в пробирку кусочек гранулированного цинка и прилейте 3-5 мл 2 М серной кислоты. Обратите внимание на медленное выделение водорода. Прилейте в пробирку несколько капель 0,5 н. раствора сульфата меди. Что наблюдается? Составьте схему образующейся гальванопары и объясните наблюдаемые явления.
Опыт № 2
Коррозия при контакте различных металлов
Налейте в пробирку 5-6 мл 0,1 н. серной кислоты и опустите в нее медную проволоку. Что наблюдается? Выньте медную проволоку из пробирки и поместите на ее место цинковую гранулу. Что наблюдаете? Через 2-3 минуты вновь опустите в пробирку медную проволоку таким образом, чтобы она соприкасалась с гранулой.
Объясните наблюдаемые явления и составьте схему образующейся гальванопары.
Опыт № 3
Коррозия железа в нейтральной среде при участии кислорода
В плоскодонную колбу на 25-50 мл поместите обезжиренные ацетоном и промытые дистиллированной водой чугунные или стальные опилки и смочите их 3%-ным раствором хлорида натрия. Колбу закройте резиновой пробкой с изогнутой вниз стеклянной трубкой, свободный конец которой погрузите в стакан с дистиллированной водой (рис.2.)
|
Через некоторое время отмечается подъем воды в трубке. Почему это происходит? Составьте уравнения происходящих коррозионных процессов. Чем данный процесс отличается от коррозии железа в кислой среде? Как в этом случае среда влияет на коррозию?
|
|
|
Опыт № 4
Коррозия стали
Очистите стальную пластинку наждачной бумагой, промойте дистиллированной водой и осушите фильтровальной бумагой. Затем на пластинку нанесите одну каплю реактива, полученного при смешивании 5 мл 3%-ного раствора хлорида натрия, 0,5 мл 0,5 н. раствора гексацианоферрата калия К3[Fe(CN)6] и 2-3 капли 0,1%-ного раствора фенолфталеина. Наблюдайте появление синего окрашивания в центре капли и малинового окрашивания по ее окружности. Объясните наблюдаемые явления и составьте схему образующейся гальванопары.
Контрольные вопросы
1. Что такое коррозия металлов? Какие виды коррозии Вы знаете?
2. Как будет протекать коррозия железа в кислой среде:
а) частично покрытого медью;
б) частично покрытого цинком?
3. Какие процессы протекают на поверхности стального листа во влажном воздухе?
4. Какому виду коррозии подвергается стальная деталь с медными заклепками на воздухе?
Лабораторная работа № 13
ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ
Теоретическая часть
Меры борьбы с коррозией — актуальная задача современной техники. Главное внимание в борьбе с наиболее распространенным видом коррозии — электрохимической — направлено на то, чтобы исключить возникновение макро- и микрогальванических пар.
|
|
|
Основными методами защиты металлов от коррозии являются:
Защитные покрытия
Они, в свою очередь, подразделяются на три вида:
а) химические — это искусственно создаваемые пленки различного состава (оксидирование, фосфатирование, цементация, азотирование, цианирование и т.д.);
б) неметаллические — краски, лаки, эмали, покрытие полимерными материалами;
в) металлические — бывают анодные и катодные в зависимости от химической природы металлов.
Если покрытие осуществляют металлом, имеющим меньшее значение стандартного электродного потенциала  , чем покрываемый металл, то покрытие называется анодным (например, оцинкованое железо). При нарушении целостности этого покрытия в присутствии электролита (атмосферная влага, кислоты, соли и т.д.) образуется гальванопара, в которой роль анода играет металл с меньшим значением
, чем покрываемый металл, то покрытие называется анодным (например, оцинкованое железо). При нарушении целостности этого покрытия в присутствии электролита (атмосферная влага, кислоты, соли и т.д.) образуется гальванопара, в которой роль анода играет металл с меньшим значением  , т.е. цинк. В результате покрытие будет разрушаться, а основной металл (железо) остается защищенным до тех пор, пока не будет разрушен весь защитный слой.
, т.е. цинк. В результате покрытие будет разрушаться, а основной металл (железо) остается защищенным до тех пор, пока не будет разрушен весь защитный слой.
Если же металл покрытия имеет большее значение  , чем основной металл (т.е. более активный металл покрывают менее активным), то покрытие называют катодным (например, луженое железо). При нарушении целостности покрытия разрушается защищаемый металл (железо), а металл покрытия (олово) остается неизменным.
, чем основной металл (т.е. более активный металл покрывают менее активным), то покрытие называют катодным (например, луженое железо). При нарушении целостности покрытия разрушается защищаемый металл (железо), а металл покрытия (олово) остается неизменным.
|
|
|
Дата добавления: 2019-09-13; просмотров: 746; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!

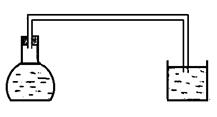 Рис. 2. Схема установки
Рис. 2. Схема установки