ОТНОШЕНИЕ МЕТАЛЛОВ К ВОДЕ, КИСЛОТАМ И
ЩЕЛОЧАМ
Теоретическая часть
Важнейшими химическими свойствами металлов являются их отношение к воде, водным растворам кислот и щелочей.
По химической активности (см. табл. «Ряд напряжений») все металлы (Ме) можно разделить на 3 группы:
- Ме высокой активности (Li…Al);
- Ме средней активности (после Al и до Н2);
- Ме неактивные (после Н2).
1. Отношение металлов к воде
Во взаимодействии металлов с водой при комнатной температуре наблюдаются следующие случаи:
1) Металлы восстанавливают водород из воды, образуя растворимые гидроксиды (щелочи) или малорастворимые гидроксиды по следующей схеме:
 ,
,
где n – валентность Ме.
Эти реакции свойственны для всех металлов от Li доAl включительно (Al должен быть очищен от оксидной пленки или нагрет).
 ,
,
 ,
,
 .
.
2) Металлы, расположенные в ряду напряжений между Al и Н2 (Ме средней активности) реагируют с водой при температурах 500…7000С, т.е. реагируют с перегретым водяным паром, образуя оксид и выделяя водород. Например,
 ,
,
 .
.
3) Металлы, расположенные в ряду напряжений после Н2 (неактивные Ме) вытеснить водород из воды не могут ни при каких условиях.
2. Отношение металлов
к разбавленным кислотам (кроме азотной)
Основным фактором оценки отношения металлов к разбавленным кислотам (кроме азотной), является их положение в таблице “Ряд напряжений”.
1) Металлы, стоящие в ряду напряжений до водорода, т.е. имеющие отрицательные значения стандартных электродных потенциалов  , растворяются в разбавленных кислотах с выделением водорода.
, растворяются в разбавленных кислотах с выделением водорода.
Например:
 ,
,
 .
.
В качестве окислителя при этом выступает ион водорода  в молекулах кислот.
в молекулах кислот.
2) Металлы, имеющие положительные значения стандартных электродных потенциалов  , с разбавленными кислотами не взаимодействуют. К числу таких металлов относятся: Аu, Аg, Ru, Rh, Pd, Os, Ir, Pt, а также Cu, Hg, Вi.
, с разбавленными кислотами не взаимодействуют. К числу таких металлов относятся: Аu, Аg, Ru, Rh, Pd, Os, Ir, Pt, а также Cu, Hg, Вi.
Например:
 ,
,
 .
.
Однако, следует иметь в виду, что рядом напряжений следует пользоваться с учетом особенностей рассматриваемых реакций. Так, свинец  практически не растворяется в разбавленной соляной и серной кислотах вследствие образования на его поверхности нерастворимых хлоридной и сульфатной пленок (происходит пассивирование):
практически не растворяется в разбавленной соляной и серной кислотах вследствие образования на его поверхности нерастворимых хлоридной и сульфатной пленок (происходит пассивирование):
 ;
;
 .
.
Отношение металлов к разбавленной азотной кислоте
Азотная кислота обладает ярко выраженной окислительной активностью. Роль окислителя в ней выполняет не ион Н+, а ион 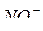 ,
,  , поэтому водород из азотной кислоты не вытесняется.
, поэтому водород из азотной кислоты не вытесняется.
В зависимости от активности Ме, реагирующего с разбавленной
НNO3, восстановление  идет по следующей схеме:
идет по следующей схеме:
(NH3 + HNO3) = 

 - Ме от Li до Al
- Ме от Li до Al
+8ē
+5ē  - Me от Al до Cd
- Me от Al до Cd

+4ē
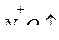 - Me от Cd до H2
- Me от Cd до H2
+3ē
 - Me после H2
- Me после H2
Не реагируют с HNO3(р) благородные металлы, кроме серебра и палладия. Например:
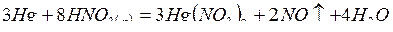 ;
;
 ;
;
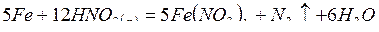 ;
;
 ;
;
4. Отношение металлов
к концентрированной азотной кислоте и “царской водке”
В концентрированной азотной кислоте так же, как и в разбавленной, роль окислителя выполняет ион 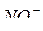
 .
.
Восстановление  идет по следующей схеме:
идет по следующей схеме:
 +3ē
+3ē  (Ме от Li до Al)
(Ме от Li до Al)

+ē  (остальные Ме)
(остальные Ме)
Например,
 ;
;
 ;
;
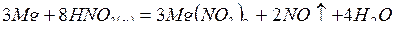 .
.
Концентрированная азотная кислота (С ³ 70 %) не реагирует:
1) с благородными металлами (кроме Аg и Рd);
2) с пассивирующимися металлами, на поверхности которых легко образуется пленка малорастворимых оксидов. Наличием защитной оксидной пленки объясняется пассивность данных металлов по отношению к концентрированным растворам кислот-окислителей на холоду. К числу пассивирующихся металлов относятся Ве, Аl, Тi, Zn, Нf, V, Мn, Сr, Мо, W, Fе, Со, Ni, Вi. В горячей концентрированной азотной кислоте пассивирующиеся Ме растворяются.
Смесь азотной и соляной кислот в соотношении 1:3 (“царская водка”) — более активный окислитель, чем азотная кислота. Название (царская водка) происходит от того, что эта смесь растворяет «царя металлов» золото и другие благородные Ме. Так Аu и Рt легко растворяются в ней с образованием соответствующих хлоридов:

 .
.
5. Отношение металлов
к концентрированной серной кислоте
При действии концентрированной серной кислоты на металлы роль окислителя играет не ион Н+, как в разбавленной Н2SО4, а ион  поэтому водород не выделяется, а образуются соединения серы (SО2, S или Н2S).
поэтому водород не выделяется, а образуются соединения серы (SО2, S или Н2S).
Восстановление  идет по следующей схеме в зависимости от активности растворяющегося Ме:
идет по следующей схеме в зависимости от активности растворяющегося Ме:
 +8ē
+8ē  (Me от Li до Al)
(Me от Li до Al)
 +6ē
+6ē  (Ме от Al до H2)
(Ме от Al до H2)
+2ē  (Ме после Н2)
(Ме после Н2)
Например:
 ;
;
 ;
;
 .
.
Не растворяются в концентрированной серной кислоте:
1) благородные Ме, кроме Ag и Pd;
2) если  ≥ 90%, то на холоду не растворяются пассивирующиеся Ме; в горячей концентрированной серной кислоте пассивирующиеся Ме растворяются.
≥ 90%, то на холоду не растворяются пассивирующиеся Ме; в горячей концентрированной серной кислоте пассивирующиеся Ме растворяются.
Например:
 ,
,
 .
.
Необходимо отметить, что в реакциях концентрированной серной кислоты с металлами, стоящими в ряду напряжений до водорода, в зависимости от условий протекания реакции (концентрация кислоты и температура) может выделиться любое из соединений серы (SO2, S, или H2S). Чем меньше концентрация кислоты, тем более вероятно самое глубокое восстановление  металлом (выделение сероводорода Н2S).
металлом (выделение сероводорода Н2S).
6. Отношение металлов
к водным растворам щелочей
С водными растворами щелочей могут реагировать металлы (Ве, Аl, Zn, Sn, Рb), дающие амфотерные гидроксиды. В результате образуется комплексная соль данного металла и выделяется водород.
Например:
 ,
,
 — тетрагидроксоалюминат натрия,
— тетрагидроксоалюминат натрия,
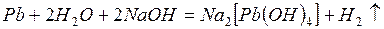 ,
,
 — тетрагидроксоплюмбат натрия.
— тетрагидроксоплюмбат натрия.
Экспериментальная часть
Цель работы: изучить отношение некоторых технически важных металлов к воде, водным растворам кислот и щелочей.
Опыт № 1
Отношение металлов к воде
В пять пробирок налейте по 2-3мл Н2О. В первую пробирку поместите кусочек Nа, во вторую — кусочек Са, в третью насыпьте немного порошка Мg, в четвертую — железные опилки, в пятую — медную стружку. Третью, четвертую и пятую пробирки подогрейте. Что наблюдается? Во все пробирки добавьте по 2-3 капли фенолфталеина. Во всех ли пробирках изменилась окраска? Почему? Какие металлы не вступают во взаимодействие с водой? Объясните причину. Составьте уравнения реакций.
Опыт № 2
Дата добавления: 2019-09-13; просмотров: 2384; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
