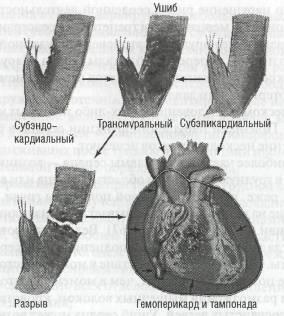
ПЕРВИЧНЫЕ ДОБРОКАЧЕСТВЕННЫЕ ОПУХОЛИ
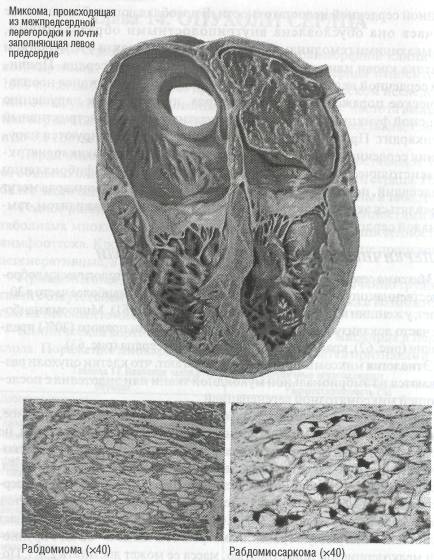
Миксома сердца — первичная внутриполостная гистологически доброкачественная опухоль, встречается в любом возрасте, наиболее часто в 30-60 лет, у женщин в 2-4 раза чаще, чем у мужчин (рис. 61). Миксома наиболее часто локализуется в полости левого (75% ) или правого (20%) предсердия (рис. 62), крайне редко — в желудочках сердца (рис. 63).
Этиология миксомы неясна. Предполагают, что клетки опухоли развиваются из эмбриональной мукоидной ткани или эндотелия с последующей миксоматозной дегенерацией.
Патологическая анатомия. Миксома представляет собой солитарное, реже множественное новообразование округлой или овальной формы, не распространяющееся далее субэндокардиальных слоев сердца. Макроскопически миксомы имеют две разновидности: первая — полупрозрачная, бесцветнаяжелатинозная по консистенции, фиксированная к стенке сердца более или менее широким основанием; вторая — округлая плотная масса, свисающая на ножке (80%). Внешний вид опухоли напоминает полип или виноградную гроздь диаметром от 5 мм до 8 -12 см с крупно-или мелкозернистой поверхностью, масса ее может достигать 250 г. Поверхность опухоли блестящая, капсула отчетливо выражена. Цвет может
 427
427
Некоронарогенные болезни сердца
Некоронарогенные болезни сердца
|
|
Рис. 61. Первичные опухоли сердца (по F. Netter, 1969, с изменениями)
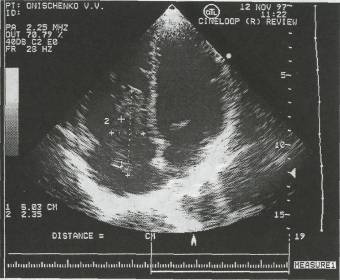
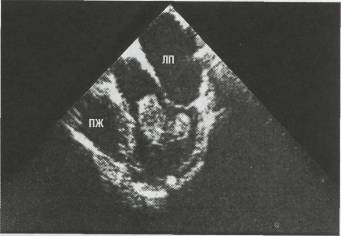
Рис . 62. ЭхоКГ миксомы правого предсердия (В-режим)
|
|
|
варьировать от зеленовато-серого до желтовато-коричневого, опухоль желеобразной или значительно реже эластической консистенции. В самой опухоли могут обнаруживаться дистрофические изменения — некрозы , кровоизлияния, реже происходит обызвествление.
Гистологическое строение миксомы неоднородно. Основная субстанция (матрикс) представлена аморфным оксифильным веществом, в котором рассеяны клетки опухоли веретенообразной формы с круглым или овальным ядром, четким ядрышком, иногда образующие синцитиаль-ные группы, формируя сигарообразные и кольцевидные структуры или тесно окружающие сосуды капиллярного типа. Опухолевые клетки по ультраструктуре напоминают эндотелиальные и могут участвовать в формировании сосудов. Гистологически часто выявляется фиброзное утолщение эндокарда створок атриовентрикулярных клапанов и нижней части предсердия, что обусловлено отложением фибрина на поверхности эндокарда и увеличением количества коллагеновых и эластических
|
|
| Некоронарогенные болезни сердца |
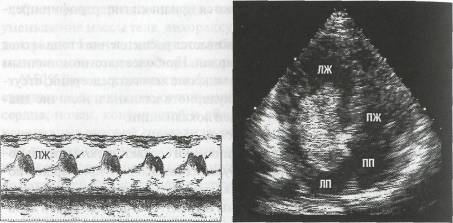
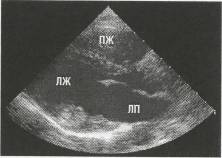
Рис. 63. Чреспищеводная эхоКГ двухдольчатой миксомы левого желудочка (по Н. Feigenbaum, 1987, с изменениями)
волокон в связи с постоянным трением тела опухоли об эндокард. При выраженном кальцинозе миксомы наблюдается деструкция створок атриовентрикулярных клапанов.
|
|
|
Патологическая физиология. Миксома левого предсердия суживает левое атриовентрикулярное отверстие, возможно также нарушение оттока из легочных вен из-за сужения их отверстий. Обструкция митрального отверстия или легочных вен приводит к легочной венозной и артериальной гипертензии, а также к вторичной правожелудочковой сердечной недостаточности.
Опухоль правого предсердия стенозирует правое атриовентрикулярное отверстие, может затруднять отток из полых вен, что приводит к появлению системной венозной гипертензии. Если миксома пролаби-рует в левый желудочек, то во время ранней систолы она движется от желудочка к предсердию, вызывая в последнем значительное повышение давления, во время ранней диастолы опухоль «проваливается» в полость желудочка, что способствует резкому снижению внутрипред-
430
Некоронарогенные болезни сердца
 сердного давления. Если опухоль не пролабирует, остается в предсердии и препятствует прохождению крови через атриовентрикулярное отверстие во время диастолы, то гемодинамика похожа на таковую при митральном или трикуспидальном стенозе с замедленным кровотоком через отверстие во время диастолы.
сердного давления. Если опухоль не пролабирует, остается в предсердии и препятствует прохождению крови через атриовентрикулярное отверстие во время диастолы, то гемодинамика похожа на таковую при митральном или трикуспидальном стенозе с замедленным кровотоком через отверстие во время диастолы.
|
|
|
Опухоль левого желудочка суживает его выходной тракт, имитируя обструктивную кардиомиопатию. Правожелудочковая миксома может стенозировать устье легочного ствола.
Клиника и диагностика. Миксома левого предсердия проявляется разнообразной клинической симптоматикой, имитируя ряд заболеваний сердечно-сосудистой системы. Больные обычно предъявляют жалобы общего характера, а также присущие эмболическим осложнениям и вызванные препятствием кровотоку. У больных с миксомой левых отделов сердца преобладают жалобы, обусловленные нарушением кровообращения в малом круге кровообращения: одышка, кровохарканье; у больных с опухолью правых отделов сердца доминируют симптомы, характерные для нарушения кровообращения в большом круге: увеличение печени, отеки.
Небольшие миксомы, если они не приводят к эмболии, обычно асимптоматичны. Опухоли на ножке могут вызывать преходящую обструкцию, например, при перемене положения тела, проявляющуюся эпизодами потери сознания или внезапной смертью. Обструкция кровотоку проявляется обычно в виде какого-либо заболевания сердца, имитируя нередко симптомы порока, чаще всего митрального. При аускультации в фазу ранней или средней диастолы выслушивается низкочастотный шум, называемый опухолевым хлопком ( tumorplop ), который возникает вследствие резкой остановки опухоли при ударе ее о стенку желудочка или фиброзное кольцо митрального клапана в начале диастолы. Миксома правого предсердия часто манифестирует эмболией легочной артерии, которая может быть причиной летального исхода. При обтурации кровотока на уровне трехстворчатого клапана возможны судороги и другие расстройства функции центральной нервной системы или внезапная смерть.
|
|
|
 431
431
Некоронарогенные болезни сердца
Системные проявления, отмечающиеся у 90% больных, включают уменьшение массы тела, лихорадку, анемию, повышение СОЭ и концентрации иммуноглобулинов (обычно класса G). Как правило, эти симптомы исчезают после удаления опухоли.
У 50% больных вследствие фрагментации опухоли развиваются системные эмболические осложнения с поражением головного мозга, сердца, почек, конечностей и области бифуркации аорты. Эмболия коронарных артерий приводит к острому инфаркту миокарда, эмболия сосудов головного мозга создает многообразие неврологических поражений от динамического нарушения мозгового кровообращения до параличей или внезапной смерти. Первым признаком миксомы может быть эмболия периферических сосудов.
Выделяют основные клинические симптомы, на основании которых можно заподозрить или диагностировать миксому сердца:
1) внезапное появление клинических признаков порока сердца (шу
мов) у больного без ревматического анамнеза, которые изменяются при
перемене положения тела (вследствие смещения опухоли относитель
но клапана);
2) быстрое развитие сердечно-сосудистой недостаточности без ви
димых причин, резистентной к терапии;
3) небольшая длительность заболевания по сравнению с ревмати
ческими пороками сердца, прогрессирующее течение и неожиданные
«ремиссии»;
4) возникновение эмболии периферических сосудов или сосудов
легких на фоне синусового ритма, особенно у молодых людей;
5) одышка или кратковременная потеря сознания, артериальная
гипотензия, тахикардия, появляющаяся внезапно без видимых причин
(возникают при обтурации миксомой клапанных отверстий);
6) течение заболевания под маской инфекционного эндокардита:
необъяснимая лихорадка, анемия, увеличение СОЭ, несмотря на ле
чение антибиотиками.
ЭКГ не имеет диагностического значения. Степень выраженности изменений зависит от величины стеноза, обусловленного опухолью.
 432
432
Некоронарогенные болезни сердца
При миксомах предсердий отмечаются признаки гипертрофии предсердий, реже — желудочков.
При фонокардиографии обнаруживается расщепление I тона за счет затрудненного опорожнения предсердий. Наиболее патогномоничным признаком является, особенно при миксоме левого предсердия, отсутствие тона открытия атриовентрикулярного клапана и наличие диа-столического шума соответствующей локализации.
Особенностью рентгенологической картины при миксоме левого предсердия, если нарушения гемодинамики соответствуют митральному стенозу, является отсутствие выбухания ушка левого предсердия, полость левого предсердия расширена меньше, чем при митральном стенозе. При обызвествлении миксомы на рентгенограммах виден каль-циноз.
Метод эхокардиографии позволяет верифицировать диагноз. Опухоль левого предсердия вызывает появление «облачка» эхо-сигнала между створками митрального клапана во время диастолы желудочков, во время систолы он виден в полости левого предсердия. При линейном сканировании на протяжении сердечного цикла можно проследить за движением «облачка» из левого предсердия в левый желудочек и обратно. Опухоль искажает характер кривой движения передней створки митрального клапана, вызывая деформацию диастолического движения, и приводит к смещению этой створки к межжелудочковой перегородке. Плотная гладкая капсула миксомы дает четкие контуры отраженного эхо-сигнала, тогда как опухолевые массы без оболочки имеют смазанный контур. При двухмерной эхокардиографии миксо-ма видна в полостях сердца в виде более светлого образования на темном фоне, движение опухоли визуализируется на протяжении всего сердечного цикла (рис. 64).
Ангиокардиография получила широкое распространение в диагностике миксом сердца. Характерным симптомом является стойкий дефект наполнения округлой формы с ровными и гладкими контурами, обтекаемый кровью с контрастом.
 433
433
|
|
| Некоронарогенные болезни сердца |
Рис. 64. Миксома сердца:
А — эхоКГ в М-режиме миксомы ЛП (парастернальная позиция); Б — диастолическое изображение обширной миксомы ЛП, выбухающей в полость ЛЖ (В-режим)
Для подтверждения диагноза миксомы необходимо гистологическое исследование всех хирургически удаленных эмболов. Миксому следует подозревать при возникновении эмболических осложнений у молодых пациентов, особенно при синусовом ритме.
Дифференциальную диагностику проводят с ревматическим митральным пороком сердца, часто имитирующим опухоль. О наличии опухоли свидетельствуют отсутствие ревматической лихорадки в анамнезе, внезапное начало и быстрое прогрессирование симптомов, несоответствие тяжести состояния и степени нарушения кровообращения незначительно выраженным изменениям контуров сердца, зависимость выраженности симптомов от определенного положения тела, отсутствие тона открытия митрального клапана или несоответствие времени его появления тяжести митральной обструкции, эмболии на фоне синусового ритма, рентгенологические данные о подвижных массах кальция в левых полостях сердца.
 434
434
Некоронарогенные болезни сердца
Дифференциальная диагностика с инфекционным эндокардитом затруднена, тем более что сама опухоль создает условия для возникновения вторичного инфекционного эндокардита.
Миксома правого предсердия клинически имитирует трикуспидаль-ный стеноз, который практически не встречается как изолированный ревматический порок сердца, или констриктивный перикардит. При последнем обычно рентгенологически выявляют обызвествление перикарда. Изолированная правожелудочковая недостаточность без стеноза легочной артерии должна навести на мысль о наличии миксомы правого предсердия, особенно при признаках трикуспидального стеноза.
Течение. Длительность заболевания миксомой различна. При отсутствии лечения у 30% больных с миксомой наступает внезапная смерть, остальные умирают от сердечной недостаточности или эмболии.
Лечение. Удаление миксомы является единственным радикальным методом лечения, отсрочку операции следует считать грубой ошибкой. Хирургическое лечение опухоли заключается в иссечении места ее прикрепления и ушивании образовавшегося дефекта. У большинства оперированных больных наступает значительное улучшение состояния или полное выздоровление. Госпитальная летальность минимальная.
Липома сердца — доброкачественная опухоль, происходящая из жировой ткани, встречается в любом возрасте. Наиболее часто представляет собой солитарное образование, располагающееся в любом отделе сердца, но чаще в левом желудочке, правом предсердии или межжелудочковой перегородке.
Патологическая анатомия. Макроскопически характерна узловатая форма опухоли размером от 1 до 15 см в диаметре с четко выраженной капсулой. Массалипомыможетдостигатьболее2кг. Опухоль может располагаться внутримиокардиально или субэпикардиально, но чаще субэн-докардиально. Микроскопически состоит из типичных жировых клеток и изредка содержит фиброзную ткань (фибролипома), мышечную ткань (миолипома), кровеносные сосуды. Характерны различные размеры жировых клеток и долек, наличие эмбриональных жировых клеток.
 435
435
Некоронарогенные болезни сердца
Некоторые исследователи выделяют патологию, называемую липоматозной гипертрофией межпредсердной перегородки, которая является скорее гиперплазией первичной жировой ткани, чем истинной неоплазмой. Она представляет собой неинкапсулированную массу жировой ткани, расположенную под эндокардом межпредсердной перегородки. Образование имеет коричневую окраску, размеры от 1 до 8 см в диаметре, более часто расположено кпереди от овальной ямки со стороны правого предсердия, но также может распространяться на область атриовентрикулярного узла. Гистологически липоматозная гипертрофия межпредсердной перегородки представлена различным соотношением зрелых и эмбриональных жировых клеток, фиброзной тканью и очагами хронического воспаления, преимущественно в виде скопления лимфоцитов и плазматических клеток.
Клиника. Обычно интрамуральные липомы бессимптомны, но могут обнаруживаться признаки снижения сократительной способности сердца, нарушения ритма сердца, атриовентрикулярной или внутрижелудочковой проводимости. Субэндокардиальные опухоли проявляются симптомами, соответствующими их локализации, в то время как субэпикардиальные опухоли могут вызывать сдавление сердца и выпот в перикард.
В случае образования липоматозной гипертрофии межпредсердной перегородки могут возникать нарушения ритма, застойная сердечная недостаточность или внезапная смерть.
Прогноз. До 25% больных умирают внезапно, что связано с различными нарушениями ритма сердца.
Папиллярная фиброэластома — доброкачественная опухоль сердца, происходящая из эндокарда, может располагаться в любом отделе сердца, но наиболее часто поражает клапанный аппарат.
Патологическая анатомия. При микроскопическом исследовании обнаруживаются множественные отростки к эндокарду или непосредственно к одному из клапанов сердца диаметром 3-4 см. У взрослых чаще поражается аортальный клапан. Гистологически опухоль покрыта эндотелием, который окружает центральную часть (сердцевину) опухоли, состоящую из плотной соединительной ткани, включающей мат-
 436
436
Некоронарогенные болезни сердца
рикс из кислых мукополисахаридов, эластичные волокна и гладкомы-шечные клетки. Гистогенез опухоли не известен.
Прогноз. В преобладающем большинстве случаев опухоль бессимптомна и случайно обнаруживается при аутопсии. В некоторых случаях отмечается внезапная смерть.
Рабдомиома — доброкачественная внутримышечная опухоль, встречается наиболее часто у детей в возрасте до 15 лет и составляет 7- 20% всех первичных новообразований сердца. Впервые рабдомиома сердца была описана F. Recklinghausen в 1862 г. В 30- 50% случаев рабдомиома сопровождается туберозным склерозом коры головного мозга, а также множественными аденомами и аденофибролипомами почек и аденомами кожи.
Этиология рабдомиомы до настоящего времени остается неустановленной. Существуют предположения, что она происходит из миоблас-тов или атипичных клеток Пуркинье или является признакам врожденного нарушения углеводного обмена.
Макроскопически рабдомиома может располагаться в любом отделе сердца, исключая клапанный аппарат, наиболее часто — в желудочках сердца, зачастую имеет внутриполостной характер роста. Размеры опухоли могут варьировать от нескольких миллиметров до нескольких сантиметров. Рабдомиома имеет белесоватую или коричневатую окраску, четко отграничена от окружающих тканей, но не имеет капсулы. Микроскопически опухоль состоит из клеток разнообразной формы с большим содержанием гликогена. Типичными для рабдомиомы являются паукообразные клетки с центрально расположенными круглыми ядрами и наличием в цитоплазме миофибрилл с поперечной исчерченностью (см. рис. 61).
Прогноз неблагоприятный. Чаще смерть наступает внезапно.
Фиброма — доброкачественная соединительнотканная опухоль, выявляемая у лиц обоего пола в любом возрасте.
Фиброма может располагаться в разных отделах сердца, наиболее часто — в желудочках или межжелудочковой перегородке. Как правило, она представляет собой солитарное образование диаметром 3-10 см плотной консистенции, имеющее серовато-белую окраску (рис. 65). Опухоль четко отграничена от окружающих тканей, но не имеет кап-
 437
437
|
|
| Некоронарогенные болезни сердца |
Рис. 65. ЭхоКГ фибромы ЛЖ (парастернальная позиция по длинной оси; В-режим)
сулы, характеризуется инвазивным ростом. При микроскопическом исследовании центральная часть опухоли состоит из гиалинизирован-ной фиброзной ткани с множественными очагами кальциноза и кис-тозной дегенерации, на периферии находятся веретенообразные клетки типа фибробластов с зернистой цитоплазмой и овальными ядрами с 1-2 ядрышками. Клетки располагаются между пучками коллагеновых волокон, имеющих различное направление.
При росте опухоли часто в патологический процесс вовлекается проводящая система сердца, что обусловливает высокую частоту случаев внезапной смерти.
Гемашиолш — доброкачественная сосудистая опухоль, характеризующаяся внугриполостным, внутримышечным или эпикардиальным ростом. Опухоль может поражать любой отдел сердца. Макроскопически гемангиома небольшого размера, имеет вид виноградной грозди или полштовидного разрастания сине-багрового цвета. На разрезе имеет губчатое строение.
Прогноз при гемангиомах не изучен, зависит от локализации и размера опухоли, в 50% случаев их выявляют случайно при аутопсии.
Тератома — опухоль, содержащая элементы всех трех зародышевых листков. Внутрисердечная тератома представляет собой очень редкое заболевание, выявляется преимущественно у женщин. Морфологически имеет грушевидную форму и может достигать до 15 см в диаметре. На разрезе имеет поликистозное строение.
~43~8
Некоронарогенные болезни сердца
Прогноз не изучен, однако описаны возникновение рефрактерной сердечной недостаточности и случаи внезапной смерти.
Мезотелиомаатриовентрикулярногоузла — доброкачественная опухоль, избирательно поражающая атриовентрикулярный узел. Выявляется преимущественно у женщин в любом возрасте.
Гистогенез опухоли не ясен. Макроскопически опухоль имеет вид множественных узелков, расположенных в области атриовентрикулярного узла, не имеет четких границ. Характерно отсутствие метастазов и прорастания опухолью трехстворчатого клапана и миокарда правого желудочка.
Прогноз неблагоприятный, что обусловлено возникновением асистолии или фибрилляции желудочков на фоне полной поперечной блокады сердца.
ПЕРВИЧНЫЕ ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ
Первичные злокачественные опухоли составляют 25% от общего количества первичных опухолевых поражений сердца. Наиболее частой их разновидностью является саркома, которая происходит из мезенхимы и поэтому может проявляться многообразием морфологических типов (см. табл. 17) и обусловливать сложность гистологической верификации. Саркома может возникнуть в любом возрасте, но наиболее часто в 30- 50 лет, одинаково часто у мужчин и женщин. Опухоль поражает преимущественно правые отделы сердца, исходя, как правило, из эндокарда или перикарда. Первичная саркома сердца может вызвать окклюзию клапанных отверстий и выходных отделов желудочков, сдавливать и прорастать коронарные сосуды, крупные артерии и вены. Она отличается быстрым инвазивным ростом, прорастает все слои сердца и близлежащие органы, а также быстро и обширно метастазирует в легкие, средостение, трахеобронхиальные и ретроперитонеальные лимфатические узлы, надпочечники, мозг.
Ангиосаркома — наиболее частая разновидность, составляющая 33% первичных злокачественных опухолей. У мужчин встречается в 2- 3 раза чаще, чем у женщин. Опухоль может поражать любые отделы сердца, наиболее часто — правое предсердие.
 439
439
Некоронарогенные болезни сердца
 Ангиосаркома макроскопически представляет собой плотное бугристое образование, инфильтрирующее ткани. На разрезе видны очаги некроза и кровооизлияний. Микроскопически определяются веретенообразные, полигональные или округлые клетки, образующие синцитий и складывающиеся в беспорядочно расположенные тяжи. Характерным является образование различных по размерам и форме сосудистых полостей, заполненных кровью и сообщающихся между собой. Между клетками опухоли находятся рыхлые сети аргирофильных волокон, напоминающих базальную мембрану.
Ангиосаркома макроскопически представляет собой плотное бугристое образование, инфильтрирующее ткани. На разрезе видны очаги некроза и кровооизлияний. Микроскопически определяются веретенообразные, полигональные или округлые клетки, образующие синцитий и складывающиеся в беспорядочно расположенные тяжи. Характерным является образование различных по размерам и форме сосудистых полостей, заполненных кровью и сообщающихся между собой. Между клетками опухоли находятся рыхлые сети аргирофильных волокон, напоминающих базальную мембрану.
Рабдомиосаркома происходит из сердечной исчерченной мышечной ткани, встречается в любом возрасте, несколько чаще у мужчин, составляет 20% всех первичных злокачественных опухолей сердца.
Макроскопически рабдомиосаркома определяется как узел мягкой консистенции белого или бледно-розового цвета, расположенный в толще миокарда. На разрезе обнаруживают очаги кровоизлияний и некрозов. Микроскопически определяется различное соотношение мелких округлых или овальных, веретенообразных клеток. Важное диагностическое значение имеет их выраженный полиморфизм: они могут напоминать теннисную ракетку, имея округлое тело с ядром и один толстый цитоплазматический отросток, или иметь паукообразную форму с центрально расположенным ядром и крупными вакуолями гликогена по периферии (см. рис. 61). В цитоплазме обнаруживаются миофибриллы с поперечной исчерченностью. Клетки опухоли могут располагаться сплошными полями или формировать альвеолярные и пучковые структуры, заключенные в сеть аргирофильных и коллагеновых волокон.
Фибросаркомаявляется мезенхимальной опухолью, составляющей 10% всех первичных злокачественных новообразований сердца. Возникает улиц обоего пола в любом возрасте.
Макроскопически фибросаркома представляет собой четко отграниченный плотный узел белого или серовато-белого цвета либо имеет ин-фильтративный рост. Микроскопически обнаруживаются фибробласто-подобные клетки с различной степенью дифференцировки и коллаге-новые волокна. Клетки расположены в виде переплетающихся пучков.
 440
440
Некоронарогенные болезни сердца
Другие первичные злокачественные опухоли, в том числе мезотели-ома и лимфома, выявляются редко. Необходимы детальные исследования их морфологических и клинических особенностей.
Клиника и диагностика. Клиническая картина зависит от локализации опухоли и величины обструкции полостей сердца. Типичным являются необъяснимая, быстро прогрессирующая сердечная недостаточность с увеличением размеров сердца, выпотом в перикард (геморрагическим), тампонадой, болью в области грудной клетки, аритмиями, нарушениями проводимости, обструкцией полой вены и внезапная смерть. Опухоли, ограниченные миокардом без распространения внутрь полости, могут некоторое время протекать бессимптомно или вызывать аритмии и нарушения проводимости.
Заподозрить наличие злокачественного новообразования можно по следующим симптомам:
• боль внутри грудной клетки является ранним и частым симпто
мом злокачественного поражения;
• наличие гемоперикарда при отсутствии травмы в анамнезе;
• необходимость проведения повторных перикардиоцентезов (цито
логическое исследование эвакуированной жидкости обязательно);
• прогрессирование синдрома верхней полой вены при отсутствии
тампонады сердца.
При распространении опухоли на перикардиальное пространство часто образуется геморрагический выпот в перикард и может возникнуть тампонада. Поскольку наиболее часто поражается правая часть сердца, саркома нередко вызывает симптомы правожелудочковой недостаточности вследствие обструкции правого предсердия, правого желудочка, трехстворчатого клапана или клапана легочной артерии. Обструкция верхней полой вены может приводить к отеку лица и верхних конечностей, тогда как обструкция нижней полой вены вызывает застой во внутренних органах.
Эхокардиография рассматривается как метод выбора в диагностике опухолей сердца, достаточный для выработки соответствующей хирургической тактики.
 441
441
Некоронарогенные болезни сердца
В последнее время все большее признание в диагностике приобретает метод компьютерной томографии - метод отличается высокой чувствительностью и надежностью, позволяет проводить топическую диагностику опухоли и определить место ее фиксации. Другим достоверным методом топической диагностики опухолей сердца является магнитно-резонансная томография.
Прогноз неблагоприятный. При улэдювлении диагноза саркомы сердца у 80% больных уже имеются метастазы. Как правило, больные умирают в течение 6~ 12 мес после появления первых клинических симптомов.
Лечение злокачественных опухолей сердца чаще всего симптоматическое. Хирургическое лечение преобладающего большинства больных с первичными злокачественными новообразованиями сердца неэффективно в связи с тем, что к моменту диагностики отмечается значительное распространение опухоли как в пределах самого миокарда, так и на близлежащие органы и ткани. Чаще всего проводят лучевую терапию с системной химиотерапией или без нее, что позволяет временно уменьшить клиническую выраженность заболевания и в ряде случаев увеличить продолжительность жизни до 5 лет после начала лечения.
Некоронарогенные болезни сердца
Глава 15. ТРАВМЫ СЕРДЦА
Повреждения сердца, магистральных сосудов и перикарда при проникающих ранениях грудной клетки встречаются в 10-15% случаев и являются причиной смерти у большей части погибших от травмы лиц.
К наиболее распространенным причинам травматического повреждения сердца относятся:
• проникающие ранения,
• огнестрельные ранения,
• механические воздействия — ушиб или сдавление грудной клет
ки, падение с высоты, воздействие ударной воздушной волны,
• ятрогенные травмы при выполнении ангиопластики, катетериза
ции полостей сердца, пункции полости перикарда, коронарогра-
фии, сердечно-легочной реанимации, введении различных кате
теров и постановки электродов для кардиостимуляции,
• повреждения при воздействии ионизирующей радиации,
• повреждения при воздействии электрического тока.
Из проникающих ранений сердца в мирное время наиболее частыми являются колото-резаные, реже огнестрельные раны.
В основном колото-резаные раны локализуются на передней поверхности грудной клетки (рис. 66). При этом могут повреждаться любые структуры сердца: стенка, межпредсердная и межжелудочковая перегородки, клапаны сердца, коронарные артерии и/или перикард. Проникающие ранения сердца, как правило, приводят к тампонаде сердца или значительной кровопотере.
Известны случаи, когда ранения сердца протекают со стертой клинической симптоматикой и в течение длительного времени больной может не предъявлять жалоб и ничего, кроме наружной раны, может не указывать на повреждение сердца. У таких больных постепенно или внезапно развиваются явления тампонады сердца. Расположение раны в проекции сердца является объективным признаком, дающим возможность заподозрить проникающее ранение сердца. Бледность кожи, цианоз, холодный пот, обморочное или сопорозное состояние должны на-
 443
443
| Некоронарогенные болезни сердца |
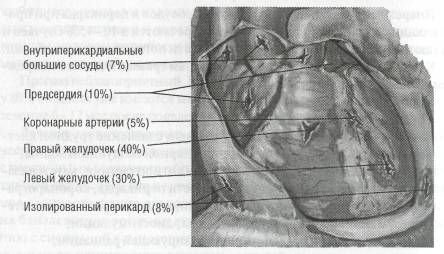
Рис. 66. Проникающие ранения сердца (по F. Netter, 1969, с изменениями)
сторожить врача. Больные с сохраненным сознанием жалуются на слабость, головокружение, одышку, кашель. По мере усугубления тампонады сердца усиливается одышка, снижается артериальное давление, учащается и становится нитевидным пульс. Значительного наружного кровотечения не наблюдается, кровь обычно изливается в перикард, а затем в плевральную полость. Уже при наличии в полости перикарда 200 мл крови появляются симптомы сдавления сердца — повышение венозного давления. При значительном гемоперикарде тоны сердца очень глухие или не прослушиваются.
ЭКГ имеет диагностическую значимость: признаком тампонады может быть снижение вольтажа зубцов. Изменения, напоминающие инфаркт миокарда, выявляются при ранении желудочков: имеется монофазный характер комплекса QRST c последующим снижением интервала S — Т к изолинии и появлением отрицательного зубца Т.
Некоронарогенные болезни сердца
При рентгеноскопическом исследовании тень сердца увеличена, талия сглажена, резко снижена пульсация контуров сердечной тени.
При пункции перикарда выявляется наличие крови.
Диагноз проникающего ранения сердца может быть установлен на основании ряда симптомов. Вероятными признаками ранения сердца
могут быть:
• кровоточащая рана грудной клетки в области сердца,
• тяжелое состояние при небольших размерах раны грудной стенки,
• одышка,
• снижение артериального давления,
• учащение и слабое наполнение пульса,
• бледность кожных покровов,
• тревожное или полубессознательное состояние,
• глухие непрослушивающиесятоны сердца,
• увеличение границ сердца,
• снижение уровня гемоглобина и показателя гематокрита.
Достоверными признаками ранения сердца являются:
• тампонада сердца,
• изменения на ЭКГ по типу инфаркта миокарда.
Лечение. При подозрении на имеющееся ранение сердца и перикарда показания к операции являются абсолютными. У большинства выживших после операции больных травма компенсируется в такой степени, что патологические изменения сердца не выявляются.
Из непроникающих травм любое непосредственное тупое воздействие на грудную клетку, особенно на переднюю ее стенку (удар ногой, кулаком, спортивным снарядом, копытом животного), может вызвать повреждение любой структуры сердца, приводя ко множеству патофизиологических изменений. Следует указать, что повреждения сердца и магистральных сосудов могут происходить и при травмах других частей тела, например, при внезапной компрессии живота и нижних конечностей, что приводит к повышению давления в грудной клетке.
При патологоанатомическом исследовании обычно обнаруживается перикардит, что может быть связано с поздним развитием конст-
 445
445
Некоронарогенные болезни сердца
 рикции. Изменения в сердце варьируют от небольших участков с мелкими петехиями в субэндокардиальных или субэпикардиальных областях до обширных трансмуральных кровоизлияний в миокард. Могут происходить надрывы оболочек, стенок или клапанов, размозжение стенок сердца. При микроскопическом исследовании в области кровоизлияния обнаруживают отечные, фрагментированные или некроти-зированные мышечные волокна, окруженные вначале множеством эритроцитов, в дальнейшем — скоплениями полиморфонуклеарных лейкоцитов. У выживших после травмы впоследствии происходит развитие соединительной ткани с образованием рубца.
рикции. Изменения в сердце варьируют от небольших участков с мелкими петехиями в субэндокардиальных или субэпикардиальных областях до обширных трансмуральных кровоизлияний в миокард. Могут происходить надрывы оболочек, стенок или клапанов, размозжение стенок сердца. При микроскопическом исследовании в области кровоизлияния обнаруживают отечные, фрагментированные или некроти-зированные мышечные волокна, окруженные вначале множеством эритроцитов, в дальнейшем — скоплениями полиморфонуклеарных лейкоцитов. У выживших после травмы впоследствии происходит развитие соединительной ткани с образованием рубца.
Патогенез поражения сердца при тупых травмах грудной клетки очень сложен и окончательно не изучен. Имеют значение локализация травмы грудной клетки, направление и сила удара, гидродинамическое воздействие крови, циркулирующей в полостях сердца, эластичность ребер, возраст больного. В патогенезе травматического повреждения сердца можно выделить три основных механизма:
• внезапное сдавление всех отделов сердца с повышением внутри-
сердечного давления;
• внезапный удар в проекции сердца или повреждение сердца от
ломками ребер;
• смещение сердца при ушибе грудной клетки.
Закрытые повреждения сердца подразделяют на несколько видов:
1) сотрясение сердца (28%);
2) ушиб сердца (35%);
3) разрыв сердца (31%), в том числе наружный (11%), внутренний
(17%), комбинированный (в 3%);
4) «травматический» инфаркт миокарда (до 6%).
Сотрясение сердца — синдром функциональных сердечно-сосудистых нарушений, остро возникающих после резкого удара по грудной клетке точно над областью сердца. При сотрясении сердца происходит спазм венечных артерий с последующей ишемией миокарда. Клинические проявления развиваются немедленно после травмы или спустя короткое время после нее и быстро исчезают. Боль в области сердца возникает крайне редко в виде кратковременных приступов.
 446
446
Некоронарогенные болезни сердца
Характерно нарушение ритма сердечной деятельности: экстрасистолическая аритмия, мерцание или трепетание предсердий, брадикар-дия, атакже различные нарушения атриовентрикулярной проводимости, вплоть до полной поперечной блокады сердца. Нарушение периферического кровообращения проявляется повышением венозного и снижением артериального давления.
При физическом обследовании каких-либо значимых изменений не наблюдается. Признаки нарушений функции сердца в большинстве случаев в течение нескольких часов исчезают.
Ушиб — наиболее частый вид травмы сердца — возникает при внезапном ударе в грудную клетку над областью сердца или в левую половину груди и, реже, при травме правой половины груди. Механическое воздействие на грудную клетку вызывает кровоизлияние в миокард, под эпикард или под эндокард (рис. 67). Величина кровоизлияния в миокард иногда зависит от степени наполнения камер сердца кровью в момент травмы. Гидравлическое действие в момент систолы вызывает более тяжелое повреждение сердца, чем в момент диастолы. Возможны разрывы и размозжения мышечных волокон, кровотечения из поврежденных сосудистых ветвей. Ушиб сердца может возникнуть и без повреждения костного скелета грудной клетки. В результате кровоизлияния в миокард может произойти сдавление коронарного сосуда и развитие инфаркта миокарда. Последний может возникнуть и в случае образования тромба на поврежденной интиме коронарной артерии. Среди ушибов сердца можно выделить несколько вариантов:
• повреждение клапанов,
• повреждение миокарда и проводящих путей,
• повреждение коронарных сосудов,
• комбинированные повреждения.
Часто ушиб сердца остается нераспознанным, так как может протекать бессимптомно или маскироваться повреждением грудной клетки или других органов. Ушиб сердца не всегда вызывает развитие немедленных функциональных расстройств и поэтому не всегда при травме грудной клетки обращают внимание на состояние сердца и пропускают случаи его повреждения.
 447
447
|
|
| Некоронарогенные болезни сердца |
Рис. 67. Патогенез и различные варианты непроникающих травм сердца (по F. Netter, 1969, с изменениями)
Самой частой жалобой является боль в прекардиальной области, которая может возникнуть сразу же или через несколько часов после травмы и быть обусловлена как ушибом грудной клетки, так и переломом ребер, повреждением плевры или сердца. Чаще всего боль локализуется в месте ушиба, иногда за грудиной, может иррадиировать в спину, обе руки, в челюсть, имитируя стенокардию или появляться только при физической нагрузке через несколько часов илидней послетравмы. Прием нитроглицерина мало влияетна интенсивность боли. Могут быть также жалобы на ощущение сердцебиения, перебоев в работе сердца, одышку или общую слабость.
При осмотре грудной клетки обнаруживаются внешние признаки закрытой травмы. Следует помнить, что отсутствие очевидных призна ков повреждения после травмы ни в коем случае не является основанием для исключения возможности закрытой травмы сердца.
 448
448
Некоронарогенные болезни сердца
Часто отмечаются нарушения ритма сердца: синусовая тахикардия, реже брадикардия, желудочковая экстрасистолическая аритмия, мерцание и трепетание предсердий. Могут возникать преходящие нарушения внугрижелудочковой проводимости, блокады ножек пучка Гиса или их ветвей, различные нарушения атриовентрикулярной проводимости, включая полную AV-блокаду сердца, которая носит преходящий характер. Точный механизм нарушений ритма не известен.
При выслушивании сердца нередко отмечается глухость тонов, иногда шум трения перикарда, маятникообразный ритм или ритм галопа.
При ушибе сердца клинические симптомы нарастают постепенно и обратное их развитие происходит медленно. На ЭКГ часто выявляются неспецифические изменения ^Тили классические признаки перикардита, отмечаются различные аритмии, включая желудочковую тахикардию. Диагностическое значение может иметь обнаружение МВ-фракции креатинфосфокиназы для определения наличия некроза.
Разрыв сердца — нарушение целости стенки сердца или его перегородки (межжелудочковой или межпредсердной). Разрыв сердца при травме может происходить двумя путями:
1) острый разрыв в результате компрессии сердца вследствие пря
мого воздействия,
2) ушиб и кровоизлияние, приводящие к некрозу, размягчению и
разрыву через несколько дней после травмы.
Различают два вида разрывов сердца: внешний, при котором образуется сообщение с соседними органами или полостями тела (средостение, плевральная полость и полость перикарда), и внутренний, при котором возникают патологические сообщения между отдельными полостями сердца (разрывы клапанов или перегородок).
При внешних разрывах, как правило, смерть наступает немедленно. У выживших в течение первых минут клиническая картина внешнего разрыва сердца складывается из признаков гемотампонады сердца и симптомов кровотечения с повреждением или без повреждения коронарных сосудов, проводящих путей сердца. При осмотре отмечают бледность кожных покровов, выраженную одышку, нитевидный частый пульс, коллапс. Границы сердца расширены. При аускультации
Некоронарогенные болезни сердца
выслушать тоны удается с трудом. Нередко развиваются различные нарушения сердечного ритма и проводимости.
Закрытые разрывы сердца трудно диагностируются. Могут выявляться признаки повреждения клапанов. Разрыв межжелудочковой перегородки должен быть заподозрен у больных в случае развития тяжелой застойной сердечной недостаточности непосредственно или в течение нескольких дней после травмы, вместе с появлением голоси-столического шума вдоль левого края грудины. Сердце особенно уязвимо для разрыва межжелудочковой перегородки, когда травма возникает внезапно, как в поздней диастоле, так и во время изоволюметриче-ского сокращения, когда полости желудочков наполнены. При разрыве межжелудочковой перегородки отмечаются артериальная гипотензия, тахикардия, выраженная одышка, цианоз, увеличение печени. Над всей областью сердца выслушивается грубый систолический шум.
«Травматический» инфаркт миокарда развивается, как правило, у лиц пожилого возраста с атеросклеротическим кардиосклерозом, артериальной гипертензией. Клинические проявления существенно не отличаются от таковых при инфаркте миокарда коронарного генеза. Основным клиническим критерием «травматического» инфаркта миокарда является развитие ангинозного или реже астматического статуса сразу после травмы или в ближайшие часы после нее. Инфаркт, как правило, локализуется в передней или переднебоковой стенке левого желудочка, реже в области задней стенки, крупноочаговый. Часто возникают нарушения ритма: экстрасистолическая аритмия, преимущественно желудочковая, фибрилляция предсердий, пароксизмальная тахикардия. Течение инфаркта миокарда в большинстве случаев тяжелое, нередко развивается острая левожелудочковая недостаточность.
Диагностика травматического поражения сердца затруднена, особенно в случае множественных или сочетанных повреждений, осложненных шоковым состоянием. Существенным для диагностики является уточнение механизма травмы грудной клетки. Отсутствие видимых следов травмы грудной клетки не исключает возможности повреждения сердца. Легкие изменения функции сердца при закрытой травме груди чаще не диагностируются.
Некоронарогенные болезни сердца
Патогномоничных ЭКГ-признаков, кроме таковых при «травматическом» инфаркте миокарда, не выявлено. Наиболее типичными изменениями являются нарушения ритма сердечной деятельности, внутрижелудоч-ковой или атриовентрикулярной проводимости вплоть до развития полной поперечной блокады, изменения зубца Т (инверсия или двухфазность или уплощение), смещение сегмента 5Твниз или вверх от изолинии, повышение амплитуды зубца Р в правых грудных отведениях.
Для подтверждения диагноза непроникающих ранений сердца используют рентгенологический и ангиокардиографический методы исследования, зондирование полостей сердца, эхо кардиографию, сцин-тиграфию сердца.
В течении закрытой травмы сердца выделяют несколько периодов:
1) первичные травматические нарушения,
2) травматический миокардит,
3) стабилизация процесса,
4) исход.
Лечение. Больные с закрытой травмой сердца подлежат обязательной госпитализации в специализированное отделение. Лечение травматического поражения сердца включает:
1) купирование болевого синдрома — эффективной является ней-
ролептаналгезия (фентанил с дроперидолом), применение наркотичес
ких аналгетиков;
2) назначение антиаритмических средств при появлении частых или
групповых предсердных или желудочковых экстрасистол для преду
преждения развития фибрилляции желудочков, фибрилляции предсер
дий, пароксизмальной тахикардии — верапамила, блокаторов β-anpe-
норецепторов, новокаинамида, возможно применение этмозина, эта-
цизина. При развитии AV-блокады II степени показано внутривенное
введение атропина, изопреналина, при развитии полной поперечной
блокады целесообразна электрокардиостимуляция;
3) нормализация гемодинамических показателей и восстановление со
кратительной способности миокарда — в случаях развития острой лево-
желудочковой недостаточности показано применение сердечных глико-
 15* 451
15* 451
Некоронарогенные болезни сердца
зидов, мочегонных средств. Следует соблюдать осторожность при применении сердечных гликозидов в острый период травмы, при котором наблюдается гипокалиемия (особенно при множественной травме) — сердечные гликозиды могут не только вызывать желудочковые экстрасистолы, но и способствовать возникновению фибрилляции желудочков;
4) улучшение обменных процессов в миокарде, которые в той или иной степени нарушаются при любом виде закрытой травмы сердца, — терапия должна включать метаболические препараты, в том числе анаболические гормоны.
Применение антикоагулянтов больным с закрытой травмой сердца противопоказано.
Прогноз благоприятен при своевременном распознавании и активном лечении. Заболевание может закончиться полным выздоровлением и восстановлением трудоспособности или неполным выздоровлением, если сохраняются боль в сердце, нарушения ритма, развивается застойная сердечная недостаточность. Летальный исход при закрытой травме сердца наступает в 42- 89% случаев и обусловлен фибрилляцией желудочков, сердечной недостаточностью и разрывом сердца.
Некоронарогенные болезни сердца
Литература
Аббакумов С.А., Маколкин В.И. Проблемы нейроциркуляторной дис-тонии и экспертизы трудоспособности // Терапевт, арх. — 1996. — № 4. — С. 19-21.
Амосова Е.Н. Клиническая кардиология. — В 2т. — К.: Здоров'я, 1998. — X і. _ 704с.
Амосова Е.Н. Кардиомиопатии. — К.: Книга плюс, 1999. — 422 с.
Амосова Е.Н. Миокардиты // Междунар. мед. журн. — 2000.— № 1. — С. 22-25.
Антитела к возбудителю болезни Лайма у больных миокардитом и дила-тационной кардиомиопатией/И.А. Скрипникова, М.Ю. Самсонов, Е.Л. Насонов и др. // Клин, медицина. — 1993. — № 2. — С. 38-41.
Артемчук А.Ф. Клинические особенности и терапия сердечно-сосудистых нарушений при алкоголизме // Укр. кардіол. журн. — 2000. — № 4. — С. 68-71.
Багирова ГГ., Баталина М.В. Лечение хронической сердечной недостаточности у больных с митральными и аортальными пороками сердца ревматической этиологии // Терапевт, арх. — 2000. — № 9. — С. 63-66.
Барац С.С, Закроева А.Г. Диастолическая дисфункция сердца по показателям трансмитрального кровотока и потока в легочных венах: дискуссионные вопросы патогенеза, терминологии и классификации // Кардиология. — 1998.-№5.-С. 69-76.
Барт Б.Я. Инфекционный эндокардит у лиц пожилого возраста // Кардиология. — 1999. - № 11. - С. 92-96.
Барштейн Ю.А., Кононенко В.В., Боброва И.А. Поражение миокарда при инфекционных заболеваниях//Укр. кардіол.журн. — 1996. — № 2. — С. 8-12.
Беленков Ю.Н. Роль нарушений систолы и диастолы в развитии сердечной недостаточности // Терапевт, арх. — 1994. — № 9. — С. 3-7.
Белобородов В.Б. Современные представления о применении методов экстракорпоральной детоксикации у пациентов с бактериальными инфек-циями//Клин. антимикробная химиотерапия. — 2000. — № 1. — С. 28—31.
Благосклонов О.В., Сторожаков Г.И., Verdenet J., Sabbah A., Cardot J.С. Количественный анализ изображений изотопной вентрикулографии для оценки сократимости миокарда правого желудочка//Кардиология. — 2000. — №1.-С. 51-53.
Бобров В.А., Волченко Г.В., КитураО.Е. Миокардиальная дисфункция и потенциальные возможности блокаторовбета-адренорецепторов в лечении
 453
453
Некоронарогенные болезни сердца
 больных с сердечной недостаточностью // Укр. терапевт, журн. — 2001. — № 1.-С. 34-40.
больных с сердечной недостаточностью // Укр. терапевт, журн. — 2001. — № 1.-С. 34-40.
Брусина Е.Б., Коломыцев А.В., Барбараш О.Л., Бурматов Н.П. Инфекционный эндокардит — эволюция болезни // Терапевт, арх. — 2000. — № 9. — С. 47-50.
Буткевич О.М., Виноградова Т.Л. Инфекционный эндокардит. — М, 1997.-96 с.
Буткевич О.М., Виноградова Т.Л. Некоторые вопросы современной терапии инфекционного эндокардита // Терапевт, арх. — 2000. — № 9. — С. 54-57.
Василенко В.Х., Фельдман СБ., Хитров Н.К. Миокардиодистрофия.— М.: Медицина, 1989. - 272 с.
Вейн A.M., Соловьева А.Д., КолосоваО.А. Вегетососудистаядистония. — М.: Медицина, 1981.- 318 с.
Вейн A.M. (ред.) Вегетативные расстройства. Клиника, диагностика, лечение. — М.: Медицина, 1998. — 740 с.
Виноградов А.В. Дифференциальный диагноз внутренних болезней. — М.: Медицина, 1987. - 592 с.
Виноградова О.М. Первичный и генетический варианты амилоидоза. — М.: Медицина, 1980.- 156 с.
Внутренние болезни: В 10 кн.: Пер. с англ.; Под ред. Е. Браунвальда. — М.: Медицина, 1993. - Кн. 3. - 480 с.
Внутренние болезни: В 10 кн.: Пер. с англ.; Под ред. Е. Браунвальда. — М.: Медицина, 1994. - Кн. 4. - 496 с.
Внутренние болезни: В 10 кн.: Пер. с англ.; Под ред. Е. Браунвальда. — М.: Медицина, 1995. - Кн. 5. - 448 с.
Волков B.C., Поздняков Ю.М., Виноградов В.Ф. О патогенезе сердечно-болевого синдрома у больных нейроциркуляторной дистонией // Кардиология. - 1997. - № 6. - С. 84-86.
Воробьев А.И., Шишкова ТВ., Коломойцева И.П. Кардиалгии. — М.: Медицина, 1980.- 190 с.
Воробьева A.M., Руденко А. В,, Ходаковская Л. Н., Баланник 3 .Т. Опыт применения препарата вобензим для лечения хирургических больных с инфекционным эндокардитом // Укр. кардіол. журн. — 1998. — № 3. — С. 52-54.
ВоронковЛ.Г, Коваленко В.Н., Рябенко Д.В. Хроническая сердечная недостаточность: механизмы, стандарты диагностики и лечения/Под ред. В.Н. Коваленко. - К.: Морион, 1999. - 128 с.
Некоронарогенные болезни сердца
ВоронковЛ.Г, СердюкТЕ., Рябенко Д.В., ПаращенюкЛ.П. Сравнительная оценка клинико-гемодинамических эффектов метопролола (Корвито-ла) и его сочетания с ингибиторами ангиотензинпревращающего фермента у больных с хронической сердечной недостаточностью // Укр. кардіол. журн. - 2000. - № 4. - С. 57-59.
Воронков Л.Г. Хроническая сердечная недостаточность как иммунопатологический и дисметаболический синдром // Укр. терапевт, журн. — 2001.-№1.-С. 17-20.
Гянджа І.М., Лисенко П., Мінаков О.І. Некоронарогенні захворювання серцевого м'яза. — К.: Здоров'я, 1993.— 126 с.
Грицюк А.И., Чувыкина В.Т., Щигельский В.И. Воспалительные заболевания сердца. — К.: Здоров'я, 1986. — 232 с.
Гуревич М.И.,БерштейнС.А. Основы гемодинамики. — К.: Наук, думка, 1979.-232с.
Гуревич М.А., Янковская М.О. Рестриктивная кардиомиопатия // Кардиология. - 1988. -№ П.-С. 125-129.
Гуревич М.А., Янковская М.О. Ведение больных с дилатационной кар-диомиопатией // Кардиология. — 1988. — № 6. — С. 126-128.
Дембо А.Г. Заболевания и повреждения сердца при занятиях спортом. — Л.: Медицина, 1984. - 302 с.
Демин А.А., Демин Ал .А. Бактериальные эндокардиты. — М., 1978. — 165 с.
Демин А.А., Дробышева В.П. Цефтриаксон влечении стафилококкового эндокардита // Антибиотики и химиотерапевт. — 1998. — № 4. — С. 12-15.
Демин А.А., Дробышева В.П. Антибактериальная химиотерапия инфекционного эндокардита // Клин, антимикробная химиотерапия. — 2000. — № 1.-С. 25-27.
Демин А.А., Дробышева В.П., Вельтер О.Ю. Инфекционный эндокардит у «инъекционных наркоманов» // Клин, медицина. — 2000. — № 8. — С. 47—51.
Диагностика и лечение внутренних болезней: Руководство для врачей/ Под общей ред. Ф.И. Комарова. — М.: Медицина, 1999. — Т. I. — 560 с.
Зимакова И.Е., Карпов A.M., Тагирова ТС. и др. Анализ разнообразия эффектов транквилизатора мебикара в экспериментальной и клинической медицине // Клин, и теор. медицина. — 1995. — № 2. — С. 85-87.
Зозуля I.C. Синдром вегетосудинної дистонії (клініка, діагностика, лікування) // Укр. мед. часопис. - 1997. - № 2 (2). - С. 17-21.
 455
455
Некоронарогенные болезни сердца
 Избранные вопросы ревматологии в клинике внутренних болезней/В.Н. Коваленко, Л.Л. Коваленко, В.И. Мальцев и др. — К., 1994. — Ч. 1. — С. 122-123.
Избранные вопросы ревматологии в клинике внутренних болезней/В.Н. Коваленко, Л.Л. Коваленко, В.И. Мальцев и др. — К., 1994. — Ч. 1. — С. 122-123.
ІлляшМ.Г, БазикаО.Є., РябенкоД.В.таін. Імунологічні аспекти діагностики інфекційно-алергічного міокардиту та дилатаційної кардіоміопатії // Щорічник наук, праць сер.-суд. хірургії України. — 1999. — Вип. 7. — С. 123— 126.
Капелько В.И. Внеклеточный матрикс миокарда и его изменения при заболеваниях сердца // Кардиология. — 2000. — № 9. — С. 78—90.
Кедров А.А. Миокардиты // Руководство по кардиологии/Под ред. Е.И.Чазова.- М.: Медицина, 1982. - Т. 3. - С. 119-145.
Класифікація кардіоміопатій, міокардитів та перикардитів (інформація Українського наукового товариства кардіологів) // Укр. кардіол. журн. — 2000.-№1-2.-С 122-124.
Кнышов Г.В., Вендет Я.А. О классификации приобретенных пороков сердца // Укр. кардіол. журн. — 1996. — № 3. — С. 82-86.
Кнышов Г.В., Вендет Я.А. Приобретенные пороки сердца. — К.: Институт сердечно-сосудистой хирургии, 1997. — 280 с.
Коваленко В.Н., Синяченко О.В., Астахов А.Л. и др. Системная энзимо-терапия как путь коррекции метаболических расстройств при гипертрофической кардиомиопатии // Укр. кардіол. журн. — 1999. — № 3. — С. 43—46.
Коваленко В. М. Систематизація та класифікація некоронарогенних хвороб серця, уніфіковані стандарти та критерії діагностики // Укр. ревматол. журн. - 2000. - № 2. - С. 3-6.
Коваленко В.Н., Рябенко Д.В. Механизмы развития и направления патогенетической терапии вирусного миокардита// Укр. кардіол. журн. — 2000. — №5-6. -С. 104-109.
Коваленко В.Н. Обоснование и методические подходы к диагностике сердечной недостаточности с учетом геометрии сокращения левого желудочка // Укр. терапевт, журн. — 2001. — № 1. — С. 65-68.
Козловская Л.В. Амилоидоз//Терапевт, арх. — 1998. — № 6. — С. 62—70.
Коровина Е.П., Моисеев B.C. Недостаточность кровообращения при гипертрофической кардиомиопатии // Кардиология. — 1997. — № 11. — С. 31-35.
Кошечкин В.А. К вопросу о генетике некоронарогенных поражений мышцы сердца // Бюл. ВКНЦ. - 1988. - № 2. - С. 106-114.
Кушаковский М.С. Хроническая застойная сердечная недостаточность. — СПб.: ИКФ «Фолиант», 1997. - С. 1-216.
Некоронарогенные болезни сердца
Ланг Г.Ф. Классификация и номенклатура болезней системы кровообращения // Вопр. кардиологии. — Л.: Б.и., 1936. — С. 3-46.
Лікування серцевої недостатності. Робоча група з серцевої недостатності Європейського товариства кардіологів //Укр. кардіол.журн. — 1998. — № 1. — С 89-95.
Логановский К.Н. Синдром хронической усталости— болезнь тысячи наименований//Укр. мед. часопис. — 1998. — № 5 (7). — С. 6-15.
Маколкин В.И., Аббакумов С.А. Нейроциркуляторная дистония в терапевтической практике. — М.: Медицина, 1985. — 192 с.
Маколкин В.И. Нейроциркуляторная дистония//Терапевт, арх. — 1995. — №6.-С. 66-70.
МалаяЛ.Т, ГорбЮ.Г, Рачинский И.Д. Хроническая недостаточность кровообращения. — К.: Здоров'я, 1994. — 624с.
Малая Л.Т. Новое в лечении хронической недостаточности кровообращения // Укр. терапевт, журн. — 2001. — № 1. — С. 5—16.
Мартынов А.И., СтепураО.Б., Остроумова О.Д. и др. Пролапс митрального клапана//Кардиология. — 1998. — № 2. — С. 74—81.
МачеретЕ.Л., Мурашко Н.К., ПисарукА.В. Методы диагностики вегетативной дисфункции // Укр. мед. часопис. — 2000. — № 2 (16). — С. 89-94.
Место современных ингибиторов ангиотензинпревращающего фермента в лечении сердечно-сосудистых заболеваний // Кардиология. — 2000. — №10.-С. 92-104.
Метелица В.И. Метелица В.И. Блокаторы рецепторов ангиотензина II// Терапевт, арх. — 1996. — № 8. - С. 64-67.
Минкин Р.Б. Болезни сердечно-сосудистой системы. — СПб: Акация, 1994.-273 с.
Миокардит и дилатационная кардиомиопатия (анализ вопросов этиологии, патогенеза и дифференциального диагноза на клиническом примере)/ М.Ю. Самсонов, В.Г. Наумов, А.Ю. Ибрагимов и др. // Бюл. ВКНЦ. — 1988.- №2. -С. 13-18.
Миррахимов М.М., Руденко Р.И., МеманалиевТ. Правосторонние гипертрофические кардиомиопатии // Терапевт, арх. — 1988. — № 7. — С. 20—24.
Моисеев B.C., Моисеев СВ. Рестриктивные поражения миокарда// Кардиология.— 1990.— № 2.— С. 114-117.
Моисеев B.C., Сумароков А.В., Стяжкин В.Ю. Кардиомиопатии. — М.: Медицина, 1993.- 218 с.
Моисеев B.C. Кардиомиопатии и миокардиты (достижения и перспективы) // Кардиология. — 1996. - № 8. - С. 74-85.
Некоронарогенные болезни сердца
 Моисеев СВ. Инфильтративные поражения миокарда. Рестриктивная кардиомиопатия. Приложение к журналу «Клиническая фармакология и терапия». — М.: Фарма Пресс, 1998. — 144 с.
Моисеев СВ. Инфильтративные поражения миокарда. Рестриктивная кардиомиопатия. Приложение к журналу «Клиническая фармакология и терапия». — М.: Фарма Пресс, 1998. — 144 с.
Мравян СР., Фролов А.Н. Биопсия миокарда и ее диагностические возможности при миокардитах, гипертрофической и дилатационной кардио-миопатиях//Кардиология. — 1986. — № 3. — С 110-115.
Мравян СР., Канвар С, Голухова Е.З. Клинико-инструментальные показатели в оценке прогноза миокардита и дилатационной кардиомиопа-тии // Кардиология. - 1997. - № 7. - С. 67-72.
Набуті вади серця та інфекційний ендокардит (Інформація Українського наукового товариства кардіологів) // Укр. кардіол. журн. — 2000. — № 1-2. — С 125-128.
Насонова В.А., Астапенко М.Г. Клиническая ревматология (руководство). — М.: Медицина. — 1989. — 592 с.
Несукай Е.Г., Ильяш М.Г. Миокардит. Современное состояние проблемы // Укр. кардіол. журн. - 1994. - № 5-6. - С. 94-99.
Несукай Е.Г., Ильяш М.Г. Миокардит как полиэтиологическое заболевание // Укр. кардіол. журн. — 1996. - № 2. - С 63-69.
Несукай Е.Г. Эндотелий — новая мишень для терапевтического воздей-ствияприсердечно-сосудистыхзаболеваниях//Укр.кардіол.журн. — 1999. — № 6. - С 82-89.
Нетяженко В .3., Лапшин О .В. Діагностика та лікування хронічної серцевої недостатності // Укр. терапевт, журн. — 2001. — № 1. — С 45-55.
Новиков Ю.И. О диагностике неревматических миокардитов // Кардиология. - 1983. - № 5. - С 50-55.
Новиков Ю.И. Неревматические миокардиты и дилатационная кардиомиопатия (вопросы этиологии, клиника, диагностика, лечения и результаты катамнестических наблюдений): Автореф. дис. ... д-ра мед. наук. — М., 1988. -48 с.
Новиков Ю.И., Стулова М.А. Ранняя желудочковая реполяризация при остром вирусном и идиопатическом миокардите // Клин, медицина. — 2000. - Т. 78, № 2. - С 14-20.
Новый взгляд на ингибиторы ангиотензинпревращающего фермента // Кардиология. - 2000. - № 6. - С. 91-104.
Ольбинская Л.И., ИгнатенкоСБ. Современное представление о патогенезе и лечении хронической сердечной недостаточности // Клин, медицина. - 2000. - № 8. - С. 22-27.
Некоронарогенные болезни сердца
Ордян A.M., Ющук Н.Д., Кареткина ПН. и др. Клиническое и прогностическое значение нарушений глобальной и регионарной сократимости левого желудочка при дифтерийных миокардитах//Клин, медицина. — 2000. — № 2. - С. 20-23.
Палеев Н.Р. Миокардиты // Болезни сердца и сосудов. — М.: Медицина. - 1992. - Т. 2. - С 178-198.
Палеев Н.Р., ОдиноковаВ.А., Гуревич М.А., Найштут Г.М. Миокардиты. — М.: Медицина, 1982. - 272 с.
Палеев Ф.Н. Популяционный и субпопуляционный состав и экспрессия активационных маркеров лимфоцитов при инфекционно-аллергическом миокардите // Кардиология, — 1999. — № 8. — С 53-58.
Пантелеева СВ., Новиков Ю.И. Поражение сердца при гриппе // Вопр. ревматизма. - 1980. - № 4. - С 54-58.
Пархоменко А.Н. Аритмогенная крдиомиопатия правого желудочка: диагностика, лечение, прогноз // Кардиология. — 1998. — № 2. — С. 59-64.
ПоложенцевС.Д., Маклаков А.Г., ФедорецВ.Н., РудневД.А. Психологические особенности больных нейроциркуляторной дистонией // Кардиология. - 1995. - № 5. - С 70-72.
Преображенский Д. В., Сидоренко Б.А. Успехи и неудачи в разработке новых подходов к медикаментозной терапии хронической сердечной недостаточности. Часть 1. Кардиология. — 2000. — № 3. — С 52-60.
Преображенский Д.В., Сидоренко Б.А. Успехи и неудачи в разработке новых подходов к медикаментозной терапии хронической сердечной недостаточности. Часть 2. Кардиология. — 2000. - № 4. - С. 67— 76.
Преображенский Д.В., Савченко М.В., Киктев В.Г., Сидоренко Б.А. Фозиноприл — первый представитель нового поколения ингибиторов ангиотензинпревращающего фермента // Кардиология. — 2000. — № 5 — С 75-81.
Ребров А.П., Пономарева Е.Ю., Белова А.А., Кароли М.А. Инфекционный эндокардит: качество диагностики и клинические особенности // Терапевт, арх. — 2000. — № 9. — С 50-53.
Руднов В.А. Сепсис: современный взгляд на проблему// Клин, антимикробная химиотерапия. — 2000. — № 1. — С 4-Ю.
Симоненко В.Б., Бойцов С.А., Глухов А.А. Апоптоз и патология миокарда// Клин, медицина. — 2000. — № 8. — С 12-16.
Скворцов А.А., МареевВ.Ю., БеленковЮ.Н. Блокаторы рецепторов ан-гиотензина II (механизмы, первые клинические результаты) // Кардиология. - 1998. - № 4. - С 36-50.
Некоронарогенные болезни сердца
Славина Л.С. Сердце при эндокринных заболеваниях. — М.: Медицина, 1979.-184с.
СпасокукоцкийА.Ю., Валько А.С. Инфекционный эндокардит. — К.: Здоров'я, 1983.— 95 с.
Сумароков А.В., Моисеев B.C., Шелепин А.А., Стяжкин В.Ю. Кардио-миопатии, миокардит, алкогольное поражение сердца // Терапевт, арх. — 1984.-№ 9.-С. 75-81.
Сучасне лікування хронічної серцевої недостатності: Метод, рекомендації/ Уклад. Л.Г. Воронков та ін. - К., 1998. — 28 с.
Тазина С.Я., Гуревич М.А. Современный инфекционный эндокардит (часть І) // Клин, медицина. - 1999. - № 12 - С. 19-23.
Тазина С.Я., Гуревич М.А. Современный инфекционный эндокардит (часть II) // Клин, медицина. — 2000. — № 1. — С. 15-20.
Терещенко С.Н.,ДжаианиН.А., Моисеев B.C. Генетические аспекты хронической сердечной недостаточности // Терапевт, арх. — 2000. — № 4. — С. 75-77.
Тюрин В.П. Глюкокортикоиды при инфекционном эндокардите: вред или польза? // Терапевт, арх. - 2000. - № 6. - С. 60-63.
Тюрин В.П., Дубинина СВ. Инфекционный эндокардит у лиц пожилого и старческого возраста// Клин, медицина. — 2000 — № 4. — С. 53—56.
Флоря В.Г., Мареев В.Ю., Самко А.Н. идр. Ремоделирование левого желудочка у пациентов с первичным поражением миокарда // Кардиология. — 1997.-№2-С. 10-15.
Хэгглин Р. Дифференциальная диагностика внутренних болезней. Пер. с нем./Под ред. Е.М. Тареева. — М.: Фирма «Миклош» и изд-во «Инженер», 1993.-794с.
Целуйко В.И., Максимова Н.А., Кравченко Н.А., Тарнакин А.Г. Генетический аспект гипертрофической кардиомиопатии// Кардиология. — 1998. — № 6. - С. 63-65.
Яковлев В.М., Карпов PC, Гасаненко Л.Н. Пролапс митрального клапана (этиология, клиника, лечение). — Томск: Изд-во Томского ун-та, 1985. — 188 с.
Abelmann W. Virus and the heart (review) // Circulation. — 1971. — Vol. 44, № 5. - P. 950-956.
Abraham WT, Bristow V.R. Specialized centers for heart failure management // Circulation. - 1997. - Vol. 96. - P. 2755-2757.
Некоронарогенные болезни сердца
 Abraham W, William T Mechanisms of disease: hormones and hemodynamics in heart failure // New Engl. J. Med. - 1999. - Vol. 341. - P. 577-585.
Abraham W, William T Mechanisms of disease: hormones and hemodynamics in heart failure // New Engl. J. Med. - 1999. - Vol. 341. - P. 577-585.
Adams J.E., Divila-RominV.G., BesseyP.Q.etal. Improved detection of cardiac contusion with cardiac troponin I//Amer. Heart J. — 1996. — Vol. 131. — P. 308.
Akamatsu H., Amano J., Sakamoto Т. etal. Primary chylopericardium// Ann. Thorac. Surg. - 1994. - Vol. 58. - P. 262.
Angelini A., Thiene G., Boffa G.M. et al. Endocardial biopsy in arrhythmogenic right ventricular cardiomyopathy // J. Amer. Coll. Cardiol. — 1993. — Vol. 21. — P. 259A.
Archard L.C., Bowles N.E., Cunningham L. etal. Molecular probes for detection of persisting enterovirus infection of human heart and their prognostic value // Europ. Heart J.- 1991.-Vol. 12, Suppl. D. - P. 56-59.
Aretz H .T Myocarditis. The Dallas Criteria // Hum.Pathol. - 1987. - Vol. 18. -P. 619-624.
Aretz H.T., Billingham M.E., Edwards W.D. et al. Myocarditis: a histopathologic definition and classification //Amer. J. Cardiovasc. Pathol. — 1987. — Vol. 1. — P. 3-13.
Arsan S., Mercan S., Sarigl A. et al. Long-term experience with pericardiectomy: analysis of 105 consecutive patients //Thorac. Cardiovasc. Surg. — 1994.—Vol.42. — P. 340.
AuffermannW.,WichterT, BreithardtG. etal. Arrhythmogenic right ventricular disease: MR imaging versus angiography //Amer. J. Radiol. — 1993. — Vol. 161. — P. 549-555.
Aukrust P., Ueland T, Lien E. et al. Cytokine network in congestive heart failure secondary to ischemic or idiopathic dilated cardiomyopathy // Amer. J. Cardiol. — 1999.-Vol. 83.-P. 376-382.
Auten G.M., Del Bene V. Endocarditis: current guidelines on prophylaxis, diagnosis and treatment//Consultant. — 1996. — № 5. — P. 973-993.
Avierinos J. F., Mohty D. M., Sarano M. E. Determinants of mitral valve prolapse prognosis in a large population based sample//Europ. Heart J. — 2000. —Vol. 21, Abstr. Suppl. - P. 303.
Awan N.A., Mason D.T Direct selective blockade of the vascular angiotensin II receptors in therapy for hypertension and severe congestive heart failure // Amer. Heart J. - 1996. -Vol. 131. - P. 177-185.
Azizi M., ChatelierG., GuyeneT. etal. Additive effects of combined angiotensin-converting enzyme inhibition and angiotensin II antagonism on blood pressure and

 ИНН
ИНН
Некоронарогенные болезни сердца
renin release in sodium-depleted normotensives//Circulation. — 1995. — Vol. 92. — P. 825-834.
Ball A.M., Sole M.J. Oxidative stress and the pathogenesis of heart failure// Cardiol. Clin. - 1998. - Vol. 16. - P. 665-675.
Bardales R.H., Stanley M.W., Schaefer R.F. et al. Secondary pericardia] malignancies: a critical appraisal of the role of cytology, pericardial biopsy, and DNA ploidy analysis //Amer. J. Clin. Pathol. - 1996. - Vol. 106. - P. 29.
Bayer A. S. Revised diagnostic criteria for infective endocarditis // Cardiol. Clin. — 1996.-Vol. 14.-P. 345-350.
Blake L.M., Scheinman M.M., Higgins C.B. MR features of arrhythmogenic right ventricular dysplasia// Amer. J. Radiol. - 1994. - Vol. 162. - P. 809-812.
Bonow R.O., Udelson J.E. Left ventricular diastolic dysfunction as a cause of congestive heart failure: mechanisms and management // Ann. Intern. Med. — 1992. - Vol. 117, № 6. - P. 502-510.
Booz G.W., Baker K.M. Role of type 1 and type 2 angiotensin receptors in angiotensin II-induced cardiomyocyte hypertrophy // Hypertension. — 1996. — Vol. 28. - P. 635-640.
Bostman L.A., Salo J.A., Bostman O.M. Stab wounds to the pericardium and heart: an analysis of 85 consecutive patients// Europ. J. Surg. — 1992. — Vol. 158. — P. 271.
Bouhour J.B., Helias J., deLajartre A.Y. et al. Detection of myocarditis during the first year after discovery of a dilated cardiomyopathy by endomyocardial biopsy and gallium-67 myocardial scintigraphy: prospective multicentre French study of 91 patients // Europ. Heart J. - 1988. - Vol. 9. - P. 520-528.
Brandt R.R., FilzmaierK., JanssensU. etal. Increases of cardiac troponin I compared to creatin kinase in acute pericarditis // J. Amer. Coll. Cardiol. — 2000. — Vol.35, issue 2, Suppl. A. - P. 226.
Braunwald E. Heart failure.—Harrison's Principles of Internal Medicine— 13lh edition. McGraw-Hill, NY, 1994. - P. 998-1008.
Braunwald E. Heart disease/W.B.Saunders. Philadelphia, 3nd edition, 1995. — 1124p.
Braunwald E. Cardiovascular medicine at the turn of the millenium: triumphs, concerns and opportunities // New Engl. J. Med. — 1997. — Vol. 337. — P. 1360-1369.
BreithardtG., WichterT, Haverkamp W etal. Implantable cardioverter defibrillator therapy in patients with arrhythmogenic right ventricular cardiomyopathy? Long QT
Некоронарогенные болезни сердца
syndrome or no structural heart disease //Amer. Heart J.— 1994.—Vol. 127, Suppl. — P. 1151-1158.
Brown J., MacKinnon D., King A. et al. Elevated arterial blood pressure in cardiac tamponade // New Engl. J. Med. - 1992. - Vol. 327. - P. 463.
Brown M., Griffin G.E. Immune responces in endocarditis//Heart. — 1998. — Vol. 79. - P. 1-2.
Cai J., Jones D.P. Superoxide in apoptosis//J. Biol. Chem. — 1998. — Vol. 273. — P 11401-11404.
Califf R.M. Beta-blocker therapy for heart failure // J. A. M. A. - 2000. -Vol. 283, №10.-P. 1335-1337.
Carrasco H.A., Vicuna A.V., Molina C. et al. Effect of low oral doses of disopyramide and amiodarone on ventricular and atrial arrhythmias of chagasic patients with advanced myocardial damage // Int. J. Cardiol. — 1985. — Vol. 9. — P. 425-428.
Castells E., Ferran V, Octavio de Toledo M.C. et al. Cardiac myxomas: surgical treatment, long-term results and recurrence//J. Cardiovasc. Surg. — 1993. — Vol. 34. _ R 49.
CharronPh., TessonR, PoirierO.etal. Identification of a genetic risk factor for idiopathic dilated cardiomyopathy//Europ. Heart J. — 1999. —Vol.20. — P. 1587-1591.
Chojnowska L., Ruzyllo W. Rodzinna kardiomiopatia przerostowa // Kardiol. Pol. - 2000. - Vol. 53, Suppl. III. - P. 88-95.
ChowL.H., BeiselK.W, McManusB.M. Enteroviral infection of mice with severe combined immunodeficiency: evidence for direct viral pathogenesis of myocardial injury // Lab. Invest. - 1992. - Vol. 66. - P. 24-31.
Cleveland J.L., Ihle J.N. Contenders in Fas/TNF cell signalling //Cell. - 1998. -Vol. 81.-P. 479-482.
Cohen G.M. Caspases: the executioners of apoptosis//Biochem. J. — 1998. — Vol. 326.-P. 1-16.
Collier RE., Goodman G.B. Cardiac tamponade caused by central venous catheter perforation of the heart: a preventable complication //J. Am. Coll. Surg. — 1995.-Vol. 181.-P. 459.
CONSENSUS Trial Study Group. Effects of enalapril on mortality in severe congestive heart failure//New Engl. J. Med. — 1987. - Vol. 316. - P. 1429-1435.
CookS.A., Poole-Wilson P.A. Cardiac myocyte apoptosis//Europ. Heart J. — 1999. - Vol. 20. - P. 1619-1629.
Некоронарогенные болезни сердца
Cowburn P.J., Cleland J.Y.F., Coats A.J.S. et al. Risk stratification in chronic heart failure // Europ. Heart J. - 1998. - Vol. 19. - P. 696-710.
Cowie M, R., Mosterd A., Wbod A. et al. The epidemiology of heart failure // Europ. Heart J. - 1997. - Vol. 18. - P. 208-225.
Craighead J.E., Huber S.A., Martin W.B. Murine cytomegalovirus // Europ. Heart J.- 1991.-Vol. 12 (Suppl. D). - P. 69-72.
Crozier I., Ikram H., Awan N. et al. Losartan in heart failure: Hemodynamic effects and tolerability//Circulation. — 1995. - Vol. 95, № 3. - P. 691-697.
Dabrowska-Kugacka A., Lubinski A., Baczynska A. etal. Influence of structural abnormalities on dispersion of cardiac repolarisation in hypertrophic cardiomyopathy and hypertensive left ventricular hypertrophy// Kardiol. Pol. — 2000. — Vol. 53. — P. 482-486.
Daliento L., RizzoliC.,ThieneG. etal. Diagnostic accuracy of right ventriculography in arrhythmogenic right ventricular cardiomyopathy // Amer. J. Cardiol. — 1990. - Vol. 60. - P. 741-745.
Daubert J.C., Descaves C, Foulgoc J.L. et al. Critical analysis of cineangiographic criteria for diagnosis of arrhythmogenic right ventricular dysplasia // Amer. Heart J. - 1988. - Vol. 115. - P. 448-459.
DecG.M., FusterV. Idiopathic dilated cardiomyopathy//New Engl. J. Med. —
1994. - Vol. 331. - P. 1564-1575.
Dembinska-Kiec A. Rola cytokin w patomechanizmie niewydolnosci serca // Kar-dioLPol. - 2000. - Vol. 53, Suppl. III. - P. 70-75.
Dickstein K., Chang P., Willenheimer R. et al. Comparison of the effects of losartan and enalapril on clinical status and exercise performance in patients with moderate or severe chronic heart failure // J. Amer. Coll. Cardiol. — 1995. — Vol. 26.-P. 438-445.
Dougherty A. H. Congestive heart failure with normal systolic function // Amer. J. Cardiol. - 1984. - Vol. 54. - P. 778-782.
DurackD.T., Bright D.K., Lukes A.S. Duke Endocarditis Service. New criteria for diagnosis of infective endocarditis //Amer. J. Med. — 1994. —Vol.96. — P. 200-209.
Dutka D.P., Elborn J.S., Delamere F. et al. Tumour necrosis factoralpha in severe congestive cardiac failure//Brit. Heart J. — 1993.—Vol. 70. — P. 141-143.
Eriksson H. Heart failure: agrowing public health problem//J. Intern. Med. —
1995. -Vol. 237. -P. 135-141.
Espinosa R., Carrasco H.A., Belandria F. et al. Life expectancy analysis in patients with Сhagas disease. Prognosis after one decade (1973-1983)//Int. J. Cardiol. — 1985.-Vol. 8.-P. 45-48.
Некоронарогенные болезни сердца
Evan G., Littlewood X A matter of life and cell death // Science. — 1998. -Vol. 281.-P. 1317-1321.
Feeley K. Necropsy diagnosis of myocarditis: a retrospective study using CD45RO immunohistochemistry//J. Clin. Pathol. - 2000. - Vol. 53, № 2. - P. 147-149.
Feneley M.P. HIV-related cardiovascular disease // Med. J. Aust. — 1996. — Vol. 164.-P. 482.
Ferrari R. Tumor necrosis factor in chronic heart failure: a double facet cytokine // Cardiovasc. Res. - 1998. - \fol. 37. - P. 554-559.
Ferrari R., Bachetti Т., Agnoletti L. et al. Endothelial function and dysfunction in heart failure//Europ. Heart J.- 1998.-Vol. 19, Suppl. G. - P. 41-47.
Ferrari R. Origin of heart failure: cardiac or generalized myopathy? // Europ. Heart J. - 1999. - Vol. 20. - P. 1613-1614.
Feuerstein G., Bril A., Ruffolo R. Protective effects of carvedilol in the myocardium//Amer. J. Cardiol. - 1997. - Vol. 80. - P. 41-45.
Figueroa W., Alankar S., Pai N. et al. Subxiphoid pericardial window for pericardial effusion in end-stage renal disease // Amer. J. Kidney Dis. — 1996. — Vol. 27.-P. 664.
Filipiak K.J., Tarchalska-Krynska В., Opolski F. Metaloproteinazy i ich udzial w przebudowie miesnia sercowego // Kardiol. Pol. — 2000. — Vol. 53, Suppl. III. — P. 83-87.
Fowler N.O. Cardiac tamponade: a clinical or an echocardiographic diagnosis? (editorial)//Circulation. - 1993. - Vol. 87. - P. 1738.
Fowler N.O. Constrictive pericarditis: its history and current status // Clin. Cardiol.- 1995.-Vol. 18.-P. 341.
Friedrich S.P. Intracardiac angiotensin-converting enzyme inhibition improves diastolic function in patients with left ventricular hypertrophy due to aortic stenosis // Circulation. - 1991. - Vol. 90, № 6. - P. 2761-2771.
Friman G. Myocarditis. Epidemiology, etiology and clinical aspects // Europ. Heart J. - 1995. - Vol. 16. - P. 173-175.
FuldaG., Rodriguez A., Turney S.Z. etal. Blunt traumatic pericardial rupture: a ten-year experience, 1979 to 1989 // J. Cardiovasc. Surg. - 1990. - Vol. 31. -P. 525.
Gaasch W.H. Diagnosis and treatment of heart failure based on left ventricular systolic or diastolic dysfunction // JAMA. - 1994. - Vol. 271, № 16. - P. 1276-1280.
Gandhi S.K., Marts B.C., MistryB.M. etal. Selective management ofembolized intracardiac missiles//Ann. Thorac. Surg.- 1996. - Vol. 62. - P. 290.
 465
465
Некоронарогенные болезни сердца
Garcia M.J., Rodriguez L., Ares M. et al. Differentiation of constrictive pericarditis from restrictive cardiomyopathy: assessment of left ventricular diastolic velocities in longitudinal axis by Doppler tissue imaging // J. Amen Coll. Cardiol. — 1996.-Vol.27.-P. 108.
Gavras I. Bradykinin-mediated effects of ACE inhibition //Kidney Int. — 1992. — Vol. 42.-P. 1020-1029.
Gottlieb S,S., Dickstein K., Fleck E. et al. Hemodynamic and neurohormonal effects of the angiotensin II antagonist losartan in patients with congestive heart failure // Circulation. - 1993. - \fol. 88. - P. 1602-1609.
Granville D.J., Carthy СМ., Hunt D.W.C. etal. Apoptosis: molecular aspects of cell death and disease// Lab.Invest. - 1998. - Vol. 78. - P. 893-913.
Graupner C, Vilacosta I., San Roman J.A. et al. Risk of embolization after institution of antibiotic therapy in endocarditis //Europ. Heart J. — 2000. —Vol. 21, Abstr. Suppl. — P. 304.
Graupner C, Vilacosta L, Fernandez C. et al. Echocardiographic prognostic indicators in infective endocarditis // Europ. Heart J. — 2000. — Vol. 21, Abstr. Suppl. - P. 692.
Green D.R., ReedJ.C. Mitochondria and apoptosis//Science. — 1998. —Vol. 281.-P. 1309-1312.
Grossman W. Diastolic dysfunction in congestive heart failure // New Engl. J. Med.- 1991.-Vol. 325, №22. - P. 1557-1564.
Gullestad L., Aass H., Fjeld J. et al. Immunomodulating therapy with intravenous immunoglobulin in patients with chronic heart failure // Circulation. — 2001. — Vol. 103.-P. 220-225.
HajjarR.J., RoseG.A., Madsen J.C. etal. Extrapericardial cardiac tamponade after blunt chest trauma (pt I)//Amer. Heart J.— 1995. — Vol. 130. — P. 620.
HamrellB.B., Huber S.A., Leslie K.O. Reduced unloaded sarcomere shortening velocity and a shift to a slower myosin isoform in acute murine coxsackievirus myocarditis // Circulation Res. - 1994. - Vol. 75, № 3. - P. 462—472.
Hancock E.W. On the elastic and rigid forms of constrictive pericarditis // Amer. Heart J.- 1980.-Vol. 100.-P. 917.
Hancock E.W. Subacute effusive-constrictive pericarditis // Circulation. — I971.-Vol.43.-P. 183.
Hayashida W. Regional remodeling and nonuniform changes in diastolic function in patients with left ventricular dysfunction: Modification by long-term enalapril treatment //J. Amer. Coll. Cardiol. - 1993. - Vol. 22, № 5. - P. 1403-1410.
 466
466
Некоронарогенные болезни сердца
Hazelrigg S.R., Mack M.J., Landreneau R.J. etal. Thoracoscopicpericardiectomy for effusive pericardial disease//Ann. Thorac. Surg. — 1993. — Vol. 56. — P. 792. Heart disease/Ed. E. Braunwald.- W.B. Saunders Company, 1988. - P. 1410—
1469.
Heart Outcomes Prevention Evaluation (HOPE) Study Investigators. Effect of an angiotensin converting enzyme inhibitor, ramipril, on cardiovascular events in high-risk patients // New Engl. J. Med. - 2000. - Vol. 342. - P. 145-153.
Hengstenberg C, Maisch B. Neue aspekte in derdiagnostik entzundlicherund dilatativer herzmuskelerkrankungen // Herz Kreisl. — 1992. — Vol. 24, № 6. — P. 179-183.
Herrera-Ganza E.H., Stetson S.J., Cubillos-Garzon A. et al. Tumor necrosis factor-a. A mediator of disease progression in the failing human heart // Chest. — 1999- - Vol. 115. - P. 1170-1174.
Herskowitz A., Ahmed-Ansari A. Myocarditis // Curr. Opinion in Cardiology. — 1992. - Vol. 7, № 3. - P. 469-475.
Hersum M., Maisch B. Humoral and cellular immune reactions to the myocardium in myocarditis // Herz. — 1992. — Vol. 17, № 2. - P. 91-96.
Hilgenberg A.D., Logan D.L., Akins C.W. et al. Blunt injuries of the thoracic aorta//Ann. Thorac. Surg. - 1992.- Vol. 53. - P. 233.
Hjalmarson A., Goldstein S., Fagenberg B. et al. Effects of controlled-release metoprolol on total mortality, hospitalization and well-being in patients with heart failure: the metoprolol CR/XL randomized intervention trial in congestive heart failure (MERIT-HF) //JAMA. - 2000. - Vol. 283, № 10. - P. 1295-1302.
Ho K.K.L.,.Anderson K.M., Kannel W.B. et al. Survival after the onset of congestive heart failure in Framingham Heart Study Subjects // Circulation. — 1993.-Vol. 88.-P. 107-115.
Ho K.K.L., Pinsky J.L., Kannel W.B. etal. The epidemiology of heart failure: The Framingham Study//J. Amer. Coll. Cardiol. - 1993. - Vol. 22 (Suppl. A). -P6A-13A.
Hofling K., Tracy S. Expression of an antigenic adenovirus epitope in agroup В coxsackievirus //J. Virol. - 2000. - V. 74, № 10. - P. 4570-4578.
Hornig В., Arakawa A., Huber S.A. Viral myocarditis: a tale of two diseases // Lab. Invest. - 1992. - Vol. вв . - P. 1-3.
Houghton J.L. Pericarditis and myocarditis: which is benign and which isn't? // Postgrad. Med. - 1992. - Vol. 91, № 2. - P. 273-278, 281-282.
 467
467
Некоронарогенные болезни сердца
Houser S.R., Lakatta E.G. Function of the cardiac myocyte in the conundrum of end-stage, dilated human heart failure // Circulation. — 1999. — Vol. 99. — P. 600-604.
Hunter J.J., Chien K.R. Mechanisms of disease: signalling pathways for cardiac hypertrophy and failure // New Engl. J. Med. - 1999. - Vol. 341. — P. 1276-1283.
Hurrell D.G., Nishimura R.A., Higano S.T. et al. Value of dynamic respiratory changes in left and right ventricular pressures for the diagnosis of constrictive pericarditis//Circulation. — 1996. — Vol. 93. — P. 2007.
Iaccarino G., Lefkowitz R.J., Koch W.J. Myocardial G protein-coupled receptor kinase: implications for heart failure therapy // Proc. Assoc. Am. Physicians. — 1999. - Vol. 111. - P. 399-405.
Ikram H. Identifying the patient with heart failure //J. Int. Med. Res. — 1995. — Vol. 23.-P. 139-153.
Ishyiama S., Hiroe M., Nishikawa T. et al. Inhibitory effects of vesnarione in the progression of myocardial damage in experimental autoimmune myocarditis in rats // Cardiovasc. Res. - 1999. - Vol. 43. - P. 389-397.
Jibiki Т., Terai M. Expression of tumor necrosis factor-alpha protein in the myocardium in fatal myocarditis// Pediatr. Int. — 2000. — Vol. 42, № 1. — P. 43-47.
Johnson J.A. Diastolic dysfunction in congestive heart failure // Clin. Pharm. — 1991.-Vol. 10.-P. 850-861.
Johnson M.R., Gheorgiade M. Growth hormone therapy in patients with congestive heart failure: need for further research // Amer. Heart J. — 1999. — Vol. 137.-P. 899-901.
Jonsson B. Measurement of health outcome and associated costs in cardiovascular disease //Europ. Heart J.- 1996. - Vol. 17,Suppl.A. - P. 2-7.
Kandolf R., KirschnerP, AmeisD.etal. Enteroviral heart disease: diagnosis by in situ hybridization/Schultheiss H.P. ed. New concepts in viral Heart disease. Springer-Verlag, 1988. - P. 337-348.
Kandolf R., Klingel K., Mertsching H. et al. Molecular studies on enteroviral heart disease: pattern ofacute and persistent infection//Europ. HeartJ. — 1991. — Vol.12 (Suppl. D). - P. 49-55.
Kang PM., Izumo S. Apoptosis and heart failure: a critical review of literature // Circ. Res. - 2000. - Vol. 86. - P. 1107-1113.
Kasper E.K., Agema W.R.P., Huchins G.V. et al. The cause of dilated cardiomyopathy: a clinicopathologic review of 673 consecutive patients //J. Amer. Coll. Cardiol. - 1994. - Vol. 23. - P. 586-590.
 468
468
Некоронарогенные болезни сердца
Keith M., Geranmayegan A., Sole M. et al. Increased oxidative stress in patients with congestive heart failure// J. Amer. Coll. Cardiol. - 1998. - Vol. 31. — P. 1352-1356.
King M.K., Gay D.M., Pan L.C. et al. Treatment with a growth hormone secretagogue in a model of developing heart failure // Circulation. — 2001. — Vol. 103.-P. 308-313.
Kinoshita O., Fontaine G., Rosas F. et al. Time- and frequency domain analysis of the signal-averaged ECG in patients with arrhythmogenic right ventricular dysplasia //Circulation. - 1995. - Vol. 91. - P. 715-721.
Klein J., Stanek G., Bittner R. et al. Lyme borreliosis as a cause of myocarditis and heart muscle disease //Europ. HeartJ.- 1991.-Vol. 12, Suppl. D. - P. 73-75.
Klingel K., Hohenadl C, Canu et al. Ongoing enterovirus-induced myocarditis is associated with persistent heart muscle infection: quantitative analysis of virus replication, tissue damage and inflammation // Proc. Natl. Acad. Sci. USA. — 1992.-Vol. 89.-P. 314-318.
Knott-Craig C.J., Dalton R.P., Rossouw G.J., et al. Penetrating cardiac trauma: management strategy based on 129 surgical emergencies over 2 years//Ann. Thorac. Surg. - 1992. - Vol. 53. - P. 1006.
Kojda G., Harrison D. Interactions between NO and reactive oxygen species: pathophysiological importance in atherosclerosis, hypertension, diabetes and heart failure // Cardiovasc. Res. - 1999. - Vol. 43. - P. 562-571.
Krown K., Page T.P., Nguyen C. et al. Tumour necrosis factor alpha-induced apoptosis in cardiac myocytes //J. Clin. Invest. - 1996. - Vol. 98. - P. 2854-2865.
Kubota X, McNamara D.M., Wang J.J. et al. Effects of tumor necrosis factor gene polymorphisms on patients with congestive heart failure // Circulation. — 1998. - Vol. 97. - P. 2499-2501.
LabibS., UdelsonJ.E., PandianN.G. Echocardiography in low pressure cardiac tamponade//Amer. J. Cardiol. - 1989. - Vol. 63. - P. 1156.
Laham R.J., Cohen D.J., Kuntz R.E. et al. Pericardial effusion in patients with cancer: outcome with contemporary management strategies // Heart. — 1996. — Vol. 75. - P. 67.
Lang K., Borner A., Figulla H. Comparison ofbiochemical markers for the detection of minimal myocardial injury: superior sensitivity of cardiac troponin-T//J. Intern. Med. - 2000. - V 247. - № 1. - P. 119-123.
Lechat P. Prevention of heart failure progression: current approaches // Eur. Heart J. — 1998. - Vol. 19, Suppl. B. - P. 12-18.
 469
469
Некоронарогенные болезни сердца
Leclercq J.F., Coumel P. Late potentials in arrhythmogenic right ventricular dysplasia//Europ. Heart J.- 1993.-Vol. 14, Suppl. H. - P. 67-93.
Leport C. Antibiotic prophylaxis for infective endocarditis // Clin. Microbiol Infect. - 1998. - Vol. 4. - P. 56-61.
Levin S., Maldonada I., Rehm C. et al. Cardiac tamponade without pericardial effusion after blunt chest trauma //Amer. Heart J.— 1996. —Vol. 131. — P. 198.
Levine M.J., Lorell B.H., DiverD.J. etal. Implicationsofechocardiographically assisted diagnosis of pericardial tamponade in contemporary medical patients: detection before hemodynamic embarrassment//J. Amer. Coll. Cardiol. — 1991. — Vol. 17.-P. 59.
Levy D., Larson M.G., Vasan R.S. et al. The progression from hypertension to congestive heart failure //J. A. M. A. - 1996. - Vol. 275. - P. 1557-1562.
Li Y, Peng Т., Yang Y High prevalence of enteroviral genomic sequences in myocardium// Heart. — 2000. — V. 83, № 6. - P. 696-701.
Lie J.T. Myocarditis and endomyocardial biopsy in unexplained heart failure: a diagnosis in search of a disease //Ann. Int. Med. — 1988. — Vol. 109. — P. 25-28.
Lieberman E.B., Hutchins G.M., Herskowitz A. et al. A clinicopathologic description of myocarditis//J. Amer. Coll. Cardiol. — 1991. — Vol. 18. — P. 1617-1626.
Lindner J. R., Case R.A., Dent J.M. etal. Diagnostic value of echocardiography in suspected endocarditis // Circulation. — 1996. — Vol. 93. — P. 730-736.
Lobo F.V., Heggtveit H.A., Butany J. et al. Right ventricular dysplasia: morphological findings in 13 cases//Can. J. Cardiol. — 1992. — Vol. 8. — P. 261-268.
Lorell B.H. Left ventricular hypertrophy and diastolic dysfunction // Hosp. Pract. - 1992. - Vol. 27, № 10. - P. 189-209.
LucherT.F, Barton M. Biology of the endothelium//Clin. Cardiol. — 1997. — Vol. 10 (Suppl II).- P. 3-10.
Maenza R.L., Seaberg D., D'Amico F. A meta-analysis ofblunt cardiac trauma: ending myocardial confusion//Amer. J. Emerg. Med. — 1996. — Vol. 14. — P. 237.
Mahapatra R.K., Ellis G.H. Myocarditis and hepatitis В virus // Angiology. — 1985.-Vol. 36.-P. 116-118.
Maisch B. The European study of epidemiology and treatment of cardiac inflammatory disease//Europ. Heart J. - 1997.-Vol. 116.— P. 1248-1254.
Maisch В., Portig I., Ristic A.etal. Definition of inflammatory cardiomyopathy (myocarditis): on the way to Consensus. A status report//Herz. — 2000. —Vol. 25, issue 3.-P. 200-209.
Некоронарогенные болезни сердца
Mallat Z., Tedgui A., Fontaliran F. et al. Evidence of apoptosis in arrhythmogenic right ventricular dysplasia //New Engl. J. Med. - 1996. - Vol. 335. - P. 1224-1226.
Mann D.L. Mechanisms and models in heart failure: a combination approach // Circulation. - 1999. - Vol. 100. - P. 999-1008.
Manolio T.A., Baughman K.L., Rodeheffer R. et al. Prevalence and etiology of idiopathic dilated cardiomyopathy//Amer. J. Cardiol. — 1992. —Vol.69. — P. 1458-1466.
Marcolongo R., Russo R., LavederF. etal. Immunosuppressive therapy prevents recurrent pericarditis // J. Amer. Coll. Cardiol. - 1995. - Vol. 26. - P. 1276.
Marcus F.I., Fontaine G., GuiraudonG. etal. Right ventricular dysplasia: a report of 24 cases //Circulation. - 1982. - Vol. 65. - P. 384-399.
Marcus L.C., Steere A.C., Duray PH. et al. Fatal pancarditis in a patient with coexistent Lyme disease and babesiosis//Ann. Intern. Med. — 1985. —Vol. 103. — P. 374-376.
Mason J.W. Distinct forms of myocarditis// Circulation. — 1991. — Vol. 83. — P. 1110—1111.
Masui Т., Finck S., Higgins C.B. Constrictive pericarditis and restrictive cardiomyopathy: evaluation with MR imaging //Radiology. — 1991. —Vol. 182. — P. 369.
Matsubara H. Pathophysiological role of angiotensin II type 2 receptor in cardiovascular and renal disease//Circ. Res. - 1998. - Vol. 83. - P. 1182-1191.
McCarthy R.E., Bochmer J.P., Hruban R.H. et al. Long-term outcome of fulminant myocarditis as compared with acute (nonfulminant) myocarditis // New Engl. J. Med. - 2000. - Vol. 342. - P. 690-694.
McKenna W.J., Thiene G., Nava A. et al. Diagnosis of arrhythmogenic right ventricular dysplasia/cardiomyopathy Task Force of the Working Group Myocardial and Pericardial Disease of the European Society of Cardiology and of the Scientific Council on Cardiomyopathies of the International Society and Federation of Cardiology//Brit. Heart J. - 1994. - Vol. 71. - P. 215-218.
McManus B.M., Chow L.H., Radio S.J. et al. Progress and challenges in the pathological diagnosis of myocarditis// Eur. Heart J. — 1991. —Vol. 12, Suppl. D. — P. 18-21.
MeldrumD.R. Tumour necrosis factor in the heart// Amer. J. Physiol. — 1998. — Vol. 274.-P. 577-595.
Mendosa I., Camardo J., Moleiro F. et al. Sustained ventricular tachycardia in chronic chagasic myocarditis //Amer. J. Cardiol. — 1986. — Vol. 57. — P. 423-424.
 4 Л
4 Л
Некоронарогенные болезни сердца
 Melchior Т.М., Ringsdal V., Hildebrandt P. et al. Recurrent acute idiopathic pericarditis treated with intravenous methylprednisolone given as pulse therapy// Amer. Heart J.- 1991. — Vol. 123. — P. 1086.
Melchior Т.М., Ringsdal V., Hildebrandt P. et al. Recurrent acute idiopathic pericarditis treated with intravenous methylprednisolone given as pulse therapy// Amer. Heart J.- 1991. — Vol. 123. — P. 1086.
Milei J., BortmanG., Fernandez-AlonsoG. etal. Immunohistochemicalstaining of lymphocytes for the reliable diagnosis of myocarditis in endomyocardial biopsies // Cardiology. - 1990. - Vol. 77, № 2. — P. 77-85.
Millaire A., de Groote P., Decoulx L. et al. Treatment of recurrent pericarditis with colchicine//Europ. Heart J. - 1994. - Vol. 15. — P. 120.
Moores D.W.O., Allen К. В., Faber L.P. et al. Subxiphoid pericardial drainage for pericardial tamponade//J. Thorac. Cardiovasc. Surg. — 1995. —Vol. 109. — P. 546.
Muller J., 'Vv&llukat G., Dandel M. et al. Immunoglobulin absorption in patients with idiopathic dilated cardiomyopathy//Circulation. — 2000. — Vol. 101. — P. 385-391.
Nabauer M., Kaab S. Potassium channels down-regulation in heart failure // Cardiovasc. Res. - 1998. - Vol. 37. - P. 324-334.
Nagaratnam N., deSilva D.P.K.M., Gunawardene K.R.W. Myocardial involvement in infectious hepatitis//Postgrad. Med. J. — 1971. —Vol.47. — P. 785-788.
Narang R., Swedberg K., Cleland J.G. F What is the ideal study design for evaluation of treatment for heart failure? Insights from trials assessing the effects of ACE inhibitors on exercise capacity//Europ. Heart J. — 1996. — Vol. 17. — P. 120-134.
Narula J., Haider N., Virmani R. et al. Apoptosis in myocytes in end-stage heart failure // New Engl. J. Med. - 1996. - Vol. 335. - P. 1182-1189.
Nava A., Thiene G., Canciani B. et al. Familial occurrence of right ventricular dysplasia: a study involving nine families // J. Amer. Coll. Cardiol. — 1988. — Vol. 12.-P. 1222-1228.
NelsonG.S., BergerR.D., FebicsB.J. etal. Left ventricular orbiventricular pacing improves cardiac function at diminished energy cost in patients with dilated cardiomyopathy and left bundle-branch block//Circulation. — 2000. — Vol. 102. — P. 3053-3059.
Nieminen M.A., Heikkila J., Karjalainen J. Echocardiography in acute infectious myocarditis: Relation to clinical and electrocardiographic findings // Amer. J. Cardiol. - 1984. - Vol. 53. - P. 1331-1334.
Niggli E. Ca 2+ sparks in cardiac muscle: is there life without them? // News Physiol. - 1999. - Vol. 14. - P. 129-134.
Nimura H., Bachinski L., Songwatanaroj S. et al. Mutations in the gene for cardiac myosin-binding protein-C and late-onset familial hypertrophic cardiomyopathy// New Engl. J. Med. - 1998. - Vol. 338. - P. 1248-1257.
 472
472
Некоронарогенные болезни сердца
Nishiyama Y, Ikeda H., Haramaki N. et al. Oxidative stress is related to exercise intolerance in patients with heart failure // Amer. Heart J. — 1998. — Vol. 135. — P. 115-120.
NugueO., Millaire A., Porte H. etal. Pericardioscopy in the etiologic diagnosis of pericardial effusion in 141 consecutive patients//Circulation. — 1996. — Vol. 94. — P. 1635.
O'Connell J.B. Diagnosis and medical treatment of inflammatory cardiomyopathy// Card. Vase. Dis. - 1998. - Vol. 3. - P. 132-143.
OhJ.K., HatleL., Seward J.B. etal. Diagnostic role of Doppler echocardiography in constrictive pericarditis //J. Amer. Coll. Cardiol. — 1994. — Vol. 23.— P. 154.
Okuno M., Nakagava M., Shimada M. Expressional patterns of cytokines in murine model of acute myocarditis // Lab. Invest. — 2000. — Vol. 80, № 3. — p 433-440.
Oliveira J\S., Correa De Araujo R.R., Navarro M.A. et al. Cardiac thrombosis and thromboembolism in chronic Chagas heart disease //Amer. J. Cardiol. — 1983. — Vol. 52.-P. 147-152.
Olivetti G., Abbi R., Quaini F. et al. Apoptosis in the failing human heart // New Engl. J. Med. - 1997. - Vol. 336. - P. 1131-1141.
Olsen E.G.J. The value of endomyocardial biopsies in myocarditis and dilated cardiomyopathy//Europ. Heart J. - 1991. - Vol. 12, Suppl. D. - P. 10-12.
Olsen E.G.J., Rose M.L., Meany B. et al. Molecular probes for detection of persisting enterovirus infection of human heart and their prognostic value // Europ. Heart J. - 1991. - Vol. 12 (Suppl.D). - P. 56-59.
Opie L.H. Angiotensin converting enzyme inhibition. 3th edition. New York: Wiley-Liss, 1999.-275 p.
Parmley WW Neuroendocrine changes in heart failure and their clinical relevance // Clin. Cardiol.- 1995. - \Ы. 18. - P. 440-445.
PaulusW.J., Shah A.M. NO and cardiac diastolic function //Cardiovasc. Res. — 1999.-Vol. 43.-P. 595-606.
Permanyer-Miralda G., Sagrista-Sauleda J., Soler-Soler J. Primary acute pericardial disease: a prospective series of 231 consecutive patients // Amer. J. Cardiol. - 1985. - Vol. 56. - P. 623.
Peters N.S., Poole-Wilson Ph.A. Myocarditis-continuing clinical and pathologic confusion//Amer. Heart J. - 1991. - Vol. 121. - P. 942-947.
Pfeffer J.M., Pfeffer M.A. Angiotensin converting enzyme inhibition and ventricular remodelling in heart failure // Amer. J. Med. — 1988. — Vol. 84, Suppl. ЗА. - P. 37-44.
Pichardo J., Palace V, Farahmand F. et al. Myocardial oxidation stress changes during compensated right heart failure in rats // Mol. Cell. Biochem. — 1999. — Vol. 196.-P. 51-57.
 473
473
Некоронарогенные болезни сердца
 Pinamonti В., Singara G., Salvi A. et al. Left ventricular involvement in right ventricular dysplasia//Amer. Heart J. - 1992. - Vol. 123. - P. 711-724.
Pinamonti В., Singara G., Salvi A. et al. Left ventricular involvement in right ventricular dysplasia//Amer. Heart J. - 1992. - Vol. 123. - P. 711-724.
Piovaccari G., Ferretti R.M., Prati F. et al. Cardiac disease after chest irradiation for Hodgkin's disease: incidence in 108 patients with long follow-up //Int. J. Cardiol. ~ 1995. - Vol. 49. - P. 39.
Ponicke K.,Vogelsang M., Heinroth M. et al. Endothelin receptors in the failing and nonfailing human heart//Circulation. - 1998. -Vol.97. — P. 744-751.
Post S.R., Hammond H.K., Insel PA. β-adrenergic receptors and receptor signaling in heart failure // Ann. Rev. Pharmacol. Toxicol. — 1999. — Vol. 39. — P 343-360.
PouleurH.etal. Effects of long-term enalapril therapy on left ventricular diastolic properties in patients with depressed ejection fraction // Circulation. — 1993. — Vol. 88, № 2.- P. 481-491.
Ram P., Chandra M.S. Unusual electrocardiographic abnormality in leptospirosis: Case reports//Angiology. - 1985. - Vol. 36. - P. 477-452.
Ramos H.C., EliasP.R., Barrucand L. etal. The protective effect of carnitine in human diphtheric myocarditis// Pediatr. Res. — 1984. — Vol. 18. — P. 815-817.
Rampazzo A., Nava A., Danieli G.A. et al. The gene for arrhythmogenic right ventricular cardiomyopathy maps to chromosome 14q23-q24 // Hum. Mol. Genet. - 1994. - Vol. 3. - P. 959-962.
Rampazzo A., Nava A., Erne P. et al. A new locus for arrhythmogenic right ventricular cardiomyopathy (ARVD2) maps to chromosome Iq42—q43// Hum. Mol. Genet. - 1995. - Vol. 4. - P. 2151-2154.
Rauchhaus M., Doehner W, Francis D.P. et al. Plasma cytokine parameters and mortality in patients with chronic heart failure//Circulation. — 2000. — Vol. 102. — P. 3060-3067.
Recomendations for exercise training in chronic heart failure patients. Working Group Report// Europ.Heart J. - 2001. - Vol. 22. - P. 125-135.
Reddy PS., Curtiss E.L., Uretsky B.A. Spectrum of hemodynamic changes in cardiac tamponade//Am. J.Cardiol.— 1990. - Vol. 66. - P. 1487.
Regitz-Zagrosek V, Neuss M., Fleck E. Effects of angiotensin receptor antagonists in heart failure: clinical and experimental aspects // Europ. Heart J. — 1995. — Vol. 16, Suppl. N.~ P. 86-91.
Report of the WHO/ISFC task force on the definition and classification of cardiomyopaties// Circulation. - 1996. - Vol. 93. - P. 841-842.
Rerkrattanapipat P., Wongpraparut N. Cardiac manifestations of acqured immunodeficiency syndrome // Arch. Intern. Med. — 2000. — Vol.160, № 5. — P. 602-608.
 474
474
Некоронарогенные болезни сердца
 Reynen К. Cardiac myxomas //New Engl. J. Med.— 1995.-Vol.333. - P. 1610.
Reynen К. Cardiac myxomas //New Engl. J. Med.— 1995.-Vol.333. - P. 1610.
RobbMacLellanW. Death by design//Circ. Res. - 1997. — Vol. 81. — P. 137-144.
Rodriguez-Artalejo E, Fuallar-Castillon P., Banegas Banegas J.R. et al. Trends in hospitalization and mortality for heart failure in Spain, 1988-1993 // Europ. Heart J. — 1997. - Vol. 18. - P. 1771-1779.
Rogg H. Angiotensin II receptor subtypes in human atria and evidence for alteration in patients with cardiac dysfunction//Europ. HeartJ. — 1996. —Vol. 17. — P. 1112-1120.
Roig E., Perez-Villa F, Morales M. etal. Clinical implications of increased plasma angiotensin II despite angiotensin converting enzyme inhibitor therapy in patients with chronic heart failure // Europ. Heart J. - 2000. - Vol. 2. - P. 53-57.
RozyckiG.S.,FelicianoD.V, Schmidt J.A. etal. The role of surgeon-performed ultrasound in patients with possible cardiac wounds // Ann. Surg. — 1996. — Vol. 223.-P. 737.
Rubinstein E.> Carbon С Staphylococcal endocarditis- recommendations for therapy// Clin. Microbiol. Infect. - 1998. - Vol. 4. - P. 27-33.
Rush J., Rajfer S. Theoretical basis for the use of angiotensin II antagonists in the treatment of heart failure// J. Hypert. - 1993.—Vol. 11 (Suppl. 3). - S. 69-71.
Saadia R., Levy R.D., Degiannis E. et al. Penetrating cardiac injuries: clinical classification and management strategy//Brit. J. Surg. — 1994. —Vol.81. — P. 1572.
Sagrista-Sauleda J., Permanyer-Miralda G., Candell-Riera J. et al. Transient cardiac constriction: an unrecognized pattern of evolution in effusive acute idiopathic pericarditis //Amer. J. Cardiol. - 1987. -Vol. 59. - P. 961.
Schick E.C. Jr. Nonpenetrating cardiac trauma // Cardiol. Clin. — 1995. — Vol. 13.-P. 241.
SchinkelA.,BaxJ. Echocardiographic follow-up of Chlamidia psittaci myocarditis// Chest. - 2000. - Vol. 117, № 4. - P. 1203-1205.
Schonian U., Crombach M., Maisch D. Does CMV infection play a role in myocarditis? New aspects from in situ hybridization//Europ. HeartJ. — 1991. — Vol. 12 (Suppl. D). - P. 65-68.
Sekido M., Takano T, Takayama M. et al. Survey of infective endocarditis in the last 10 years: analysis of clinical, microbiological and therapeutic features // J. Cardiol. — 1999.-Vol. 33.-P. 209-215.
Seko Y, Shinkai Y, Kawasaki A. et al. Expression of perforin in infiltrating cells in murine hearts with acute myocarditis caused by coxsackievirus B-3 // Circulation. — 1991.-Vol. 84.-P. 788-795.
 475
475
Некоронарогенные болезни сердца
 SharpeN., Doughty R.N. Left ventricular remodelling and improved long-term outcomes in chronic heart failure//Europ. HeartJ. — 1998. —Vol. 19, Suppl. B. — P. 36-39.
SharpeN., Doughty R.N. Left ventricular remodelling and improved long-term outcomes in chronic heart failure//Europ. HeartJ. — 1998. —Vol. 19, Suppl. B. — P. 36-39.
Shen W.K., Edwards WD., Hammil S.C. etal. Right ventricular dysplasia: a need for precise pathological definition for interpretation of sudden death // J. Amer. Coll. Cardiol. - 1994. - Vol. 23. -P. 34A.
Singal P.K., Khaper N., Palace V. et al. The role of oxidative stress in the genesis of heart disease // Cardiovasc. Rres. - 1998. - Vol. 40. - P. 426-432.
Smith S.C, Ladenson J.H., Mason J.W. et al. Elevations of cardiac troponin I associated with myocarditis//Circulation. — 1997. — Vol. 95. — P. 163-168.
Spinale EG., Cocker M.L., Krombach S.R. et al. Matrix metalloproteinase inhibition during the development of chronic heart failure- effects on left ventricular dimensions and function // Circ. Res. - 1999. - Vol. 85. - P. 364-376.
Srivastava S.C, Puri D.S., Lumba S.T. An electrocardiographic study of myocarditis and diphtheria//J. Assoc. Phys. India. - 1966. - Vol. 14. - P. 365-368.
Stanek G., Klein J., Bittner R. et al. Isolation of Borrelia burgdorferi from the myocardium of a patient with long-standing cardiomyopathy// New Engl. J. Med. — 1990. - Vol. 322. - P. 249-252.
Steere A.C., Batsford W.P., Weinberg M. et al. Lyme carditis: Cardiac abnormalities of Lyme disease//Ann. Intern. Med. — 1980. — Vol.93. — P. 8-16.
Steere A.C., Taylor E., Wilson M. L. et al. Longitudinal assessment of the clinical and epidemiological features of Lyme disease in a defined population //J. Infect. Dis. - 1986. - Vol. 154. - P. 295-300.
Stevens P.J., Underwood Ground K.E. Occurence and significance of myocarditis in trauma//Aerospace Med. - 1970. — Vol. 41. - P. 776-779.
Swynghedauw B. Molecular mechanisms of myocardial remodelling // Physiol. Rev. - 1999. - Vol. 79. - P. 215-262.
Symbas P.N. Traumatic heart disease//Curr. Probl. Cardiol. - 1991. - Vol. 16. -P. 537.
Takach T.J., Reul G.J., Ott D.A. et al. Primary cardiac tumors in infants and children: immediate and long-term operative results//Ann. Thorac. Surg. — 1996. — Vol. 62. - P. 559.
Tazelaar H.D., Locke T.J., McGregor C.G.A. Pathology of surgically excised primary cardiac tumors // Mayo Clin. Proc. — 1992. — Vol. 67. — P. 957.
Tesson F, Charron P., Peuchmaurd M.et al. Characterization of a unique genetic variant in the beta-1 adrenoceptor gene and evaluation of its role in idiopathic dilated cardiomyopathy//J. Mol. Cell Cardiol. - 1999. - Vol. 31. - P. 1025-1032.
 476
476
Некоронарогенные болезни сердца
The SOLVE) investigator. Effect of enalapril on mortality and the development of heart failure in asymptomatic patients with reduced left ventricular ejection fractions // New Engl. J. Med. - 1992. - Vol. 327. - P. 685-691.
Thiene G., Nava A., Corrado D. et al. Right ventricular cardiomyopathy and sudden death in young people//New Engl. J. Med. - 1988. - Vol. 318. - P. 129-133.
Thisyakorn U., Wongvanich J., Rampens V. Failure corticosteroid therapy to prevent diphtheritic myocarditis or neuritis//Pediatr. Infect. Dis. — 1984. —Vol. 3. — P. 126-130.
Tonet J., Castro Miranda R., Iwa T et al. Frequency of supraventricular tachyarrhythmias in arrhythmogenic right ventricular dysplasia //Amer. J. Cardiol. — 1991.-Vol. 67.-P. 1153.
Tracova R., Niroumand M., Lorenzi-Filho G. et al. Overnight shift from obstructive to central apneas in patients with heart failure//Circulation. — 2001. — Vol. 103.-P. 238-243.
UrataH., NishimuraH.,Ganten D. Mechanisms of angiotensin II formation in humans // Europ. Heart J. - 1995. - Vol. 16, Suppl. N. - P. 79-85.
Ursell PC, Habib A., SharmaP.etal. Hepatitis В virus and myocarditis// Hum. Pathol- 1984.-Vol. 15. - P. 481-485.
Vaitkus P.T., Kussmaul W.G. Constrictive pericarditis versus restrictive cardiomyopathy: a reappraisal and update of diagnostic criteria//Amer. Heart J. — 1991.-Vol. 122.-P. 1431.
VanderLinde M.R., Crijus H.J.G.M., Koning J. etal. Range of atrioventricular conduction disturbances in Lyme borreliosis: a report of four cases and review of other published reports// Brit. HeartJ. - 1990. - Vol. 63. - P. 162-168.
Vanhouten N., Huber S.A. Genetics of Coxsackie-B3 myocarditis // Europ. HeartJ.- 1991.-Vol. 12 (Suppl. D.). - P. 108-112.
Waller B.F., Slack J.D., Prs CD. et al. "Flaming", "smoldering" and "burned out": the fireside saga of myocarditis // J. Amer. Coll. Cardiol. — 1991. —Vol. 18. — P. 1627-1630.
Walton B.I., Wallace S.M., Kharbanda R. et al. Factors associated with increased morbidity and mortality in the initial assessment of patients presenting with acute infective endocarditis //J. Amer. Coll. Cardiol. - 2000. - \Ы. 35, issue 2, Suppl.A. - P. 537.
Weinstein M.P., Towns M.L., Quartey S.M. et al. The clinical significance of positive blood cultures in the 1990s: a prospective comprehensive evaluation of the microbiology, epidemiology and outcome of bacteremia and fungemia in adults // Clin. Infect. Dis. - 1997. - Vol. 24. - P. 584-602.
Weiss L.M., Movahed L.A., BillinghamM.E. etal. Detection of Coxsackievirus B3 RNA in myocardial tissues by the polymerase chain reaction // Amer. J. Pathol. — 1991.- Vol. 138. - P. 497-503.
 477
477
Некоронарогенные болезни сердца
Wfeiss R.L., Brier J.A., O'Connor W. et al. The usefulness of transesophageal echocardiography in diagnosing cardiac contusions//Chest.— 1996.— Vol. 109.— P. 73.
WichterT, Borggrefe M, BreithardtG. Arrhythmogenic right ventricular disease// Z. Kardiol. - 1991. - Vol. 80. - P. 107-125.
Wichter Т., Breithardt G., Block M. et al. Management of patients with arrhythmogenic right ventricular cardiomyopathy: results in 127 patients // New Trends Arrhythm. - 1993. - Vol. 9. - P. 749-755.
Wilson W.R. Antibiotic treatment of infective endocarditis due to viridans streptococci, enterococci and other streptococci//Clin. Infect. — 1998. —Vol.4. — P. 17-26.
Winearls C.G., Chan L., Coghlan J.D. et al. Acute failure due to leptospirosis: Clinical features and outcome in six cases // Amer. J. Med. — 1984. — Vol. 53. — R 487-489.
Wojnicz R., Nowalany-Kozielska E., Wilczewski P. et al. Effect of short-term immunosuppressive therapy on chronic inflammatory cardiomyopathy: two-year follow-up results//Europ. Heart J. — 2000. — Vol. 21,Abstr. Suppl. — P. 489.
Woodruff J.F. Viral myocarditis: a review//Amer. J. Pathol. — 1980. — Vol. 101. — P. 427-479.
Wynne J., Braunwald E. The cardiomyopathies and myocardities/ Heart disease-WB.Saunders Company, 1988. — P. 1410-1469.
Zahger D., Miltgalter E. A broken heart // New Engl. J. Med. — 1996. — Vol. 334.-P. 319.
Zannad F, Alia F, Dousset B. etal. Limitation of excessive extracellular matrix turnover may contribute to survival benefit of spironolactone therapy in patients with congestive heart failure. Insights from the Randomised Aldactone Evaluation Study (RALES)//Circulation. - 2000. - Vol. 102. - P. 2700-2706.
ZhangH., LiY, Peng T eta!. New evidence of enterovirus persistence in myocytes in endomyocardial biopsy samples or explanted myocardium from patients with myocarditis or dilated cardiomyopathy: an immunohistochemical study// Europ. Heart J. - 2000. - Vol. 21, Abstr. Suppl. - P. 23.
Zhang H., Li Y Localization of enteroviral antigen in myocardium from pts with heart muscle disease//J. Histochem. Cytochem. - 2000. - Vol. 48, № 5. - P. 579-84.
Ziskind A.A., Pearce A.C., Lemmon C.C. et al. Percutaneous balloon pericardiotomy for the treatment of cardiac tamponade and large pericardial effusions: description of technique and report of the first 50 cases// J. Amer. Coll. Cardiol. — 1993.-Vol. 21.-P. 1.
 478
478
Некоронарогенные болезни сердца
ОГЛАВЛЕНИЕ
ВВЕДЕНИЕ...................................................................................................................... з
Глава 1. НЕКОРОНАРОГЕННЫЕ БОЛЕЗНИ СЕРДЦА:
КЛАССИФИКАЦИЯ И КЛИНИЧЕСКАЯ СИСТЕМАТИЗАЦИЯ,
КРИТЕРИИ ДИАГНОСТИКИ...................................................................... 5
Глава 2. ФУНКЦИОНАЛЬНЫЕ БОЛЕЗНИ СЕРДЦА............................................ I 6
Глава 3. МЕТАБОЛИЧЕСКИЕ И ДЕГЕНЕРАТИВНЫЕ (ДИСТРОФИЧЕСКИЕ)
ЗАБОЛЕВАНИЯ СЕРДЦА - МЕТАБОЛИЧЕСКИЕ
КАРДИОМИОПАТИИ.................................................................................. 53
Глава 4. ПЕРИКАРДИТЫ........................................................................................... 87
Глава 5. ЭНДОКАРДИТЫ.......................................................................................... 107
Глава 6. МИОКАРДИТЫ.......................................................................................... 151
Глава 7. ПРОЛАПС МИТРАЛЬНОГО КЛАПАНА................................................ 194
Глава 8. ПРИОБРЕТЕННЫЕ ПОРОКИ СЕРДЦА................................................. 213
Глава 9. ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА......................................................... 272
Глава 10. ДИЛАТАЦИОННАЯ КАРДИОМИОПАТИЯ....................................... 325
Глава 11. ГИПЕРТРОФИЧЕСКАЯ КАРДИОМИОПАТИЯ................................. 381
Глава 12. РЕСТРИКТИВНАЯ КАРДИОМИОПАТИЯ ......................................... 410
Глава 13. АРИТМОГЕННАЯ КАРДИОМИОПАТИЯ
(ДИСПЛАЗИЯ) ПРАВОГО ЖЕЛУДОЧКА.............................................. 420
Глава 14. ОПУХОЛИ СЕРДЦА................................................................................. 426
Глава 15. ТРАВМЫ СЕРДЦА...................................................................................... 443
ЛИТЕРАТУРА............................................................................................................... 453
Дата добавления: 2019-03-09; просмотров: 137; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!