АНОМАЛИИ МЕЖЖЕЛУДО ЧКОВОЙ ПЕРЕГОРОДКИ 10 страница
Результаты молекулярно-генетических исследований свидетельствуют, что все мутации генов касаются белков миофибрилл:
1) саркомерных сократительных белков:
• бета-миозина тяжелой цепи (14-я хромосома, ген MYH7)
• дополнительной легкой цепи-1 желудочкового миозина (3-я хро
мосома, ген MYL3)
• регуляторной легкой цепи-2 желудочкового миозина (12-я хромо
сома, ген MYL2)
2) ассоциированных белков:
• сердечного тропонина-Т (1-я хромосома, ген TNNT2)
• сердечного тропонина-I (ген TNNI3)
381
|
|
| Некоронарогенные болезни сердца |
Некоронарогенные болезни сердца
• а-тропомиозина (15-я хромосома, ген ТРМ1)
3) миозинсвязывающего белка:
• связывающего протеин-С сердечного миозина (11-я хромосома, ген
MYBPC3).
В возникновении заболевания может также иметь значение нарушение взаимодействия развивающегося сердца плода с катехоламина-ми, тиреоидными гормонами, соматотро пином, аденозином.
Распространенность и локализация гипертрофии значительно варьирует, даже среди родственников. Одинаковая мутация может привести к тяжелой гипертрофии желудочка у одного члена семьи и умеренной гипертрофии у другого. Причины этих фенотипических различий у лиц с идентичной генетической мутацией не совсем понятны, но могут быть следствием других генетических факторов, которые играют роль в экспрессии гипертрофии сердца, таких, как DD-генотип ангиотензинпревращающего фермента, натрийуретические пептиды и другие детерминанты роста миоци-тов. Установлено, что DD-генотип ангиотензинпревращающего фермента наиболее часто обнаруживается у больных с тяжелой гипертрофией и у больных из семей с высокой частотой внезапной коронарной смерти.
|
|
|
Патологическая анатомия. Макроскопически гипертрофическая кардиомиопатия наблюдается в виде трех вариантов:
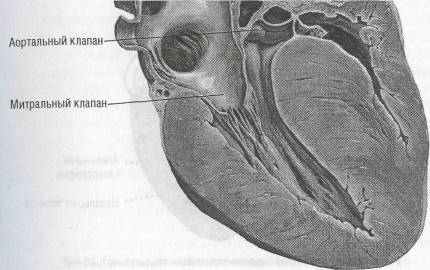
• асимметричная — изолированная гипертрофия межжелудочковой
перегородки (изолированный гипертрофический субаортальный
стеноз) (рис. 49);
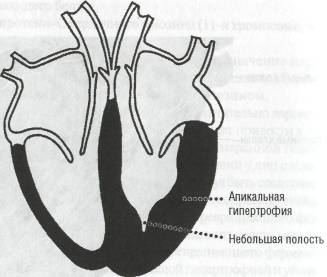
• гипертрофия различных отделов левого желудочка, чаще апикаль
ной части (рис. 50);
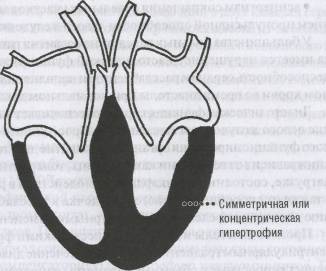
•симметричная— тотальная концентрическая гипертрофия (рис. 51).
При морфологическом исследовании чаще (60- 95%) выявляется асимметричная гипертрофия левого желудочка — преимущественная гипертрофия межжелудочковой перегородки, при которой часто стенозируется выносящий тракт левого желудочка. Иногда следствием гипертрофии является одновременное сужение выносящего тракта правого желудочка. Гораздо реже отмечается симметричная гипертрофия, верхушечная гипертрофия, гипертрофия средней части или свободной стенки левого желудочка. Рав-
 382
382
Рис. 49. Гипертрофическая кардиомиопатия (идиопатический гипертрофический субаортальный стеноз; по F. Netter, 1969, с изменениями)
|
|
|
номерная концентрическая гипертрофия миокарда сопровождается значительным увеличением массы сердца, но обструкции желудочков не наблюдается. Правый желудочек вовлекается в патологический процесс примерно в 50% случаев, что значительно усугубляет течение заболевания.
В зависимости от выраженности утолщения миокарда выделяют три степени гипертрофии:
• умеренная гипертрофия — 15-20 мм,
• средней степени — 21-25 мм,
• выраженная гипертрофия — более 25 мм.
383
Некоронарогенные болезни сердца
Некоронарогенные болезни сердца
 |  |
|
|
|
Рис.50. Гипертрофическая кардиомиопатия (апикальная гипертрофия)
Характерным анатомическим признаком гипертрофической кардиомио-патии является структурное изменение митрального клапана, передняя створка которого расположена под углом к плоскости клапана, утолщена и «выпадает» в просвет выносящего тракта левого желудочка, образуя дополнительное препятствие кровотоку. Полость левого желудочка небольших размеров, левое предсердие часто гипертрофировано и дилатировано.
Типичные патогистологические изменения включают гипертрофию кардиомиоцитов и нарушение взаимной ориентации мышечных волокон (как наиболее частый результат мутаций саркомеров), а также очаги фиброза и рубцовые изменения вследствие некроза миокарда. Волокна размещаются короткими рядами, имеют склонность к закручиванию при отсутствии изменений интрамуральных сосудов. Ядра клеток изменены, имеют уродливую форму, часто окружены светлой зоной («пери-нуклеарным нимбом»), в которой отмечается накопление гликогена.
|
|
|
Рис.51. Гипертрофическая кардиомиопатия (симметричная гипертрофия)
Патогенез и патофизиология. При гипертрофической кардиомиопа-тии генетическая неполноценность сократительных белков обусловливает нарушение обменных и сократительных процессов в гипертрофированной мышце. Морфологические изменения левого желудочка определяют состояние кардиогемодинамики.
К основным патогенетическим факторам гипертрофической кар-диомиопатии относятся:
• снижение эластичности и сократительной способности гипертро
фированного миокарда левого желудочка с ухудшением его диастоли-
ческого наполнения, в результате чего в пересчете на единицу массы
миокарда работа сердца существенно уменьшается;
|
|
|
• несоответствие коронарного кровотока в неизмененных сосудах
степени гипертрофии миокарда;
• сдавление коронарных сосудов гипертрофированным миокардом;
Некоронарогенные болезни сердца
 •нарушение скорости проведения возбуждения в желудочках с асинхронным сокращением различных отделов миокарда;
•нарушение скорости проведения возбуждения в желудочках с асинхронным сокращением различных отделов миокарда;
• асинергизм сокращения отдельных участков миокарда со снижением пропульсивной способности левого желудочка.
У большинства больных вследствие развития гипертрофии миокарда имеется нарушение диастолической функции левого желудочка — неспособность сердца к расслаблению и наполнению адекватным объемом крови во время диастолы при нормальном давлении наполнения.
Диастолическая функция сердца обеспечивает адекватное наполнение левого желудочка и сердечный выброс, достаточный для нормального функционирования организма. Развитие диастолической дисфункции зависит от геометрии камер сердца, толерантности желудочков к нагрузке, состояния перикарда, взаимодействия в работе желудочков, а также от способности левого желудочка к расслаблению и наполнению, которая определяется структурными изменениями миокарда.
Процесс диастолы модулируется несколькими факторами: 1) атрио-вентрикулярным градиентом давления в течение диастолы, который изменяет скоростные и объемные параметры наполнения левого желудочка и зависит от сократимости левого предсердия, конечно-систолического объема левого желудочка, расслабления и жесткости камер сердца; 2) активной релаксацией камер сердца, которая захватывает по времени вторую половину систолы, период изоволюмического расслабления и начало фазы быстрого наполнения левого желудочка и зависит от структурных изменений миокарда; 3) жесткостью миокарда и общей жесткостью камер (левого предсердия и левого желудочка) — пассивными характеристиками диастолы, проявляющимися после полного завершения процессов расслабления. Повышенная жесткость миокарда желудочка приводит к увеличению сопротивления диастолическому току крови в него и ухудшению диастолического расслабления.
Диастолическая функция включает в себя активные и пассивные фазы. После закрытия аортального клапана происходитизоволюмическое расслабление левого желудочка, при котором меняется форма камеры сердца, однако ее объем не увеличивается, эта фаза требует энергетических затрат (см.
 386
386
Некоронарогенные болезни сердца
рис. 47). Когда открывается митральный клапан, начинается фаза быстрого наполнения, во время которой кровоток из левого предсердия в левый желудочек осуществляется за счет разницы давления в двух камерах сердца (см. рис. 21). В начале диастолы скорость кровотока высока из-за большой разницы в давлении, которая уменьшается по мере наполнения левого же -лудочка, и наступает фаза медленного наполнения. Когда давление в левом предсердии и желудочке выравнивается, дальнейшее пассивное наполнение желудочка становится невозможным и дополнительное наполнение обеспечивается за счет сокращения предсердия (фаза систолы предсердий). При отсутствии патологии сердца наполнение левого желудочка происходит в основном в фазу медленного наполнения, доля которой составляет около 50-60%. Доля фаз быстрого наполнения и систолы предсердий составляет 25- 30% и 15- 20% соответственно.
При гипертрофической кардиомиопатии первичное повреждение происходит в кардиомиоцитах, где осуществляются мутации генов сократительных белков. Повышение нагрузки на оставшиеся интактны-ми части миофибрилл сопровождается повышением силы сокращения и стимулирует компенсаторную гипертрофию кардиомиоцитов. При развитии гипертрофии левого желудочка происходит структурное ре-моделирование миокардиальной ткани, обусловленное изменением внеклеточного матрикса — коллагеновой сети, состоящей преимущественно из коллагена и белков, связывающих коллагеновую сеть с мембраной кардиомиоцитов и миофибриллами. Состав коллагеновой сети во многом определяет механические свойства миокарда во время диастолы. Изменение нагрузки на сердечную мышцу требует соответствующего уплотнения коллагеновой сети, вследствие чего возникает реактивный или добавочный фиброз. При гипертрофической кардиомиопатии отмечается также ишемическое повреждение миокарда, которое сопровождается некрозом кардиомиоцитов, на месте которых происходит разрастание коллагеновых волокон, закрывающее дефект, — развивается также репаративный, или заместительный фиброз. Фиброз миокарда сочетается с преимущественным накоплением коллагена I типа.
Содержание коллагена во внеклеточном матриксе находится под контролем ренин-ангиотензиновой системы, циркулирующий ангио-
Некоронарогенные болезни сердца
тензин II может прямо стимулировать синтез коллагена и ингибиро-вать активность коллагеназы — ключевого энзима в процессе распада коллагена. В настоящее время многие исследователи допускают также возможность прямой паракринной или опосредованной регуляции диастолической функции за счет высвобождения медиаторов из коронарного эндотелия (оксида азота, эндотелина-1, предсердного натрий -уретического фактора или других неизвестных агентов).
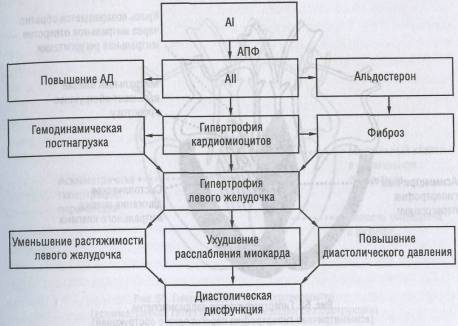
При гипертрофической кардиомиопатии рост коллагеновой сети продолжается непрерывно. Связанная с ростом матрикса возрастающая упругость миокарда облегчает сокращение во время систолы, но в значительной мере затрудняет наполнение камер сердца во время диастолы. Фиброз миокарда ухудшает расслабление миокарда и растяжимость левого желудочка, что приводит к повышению диастолического давления при любом фиксированном объеме наполнения (схема 9).
Ухудшение диастолической функции также может вызывать тканевый ангиотензин II, который ухудшает расслабление миокарда путем повышения концентрации свободных ионов кальция в кардиомиоцитах.
В результате диастолической дисфункции возникает хроническое повышение конечно-диастолического давления левого желудочка, давления заклинивания капилляров легочной артерии, застой в легких, прогрессирующая гипертрофия предсердий, фибрилляция предсердий. В измененных участках миокарда электрический сигнал может стать нестабильным вследствие наличия участков фиброза и дезориентированных кардиомиоцитов. Нарушение взаимной ориентации кардиомиоци-тов является патологическим субстратом для развития злокачественных желудочковых аритмий, которые могут быть причиной внезапной смерти. Вероятно, провоцирующими факторами являются ишемия и/или чрезмерная катехоламиновая стимуляция миокарда при нагрузках.
Нарушение диастолической функции еще больше усиливается во время тахикардии — из-за уменьшения продолжительности диастолы и ослабления систолы предсердий (уменьшения «предсердной надбавки»). Брадикардию больные также плохо переносят из-за невозможности компенсаторного расширения сердца с увеличением ударного объема.
388
Некоронарогенные болезни сердца Схема 9. Роль ренин-ангиотензиновой системы в патогенезе диастолической дисфункции
Систолическая функция при гипертрофической кардиомиопатии не нарушена или даже усилена вследствие гипердинамичности левого желудочка (фракция выброса достигает 80-90%). Левый желудочек выбрасывает почти всю кровь, поступающую в него во время диастолы, однако этого объема крови нередко бывает недостаточно для поддержания адекватной гемодинамики, так как конечно-диа-столический объем уменьшен (нередко менее 100 мл, иногда даже менее 70 мл).
В зависимости от степени выраженности преграды оттоку крови выделяют две основные формы гипертрофической кардиомиопатии:
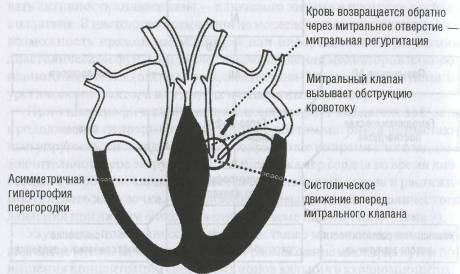
обструктывная — характеризуется наличием градиента давления между полостью левого желудочка и аортой (рис. 52)
необструктывная — без градиента давления (рис. 53).
389
Некоронарогенные болезни сердца
Некоронарогенные болезни сердца
|
|
|
|
Рис. 52. Гипертрофическая кардиомиопатия (асимметричная гипертрофия перегородки с обструкцией)
Возникновение обструкции объясняют противопоставлением гипертрофированной межжелудочковой перегородки и передней створки митрального клапана во время систолы (передняя створка митрального клапана втягивается в выходной тракт левого желудочка). Обструкция может быть постоянной (регистрироваться в покое) или латентной (динамической), возникающей только при инотропной стимуляции и/или уменьшении объема левого желудочка. У некоторых больных отмечается не обструкция, а скорее элиминация полости левого желудочка — соприкосновение стенок левого желудочка во время систолы с почти полным исчезновением полости. Первоначально именно обструкции придавали основное значение в возникновении нарушений гемодинамики при гипертрофической кардиомиопатии, однако последующие исследования показали, что хотя обструкция, несом-
390
Рис. 53. Гипертрофическая кардиомиопатия (асимметричная гипертрофия перегородки без обструкции)
ненно, играет важную роль в характере клинических симптомов, в диагностике и выборе лечебных мероприятий, определяющим моментом является нарушение диастолической функции.
Клиника и диагностика. Степень обструкции и гипертрофии левого желудочка не коррелирует с наличием клинических симптомов. Гипертрофическая кардиомиопатия может быть полностью бессимптомной или манифестировать в любом возрасте. Появление симптомов прежде всего обусловлено нарушением диастолической функции, а также возникновением аритмий, которые ее усиливают. В некоторых случаях внезапная смерть может быть первым проявлением заболевания. Наиболее часто симптомы проявляются у 40- 50-летних пациентов.
Классическая триада симптомов при гипертрофической кардиомиопатии включает стенокардию напряжения, одышку при нагрузке и обмороки.
Некоронарогенные болезни сердца
Болевые ощущения в грудной клетке отмечаются у 75% больных с гипертрофической кардиомиопатией, классическая стенокардия напряжения— у 25%. Последняя может наблюдаться у больных с интактными коронарными артериями и обусловлена нарушением диастолического расслабления стенки левого желудочка, что приводит к повышению внут-римиокардиального напряжения гипертрофированного миокарда и ин-трамиокардиальному сдавлению коронарных сосудов. Стенокардия возникает как результат нарушения баланса между потребностью гипертрофированного миокарда в кислороде и потреблением кислорода, доставляемого коронарными артериями, сдавленными жестким миокардом. У многих больных отмечается послеобеденная стенокардия.
Причиной левожелудочковой недостаточности (одышка при нагрузке, приступы сердечной астмы, отек легких) является быстрый подъем конечно-диастолического давления и давления заклинивания капилляров легочной артерии при ускорении кровотока вследствие диасто-лической дисфункции. Систолическая функция обычно не нарушена.
Синкопальное состояние — наиболее тяжелое проявление гипертрофической кардиомиопатии, основными причинами его являются нарушение диастолического наполнения левого желудочка, возникновение аритмий, обструкция выносящего тракта. Сердце не способно увеличить сердечный выброс при физической нагрузке, в результате происходит перераспределение кровотока к работающим мышцам и наступает ишемия мозга с кратковременной потерей сознания. Обмороки вызваны увеличением степени обструкции (и снижением сердечного выброса) вследствие редуцированного периода диастолического наполнения, что обусловлено синусовой тахикардией при физической нагрузке. Чаще всего обмороки наблюдаются у больных молодого возраста, у многих из них при суточном мониториро-вании ЭКГ регистрируются эпизоды желудочковой тахикардии, нарушений проводимости.
У значительного числа больных (5-28%) возникает фибрилляция предсердий, повышающая риск развития тромбоэмболических ослож-
392
Некоронарогенные болезни сердца
нений. При тяжелой диастолической дисфункции ее возникновение приводит к увеличению выраженности симптомов вследствие потери «вклада» предсердий в диастолическое наполнение желудочков.
При обструктывной форме гипертрофической кардиомиопатии выявляют следующие симптомы:
• систолический шум ( crescendo - diminuendo ), который не проводится
или слабо проводится на сонные артерии и в область спины. Шум
вызван обструкцией при изгнании крови из левого желудочка (воз
никает в систолу, когда гипертрофированная межжелудочковая пе
регородка и передняя створка митрального клапана движутся на
встречу друг другу);
• шум усиливается при уменьшении наполнения сердца и сниже
нии общего периферического сосудистого сопротивления (вста
вание из положения сидя на корточках, натуживание, прием нит
роглицерина) и ослабевает при увеличении наполнения сердца,
повышении общего периферического сосудистого сопротивления
(в положении лежа, сидя на корточках, при сжимании кулаков);
Дата добавления: 2019-03-09; просмотров: 117; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!