ТРИКУСПИДАЛЬНАЯНЕДОСТАТО ЧНОСТЬ
Патологическая анатомия. Для органической недостаточности трехстворчатого клапана характерно значительное расширение фиброзного кольца за счет области передней и задней створок и соответствующих комиссур. Часть фиброзного кольца, соответствующая основанию перегородочной створки, не дилатируется и является единым целым с перегородочной частью межжелудочковой перегородки. Относительная недостаточность характеризуется отсутствием фиброзных изменений, отмечается лишь утолщение краев створок, вызванное постоянным воздействием волны регургитации.
Некоронарогенные болезни сердца
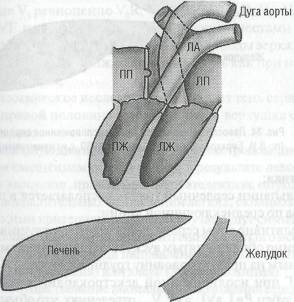
 Патологическая физиология. Регургитация крови из правого желудочка в правое предсердие относительно быстро ведет к дилатации правого предсердия без существенной его гипертрофии (см. рис. 32). Компенсация порока осуществляется подобно митральной недостаточности, однако компенсирующие возможности правого предсердия меньше, поэтому рано формируются венозная гипертензия и венозный застой с депонированием крови в печени и других органах брюшной полости.
Патологическая физиология. Регургитация крови из правого желудочка в правое предсердие относительно быстро ведет к дилатации правого предсердия без существенной его гипертрофии (см. рис. 32). Компенсация порока осуществляется подобно митральной недостаточности, однако компенсирующие возможности правого предсердия меньше, поэтому рано формируются венозная гипертензия и венозный застой с депонированием крови в печени и других органах брюшной полости.
Недостаточность трехстворчатого клапана с большим объемом ре-гургитации создаете систолу волну обратного тока, которая приводит к систолической пульсации яремных вен и печени. Среднее давление в полости правого предсердия повышено в 2-3 раза и более. Как и при недостаточности митрального клапана, вследствие большей податливости к растяжению сердечной мышцы, чем фиброзного кольца, возможно появление относительного стеноза с небольшим градиентом диастолического давления между правым предсердием и правым желудочком, манифестирующего слабым диастолическим шумом.
|
|
|
Клиническая картина. Типичны жалобы на одышку, слабость, сердцебиение, тяжесть в правом подреберье. Если порок формируется у больного с ранее имевшимся митральным стенозом, застойные явления в малом круге кровообращения уменьшаются, одышка ослабевает, больной легче переносит горизонтальное положение.
При осмотре обращают на себя внимание систолическая пульсация шейных вен, обусловленная обратным током крови из правого желудочка, набухание шейных вен в положении лежа, выраженная пульсация в эпигастральнои области, в области печени. Аускультативно определяется систолический шум средней интенсивности, усиливающийся ко II тону и определяющийся у основания мечевидного отростка, слева у нижнего края грудины, шум усиливается на вдохе (симптом Риверо — Корвало).
На электрокардиограмме определяются признаки гипертрофии правого желудочка в виде увеличенной амплитуды зубцов комплекса QRS b соответствующих отведениях в сочетании с измененной конечной частью желудочкового комплекса (уплощение, инверсия зубца Т, снижение сегмента ST ) в тех же отведениях, увеличение зубца Р в отведениях II , III и aVF
|
|
|
Некоронарогенные болезни сердца
фонокардиографически определяются снижение амплитуды I тона я областью проекции клапана. Систолический шум имеет лентовид-форму и занимает всю систолу, шум усиливается на вдохе и в положении на правом боку.
Рентгенологически определяются расширение верхней полой вены, преобладающее увеличение правых отделов сердца, закругление их контуров во всех проекциях, увеличение правого предсердия и желудочка во второй косой проекции.
При эхокардиографическом исследовании определяется расширение полости правого желудочка, признаки регургитации на трехстворчатом клапане.
О наличии и выраженности трикуспидальной недостаточности можно судить по кривым давления в правом предсердии.
Диагностика порока основывается на признаках венозного полнокровия, положительного венного пульса, обнаружении систолического шума с характерной топографией, а также на данных рентгенографии сердца.
Течение органической трикуспидальной недостаточности, как правило, быстро прогрессирующее, рефрактерное к терапии. Наиболее тяжело протекает органическая трикуспидальная недостаточность, которая присоединяется к сформированному митральному пороку, поскольку быстро нарастают нарушения кровообращения. Осложнениями порока часто бывают мерцание предсердий, тромбирование полости правого предсердия с тромбоэмболией легочной артерии, иногда желудочно-кишечные кровотечения.
|
|
|
Лечение. Специфических консервативных методов лечения трикуспидальной недостаточности нет, развивающуюся сердечную недостаточность лечат, используя общепринятые методы. По показаниям назначают мочегонные препараты, периферические вазодилататоры, блокато-ры р-адренорецепторов (втом числе карведилол), сердечные гликозиды, антикоагулянты, метаболические препараты. Лечение направлено на Уменьшение застоя в большом круге кровообращения, уменьшение объема выброса из правого желудочка, коррекцию метаболизма миокарда и гомеостаза.
Некоронарогенные болезни сердца
Глава 9. ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА
Врожденные пороки сердца представляют собой аномалии и деформации клапанов, отверстий или перегородок между камерами сердца или отходящих от него сосудов, нарушающие внутрисердечную и системную гемодинамику, предрасполагающие к развитию острой или хронической недостаточности кровообращения. Частота врожденных пороков сердца составляет до 1 % всех заболеваний сердца.
|
|
|
Врожденные пороки сердца являются следствием определенных нарушений в период его эмбрионального формирования. Основное развитие сердца происходит с 21-го по 42-й дни жизни плода. В кау-дальном конце сердечной трубки располагается венозный синус, в который впадают большие вены, за ним следует область предсердий, часть трубки образует общий желудочек. К концу первого месяца намечаются первые признаки разделения сердца на правую и левую половины (полное разделение потоков крови завершается только в постнаталь-ный период). Формирование так называемой первичной межпредсерд-ной перегородки ( septum primum ) почти полностью разделяет общее первичное предсердие на две половины, остается лишь небольшое сообщение— межпредсердное отверстие (ostium primum ). К этому времени венозный синус смещается в правое предсердие. Дальнейшее развитие первичной перегородки приводит к полному закрытию первичного отверстия, но полного разобщения предсердий не происходит, поскольку одновременно в краниальном отделе первичной перегородки образуется новое отверстие — вторичное межпредсердное отверстие (ostium secundum), через которое кровь продолжает поступать из правого предсердия в левое, что является условием нормального внутриутробного кровообращения плода. В этот же период образуется вторичная межпредсердная перегородка, которая возникает также от краниального участка стенки правого предсердия, несколько правее первичной перегородки. Эта перегородка сплошная, имеет вид полумесяца, образуя своими краями овальное окно (fenestra ovalis), которое не совпадает с вторичным отверстием в первичной перегородке (ПО-
Некоронарогенные болезни сердца
леднее расположено выше у самой стенки предсердия). Нерезорбиро-авшаяся часть первичной перегородки прикрывает овальное отверстие в виде одностороннего клапана, допускающего движение крови только из правого предсердия в левое.
При нарушениях нормального процесса развития первичной и вторичной межпредсердных перегородок и эндокардиальных подушек могут образовываться различные врожденные пороки сердца. Неполное развитие первичной перегородки приводит к образованию дефекта меж-предсердной перегородки типа ostium primum, при нормально развитой первичной перегородке и нарушении развития вторичной перегородки образуется дефект типа ostium secundum — высокий дефект межпредсерд-ной перегородки. Сочетание нарушения развития перегородок предсердия с неправильным расположением венозного синуса приводит к образованию сложных дефектов межпредсердной перегородки.
Формирование перегородки и окончательное закрытие сообщения между желудочками происходит благодаря формированию соединительнотканного образования, развивающегося на основании эндокардиальных подушек, края мышечной части мышечной перегородки и эндокардиальных складок артериального конуса. Это образование в дальнейшем истончается, образуя так называемую мембранозную часть межжелудочковой перегородки. При нарушении развития мышечной части межжелудочковой перегородки в ней образуются единичные или множественные отверстия, которые обычно не вызывают нарушения гемодинамики, поскольку сжимаются во время сокращения миокарда желудочков в период систолы. Чаще дефекты образуются в мембранозной части межжелудочковой перегородки, при этом в зависимости от нарушения развития различных отделов этой части перегородки образуются высокие или низкие ее дефекты, нередко они захватывают нижележащую часть мышечной перегородки. Клапанный аппарат атриовентрикулярных отверстий формируется из соединительной ткани эндокардиальных подушек.
К моменту окончательного закрытия межжелудочкового сообщения происходит разделение артериального ствола на аорту и легочную артерию. Перегородка между ними, а также клапанный аппарат форми-
 ~273
~273
Некоронарогенные болезни сердца
руются из разрастания эндокардиальных соединительнотканных складок артериального ствола. Нарушение развития аортолегочной перегородки может быть локальным, на небольшом протяжении, тогда формируется порок типа аортолегочного свища. Иногда разделения артериального ствола на аорту и легочную артерию вообще не происходит, и формируется порок, называемый общим артериальным стволом. В процессе формирования этой перегородки направление ее роста может нарушиться и идти не по спирали, как обычно, а прямо — в таких случаях формируется порок, называемый транспозицией аорты и легочной артерии (аорта отходит от правого желудочка, а легочная артерия — от левого). В ряде случаев нарушения развития перегородки артериального конуса приводят к ее отклонению в ту или иную сторону, вследствие чего возникает сужение аорты или легочной артерии. К сужению последней часто присоединяется нарушение развития складок конуса в месте, где они участвуют в формировании мембранозной части перегородки, — образуется дефект в ней, расширенная аорта сдвигается вправо и оказывается расположенной прямо над дефектом — развивается порок, получивший название «тетрада Фалло».
Возникновение ряда врожденных пороков сердца и магистральных сосудов связано с нарушениями в постнатальный период. С момента рождения ребенка, первого вдоха начинают функционировать легкие, через которые осуществляется газообмен. Артериальный проток, благодаря сокращению гладких мышц его стенки, функционально закрывается, затем происходит его анатомическое закрытие. Увеличение легочного кровообращения и соответственно поступление большого количества крови в левое предсердие приводят к увеличению давления в нем по сравнению с правым предсердием, вследствие чего происходит функциональное закрытие овального отверстия имеющимся клапаном, а затем приращение его к краям овального отверстия — так формируется целостная межпредсердная перегородка. Полное анатомическое закрытие овального отверстия происходит к концу 1-го года жизни. Нарушение в процессе нормального закрытия артериального протока приводит к формированию порока, известного как открытый артериальный проток. При
 274
274
Некоронарогенные болезни сердца
очетании незаращения овального отверстия с недоразвитием вторичной перегородки формируется дефект межпредсердной перегородки в области овального окна.
Описано несколько сот различных вариантов и сочетаний шунтов, по-гючных сообщений между большим и малым кругом кровообращения, атипичных расположений клапанов, впадений или отхождений сосудов и других сложных аномалий, что обусловило многообразие их классификаций. По этиологии врожденные пороки подразделяются на две группы:
1. Первая (основная) группа - пороки, обусловленные нарушени
ем формообразования, являющиеся патологией эмбрионального раз
вития сердечно-сосудистой системы.
2. Вторая группа, меньшая по численности, — пороки, развившие
ся вследствие заболеваний эндокарда, перенесенных во внутриутроб
ный период.
Дифференцировать клинически эти две группы практически невозможно, так как клиническая симптоматика их сходна: поражается преимущественно трехстворчатый клапан и клапан легочной артерии (то есть порок правой половины сердца).
Возникновение пороков эмбрионального развития может быть обусловлено:
1) генными мутациями,
2) различными инфекционными процессами в период беременности,
3) интоксикациями (эндогенными и экзогенными в период бере
менности).
С учетом морфологии поражения среди врожденных пороков сердца выделяют:
• изменения положения сердца,
• аномалии предсердной перегородки,
• аномалии межжелудочковой перегородки,
• аномалии легочной артерии,
• аномалии артериального протока,
• аномалии аорты,
• перемещение больших сосудов,
• аномалии клапанного аппарата сердца.
275
Некоронарогенные болезни сердца
В клинической практике существует деление врожденных пороков на «синие» (когда происходит смешивание артериальной и венозной крови и кожные покровы, губы, ушные раковины, ногти приобретают синюшный оттенок) и «белые» (не сопровождаются изменением цвета кожных покровов).
Классификация врожденных пороков сердца ( Perloff J . K ., 1987):
Общие
• врожденная корригированная транспозиция магистральных артерий,
• аномалии расположения сердца,
• врожденная полная блокада сердца.
Пороки сердца «белые» с шунтированием крови слева направо
1. Шунт крови на уровне предсердий:
1) дефект межпредсердной перегородки,
2) дефект межпредсердной перегородки в сочетании с митраль
ным стенозом (синдром Лютамбаше),
3) частичное аномальное присоединение легочных вен.
2. Шунт крови на уровне желудочков:
1)дефект межжелудочковой перегородки,
2)дефект межжелудочковой перегородки в сочетании с недоста
точностью клапана аорты,
3)дефект межжелудочковой перегородки со сбросом крови из ле
вого желудочка в правое предсердие.
3. Шунт крови из устья аорты в правую часть сердца:
1) разрыв аневризмы синуса Вальсальвы,
2) коронарная артериовенозная фистула,
3) аномальное отхождение выхода левой коронарной артерии из
ствола легочной артерии.
4. Шунт крови между аортой и легочной артерией:
1) аортопульмональное окно,
2) открытый артериальный проток.
5. Многоуровневые шунты крови:
1) полный общий предсердно-желудочковый канал,
2) сочетание дефекта межжелудочковой перегородки с дефектом
межпредсердной перегородки,
276
Некоронарогенные болезни сердца
3) сочетание дефекта межжелудочковой перегородки с открытым
артериальным протоком.
Пороки сердца «белые» без шунтирования крови 1 Пороки левых отделов сердца:
1) врожденная обструкция притоку крови в левое предсердие,
2) митральная недостаточность,
3) первичный дилатируюший фиброэластоз эндокарда,
4) стеноз устья аорты,
5) недостаточность аортального клапана,
6) коарктация аорты.
2. Пороки правых отделов сердца:
1) аномалия трехстворчатого клапана Эбштейна без цианоза,
2) стеноз легочной артерии,
3) врожденная недостаточность клапана легочной артерии,
4) идиопатическое расширение ствола легочной артерии.
Пороки сердца «синие»
С усиленным легочным кровотоком:
1. Полная транспозиция магистральных артерий.
2. Синдром Тауссиг — Бинга.
3. Артериальный ствол.
4. Полная аномалия присоединения легочных вен.
5. Единственный желудочек без стеноза легочного ствола.
6. Общее предсердие.
7. Тетрада Фалло с атрезией легочного ствола и усилением колла
терального артериального кровотока.
8. Атрезия трехстворчатого клапана с большим дефектом меж
желудочковой перегородки, без стеноза легочного ствола.
9. Гипоплазия левых отделов сердца (атрезия аорты и митрально
го клапана).
С нормальным или уменьшенным легочным кровотоком:
1. Атрезия трехстворчатого клапана.
2. Аномалия Эбштейна с шунтированием крови из правого пред
сердия в левое.
Некоронарогенные болезни сердца
3. Атрезия легочного ствола с интактной межжелудочковой перего
родкой.
4. Стеноз или атрезия легочного ствола с дефектом межжелудочко
вой перегородки (тетрада Фалло).
5. Стеноз легочного ствола с шунтированием крови из правого пред
сердия в левое.
6. Полная транспозиция магистральных сосудов в сочетании со сте
нозом легочного ствола.
7. Отхождение обоих выносящих сосудов из правого желудочка в
сочетании со стенозом легочного ствола.
8. Единственный желудочек со стенозом легочного ствола.
9. Артериовенозные свищи легких.
10. Сообщение между полыми венами и левым предсердием.
Многие врожденные пороки сердца не совместимы с жизнью или комбинируются с другими тяжелыми уродствами. Существует 2-3 возрастные волны смертности: больные умирают в течение критического срока -в первые недели или месяцы после рождения, у переживших этот период после некоторой компенсации ухудшение наступает в возрасте 12-15 лет.
Возможность хирургического лечения врожденных пороков сердца обусловливает важность их прижизненной диагностики, особенно в детском возрасте. Врожденные пороки сердца относятся к категории наиболее трудных в дифференциально-диагностическом отношении видов патологии. Несмотря на выраженность аускультативной картины, позволяющей заподозрить врожденный порок сердца, точная топическая диагностика их в клинике терапевтического профиля пока еще остается проблематичной. Вторая важная проблема для врачей-терапевтов— это отбор и направление таких больных для хирургического лечения.
АНОМАЛИИ РАСПОЛОЖЕНИЯ СЕРДЦА
К аномалиям внутригрудного расположения сердца относятся: нарушения расположения верхушки сердца, ее соответствия с характером расположения органов брюшной полости и случаи неправильного формирования сердца в виде обратного или неопределенного раСПОЛОЖе-
Некоронарогенные болезни сердца
ния эмбриональных закладок правого и левого предсердий. Частота этих аномалий составляет 1,5% среди всех врожденных пороков сердца.
|
|
| Рис. 33. Правосформированное праворасположенное сердце (по В.И. Бураковскому, Л.А. Бокерия, 1989, с изменениями) |
Наиболее частыми аномалиями являются правосформированное праворасположенное сердце — изолированная декстрокардия (рис. 33) и левосформированное праворасположенное сердце (рис. 34) — «зеркальная декстрокардия» (соответственно у 54 и 33% больных с правосторонним расположением сердца). В первом случае расположение других органов грудной клетки и топография органов брюшной полости соответствуют физиологической норме, во втором случае наблюдается полное обратное расположение внутренних органов. Если строение сердца и сосудов не нарушено, оно в целом функционирует нормально, нарушения кровообращения не происходит.
Некоронарогенные болезни сердца
| Некоронарогенные болезни сердца |

Рис. 34. Левосформированное праворасположенное сердце (по В.И. Бураковскому, Л.А. Бокерия, 1989, с изменениями)
Диагностика:
• при пальпации сердечный толчок располагается в пятом межре-
берье справа по среднеключичной линии;
• аускультативно тоны сердца лучше всего прослушиваются справа
соответственно общепринятым аускультативным точкам, симметрич
но смещенным на правую половину грудной клетки;
• на ЭКГ при изолированной декстрокардии характерен поло
жительный зубец Ръ I, aVL, aVF, V,_ 4 отведениях, что объясняется обыч
ным распространением предсердной деполяризации благодаря
нормальному расположению предсердий. В грудных отведениях воль-
тажкомплексов QRS прогрессивно увеличивается от V6Rдо V1_2 и далее
снижается к V6, указывая на правостороннее расположение сердца.
При этом потенциалы правого желудочка в форме комплексов rS или
RS регистрируются в отведениях от V6R до V2, 3, левого — в виде qR
на ЭКГ при истинной декстрокардии характерен отрицательный зубец Р в I, aVL, V5, 6 отведениях, отражающий расположение синусного узла в левостороннем предсердии, положительный Рв II , III , V отведениях, отрицательные комплексы QRS в I, aVR, повышение их вольтажа от V, до V6R и снижение- otV, до V6, отрицательные Т в I aVL, V5, б. В I стандартном отведении регистрируются зубцы, имеющие противоположное обычному направление: II стандартное отведение соответствует нормальному III и наоборот, III стандартное отведение — II , отведение aVL отражает отведение aVR и наоборот, aVR-aVL, отведение V, равноценно V2R, V3- V3R, V4- V4R, V5- V5R, V6- V6R. Отведение aVF не изменяется. Если поменять местами электроды правой и левой руки и наложить грудные электроды зеркально к нормальному сердцу, то ЭКГ можно анализировать как при нормальном расположении сердца;
• рентгенологическое исследование выявляет тень сердца преимущественно в правой половине грудной клетки, верхушка сердца ориентирована вправо.
Дифференциальную диагностику проводят с декстропозицией сердца — механическим смещением сердца вправо в результате левостороннего плеврального экссудата, правостороннего ателектаза, опухоли легких и средостения, воспалительных заболеваний легких, сколиоза. Ведущими диагностическими критериями в данном случае будут симптомы сопутствующего заболевания и результаты рентгенологического исследования, позволяющие определить, куда направлена верхушка левого желудочка — вправо (декстрокардия) или влево (декстропозиция).
Само по себе существование аномального положения сердца не сопровождается расстройствами гемодинамики. Хирургическому лечению подлежат лишь больные с сопутствующими пороками сердца.
Некоронарогенные болезни сердца
 АНОМАЛИИ МЕЖПРЕДСЕРДНОЙ ПЕРЕГОРОДКИ Дефект межпредсердной перегородки
АНОМАЛИИ МЕЖПРЕДСЕРДНОЙ ПЕРЕГОРОДКИ Дефект межпредсердной перегородки
Дефект межпредсердной перегородки - это врожденный порок сердца, при котором имеется сообщение между двумя предсердиями, развивающееся в результате аномального развития первичной и вторичной межпредсердных перегородок и эндокардиальных подушек. Первое упоминание о пороке встречается в работах Галена. Наиболее полное описание патолого-анатомической картины порока принадлежит К. Rokitansky (1875). Дефект межпредсердной перегородки является наиболее частым пороком сердца у взрослых, составляя 15-20% всех врожденных пороков, у женщин встречается чаще, чем у мужчин (3:2).
Патологическая анатомия. Исходя из эмбриогенеза различают несколько анатомических вариантов дефекта межпредсердной перегородки:
1. Дефект первичной перегородки (тип ostium primurn ) представляет
собой вариант дефекта эндокарда, располагается в нижнем отделе пе
регородки непосредственно над уровнем предсердно-желудочковых от
верстий, сочетается с расщеплением створок митрального и реже трех
створчатого клапанов.
2. Дефект вторичной перегородки (тип ostium secundum) - вариант,
при котором всегда сохраняется край перегородки в нижнем отделе,
отделяющий его от уровня предсердно-желудочковых клапанов; наи
более часто локализуется в центральной части межпредсердной пере
городки в области овальной ямки. Дефекты венозного синуса чаще
встречаются высоко в межпредсердной перегородке вблизи от впаде
ния верхней полой вены и связаны с атипичным впадением легочных
вен в правое предсердие или верхнюю полую вену (рис. 35). Дефекты
венозного синуса могут также локализоваться в нижней части перего
родки над устьем нижней полой вены.
3. Общее предсердие — полное отсутствие межпредсердной перего
родки или наличие только рудиментарных ее элементов, часто сочета
ется с расщеплением атриовентрикулярных клапанов.
Открытое овальное отверстие, которое не закрывается у 20% взрослых, не следует рассматривать как разновидность дефекта межпредсердной
28~2
Некоронарогенные болезни сердца

рис. 35. Анатомические варианты дефекта межпредсердной перегородки (по F. Netter, 1969, с изменениями)
Некоронарогенные болезни сердца
перегородки, так как при истинном дефекте имеется недостаточность ткани, а при открытом овальном окне сообщение осуществляется благодаря клапану, который открывается при особых обстоятельствах. Нарушений гемодинамики при этом не наблюдается, но если давление в правом предсердии превышает давление в левом, то происходит шунтирование крови справа налево.
Гемодинамика. Наличие дефекта межпредсердной перегородки приводит к сбросу артериальной крови из левого предсердия в правое вследствие наличия градиента давления между ними (см. рис. 21). В результате возникает перегрузка объемом правой половины сердца, дилатация правого желудочка и увеличение объема циркулирующей крови в малом круге. При больших дефектах это может приводить к легочной гипер-тензии, однако выраженная гипертензия в малом круге в первые 20 лет возникает не более чем у 2% больных, что может быть обусловлено рядом факторов: отсутствием непосредственного влияния на сосуды легких высокого давления левого желудочка, передачей давления из правого желудочка в легочную артерию, значительной растяжимостью правых отделов сердца, резервной емкостью легочных сосудов и их низким сопротивлением.
Основную роль в компенсации нарушения кровообращения играет правый желудочек, работа которого увеличивается в несколько раз. Недостаточность правого желудочка и недостаточность кровообращения развивается после 10 лет существования порока, в более старшем возрасте присоединяется недостаточность левого желудочка. Последняя, вызывая уменьшение его податливости, может приводить к увеличению объема шунта слева направо.
Клинические проявления порока зависят от степени нарушения гемодинамики и изменяются с возрастом. При относительно небольшом дефекте в молодом возрасте больные могут не предъявлять жалоб, и порок выявляется при случайном обследовании. В возрасте старше 30 лет могут появиться одышка и сердцебиение при физической нагрузке, затем и в покое, нарастают слабость и утомляемость. При больших дефектах межпредсердной перегородки одышка является одним
 284
284
Некоронарогенные болезни сердца
из симптомов заболевания уже в молодом возрасте, у таких больных может также появляться синюшность кожных покровов за счет смешивания аортальной и венозной крови.
При открытом овальном отверстии, если дефект небольшой и нет других аномалий, то форма и размеры сердца не изменены. Большие дефекты приводят к гипертрофии и дилатации правого предсердия и правого желудочка. Левые отделы сердца, как правило, не изменяются.
При перкуссии отмечается расширение границ сердца преимущественно вправо, а при больших дефектах— влево. В отдельных случаях описаны наличие сердечного горба (за счет увеличения правых отделов сердца), а также систолическое дрожание у левого края грудины.
Характерна аускультативная картина: над легочной артерией слева у грудины выслушивается систолический шум умеренной интенсивности, возникающий вследствие увеличенного кровотока через клапан легочной артерии. Тембр и интенсивность шума могут быть различными, интенсивность его возрастает при задержке дыхания на выдохе. Второй тон над легочной артерией усилен и раздвоен. Реже определяется диастолический шум над нижней частью грудины, связанный с относительным стенозом отверстия трехстворчатого клапана при увеличенном количестве крови, проходящей через него. После того, как возросшее легочное сосудистое сопротивление приводит к понижению величины сброса крови слева направо , интенсивность шумов снижается, появляется диастолический шум, вызванный недостаточностью клапана легочной артерии.
Диагностика. На ЭКГ электрическая ось сердца у больных со вторичным дефектом отклонена вправо, с первичным — влево. При каждом из дефектов обнаруживается различная степень перегрузки и гипертрофии правого желудочка и правого предсердия, выраженность которой зависит от величины давления в легочном стволе. Выявляются признаки частичной блокады правой ножки пучка Гиса (феномен rsR' в правых грудных отведениях), отражающей замедление активации зад-небазальной части межжелудочковой перегородки.
На фонокардиограмме регистрируется систолический шум с максимальной интенсивностью у левого края грудины, где прикрепляется
 ~285
~285
Некоронарогенные болезни сердца
III ребро. Шум может занимать всю систолу, может носить равномерный, ромбовидный или убывающий характер. Иногда регистрируется и диастолический шум. Амплитуда колебания II тона усилена.
На рентгенограмме сердце увеличено в поперечнике, в косых проекциях определяется увеличение правых отделов сердца. Дуга легочной артерии выбухает, дуга аорты уменьшена, усилен сосудистый рисунок легких (за счет переполнения артериального русла). Корни легких расширены, характерна их пульсация.
Эхокардиография в настоящее время может служить методом верификации диагноза дефекта межпредсердной перегородки. Дефект можно непосредственно увидеть, он хорошо определяется при допплер-эхокардиографии. При эхокардиографическом исследовании выявляют следующие признаки:
• увеличение полости правого предсердия и правого желудочка,
• парадоксальное движение межжелудочковой перегородки,
• гипердинамичное движение стенок левого предсердия,
• признаки легочной гипертензии,
• признаки расщепления митрального и трехстворчатого клапанов
с проявлениями их недостаточности при первичном дефекте,
• пролапс митрального клапана при вторичном дефекте,
• шунтирование крови между предсердиями слева направо или спра
ва налево.
Катетеризация полостей сердца позволяет выявить сброс крови на уровне предсердий. При дефекте межпредсердной перегородки выявляется повышение давления в полости правого предсердия, в правом желудочке и легочной артерии (см. рис. 21). Характерным для порока является проведение катетера из правого предсердия в левое и повышение насыщения крови кислородом в полости правого предсердия по сравнению с пробами крови, взятой у устья полых вен. Разница в 2 об. % и более (или 8- 10%) рассматривается как абсолютный признак шунтирования крови.
Дифференциальная диагностика. Вторичный дефект межпредсердной перегородки дифференцируют с небольшим стенозом устья легочной
 286
286
Некоронарогенные болезни сердца
 артерии, митральным стенозом, хроническим легочным сердцем (важное значение имеют пульмонологический анамнез и обследование).
артерии, митральным стенозом, хроническим легочным сердцем (важное значение имеют пульмонологический анамнез и обследование).
Дифференциальную диагностику первичного дефекта проводят с недостаточностью митрального клапана по следующим критериям:
• определение времени возникновения шума: появление шума в
раннем детском возрасте — всегда убедительный признак врож
денного порока;
• при недостаточности митрального клапана максимум шума опре
деляется в точке Боткина и на верхушке сердца, шум проводится
хорошо по направлению клевой подмышечной впадине;
• при недостаточности митрального клапана границы сердца преиму
щественно расширены влево и вверх, что определяется при перкус
сии и рентгенологически (митральная конфигурация), на ЭКГ вы
являют признаки гипертрофии преимущественно левого желудочка;
• при катетеризации в компенсированном состоянии давление в
правом предсердии мало изменяется;
• при введении контрастного вещества в левые отделы сердца не про
исходит его сброса в правое предсердие;
• на эхокардиограмме отсутствует патология со стороны митраль
ного клапана.
Течение и прогноз. Вторичный дефект имеет благоприятное естественное течение в первые 20- 30 лет жизни, жалобы возникают после 40 лет, затем появляются аритмии, сердечная недостаточность, которая обусловлена выраженной легочной гипертензией. Причиной смерти без операции является правожелудочковая сердечная недостаточность, реже тромбоз легочной артерии, аритмии. При первичном дефекте течение менее благоприятное, раньше возникают жалобы и осложнения, основным отягощающим фактором является легочная ги-пертензия, прогноз хуже.
Лечение. Хирургическое лечение — единственный эффективный способ радикальной коррекции врожденных пороков сердца. Вследствие возможности увеличения шунта крови слева направо, появления фибрилляции предсердий и развития легочной гипертензии с возрас-
 287
287
Некоронарогенные болезни сердца
том желательно выполнение хирургической коррекции порока до появления признаков ухудшения функции сердца. Показания к хирургическому лечению:
• неэффективная медикаментозная терапия сердечной недостаточ
ности,
• значительный артериовенозный сброс,
• отставание в физическом развитии,
• повышение давления в малом круге кровообращения.
Противопоказаниями к операции являются:
1. Веноартериальный (справа налево) сброс, поскольку это признак
выраженной гипертензии и часто необратимых изменений в малом кру
ге кровообращения.
2. Выраженная левожелудочковая недостаточность.
Хирургическое лечение заключается в ушивании или пластике заплатой дефекта межпредсердной перегородки в условиях искусственного кровообращения. Мелкие дефекты зашивают, большие закрывают го-мотрансплантатами или протезами из пластмассовой губки. При первичном дефекте со значительной митральной недостаточностью дополнительно ушивают расщепленную створку или проводят протезирование митрального клапана. В результате операции улучшается состояние больного; уменьшаются одышка, сердцебиение, размеры сердца. Условием хороших результатов хирургического лечения служит своевременность операции, которую следует выполнять до 15- 16-летнего возраста, пока не возникли нарушения ритма, легочная гипертензия и дистрофические изменения миокарда вследствие длительных перегрузок.
Медикаментозная терапия включает симптоматические средства: антиаритмические препараты при фибрилляции предсердий и паро-ксизмальной суправентрикулярной тахикардии, лечение застойной сердечной недостаточности.
Синдром Лютомбаше — дефект межпредсердной перегородки в сочетании со стенозом левого атриовентрикулярного отверстия.
Патологаческая анатомия. Морфологически характеризуется наличием дефекта межпредсердной перегородки и врожденного или приобретенного
288
Некоронарогенные болезни сердца
сужения левого атриовентрикулярного отверстия. Дефект межпредсердной перегородки при этом чаще всего вторичный и локализуется в области овальной ямки, как правило небольшой. Морфологические изменения митрального клапана разнообразны и отражают все стадии приобретенного и врожденного митрального стеноза. Характерным является расширение легочной артерии, которая иногда вдвое превышает размер аорты.
Гемодинамика. Сброс крови из левого предсердия в правое происходит так же, как при изолированном дефекте межпредсердной перегородки, величина шунта увеличивается пропорционально возрастанию стенозирующего дефекта митрального отверстия. В то же время сужение левого атриовентрикулярного отверстия приводит к нарушению оттока крови из малого круга и гипертензии в системе малого круга. Таким образом, синдром Лютамбаше обусловливает более выраженные нарушения гемодинамики в малом круге, в результате чего возникают гипертрофия и расширение правого желудочка и предсердия.
Клиника и диагностика. Клиническая картина зависит от того, какой из анатомических компонентов порока превалирует. Наиболее часто отмечаются следующие симптомы:
• бледность кожных покровов, часто акроцианоз,
• резкая одышка, быстрая утомляемость,
• частые приступы сердцебиений,
• головокружение,
• слабость,
• в анамнезе частый бронхит,
• прекардиальная и эпикардиальная пульсация,
• границы сердечной тупости смещены вправо, сердце занимает сре
динное положение,
• во втором - четвертом межреберье слева определяется «кошачье
мурлыканье», выслушивается грубый систолический шум,
• над легочной артерией выслушивается систолический и диасто-
лический шум (вследствие расширения легочной артерии).
На ЭКГ электрическая ось часто отклонена вправо, выражены признаки гипертрофии правых отделов сердца. Типичны высокие зубцы Р
,10
Некоронарогенные болезни сердца
в I и II стандартных отведениях, комплекс QRS уширен, часто двухфазный. Нередко выявляется мерцание предсердий.
На фонокардиограмме отмечаются элементы шума, обусловленного дефектом межпредсердной перегородки, а также пресистолический шум и раздвоение II тона, характерные для сужения левого атриовент-рикулярного отверстия.
На рентгенограмме — увеличенное шарообразное сердце, в передне-задней проекции выступают резко увеличенный ствол легочной артерии и ее основные ветви (усиленная пульсация, «пляска корней» при рентгеноскопии). Значительно расширено правое предсердие и гипертрофирован правый желудочек, усилен рисунок корней, определяется маленькая узкая дуга аорты.
При катетеризации сердца выявляется значительное повышение давления в правых отделах сердца и легочной артерии. Можно обнаружить повышение содержания кислорода в правом предсердии вследствие сброса крови слева направо.
Дифференциальную диагностику проводят с:
• дефектом межпредсердной перегородки,
• стенозом левого атриовентрикулярного отверстия ревматической
этиологии,
• сложным митральным пороком с преобладанием стеноза или не
достаточности.
Лечение. Хирургическое лечение заключается в одномоментной коррекции — ликвидации дефекта межпредсердной перегородки и митральной комиссуротомии. Противопоказаниями к операции служат лишь тяжелая стадия легочной гипертензии и резко выраженная дистрофия миокарда, обусловливающая терминальную стадию нарушения кровообращения.
Дата добавления: 2019-03-09; просмотров: 147; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!