По этиологическому и патогенетическому механизмам развития с позиции оптимального выбора лечения ( на основе номенклатуры и классификации ВОЗ ) 12 страница
 этиотропная терапия непосредственно не влияет на экссудативный и пролиферативный компоненты воспалительного процесса.
этиотропная терапия непосредственно не влияет на экссудативный и пролиферативный компоненты воспалительного процесса.
При аллергических и аутоиммунных формах перикардита ведущей является неспецифическая противовоспалительная терапия. При легком течении сухого перикардита (эпистенокардитический, уремический) проводят лечение основного заболевания, назначают диклофе-нак, нимесулид, мелоксикам и другие нестероидные противовоспалительные препараты.
Глюкокортикоиды назначают в случаях диссеминированной красной волчанки, ревматоидного артрита, ревматизма. Преднизолон в низких дозах (10- 15 мг) применяют также при аутоаллергических перикардитах у больных с инфарктом миокарда или после операций на сердце. Высокая эффективность терапии кортикостероидами позволяет предположить аутоиммунную природу процесса, однако не исключает его инфекционного генеза.
В комплексной терапии перикардита могут применяться препараты системной энзимотерапии.
При тяжелом течении экссудативного перикардита основной метод лечения — эвакуация жидкости из полости перикарда путем его пункции.
Показания к перикардиальной пункции:
• нарастающие симптомы тампонады сердца,
• подозрение на гнойный характер процесса,
• отсутствие тенденции к рассасыванию экссудата,
• уточнение этиологии заболевания.
При хроническом экссудативном перикардите наиболее эффективным является субтотальная перикардэктомия, выздоровление наступает у большинства оперированных больных.
При констриктивном перикардите консервативное лечение неэффективно. Констриктивный перикардит иногда проходит спонтанно, когда он развивается как осложнение острого перикардита. Однако учитывая полную бесперспективность консервативного лечения больных с констриктивным перикардитом и упорное прогрессирование заболевания, верифицированный диагноз является абсолютным пока-
Некоронарогенные болезни сердца
занием к хирургическоему лечению — удалению обоих листков спаянного перикарда. Тотальная перикардэктомия гораздо более трудна для исполнения, чем удаление части париетальной пластинки. При экс-цизии спаечно-измененного перикарда возникает риск кровоизлияния от перфораций стенки сердца, в ранний послеоперационный период венозное давление может остаться повышенным, но возвращается к норме в течение 3 мес после операции. Неадекватная длительность периода реконвалесценции после хирургического удаления перикарда может отражать наличие сопутствующей болезни миокарда.
Тампонаду сердца умеренной степени тяжести в некоторых случаях можно лечить консервативно, назначая мочегонные средства с одновременной терапией основного заболевания. Повышенное центральное венозное давление в большинстве случаев требует удаления жидкости из перикарда. Перикардиальная жидкость может быть удалена с помощью пункции (перикардиоцентез) или других хирургических методик (подмечевидная перикардиостомия, торакоскопическая пери-кардиостомия, торакотомия). Наиболее острые формы тампонады сердца типа гемоперикарда, обусловленного расслоением аорты, проникающей травмы сердца или разрыва стенки сердца при остром инфаркте миокарда требуют немедленного хирургического вмешательства.
Перикардиоцентез эффективен при большинстве подострых форм тампонады, например обусловленных идиопатическим или вирусным острым перикардитом, ревматизмом, диализом и новообразованием. Торакоскопия и торакотомия обычно применяются у пациентов с рецидивирующей тампонадой, которые подверглись вначале перикардиоцен-тезу или подмечевидной перикардиостомии, обычно при опухолях.
Перикардиоцентез имеет также диагностическое значение, когда положительные результаты микробиологических или цитологических исследований жидкости подтверждают наличие инфекции или новообразования.
106
Некоронарогенные болезни сердца
Глава 5. ЭНДОКАРДИТЫ
Инфекционный эндокардит — воспалительное заболевание эндокарда инфекционной этиологии, обусловленное инвазией возбудителя с его локализацией на клапанных структурах, эндокарде, эндотелии в зоне прилегающих к сердцу магистральных сосудов, сопровождающееся, как правило, бактериемией и поражением различных органов и систем организма.
Первое описание инфекционного эндокардита относится к 1646 г., когда L. Riviere указал на повреждение эндокарда при злокачественной лихорадке. Основоположником учения об инфекционном эндокардите считают Osier, который в 1885 г. подробно описал заболевание и высказал предположение о его инфекционной природе. Он считал возможным развитие первичного патологического процесса на неизмененных клапанах, вторичного — на фоне ревматизма, пневмонии, дифтерии и др. Термин «инфекционный эндокардит» впервые использовал S. Jaccoud в 1885 г.
В течение последних 10-15 лет отмечается увеличение заболеваемости инфекционным эндокардитом, что может быть обусловлено несколькими факторами:
• распространением операций, выполняемых на сердце, — появле
нием инфекционного эндокардита протезированного клапана;
• повышенной предрасположенностью к заболеванию при наличии:
• врожденных пороков сердца (в том числе двустворчатого аор
тального клапана),
• пролапса митрального клапана,
• приобретенных пороков сердца,
• гипертрофической обструктивной кардиомиопатии,
• операции на сердце без замены клапанов;
• постинъекционными абсцессами после введения различных лекар
ственных средств;
• широким использованием инвазивной инструментальной техни
ки (катетеров, искусственных водителей ритма сердца), вводимой
в сердце и сосуды;
W 7
Некоронарогенные болезни сердца
• появлением своеобразной формы — инфекционного эндокардита у наркоманов.
Инфекционный эндокардит может возникать в любом возрасте, до создания антибиотиков наиболее часто им заболевали лица среднего возраста, в последние десятилетия пик заболеваемости сместился к 50-летнему возрасту, в 5 раз увеличилось число заболевших в возрасте старше 60 лет. Мужчины болеют в 2 раза чаще, чем женщины.
Этиология. Инфекционный эндокардит — полиэтиологическое заболевание, потенциальными возбудителями которого могут быть до 128 разновидностей микроорганизмов. Основными среди них являются стрептококк и стафилококк, которые высеваются у 75- 90% больных.
Из всех штаммов стрептококка наиболее часто высевают зеленящий стрептококк. Факторами, способствующими его инвазии, являются тонзиллит, фарингит, манипуляции в полости рта (экстракция зубов), хирургические вмешательства. Удается выделить и другие штаммы стрептококка, в том числе условно-патогенные, являющиеся компонентами нормальной микрофлоры полости рта и кишечника. Прежде всего это энтерококк, вызывающий инфекционный эндокардит в 10-18% случаев. Ему чаще предшествует мочеполовая инфекция или заболевания пищеварительного тракта, у женщин — акушерские полостные операции, катетеризация мочевого пузыря, применение внутри-маточных контрацептивов.
Повышение этиологической роли стафилококка за последние 10— 15 лет объясняется широким внедрением в клиническую практику антибиотиков, а также распространением инвазивных процедур. Инфекционный эндокардит стафилококковой этиологии часто возникает после операций на сердце, имплантации эндокардиального электрода искусственного водителя ритма сердца, инвазивных инструментальных исследований (катетеризация полостей сердца), длительного применения внутривенных катетеров, хронического гемодиализа, гемосорбции, при наличии инфицированных и гнойных ран, абсцессов, пиодермии, а также у инъекционных наркоманов. У таких больных чаще высевается золотистый стафилококк, который вызывает за-
Некоронарогенные болезни сердца
 болевание с острым началом, поражает интактные клапаны, быстро приводя к их разрушению, эндокардит протекает с гектической лихорадкой и гнойно-септическими осложнениями.
болевание с острым началом, поражает интактные клапаны, быстро приводя к их разрушению, эндокардит протекает с гектической лихорадкой и гнойно-септическими осложнениями.
Пневмококковый эндокардит особенно часто диагностируется у больных после кардиохирургического вмешательства с имплантацией искусственных материалов, а также у пациентов, перенесших в послеоперационный период пневмонию.
Реже причиной инфекционного эндокардита являются коринебак-терии (дифтероиды) — грамположительные палочки, которые входят в состав микробной флоры верхних дыхательных путей. Заболевание отличается стертостью клинической симптоматики, может осложняться развитием миокардита, нефрита, васкулита.
Наблюдения последних лет свидетельствуют об увеличении удельного веса грамотрицательной микрофлоры в этиологии инфекционного эндокардита; эшерихий, протея, сальмонелл, синегнойной палочки, клебсиелл, которые являются причиной заболевания в 3-8% случаев. Потенциальным возбудителем является кишечная палочка, для которой характерно вторичное поражение эндокарда, практически не поддающееся антибактериальной терапии.
Инфекционный эндокардит вызывают также редко встречающиеся возбудители: серрации, морракселлы, иерсинии, акинетобактер, фла-вобактер, цитробактер, энтеробактер, кардиобактер. У наркоманов гра-мотрицательные бактерии вызывают заболевание в 5-64% случаев.
Возросла и частота эндокардита, вызванного грибами (1,5-6%), из возбудителей преобладают дрожжеподобные грибы. Грибковый эндокардит возникает у ослабленных больных, длительно получающих антибактериальную, глюкокортикоидную и цитостатическую терапию, в 5-14% случаев — у наркоманов.
В последнее время в возникновении инфекционного эндокардита возросла этиологическая роль анаэробной флоры, однако механизм повреждающего действия анаэробов на эндотелий не изучен. Предполагается, что повреждающая роль анаэробных бактерий реализуется только совместно с аэробными микроорганизмами. Эндокардит, вы-
 109
109
|
|
Некоронарогенные болезни сердца
 званный анаэробной микрофлорой, характеризуется выраженной манифестацией патологического процесса с развитием тромбофлебитов, высоким риском возникновения тромбоэмболии сосудов легких, сердца, головного мозга, рефрактерностью к традиционной антибиотико-терапии, высоким уровнем летальности (до 46%).
званный анаэробной микрофлорой, характеризуется выраженной манифестацией патологического процесса с развитием тромбофлебитов, высоким риском возникновения тромбоэмболии сосудов легких, сердца, головного мозга, рефрактерностью к традиционной антибиотико-терапии, высоким уровнем летальности (до 46%).
Далеко не всегда удается выделить возбудителя из крови больных инфекционным эндокардитом, поэтому во многих случаях истинный возбудитель болезни остается неизвестным. В 50-55% случаев в острый период и в 80- 85% случаев в подострый период посевы крови оказываются стерильными. Причинами, затрудняющими идентификацию возбудителя заболевания, являются предшествующая забору крови антибактериальная терапия, несовершенное бактериологическое оборудование для проведения посева, наличие в крови бактерий, требующих применения специальных сред (анаэробы, сателлиты и штаммы стрептококка с измененными свойствами (тиол- или витамин В6-зави-симые), L-формы бактерий, бруцеллы). Для выделения вирусов, рик-кетсий, хламидий, грибов требуются специальные методы.
Патологическая анатомия. Внутренняя оболочка сердца, или эндокард, выстилает все полости сердца, плотно сращена с подлежащим мышечным слоем, образована из коллагеновых и эластичных волокон, среди которых располагаются соединительнотканные и гладкомышеч-ные клетки. Со стороны полостей сердца эндокард покрыт эндотелием. На внутреннюю оболочку отходящих от сердца и впадающих в него сосудов— полых и легочных вен, аорты и легочного ствола— эндокард переходит без резких границ.
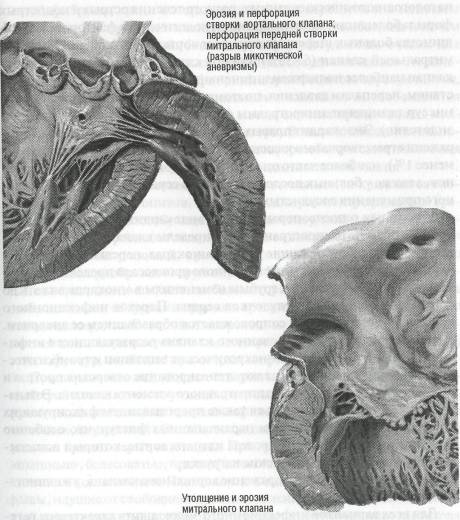
При эндокардите сердце увеличено, обычно преобладает гипертрофия левых отделов в связи с недостаточностью клапана аорты (рис. 8). В миокарде, помимо признаков воспаления, выявляют выраженные дистрофические и некробиотические поражения в виде базофильной и паренхиматозной дистрофии, атакже микромаляций и микроучастков глыбчатого распада мышечных волокон.
В вопросе о преимущественной локализации септического очага на клапанах сердца нет единого мнения ввиду различия клинических и
Некоронарогенные болезни сердца
 Рис. 8. Инфекционный эндокардит (по F. Netter, 1969, с изменениями)
Рис. 8. Инфекционный эндокардит (по F. Netter, 1969, с изменениями)
Некоронарогенные болезни сердца
 патологоанатомических данных, разного течения острых и подострых форм заболевания, многоообразия этиологических факторов. У большинства больных инфекция поражает аортальный клапан (28-45%) митральный клапан (5-36%) или оба клапана (до 35%). Аортальный клапан наиболее подвержен интенсивным гемодинамическим воздействиям, перепадам давления, поэтому по краям створок, в области ко-миссур возникают микротравмы (микрокровоизлияния, деструкция эндотелия). Эндокардит правых отделов сердца встречается реже (поражения трехстворчатого клапана — до 6%, клапана легочной артерии — менее 1 %), наиболее часто он наблюдается у инъекционных наркоманов, а также у больных после операции на сердце и в случаях длительного применения сосудистых катетеров.
патологоанатомических данных, разного течения острых и подострых форм заболевания, многоообразия этиологических факторов. У большинства больных инфекция поражает аортальный клапан (28-45%) митральный клапан (5-36%) или оба клапана (до 35%). Аортальный клапан наиболее подвержен интенсивным гемодинамическим воздействиям, перепадам давления, поэтому по краям створок, в области ко-миссур возникают микротравмы (микрокровоизлияния, деструкция эндотелия). Эндокардит правых отделов сердца встречается реже (поражения трехстворчатого клапана — до 6%, клапана легочной артерии — менее 1 %), наиболее часто он наблюдается у инъекционных наркоманов, а также у больных после операции на сердце и в случаях длительного применения сосудистых катетеров.
У больных с послеоперационным эндокардитом инфекционный процесс обычно распространяется за пределы клапана, поражая фиброзное кольцо, близлежащие участки миокарда, нередко и другие клапаны. Распространение инфекционного процесса за пределы фиброзного кольца может вести к грубым изменениям в миокарде вплоть до образования аневризм желудочков сердца. Переход инфекционного процесса на стенку аорты сопровождается образованием ее аневризм. При эндокардите протезированного клапана разрастающиеся инфицированные грануляционно-некротические вегетации и тромботичес-кие наслоения обычно вызывают стенозирование отверстия протеза и ограничение подвижности запирательного элемента клапана. Эти изменения могут сопровождаться также прорезыванием фиксирующих протез нитей и образованием параклапанных фистул, что особенно характерно для поражения протеза клапана аорты, который испытывает большие гемодинамические нагрузки.
У мужчин преобладает поражение аортального клапана, у женщин -митрального.
Для всех вариантов инфекционного эндокардита характерны вегетации, которые наиболее часто располагаются на створках клапанов и реже — на эндокарде желудочков или левого предсердия, а также на легочной или других артериях. Свежие вегетации состоят из тонких
 112
112
Некоронарогенные болезни сердца
нитей фибрина, среди которых выявляют эритроциты и в меньшем количестве — смешанно-клеточные лейкоциты, тромбоциты и почти всегда колонии бактерий. Очевидно, внутрисосудистым очагом для микроорганизмов в сердце и кровеносных сосудах являются стерильные вегетации, состоящие из фибрина и тромбоцитов, образующиеся, когда поврежденными эндотелиальными клетками высвобождается тканевой фактор. Тромботические массы сначала представляют мелкозернистые структуры, состоящие из тромбоцитов; позднее в них появляется примесь фибрина и лейкоцитов, тромботические наслоения организуются путем врастания в них соединительной ткани.
Микроорганизмы, колонизирующие вегетации, покрываются слоем фибрина и тромбоцитов, что не дает доступа нейтрофильным гра-нулоцитам, иммуноглобулинам и комплементу, таким образом позволяя патогенам противостоять защитным силам организма. Свежие вегетации имеют розовый, красный, желтый или зеленый цвет, но постепенно приобретают серую окраску. При грибковой инфекции клапанов вегетации достигают наибольших размеров, создавая опасность эмболизации и обтурации крупных артерий, что характерно для этого типа эндокардита. Вегетации митрального клапана могут распространяться вдоль хорд к вершине папиллярных мышц, приводя к разрыву этих структур, особенно при острых инфекциях.
При первичном эндокардите створки клапанов чаще тонкие, свободный край клапанов часто утолщен, что вызвано гемодинамическими нарушениями или воспалительной инфильтрацией. По свободному краю клапанов, внутренней оболочке восходящей части аорты располагаются рыхлые красно-серые вегетации. При грибковой инфекции вегетации «пышные», белесоватые, при стафилококковой — с выраженным некротическим компонентом. Чаще в аортальных клапанах наблюдаются надрывы, идущие от свободного края изъязвления, край створок бахромчатый, имеются разрывы створок поперечного и лентовидного характера. Сухожильные хорды тонкие, могут отмечаться их разрывы в области прикрепления к створкам и сосочковым мышцам, а также в центре хорд с явлениями острого некроза. На обрывках сухожильных хорд обнаружи-
 т
т
Некоронарогенные болезни сердца
 ваются вегетации. При подостром процессе наряду со свежими имеются вегетации, покрытые фиброзной капсулой, частично или полностью обызвествленные, нередко на ножке, часто организованные вегетации полностью кальцинированы. Элементы свежей деструкции створок сочетаются с перфорациями, имеющими фиброзные края. Характерно наличие фиброзных утолщений разорванных хорд. Нередко в крае разрыва видны кальциевые массы.
ваются вегетации. При подостром процессе наряду со свежими имеются вегетации, покрытые фиброзной капсулой, частично или полностью обызвествленные, нередко на ножке, часто организованные вегетации полностью кальцинированы. Элементы свежей деструкции створок сочетаются с перфорациями, имеющими фиброзные края. Характерно наличие фиброзных утолщений разорванных хорд. Нередко в крае разрыва видны кальциевые массы.
При вторичном эндокардите, когда инфекционный процесс поражает уже измененный клапан, свежие вегетации располагаются на фиброзно-измененных или кальцинированных створках, возможен отрыв хорд.
В неактивной стадии инфекционного эндокардита (стадии заживления) видны старые перфорации и разрывы створок с фиброзными краями. Вегетации представлены фиброзными бугорками или полностью кальцинированы.
При инфекционном эндокардите в связи с септикопиемией происходят многообразные вторичные дистрофические и интоксикационные изменения всех жизненно важных органов. На коже обнаруживаются множественные петехии. Селезенка увеличенная, дряблая, с большим соскобом пульпы. При микроскопическом исследовании обнаруживается инфильтрация нейтрофильными гранул оцитами, гиперплазия ретикулярных клеток, лимфатические фолликулы без четких контуров, аргирофильная строма находится в состоянии расплавления. В печени преобладают циркуляторные и дистрофические изменения. В почках обнаруживаются микроабсцессы и инфаркты различной величины.
Патогенез. Вопросы патогенеза инфекционного эндокардита сложны и окончательно не выяснены. В большинстве случаев в анамнезе имеются указания на порок сердца, атеросклероз, операции на сердце, которые предрасполагают к избирательной адгезии микроорганизмов на эндокарде. При первичном инфекционном эндокардите инфекция поражает здоровые клапаны. Однако и в этих случаях имеются микроструктурные повреждения эндокарда, являющиеся следствием ряда состояний, сопровож-
 П4
П4
Некоронарогенные болезни сердца
дающихся функциональными перегрузками сердца, во время которых усиленная работа клапанов, особенно в местах соприкосновения створок у комиссур при усиленном их захлопывании, вызывает механическую деструкцию эндотелия. Возникновение эндокардита, по-видимому, следует рассматривать как результат микроструктурных изменений в эндокарде под влиянием функциональных гемодинамических перегрузок. Эти причины в той или иной степени объясняют появление наиболее уязвимого места в эндокарде как местного фактора, обусловливающего данную локализацию инвазии возбудителя.
Дата добавления: 2019-03-09; просмотров: 127; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!