ЭТИОЛОГИЯ И ПАТОГЕНЕЗ ДВС-СИНДРОМА
Синдром диссеминированного внутрисосудистого свёртывания является неспецифическим синдромом, развивающимся как осложнение основного заболевания - индуктора, при котором в силу каких-либо обстоятельств активируется система коагуляции. Для ДВС-синдрома характерны следующие патогенетические механизмы:
• активация свёртывающей системы крови эндогенными факторами (тканевым тромбопластином, протеазами лейкоцитов, опухолевыми прокоагулянтами). На всех стадиях ДВС, даже в фазу выраженной кровоточивости, в крови циркулирует значительное количество активированных факторов свёртывания крови, что вызывает необходимость введения антикоагулянтов. Характерна тромбинемия и появление маркёров тромбинемии - растворимых фибринмономерных комплексов, D-димеров фибриногена;
• активация тромбоцитарного звена гемостаза за счёт поступления в русло тканевого тромбопластина, тромбоксана А2, приводящая к развитию сладжсиндрома. С целью деблокады микроциркуляторного русла показано применение препаратов реологического и антиагрегантного действия;
• истощение противосвёртывающих механизмов - дефицит естественных антикоагулянтов: антитромбина III, протеинов С и S, плазминогена, фибринолитической и кинин-калликреиновой систем и повышением содержания тромбомодулина (свидетельствует о повреждении сосудистой стенки).
Восполнить дефицит АТ III возможно за счёт трансфузии донорской плазмы, введения препаратов АТ III;
|
|
|
• истощение ретикулоэндотелиальной системы, системы мононуклеарных фагоцитов, что приводит к накоплению в кровотоке БАВ, активированных факторов свёртывания, поврежденных тромбоцитов, эритроцитов, микросгустков. Применение методов экстракорпоральной гемокоррекции позволяет компенсировать недостаточность системы естественной детоксикации организма;
• снижение противосвёртывающего потенциала эндотелия за счёт его качественного дефекта, поэтому оправдано введение препаратов, обладающих вазопротекторным эффектом.
Ниже приведён список патологий, потенциально опасных в плане развития ДВС-синдрома.
✧ Инфекция - бактериальный сепсис (Meningococcus, Escherichia coli, Salmonella, Pseudomonas, Pneumococcus, Staphylococcus), постспленэктомический синдром, молниеносная форма пневмококкового сепсиса, тяжёлые вирусные инфекции (лихорадка Денге, лихорадка Эбола, генерализованный герпес, ВИЧ), протозойные инфекции (малярия), лихорадка скалистых гор, кандидоз, аспергиллёз, клостридиоз, диссеминированные формы туберкулёза.
✧ Шок различной этиологии - анафилактический, септический, травматический, кардиогенный, ожоговый и др.
✧ Острый внутрисосудистый гемолиз, вызванный трансфузиями несовместимой крови, отравлениями гемолитическими ядами.
|
|
|
✧Онкологические заболевания - особенно диссеминированные формы рака, солидные опухоли, острые лейкозы, бластные кризы хронических лейкозов, синдром повышенной вязкости крови (полиглобулии, парапротеинемии).
✧ Хирургическая травма - травматичные хирургические вмешательства, трансплантация органов, тканей, сосудистое и клапанное протезирование, использование аппаратов искусственного кровообращения и исскуственной почки, аппарата вспомогательного кровообращения (внутриаортальная контрпульсация). Риск развития ДВС возрастает с ростом травматичности хирургического вмешательства и при наличии сопутствующей патологии, предрасполагающей к развитию ДВС (онкологических заболеваний, хронической сердечнососудистой патологии).
✧ Патология сердечно-сосудистой системы - острый инфаркт миокарда, врождённые и приобретённые пороки сердца, бивентрикулярная сердечная недостаточность, тромбозы глубоких вен, тромбоэмболия лёгочной артерии, аневризмы аорты, опухоли сердца, злокачественная гипертония, гигантские гемангиомы, телеангиоэктазии.
✧ Острые и хронические воспалительные, деструктивные заболевания лёгких, поджелудочной железы, печени, почек.
|
|
|
✧ Травмы: переломы трубчатых костей, жировая эмболия, травматический шок, ожоги, отморожения, электротравмы, обширные ожоги, crush-синдром и др.
✧ Акушерская патология - эмболия околоплодными водами, преждевременная отслойка плаценты, атонические маточные кровотечения, антенатальная гибель плода, плодоразрушающие операции, септический аборт, тяжёлый поздний токсикоз беременности, эклампсия. Гинекологическая патология - гигантские миомы матки, дегенеративные фибромиомы.
✧ Массивные гемотрансфузии и реинфузии крови.
✧ Иммунные патологии - СКВ, ревматоидный полиартрит, болезнь Шенлейн-Геноха, диффузный гломерулонефрит, криоглобулинемия, васкулиты и коллагенозы; тяжёлые аллергические реакции, гепарин-индуцированная тромбоцитопения, болезнь Кавасаки, саркоидоз, амилоидоз, гемолитико-уремический синдром.
✧ Отравление гемокоагулирующими ядами.
✧ Трансплантация органов и тканей.
✧ ДВС-синдром новорождённых: инфекции, родовая асфиксия, болезнь гиалиновых мембран, аспирационный синдром, ателектазы, полицитемия, переохлаждение, тромбоз крупных сосудов, фулминантная пурпура (врождённый дефицит протеинов C и S), некротизирующий энтероколит, гигантские гемангиомы, повреждение головного мозга ишемического и геморрагического характера, врождённая патология печени, почек. ✧ Терминальное состояние, остановка сердца, асфиксия, гипоксия, реанимационные мероприятия (в 100% случаев). Таким образом, можно утверждать, что ДВС-синдром сопутствует или осложняет большинство тяжёлых заболеваний и терминальных состояний. Необходимо особо отметить, что в подавляющем большинстве случаев диагностика многих из приведённых заболеваний означает, что ДВС-синдром либо уже спровоцирован, либо может
|
|
|
развиться, если не начать профилактические мероприятия (Макеев И.Н., 1998).
Перечень заболеваний и состояний, которые часто осложняет ДВС-синдром (по Воробьёву А.И. и др., 1994, с дополнениями): ✧ Аборт. ✧ Амилоидоз. ✧ Ангиопластика.
✧ Синдром Казабаха-Мерритт (множественные и гигантские ангиомы).
✧ Аневризмы грудного отдела аорты (восходящего, нисходящего отделов, дуги аорты), расслаивающие аневризмы грудного, брюшного отделов аорты.
✧ Синдром Такаясу.
✧ Ацидоз, гипоксия.
✧ Вирусные инфекции (герпес, краснуха, оспа, цитомегаловирус-
ная инфекция). ✧ Внематочная беременность. ✧ Внутрисосудистый гемолиз. ✧ Внутриутробная смерть плода. ✧ Врождённые пороки сердца. ✧ Гемолитический уремический синдром. ✧ Гемоперфузия на угольных фильтрах. ✧ Геморрагическая лихорадка. ✧ Гиперлипидемия. ✧ Гистиоцитоз.
✧ Глистная инвазия (кара-азар).
✧ Дефицит фермента глюкоза-6-фосфатдегидрогеназы (провоцированный гемолиз). ✧ Жировая эмболия.
✧ Злокачественные солидные новообразования различных локализаций.
✧ Иммунокомплексные заболевания (васкулиты).
✧ Инфаркт миокарда.
✧ Карциноид, нейробластома.
✧ Кесарево сечение.
✧ Коарктация аорты.
✧ Конфликт матери и плода по системам АВО и Rh.
✧ Малярия.
✧ Массивные кровотечения при хирургических операциях.
✧ Массивные поражения тканей (crush-синдром).
✧ Острые и хронические заболевания печени.
✧ Острый панкреатит.
✧ Осложнения родов (поздний гестоз, преждевременная отслойка нормально расположенной плаценты, внутриутробная гибель плода, эклампсия).
✧ Острый промиелоцитарный лейкоз.
✧ Отравления и интоксикации (змеиным ядом, лекарственными
средствами).
✧ Преждевременная отслойка плаценты.
✧ Переливание несовместимой крови.
✧ Рабдомиолиз.
✧ Рабдомиосаркома.
✧ Рестернотомия.
✧ Сепсис.
✧ Септический аборт.
✧ Серповидноклеточная анемия (криз).
✧ Синдром гомологичной крови.
✧ Травматичные хирургические операции.
✧ Трансплантация органов и тканей, костного мозга.
✧ Тромбоэмболии лёгочной артерии.
✧ Хронический мегакариоцитарный лейкоз.
✧ Шок (травматический, геморрагический, ожоговый, анафилактический, септический). ✧ Эклампсия. ✧ Эксикоз.
✧ Эмболия околоплодными водами. ✧ Эритремия.
Локализация, объём, тяжесть травматизации тканей, а также наличие осложняющего течение заболевания шока - наиболее важные факторы, предрасполагающие к возникновению ДВС-синдрома. Частота ДВС, осложняющего течение политравмы, достигает 30%; при этом смертность составляет около 70% всех случаев диагностированного ДВС-синдрома (Counts R.B., Haisch C., Simon T.L., 1979).
Частота диагностики клинически значимого ДВС-синдрома существенно варьирует и составляет:
• при онкологических заболеваниях до 33,8% (в случаях солидных опухолей), 12,7% - при гемобластозах;
• при патологии аорты и магистральных сосудов, соединительнотканной дисплазии, приводящей к расслоению аорты, - 10,8%;
• при инфекционных заболеваниях - до 6,4%;
• при заболеваниях печени - 2,9%;
• при акушерской патологии - 2,5%.
Установлено, что инфекции и септицемия служат основными причинами ДВС-синдрома; они составляют более 50% всех диагностированных случаев ДВС-синдрома.
Превалирующие клинические симптомы ДВС-синдрома при различных патологиях:
• полиорганная недостаточность - наиболее характерна для ДВС при инфекционных заболеваниях, сепсисе (диагностируют у 77% больных), при онкологических заболеваниях (у 33% больных);
• кровоточивость, которая сопровождает ДВС-синдром при акушерской патологии в 100% случаев, от 30 до 50% случаев диагностированного ДВС-синдрома, осложняющего течение заболеваний печени, онкологических заболеваний (гемабластозов, солидных опухолей) (Spiess B.D., Spence R., 2006).
В развитии ДВС-синдрома ведущая роль принадлежит:
• первичному поражению эндотелия сосудов;
• тромбопластическим веществам, попадающим в кровь;
• первичному поражению тромбоцитов.
В результате этих механизмов (как каждого в отдельности, так и в различных комбинациях) происходит процесс множественного микросвёртывания с тромбозами, развитие коагулопатии потребления с последующей активацией фибринолиза. ДВС-синдром классифицируют по патогенетическому, этиологическому и клиническому признакам.
Ниже представлена детализированная классификация тромбогеморрагических синдромов, предложенная М.С. Мачабели (1970, 1981) (Цит. по: Мокеев И.Н., 1998).
В патогенетической классификации выделяют следующие стадии в развитии ДВС-синдрома:
• I стадия - гиперкоагуляция и тромбообразование (характеризуется поступлением в кровоток тромбопластина);
• II стадия - нарастающая коагулопатия потребления с компенсаторным усилением фибринолитической активности;
• III стадия - дефибринационно-фибринолитическая (характеризуется глубокой гипокоагуляцией, вплоть до полной несвёртываемости крови и выраженной тромбоцитопении);
• IV стадия - восстановительная, или стадия остаточных тромбозов и микроциркуляторных нарушений органов-мишеней (характеризуется восстановлением фибриногена и других факторов свёртывания крови).
В этиологической классификации выделяют: ✧ ДВС-синдром с преобладанием активации системы гемостаза по внешнему звену вследствие поступления тромбопластина в кровоток при тяжелой сочетанной травме, травматичной операции.
• Введение извне тканевого тромбопластина.
• Введение извне тромбина.
• Хирургические вмешательства: операции на сердце, лёгких, простате, поджелудочной железе, матке.
• Тромбофилии (врождённые и приобретённые).
• Акушерская патология.
• Ожоги.
• Кровопотеря.
• Геморрагический и травматический шок.
• Метастатический рак: рак поджелудочной железы, рак простаты.
• Отравление ядами некоторых видов змей.
• Внезапная смерть.
• Мезентериальный тромбоз с геморрагическими проявлениями.
• Геморрагические инфаркты.
• Тромбоз лёгочной артерии.
• Гипоксия.
✧ ДВС-синдром с преобладанием активации системы гемостаза по внутреннему каскаду вследствие появления в кровотоке клеточно-тромбоцитарного, эритроцитарного, лейкоцитарного тромбопластина.
• Хронические лейкозы.
• Эритремия.
• Тромбоцитемии, сопровождающие другие заболевания, а также состояния после спленэктомии.
• Гемолитическая анемия.
• Переливание несовместимой крови.
• Пароксизмальная ночная гемоглобинурия.
• Гемолитический шок.
• Гемолитический уремический синдром.
• Отравление ядами некоторых видов змей.
✧ ДВС-синдром при острых и хронических васкулитах.
• Патологические состояния, при которых есть условия для поступления в кровоток бактерий.
♦ Феномен Санарелли-Здродовского.
♦ Феномен Швартцмана.
♦ Септический аборт.
♦ Дифтерия.
♦ Дизентерия.
♦ Тонзиллит.
♦ Менингококковый сепсис.
♦ Гастроэнтериты.
♦ Кумариновый некроз.
• Аллергические реакции.
♦ Феномен Артюса.
♦ Болезнь Мошкович - тромбоцитопеническая пурпура.
♦ Болезнь Шенлейна-Геноха.
♦ Анафилактические реакции.
ДВС возникает при условии мощной активации системы гемостаза, при этом активность гемокоагуляции значительно превышает возможность антитромботических механизмов контроля над свёртываемостью.
Основные механизмы активации системы гемостаза при ДВСсиндроме представлены следующим образом.
• Интенсивное высвобождение тканевого субстрата. Тканевой фактор находится на поверхности большинства клеток, максимальное его количество на поверхности эпителиальных и глиальных клеток. Клетки эндотелия сосудов, моноциты в норме не содержат тканевой фактор, но в ответ на патологическую стимуляцию эндотоксинами, фактором некроза опухоли, интерлейкином-1 происходит массивный выброс тканевого фактора из субэндотелия в сосудистое русло и активация гемостаза. Примером реализации этого механизма активации гемокоагуляции могут служить:
♦ «классический» акушерский тромбогеморрагический синдром, когда из матки в кровоток интенсивно поступают тромбопластические вещества;
♦ травматичные хирургические вмешательства, особенно на паренхиматозных органах;
♦ сепсис, септический шок, сопровождающийся выходом протеаз;
♦ реинфузия аутокрови, излившейся в рану во время операции (она содержит не только микроагрегаты клеток, но и тканевой фактор, концентрация которого пропорциональна степени травматичности операции).
• Контактная активация гемостаза: внутренний механизм и тромбоцитарное звено гемостаза активируются при контакте с «чужеродными» поверхностями, например при циркуляции крови в аппарате искусственного кровообращения, во время гемодиализа, гемодиаультрафильтрации, при контакте с искусственным клапаном сердца, сосудистым протезом, атеросклеротической бляшкой. Вероятность развития ДВС зависит от количества крови, проходящей через аппарат, от времени контакта крови с «чужеродной» поверхностью и от качества (степени тромбогенности) материала, из которого изготовлен сосудистый протез, магистрали аппарата.
• Чрезмерная активация гемокоагуляции, которая бывает при большинстве онкологических заболеваний (вырабатываются неопластические прокоагулянтные факторы), панкреатите (в кровеносное русло попадает большое количество протеолитических ферментов), при укусах ядовитых змей, приводящая к синтезу гемокоагулирующих протеаз.
• Дефицит антикоагуляционных механизмов вследствие врождённого или приобретённого дефицита естественных антикоагулянтов. Врождённый дефицит АТ III (менее 70% от нормы) приводит к тромбозам глубоких вен, ТЭЛА. Приобретённый дефицит АТ III появляется вследствие повышенного его потребления: при длительном применении больших доз гепарина натрия (гепарин♠) (более 20 000 ЕД в сутки), при постоянной активации свёртывающей системы (беременность, хронические заболевания).
Всю схему развития ДВС-синдрома можно представить в виде следующей последовательности патофизиологических процессов
(рис. 9, 10).
Большое значение в формировании ДВС имеют скорость кровотока и агрегация клеток крови (сладж-синдром), особенно в зоне микроциркуляции. Длительное сладжирование приводит к освобождению

Рис. 9. Патогенез ДВС-синдрома
клеточных тромбопластических веществ, нарушению микроциркуляции, перфузии, ацидозу, повреждению энтотелия и субэндотелия, выходу тканевого фактора и развитию микротромбирования. Это бывает при шоке, сопровождающемся падением сердечного выброса, полиглобулиях, тромбоцитозах. Клиническая классификация ДВС:
• острый (вплоть до молниеносного);
• подострый;
• хронический;
• рецидивирующий;
• латентный.
Молниеносная форма ДВС с массивными кровотечениями характерна для акушерской патологии, гемолитического посттрансфузи-
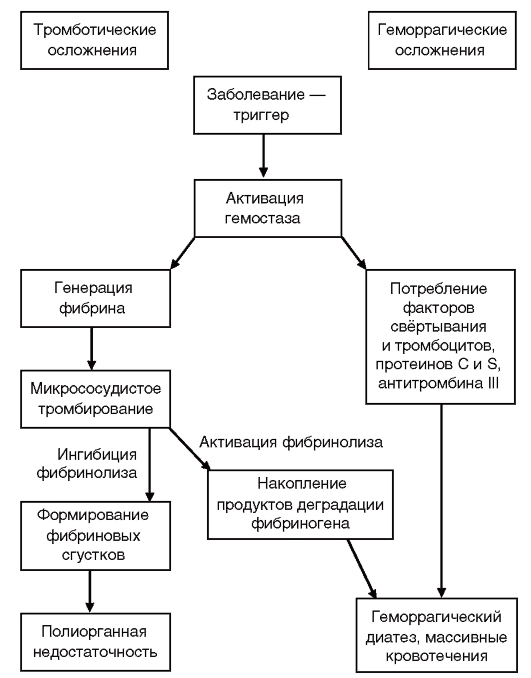
Рис. 10. Схема развития ДВС-синдрома
онного осложнения. Особенность молниеносного ДВС-синдрома - минимальный срок его развития. Кровоточивость при молниеносном ДВС носит неуправляемый, жизнеугрожающий характер, проявляется профузными маточными кровотечениями, кровотечениями из желудочно-кишечного тракта, операционной раны. Для острой формы ДВС характерны диффузная кровоточивость из операционной раны, носовые, десневые, инъекционные кровотечения, позже появляются кровотечения из органов желудочно-кишечного тракта, возможны обширные внутренние гематомы.
Острый ДВС-синдром бывает при интенсивной, длительной активации свёртывающей системы крови, при этом острота и выраженность синдрома зависят от тяжести заболевания-триггера. При остром ДВС довольно быстро развивается мультифакторный дефицит гемостаза. Таким образом, ДВС проявляется преимущественно коагулопатией потребления, поэтому появление признаков кровоточивости - зачастую наиболее ранний симптом начинающегося ДВС. Однако основные клинические проявления ДВС-синдрома определяют выраженные микротромбоэмболические поражения органов и тканей, которые становятся причиной развития полиорганной дисфункции или недостаточности. ДВС острого течения характерен для сепсиса, травматичных хирургических вмешательств, crush-синдрома, массивных гемотрансфузий, распада опухоли, при применении бактерицидных антибиотиков. Продолжительность развития острого ДВС-синдрома от нескольких часов до нескольких суток.
Подострое течение ДВС бывает при аутоиммунных заболеваниях (СКВ, аутоиммунный геморрагический васкулит), хронических инфекциях. Длительность подострого синдрома - от нескольких недель до месяцев, характеризуется менее выраженными, чем при остром течении, клиническими проявлениями с преобладанием микроциркуляторных нарушений органов.
Хроническая форма ДВС сопровождает тяжёлую терапевтическую патологию в течение нескольких лет - хроническую сердечно-сосудистую недостаточность, ИБС, лёгочное сердце, гипертоническую болезнь, сахарный диабет, диабетическую ангиопатию, хронический пиелонефрит и гломерулонефрит. Кроме этих патологий, причинами хронического, затяжного синдрома могут быть следующие патологии: хрониосепсис, в том числе септический эндокардит, хронические вирусные заболевания (гепатиты, ВИЧ), иммунное и иммуннокомплексное лечение. На начальных стадиях заболевания, как правило, хронический ДВС-синдром бессимптомен, в ряде случаев его диагностируют преимущественно на основе лабораторных показателей. Нарастание симптоматики происходит при прогрессировании заболевания, спровоцировавшего этот процесс.
Необходимо отметить однотипность микроциркуляторных изменений при различных формах ДВС - блокада микроциркуляции определяет тяжесть состояния больных, характер осложнений и
исход болезни. Наиболее тяжело поражаются органы с развитой капиллярной сетью: лёгкие, почки, печень, головной мозг, надпочечники. На аутопсии в органах находят ишемические и геморрагические инфаркты, множественные кровоизлияния. При гистологическом исследовании выявляют стаз и микроагрегаты форменных элементов крови, экстравазаты, множественные отложения фибрина внутри сосудов и под эндотелием (Зербино Д.Д., Лукасевич Л.Л., 1982).
При хроническом течении ДВС тромбоцитарное звено гемостаза находится в состоянии активности; в органах-мишенях постоянно образуются тромбоцитарные агрегаты, происходит разрастание соединительной ткани, развиваются склеротические изменения в органах, что приводит к потере их функциональной способности.
На основании лабораторных, клинических признаков диссеминированное внутрисосудистое свёртывание крови условно делят на три стадии (Лычёв В.Г., 1998) (рис. 11).
• I стадия - гиперкоагуляция. Эта стадия кратковременна при молниеносном и остром течении ДВС и быстро переходит в стадию гипокоагуляции вследствие истощения гемостатических механизмов и максимальной компенсаторной активизации фибринолиза.
• II стадия - нормокоагуляция. Период нормокоагуляции очень кратковременный, характеризуется субкомпенсацией гемостаза и отсутствием признаков кровоточивости.

Рис. 11. Стадии ДВС-синдрома
• III стадия - гипокоагуляция, причина которой - это мультифакторная недостаточность гемостаза, развивающаяся вследствие повышенного потребления факторов при диссеминированном свёртывании крови.
I стадия ДВС (гиперкоагуляционная фаза) характеризуется гиперкоагуляцией и повышенной агрегацией тромбоцитов. Длительность стадии зависит от остроты и тяжести основного заболевания. Характерное проявление этой стадии - мгновенное свёртывание крови в игле или пробирке.
На этой стадии вследствие микротромбирования возникает блокада микроциркуляции. В ответ на микротромбообразование резко активируется фибринолиз, что можно зарегистрировать посредством следующих лабораторных тестов (табл. 5). При интенсивной активации коагуляции тромбоциты находятся в активированном состоянии, контактируют друг с другом, сладжируются, выделяют в кровь тромбоцитарные факторы. Постепенно количество тромбоцитов уменьшается, истощается система физиологических антикоагулянтов.

Для II стадии ДВС (фаза нормокоагуляции) характерна нарастающая коагулопатия потребления и тромбоцитопения. Лабораторные тесты нередко подтверждают наличие нормокоагуляции, которая возможна вследствие сочетания повышения коагуляции и начинающейся коагулопатии потребления (в первую очередь истощаются плазменные факторы свёртывания - фибриноген, протромбин). Снижается содержание AT III, что связано с потреблением его на
инактивацию тромбина и активированных факторов свёртывания. Снижение АТ III ниже 70-75% - фактор тромбогенности, который отражает тяжесть ДВС. На II стадии бывают повышенная кровоточивость, кровоизлияния на коже, слизистых.
При острой форме ДВС I и II стадии носят кратковременный характер и быстро переходят в III стадию.
III стадии (гипокоагуляционная фаза) свойственны выраженная гипокоагуляция и коагулопатия потребления. В первые стадии ДВС происходит выработка значительного количества тромбина, вследствие чего резко возрастает содержание фибрин-мономеров. Максимально активируется фибринолиз, часть плазмина расщепляет фибриноген и другие нестабилизированные продукты превращения фибрина (в том числе фибрин-мономеры и их комплексы с фибриногеном). Это приводит к накоплению продуктов деградации фибриногена. Часть ПДФ поглощают макрофаги, однако большая часть ПДФ остаётся в сосудистом русле, формируя растворимые фибрин-мономерные комплексы (РКФМ). На РКФМ тромбин не оказывает свёртывающего действия - развивается гипокоагуляция. Таким образом, в крови больного находится ещё достаточное количество активизированных факторов свёртывания крови, в том числе тромбина, но коагуляция не происходит из-за блокирования перехода фибриногена в фибрин продуктами паракоагуляции. Это состояние иногда ошибочно называют афибриногенемией. Повышение содержания ПДФ и D-димеров фибриногена - наиболее надёжный диагностический признак ДВС-синдрома (Мелкумян А.Л., 2001).
На этом этапе происходит истощение системы фибринолиза, образующиеся микросгустки не подвергаются лизированию. Клинически это проявляется «неудержимой» кровоточивостью и развитием вследствие блокады микроциркуляции полиорганной недостаточности. Возникает тромбоцитопения потребления: большая часть тромбоцитов уходит в микросгустки. Отмечают также тромбоцитопатию, т.е. нарушение функции тромбоцитов, развивающееся вследствие ингибирования агрегации тромбоцитов продуктами паракоагуляции.
III стадия является критической даже при адекватном медикаментозном и хирургическом лечении основного заболевания. Благоприятный исход возможен лишь в 30-40% случаев. Длительность реконваленсценции зависит от степени тяжести поражения органов-мишеней (Баркаган З.С., 1988).
ДВС иногда сопровождается внутрисосудистым гемолизом, который усугубляет геморрагическую анемию. Гемолиз обусловлен тем, что эритроциты, потерявшие способность к деформации, при прохождении по микроциркуляторному руслу фрагментируются нитями фибрина, образующимися вследствие внутрисосудистого свертывания на фоне снижения перфузии. При этом происходит механическое повреждение эритроцитов, приводящее, в свою очередь, к нарушению целостности мембран клеток, выходу внутриклеточного содержимого в плазму, что лабораторно подтверждается наличием свободного гемоглобина в плазме крови пациентов.
При хроническом ДВС активация свёртывания носит менее выраженный характер, что подтверждают умеренные изменения лабораторных показателей:
• ПДФ - незначительное повышение;
• количество тромбоцитов - в норме или повышено;
• агрегация тромбоцитов - снижение (вследствие тромбоцитопатии);
• АТ III - умеренное снижение;
• фибриноген - повышение.
Микроциркуляторные нарушения при хронических формах ДВС играют значительную роль в прогрессировании основного заболевания, при этом нарушаются репаративные процессы, развиваются склеротические изменения органов-мишеней.
Начальная диагностика основана на анализе клинико-лабораторных признаков, позволяющих предположить наличие ДВСсиндрома:
• заболевание-триггер;
• удлинение АЧТВ;
• тромбоцитопения;
• клиника кровоточивости.
Лабораторную диагностику ДВС делят на два этапа.
I этап, минимальная диагностика: ориентировочные лабораторные тесты (к ним относят вышеуказанные методики, доступные всем лечебным учреждениям). Кратность проведения мониторинга не реже 1 раза в 4 ч, при необходимости - чаще (табл. 6).
II этап, максимальная диагностика: подтверждающие лабораторные тесты, проведение которых требует значительного времени и соответствующего оснащения клинических специализированных лабораторий. Диагностику, основанную на проведении соответ-
Таблица 6. Лабораторная диагностика ДВС-синдрома

твующих методик, нередко проводят с большим запозданием, что существенно сказывается на качестве и своевременности лечения. К этим методам относят исследования агрегационных свойств тромбоцитов, определение толерантности плазмы к гепарину, времени эуглобулинового лизиса сгустка, ХПа-зависимого фибринолиза, определение содержания тромбин-антитромбинового комплекса (ТАТ), плазмин-антиплазминового комплекса (ПАП), D-димера.
D-димер - продукт расщепления фибрина, увеличение содержания которого свидетельствует об активации свёртывания и компенсаторного фибринолиза. Тест имеет довольно значительную достоверность в диагностике ДВС-синдрома.
Тромбин-антитромбиновый комплекс (ТАТ) является комплексом тромбина и антитромбина III, избыточное количество которого образуется в результате активации свёртывания крови, характерного для диссеминированного внутрисосудистого свёртывания
крови (ДВС).
Плазмин-антиплазминовый комплекс (ПАП). Динамика этого показателя отображает образование плазмина и, соответственно, активность фибринолитических процессов при ДВС-синдроме.
Растворимые фибрин-мономерные комплексы (РФМК) - это продукт распада фибриногена; в норме отсутствуют, существенно повышаются при ДВС-синдроме.
Тромбомодулин является белком клеточной мембраны эндотелиоцитов, маркёром повреждения эндотелия, субэндотелия; повы-
шение содержания тромбомодулина свидетельствует о степени эндотелиального, тканевого повреждения; маркёр ДВС-синдрома.
Зачастую клинические проявления синдрома появляются значительно раньше лабораторных маркёров активации системы гемостаза; таким образом, в диагностике ДВС важнейшую роль отводят наличию заболевания-триггера, ассоциированного с этим серьёзным осложнением.
Основные лабораторные маркеры синдрома - это персистирующая тромбинемия, нарастание содержания в плазме растворимого фибрина и РФМК, прогрессирование клеточных маркёров ДВС, фрагментированных эритроцитов, спонтанной агрегации тромбоцитов и тромбоцитопения, а также снижение уровня физиологических антикоагулянтов - АТ, протеина С и плазминогена (Баркаган З.С., Момот А.П., 2005).
Лабораторный мониторинг позволяет не только установить диагноз ДВС, но и его стадию, форму, а также осуществить контроль эффективности лечения заболевания-триггера и ДВС.
Дата добавления: 2018-11-24; просмотров: 563; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
