Схема 1. Гормональное воздействие
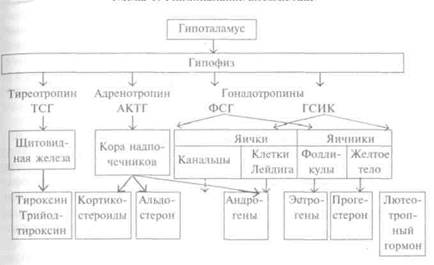
Гипоталамус является связующим звеном между эндокринной и центральной нервной системами и играет важную роль в вегетативной и нейрогуморальной регуляции. В области супра-оптических и паравентрикулярных ядер образуются так'называемые нейрогипофизарные гормоны. Кроме того, в гипоталамусе вырабатываются нейросекреторные гормоны, так называемые ре-лизинг-факторы, — пусковые механизмы, регулирующие деятельность передней доли гипофиза. Фактор, способствующий выделению адренокортикотропного гормона (АКТГ), выделяется в сером бугре и ядрах мамиллярных тел в гипоталамической области большого мозга. Предполагается, что фактор, высвобождающий гонадотропины и тиреотропины, локализуется в сером бугре и в области перекреста зрительных нервов. Секреция гипоталамуса может оказывать воздействие не только через гипофиз, но и непосредственно на эндокринную железу [например, адрено-гломерулотропин, который, по-видимому, контролирует секрецию альдостерона путем воздействия на кору надпочечников или путем прямого влияния на исполнительный орган (например, антидиуретический гормон — АДГ) оказывает прямое влияние на дистальную часть почечных канальцев]. Некоторые функции,
71



 наоборот, обеспечиваются несколькими механизмами. Гипоталамус является в то же время органом, воспринимающим импульсы и анализирующим информацию, поступающую из различных частей тела. Кроме того, гипофиз на основе механизма обратной связи позволяет поддерживать на высшем уровне регуляцию постоянства внутренней среды. В гипоталамусе вырабатываются нейроамины, специальные активные соединения, предшественниками которых являются простагландины — нечто промежуточное между гормонами и медиаторами нервной системы (ацетилхолин, серотонин). Нейроамины именуют гормонами удовольствия. Они вырабатываются так называемой опиоидной системой мозга по схожести их структуры с опиатами. Поскольку гипоталамус является центральным звеном, объединяющим различные структуры лимбической системы мозга, то в зависимости от возбудимости этих структур происходит увеличение или уменьшение их секреции.
наоборот, обеспечиваются несколькими механизмами. Гипоталамус является в то же время органом, воспринимающим импульсы и анализирующим информацию, поступающую из различных частей тела. Кроме того, гипофиз на основе механизма обратной связи позволяет поддерживать на высшем уровне регуляцию постоянства внутренней среды. В гипоталамусе вырабатываются нейроамины, специальные активные соединения, предшественниками которых являются простагландины — нечто промежуточное между гормонами и медиаторами нервной системы (ацетилхолин, серотонин). Нейроамины именуют гормонами удовольствия. Они вырабатываются так называемой опиоидной системой мозга по схожести их структуры с опиатами. Поскольку гипоталамус является центральным звеном, объединяющим различные структуры лимбической системы мозга, то в зависимости от возбудимости этих структур происходит увеличение или уменьшение их секреции.
Гипофиз является железистым органом эктодермального происхождения и состоит из передней, средней и задней долей. У взрослого масса гипофиза 0,6 г, а в пубертатном периоде его масса по сравнению с массой железы у ребенка дошкольного возраста удваивается. В гистологической структуре передней доли различают железистые клетки трех типов: главные (хромофобные), ацидофильные (окси- или эозинофильные) и базофильные (циа-нофильные).
Нейрогипофиз (задняя доля) выделяет два гормона — вазо-прессин (АДГ) и окситоцин. Они обнаруживаются в нейрогипо-физе на 4—5-м месяце антенатального периода. Концентрация АДГ в крови плода крайне низка и сохраняется такой в неонатальном периоде. Впервые антидиуретическая активность крови ребенка выявляется в 4-месячном возрасте, а к 1 году она приближается к уровню взрослых, к этому же периоду завершается созревание клеток нейрогипофиза. Антидиуретическая активность вазопрессина в первые 2 — 3 мес жизни из-за незрелости почки также низка.
Окситоцин оказывает специфическое действие на матку и молочные железы только после завершения периода полового созревания.
Аденогипофиз (передняя доля) выделяет в кровь 6 гормонов: 4 из них тропные (АКТГ, тиреотропный гормон — ТТГ, лютеине-зируюший — ЛГ, фолликулостимулирующий — ФСГ), 2 — эф-фекторные (гормон роста — ГР, пролактин — ПРИ).
Соматотропный гормон (ГР) участвует, как и у взрослого, в регуляции белкового, жирового и углеводного обмена, но особо важное значение этот гормон имеет в регуляции роста ребенка. Считают, что в период внутриутробной жизни и в первые 2 года рост тела не регулируется соматотропным гормоном; его значе-
72
ние проявляется с 2 лет и до периода полового созревания (12 — 13 лет). Половые гормоны уменьшают активность.
ПРЛ, как и гормон роста, является эффекторным гормоном. Предполагают, что он активирует процессы роста у плода, а также участвует в регуляции обмена веществ.
В крови новорожденных концентрация пролактина высока. В течение первого года она снижается и сохраняется на этом уровне до подросткового возраста. В период полового созревания концентрация ПРЛ в крови увеличивается (у девочек больше, чем у мальчиков). В организме подростков пролактин, действуя совместно с лю-теотропным гормоном (ЛТГ) и тестостероном, стимулирует рост предстательной железы и семенных пузырьков. Высокая концентрация пролактина, вероятно, способствует также преходящему увеличению молочных желез у мальчиков (пубертатная гинекомастия).
Тиротропин оказывает стимулирующее влияние на секрецию щитовидной железы со второй трети периода внутриутробного развития. Об этом свидетельствует, в частности, совпадение во времени увеличения концентрации тиротропина в крови с усилением секреции тиреоидных гормонов. В отсутствие гипофиза у плода наблюдается недоразвитие щитовидной железы. Стимулирующее влияние тиротропина на функции щитовидной железы у плода выражено слабее, чем у взрослых. После рождения содержание тиротропина в крови резко возрастает. Усиление секреции тиротропина связывают с адаптацией новорожденного к новым условиям жизни. В течение нескольких дней после рождения содержание тиротропина в крови ребенка существенно снижается, но на протяжении первых двух лет жизни сохраняется на сравнительно высоком уровне. Последующее усиление секреции тиротропина может наблюдаться в период полового созревания.
У плода АКТГ образуется мало. После рождения выделение АКТГ быстро нарастает, что стимулирует развитие коры надпочечников.
Гонадотропные гормоны (ЛГ и ФСГ) имеют особое значение в период внутриутробного развития, когда на 16-й неделе наступает Дифференциация наружных половых органов. В раннем детском возрасте они выделяются в небольших количествах и физиологического значения не имеют. В период пубертатного ускорения роста железы внутренней секреции быстро развиваются и деятельность их усиливается. Гонадотропные гормоны усиливают секрецию половых гормонов и способствуют развитию половых желез.
Нарушения функций аденогипофиза и гипоталамуса взаимосвязаны, и их трудно дифференцировать. В случае гипофункции передней доли гипофиза у ребенка наблюдается карликовый рост (гипофизарный нанизм) при сохранении относительно правильных пропорций тела и нормальном умственном развитии; поло-
73



 вое развитие задержано. В некоторых случаях развивается расстройство жирового обмена, снижается основной обмен. Это заболевание называется адипозогенитальной дистрофией. В других случаях может наступить похудание (болезнь Симмондса). Гиперфункция в детском возрасте (до периода, когда закончится окостенение трубчатых костей) приводит к гигантизму (увеличение роста при сохранении пропорций тела).
вое развитие задержано. В некоторых случаях развивается расстройство жирового обмена, снижается основной обмен. Это заболевание называется адипозогенитальной дистрофией. В других случаях может наступить похудание (болезнь Симмондса). Гиперфункция в детском возрасте (до периода, когда закончится окостенение трубчатых костей) приводит к гигантизму (увеличение роста при сохранении пропорций тела).
Таким образом, при нарушении роста, расстройствах полового созревания, ожирении или сильном исхудании ребенка следует предполагать нарушение функций гипоталамуса и гипофиза.
Оксифильные клетки составляют примерно 35 % общего числа клеток и вырабатывают соматотропный гормон (СТГ), лютео-тропный гормон (ЛТГ) и АКТГ. На долю базофильных клеток приходится примерно 15 % их числа. Они выделяют ТТГ, ФСГ и ЛГ или гормон, стимулирующий интерстициальные клетки (ГСИК). Удельный вес хромофобных клеток — около 50 % всех клеток. По-видимому, эти клетки не выделяют никаких гормонов. Места выработки остальных гормонов неизвестны. В задней доле гипофиза различают: медиальную эминенцию, гипофизарную ножку и собственно заднюю долю. Аксоны отдельных клеток образуют в гипоталамусе пучки волокон, которые оканчиваются в задней доле гипофиза. Нейросекрет гипоталамуса смещается вдоль этих лучков в заднюю долю гипофиза, где складируется и в зависимости от надобности воздействует на исполнительный орган (например, АДГ на дистальную часть почечных канальцев).
Шишковидная железа в возрасте 7 лет достигает наибольшей массы (примерно 0,15 г), а в пубертатном периоде в ней повышается образование пигмента и кальциевых отложений. Эндокринная деятельность этой железы продолжает оставаться спорной.
Щитовидная железа
Щитовидная железа (см. рис. I, цв. вкл.) начинает развиваться у эмбрионада 3-й неделе. Гормоны ее совершенно необходимы для роста и развития уже в период внутриутробной жизни, так как они участвуют в регуляции синтеза белков в митохондриях, обмена углеводов, минеральных веществ и воды. В норме у новорожденного ребенка выявлена высокая тиреоидная активность — «физиологический гипертиреоз», который длится около недели. Второй подъем активности отмечается в период полового созревания (12—15.лет). Секреция тиреоидных гормонов, а соответственно и основной обмен у детей раннего возраста выше, чем у взрослого, вследствие высоких потребностей организма в энергии, необходимой для интенсивного роста.
74
В пубертатном возрасте масса щитовидной железы может удвоиться. Железа является главным органом обмена йода. В ней задерживается неорганический йод, поступающий в организм с пищей и под влиянием сильнодействующих окислительных энзимов превращающийся в органическую форму путем связи с тирозином, в результате чего возникают монойодтирозин и дийодтирозин. Из дийодтирозина под воздействием энзимов образуются йодтиронины, важнейшими из них являются трийод-тиронин и тетрайодтиронин — тироксин. Внутри просветов долек йодтиронины вступают в связь с глобулиновой молекулой коллоида, в результате чего возникает тиреоглобулин. Тирео-глобулин является запасным веществом, из которого под влиянием ТСГ и соответственно потребностям организма в кровь выделяются низкомолекулярные йодтирониновые радикалы. Активируя ферменты, они усиливают окислительные процессы в клетках организма. Тиреоидные гормоны, обеспечивающие соотношение между процессами ассимиляции и диссимиляции, необходимы для роста, развития и дифференциации тканей (морфогенез). Впервые это было показано в опытах, проведенных Гудернером. При кормлении головастиков щитовидной железой происходили прекращение роста и превращение головастиков в микроскопических лягушек величиной 10 мм. Существенная роль тиреоидных гормонов в дифференциации нервной ткани отмечена в экспериментах на крысятах. После экстирпации щитовидной железы мозг у них оставался в малодифферен-цированном состоянии (гипоплазия нейронов, изменение электрической активности мозга, поведения).
Щитовидная железа оказывает влияние на рост, соматическое и психическое развитие всего организма. Йодсодержащие гормоны щитовидной железы участвуют в регуляции деятельности основных систем организма: нервной (повышают возбудимость), сердечно-сосудистой (усиливают работу сердца, тонус сосудов, повышают артериальное давление). Помимо йодсодержащих гормонов в щитовидной железе вырабатывается кальцитонин, который регулирует рост костей, созревание хрящей, повышает ще-лочно-фосфатазную активность и отложение кальция в костях, ускоряет развитие зубов. Обе группы гормонов обеспечивают нормальное кровоснабжение и обмен веществ кожи, работу сальных и потовых желез.
При гипофункции щитовидной железы происходят снижение основного обмена, задержка роста, появляются отеки, наблюдается выпадение волос, развивается слабоумие (кретинизм).
При гипофункции снижение активности процессов окисления, Уменьшение потребления глюкозы, замедление крово- и лимфообращения сказываются на развитии нервной системы, особенно
75

 головного мозга. При внутриутробной недостаточности щитовидной железы рождается ребенок, неполноценный в умственном отношении (врожденный кретинизм), и эти повреждения могут быть столь велики, что даже раннее лечение оказывается не вполне достаточным.
головного мозга. При внутриутробной недостаточности щитовидной железы рождается ребенок, неполноценный в умственном отношении (врожденный кретинизм), и эти повреждения могут быть столь велики, что даже раннее лечение оказывается не вполне достаточным.
Действие гормонов щитовидной железы на взрослый и растущий организм является противоположным. У взрослого избыток гормонов щитовидной железы вызывает повышение основного обмена и потерю массы тела, а у детей — усиление роста, прибавку массы тела и ускорение формирования организма.
Паращитовидные железы
Паращитовидные железы секретируют паратгормон, который вместе с витамином D является основным фактором регуляции обмена кальция и фосфора. Паратгормон имеет прямое отношение к развитию скелета. Он способствует отложению запасов кальция и фосфора в костной ткани, влияет на остеолиз и остеогенез.
Паращитовидные железы уже в грудном возрасте способны поддерживать нормальный уровень кальция и фосфора в сыворотке крови (снижают уровень фосфора и повышают уровень кальция) и, следовательно, нормальную нервно-мышечную возбудимость. Только в период новорожденности уровень кальция и фосфора несколько снижен. Этим объясняются возникающие иногда у новорожденных приступы апноэ, тетании, т.е. признаки ги-попаратиреоидизма. После паратиреоидэктомии снижается концентрация кальция в крови.
Гипофункция околощитовидных желез приводит к снижению кальция в крови и повышению возбудимости ЦНС и мышц, что сопровождается судорожными сокращениями мышц. Наблюдаются также частый жидкий стул, нарушение развития костей и роста волос и ногтей.
Гиперфункция паращитовидных желез вызывает избыточное окостенение с повышением содержания кальция в крови. Гипертрофия паращитовидных желез и их гиперфункция часто сопутствуют авитаминозу D.
Функция околощитовидных желез на протяжении пубертатного периода в общем не меняется.
Поджелудочная железа
Поджелудочная железа формируется у плода на 3-м месяце, а полностью созревает только к 4-му году жизни.
76
У плода и ребенка раннего возраста островковая ткань поджелудочной железы развита хорошо. У плода она составляет 2/3 массы железы, при рождении — 1/3, у взрослого — 1/30. У плода и детей грудного возраста островковая ткань может регенерировать. Эта способность исчезает после четвертого года жизни. Островковая ткань продуцирует два гормона: глюкагон и инсулин.
Глюкагон повышает уровень сахара в крови путем стимулирования гликогенолиза в печени, т.е. является гипергликемическим фактором. Он регулирует доставку глюкозы к клетке, поэтому особенно важен для функционирования ЦНС, которая наиболее чувствительна к недостатку глюкозы. Активность глюкагона плазмы крови к моменту рождения соответствует таковой у взрослого, но в конце первого часа она резко падает и возвращается к норме к 3-му дню жизни ребенка.
Инсулин в крови плода обнаруживается на 12-й неделе. В отличие от взрослых секреция инсулина слабо зависит от концентрации глюкозы в крови плода. Глюкоза хорошо проходит через плаценту, поэтому содержание ее в крови плода в значительной степени зависит от гомеостаза глюкозы в материнском организме. Секреция инсулина у плода имеет большое значение в приросте массы тела. Это важный анаболический гормон, способствующий синтезу белков и жиров в организме плода. Не случайно у беременных, страдающих сахарным диабетом, рождаются дети с избыточной массой тела. Гипергликемия в материнском организме сопровождается увеличением концентрации глюкозы в крови плода. Хроническая гипергликемия у плода ускоряет созревание секреторных механизмов и стимулирует у него секрецию инсулина.
В первые дни после рождения секреция инсулина снижена в связи с физиологической гипогликемией. Через несколько дней после рождения содержание инсулина в крови возрастает, но регуляция его секреции еще несовершенна. При нагрузке глюкозой выделение инсулина у новорожденных увеличивается слабее и с большим скрытым периодом, чем у более старших детей или взрослых. Функция бета-клеток совершенствуется после рождения. Однако у детей имеются индивидуальные особенности секреции инсулина. При нагрузке глюкозой у разных детей наряду с нормальным усилением секреции инсулина может наблюдаться как избыточная, так и недостаточная его секреция. Между действием глюкагона и инсулина существует синергизм. Глюкагон мобилизует гликоген печени, а инсулин обеспечивает использование полученной при этом глюкозы, открывает «ворота» в клетку.
Гипофункция инсулярного аппарата вызывает резкое нарушение углеводородного обмена, развитие сахарного диабета, резкое истощение, нарушение роста, отставание в умственном развитии.
77




 Надпочечники
Надпочечники
Надпочечники — парное образование, располагающееся над верхними полюсами почек на уровне XI —XII грудных позвонков. Масса надпочечников изменяется с возрастом. Она относительно велика у новорожденных (6,2 г), снижается к году (3,2 г), затем постепенно увеличивается, достигая у подростков 11 лет массы надпочечников новорожденного, а в пубертатном периоде — величины, свойственной взрослому человеку (8,5 — 13 г).
Надпочечники состоят из двух различных в функциональном и генетическом отношении частей — корковой и мозговой. Кора надпочечников продуцирует кортикостероиды, которые делятся на три большие группы: глюкокортикоиды, минералокортикои-ды и половые гормоны (андрогены и эстрогены). Мозговое вещество надпочечников вырабатывает адреналин и норадреналин. Кора надпочечников начинает формироваться на 4-й неделе внутриутробного развития, мозговое вещество — на 5 —7-й неделе. У новорожденных корковый слой преобладает над мозговым.
Глюкокортикоиды способны стимулировать неоглюкогенез, превращая в глюкозу белки и жиры, стимулируя отложение в печени гликогена. Высокая доза глюкокортикостероидов вызывает дезаминирование аминокислот, превращение их в глюкозу, что приводит к отрицательному азотистому балансу, прекращению роста ребенка. Гиперфункция коры надпочечников вызывает преждевременное половое созревание. При недостаточности глюкокортикостероидов нарушается углеводный и белковый обмен, снижается сопротивляемость организма. Синтез минералокортикоидов начинается на 15-й неделе внутриутробного развития. Гормоны важны для поддержания натрий-калиевого равновесия.
В период полового созревания функция надпочечников усиливается. Ранние нарушения функции коры надпочечников вызывают изменения полового развития (ложные признаки обоего пола).
Андрогены влияют на белковый обмен. Улучшая синтез белка, они приводят к увеличению мышечной силы и массы тела, ускорению роста и улучшению структуры костей. Андрогены совершенствуют резорбцию кальция в кишечнике и отложение его в костях, контролируют дифференциацию костных клеток, образование костных ядер, удерживают в организме воду, калий, фосфор. Андрогенизирующее действие выражается в стимуляции роста, развитии мужских половых органов и вторичных половых признаков.
У детей до 6 —8 лет кора надпочечников секретирует глюко- и минералокортикостероиды, но половых гормонов почти не вырабатывает.
78
Мозговое вещество надпочечников продуцирует катехолами-ны. У новорожденного выделение адреналина составляет 30 % общей продукции катехоламинов. С возрастом образование адреналина повышается и достигает 60 % катехоламинов.
Половые железы
Антенатсыьный период. Гонады (яичники и семенники) играют исключительную роль в процессе созревания. От того, как они развиваются на раннем этапе, в значительной степени зависят функции многих важных органов в течение всей последующей жизни.
У эмбриона на 5-6-й неделе формируются недифференцированные гонады. Дифференциация их на мужские и женские происходит с 7-й недели, когда начинает формироваться яичко — мужской эндокринный орган. Секреция тестостерона начинается в конце 2-го месяца антенатального периода. Плод не продуцирует эстрогены — женские половые гормоны. Однако в организме плода любого пола содержание их находится на таком же высоком уровне, как и в организме беременной, так как они поступают в кровь плода из крови матери через плаценту. Мужские половые гормоны влияют на гипоталамическую область головного мозга, которая контролирует деятельность гипофиза. Это влияние имеет решающее значение для всей последующей деятельности гипота-ламической области человека. Если новорожденным животным женского пола ввести мужской половой гормон, то у них половая система никогда не будет функционировать по женскому типу, т.е. циклически. Андрогены повреждают ту часть гипотадамиче-ской области, которая обеспечивает циклическую регуляцию деятельности гипофиза. Этот феномен носит название андрогенной стерильности особей женского пола. В женском организме плода или новорожденной девочки не выявляется высокий уровнь анд-рогенов и циклический механизм оказывается интактным.
Постнатальный период. Половые железы и у ребенка, и у взрослого одновременно вырабатывают как мужские, так и женские половые гормоны (андрогены и эстрогены). В период полового созревания происходит изменение количественного соотношения половых гормонов. К 12 годам у мальчиков андрогенов образуется в 1,5 — 2 раза больше, чем у девочек, а у взрослых мужчин — в 2>5 —3,5 раза больше, чем у женщин.
Яичник новорожденной девочки почти зрелый, в нем можно обнаружить зрелые фолликулы. Срок появления первых менструаций зависит от многих факторов: климата, питания, расы, места Жительства (город, деревня), индивидуальных особенностей. В сред-
79







 нем менструации появляются в 13 — 15 лет. Образование спермиев у мальчиков начинается около 15 лет.
нем менструации появляются в 13 — 15 лет. Образование спермиев у мальчиков начинается около 15 лет.
Половые гормоны стимулируют рост, усиливают основной обмен, повышают артериальное давление и тонус ЦНС. В период полового созревания под действием андрогенов у мальчиков увеличивается рост, изменяются морфологические (число эритроцитов) и биохимические (возрастает устойчивость буферных свойств, повышается уровень гемоглобина) показатели крови. Эстрогены оказывают анимизирующее действие. Таким образом, гормоны обусловливают не только первичные половые признаки (непосредственное строение половых органов), но также вторичные (тип оволосения, структуру скелета, развитие мускулатуры) и третичные (биохимические показатели крови).
Влияние температуры на продукцию гормонов. В условиях более низкой температуры (если яички расположены в мошонке) продуцируются преимущественно мужские половые гормоны, а в условиях более высокой температуры (если яички расположены в брюшной полости) — преимущественно женские половые гормоны. Педиатры нередко встречаются со случаями крипторхизма — не опустившегося в мошонку яичка. Яичко, не опустившееся в мошонку в возрасте до 5 лет, в дальнейшем не сможет нормально функционировать. По этой же причине мальчикам не рекомендуется постоянное ношение памперсов. Их следует надевать только на прогулку или на ночь.
Влияние эндокринной системы родителей на развитие ребенка
На развитие плода и формирование его эндокринной системы существенное влияние оказывает состояние материнского организма^ Изменение гормонального статуса беременной, прием не-которыЗГлекарственных препаратов могут нарушать развитие плода и приводить к разнообразным проявлениям патологии детского организма.
Больная сахарным диабетом (поражение инсулярного аппарата поджелудочной железы) рождает детей либо мертвых, либо с очень тяжелой патологией — гиперплазией поджелудочной железы. Недостаточность поджелудочной железы матери вызывает высокое содержание глюкозы в ее крови. Глюкоза свободно переходит через плаценту и насыщает кровь плода. Высокое содержание глюкозы в крови плода приводит к гиперплазии и гиперфункции ос-тровкового аппарата поджелудочной железы, продуцирующей инсулин. Для развития ребенка велика роль здоровья не только
80
i
материнского организма в период беременности. Судьба человека зависит от самых ранних периодов эмбрионального развития. Передаются по наследству и эндокринные заболевания отца. Известно, что преддиабет у отца (нарушение углеводного обмена, связанное с деятельностью поджелудочной железы, которое еще не проявляется клинически) приводит к повреждению спермиев, что сказывается в первую очередь на обмене веществ ребенка. Очень часто такие дети имеют избыточную массу тела.
Эндокринный контроль роста ребенка
Еосх£ебе.нка контролируется многими эндокринными железа
ми: щитовидной, гипофизом, вилочковой, половыми и надпо
чечниками. Влияние их изменяется в зависимости от возраста ре
бенка! ' ~~------------- —'
Щитовидная железа оказывает влияние на рост ребенка на всех этапах его развития. При нарушениях деятельности щитовидной железы рост задерживается. В случае недостаточности щитовидной железы, очень важной для нормального функционирования нервной системы, наряду с отставанием в росте наблюдается отставание в умственном развитии.
До периода полового созревания рост костей ускоряется гор-монамй"вйлОЧКОвой железы, который в дальнейшем передает эту функцию половым железам.
Андрогены продуцируются не только мужскими половыми железами, но и женскими, а также корковым слоем надпочечников. Андрогены также обеспечивают рост организма. Если мужской организм на определенном этапе развития растет за счет ан-дрогенов семенников и частично надпочечников, то женский организм растет только за счет андрогенов надпочечников.
В регуляции процесса роста принимает участие и соматотроп-ный гормон (гормон роста) аденогипофиза. По-видимому, он не играет роли в период внутриутробного развития и в первые 2 года жизни. Его значение проявляется в более старшем возрасте, в периоде полового созревания. Он оказывает влияние на дифференцирование структуры костей. Если ребенок не по возрасту мал ростом, но сложен пропорционально и умственно развит нормально, то в первую очередь следует предполагать недостаточную продукцию гормона роста.
Начиная с периода полового созревания, соматотропный гормон в процессах роста не играет существенной роли. Однако чрезвычайно велико его значение как регулятора белкового, жирового и углеводного обмена. Функция регуляции роста переходит к андрогенам.
 |  |
Глава 6 СИСТЕМА КРОВИ
Характеристика органов кроветворения
Антенатальный период. В онтогенезе система крови претерпевает изменения, в процессе которых можно выделить несколько узловых моментов. В антенатальном периоде различают три стадии, которые частично перекрывают друг друга.
I стадия — эмбриональное или желточное кроветворение. Она
начинается в стенке желточного мешка со 2-3-й недели и про
должается до конца 2-го — начала 3-го месяца внутриутробной
жизни.
II стадия — экстрамедуллярное, или печеночное, кроветво
рение. Начинается с конца 1-го— начала 2-го месяца эмбрио
нального развития, когда появляются очаги кроветворения в са
мом эмбрионе: сначала — повсеместно, а к концу 2-го месяца —
преимущественно в печени. На 5-м месяце внутриутробной жизни
кроветворная функция печени достигает максимума, а затем по
степенно угасает. С 3-го до 6-го месяца внутриутробного развития
кроветворную функцию выполняет и селезенка. Максимум крове
творной активности наблюдается в 4—5 мес.
III стадия — медуллярное кроветворение. Начинается на 4-м
месяце внутриутробного развития и к моменту рождения стано
вится основным.
Постнатальный период. У нормального ребенка кроветворение происходит в костном мозге сначала повсеместно, а с четвертого года жизни появляются первые признаки превращения красного костного мозга в желтый, жировой. Этот процесс продолжается до 14—15 лет. К периоду полового созревания кроветворение сохраняется только в красном костном мозге губчатого вещества тел: позвонков, ребер, грудины, костей голени и бедренных костей.
Однако при ухудшении условий жизни (неправильное питание, редкие прогулки), патологических состояниях у детей очаги кроветворения могут возникать в тех местах, где в эмбриональный период протекали процессы эритро- и лейкопоэза. Функциональная лабильность кроветворного аппарата и возможность возврата к эмбрионатьному типу кроветворения является характерной особенностью гемопоэза ребенка и делает понятными своеобра-
82
зие патогенеза болезней крови в детском возрасте, легкое их возникновение под влиянием незначительных причин и наряду с этим выраженную склонность к процессам регенерации.
Состав и количество крови
Количество крови у детей не является постоянной величиной и подвержено широким колебаниям в зависимости от возраста и массы ребенка. По отношению к массе тела у новорожденного количество циркулирующей крови составляет около 15 %, у детей 1 года — 11 %, 3 лет — 8 %, 6—9 лет, как и у взрослых, — около 7—8 %. У мальчиков относительное количество крови несколько больше, чем у девочек. Относительно больший, чем у взрослых, объем крови у детей связан с обеспечением более высокого уровня обмена веществ.
Гематокритное число (соотношение между объемом кровяных телец и всем объемом крови в процентах) в 1-й день после рождения выше, чем у взрослых (примерно 54 %), что обусловлено высокой концентрацией и большим средним объемом эритроцитов. К 5—8-му дню этот показатель снижается до 52 %, а к концу 1-го месяца —- до 42 %. В 1 год объем форменных элементов примерно 35 %, в 5 лет — 37 %, в 11—15 лет — 39 % (эти цифры соответствуют динамике эритропоэза в онтогенезе). Нормальные для взрослых величины (40—45 %) устанавливаются по завершении пубертатного периода.
|
Форменные элементы крови
Эритроциты
Плод. Первичные эритроциты (мегалоциты) появляются на стадии эмбрионального кроветворения (желточного). До 9-12-й недели в них преобладает примитивный гемоглобин (НЬР), который затем заменяется фетальным (HbF). Он становится основной формой гемоглобина в антенатальном периоде. Приблизительно с 16-й недели внутриутробного развития начинается синтез гемоглобина взрослого (НЬА), но количество его до 8-го месяца не превышает 10%. К моменту рождения НЬА составляет уже 20 — 40% гемоглобина. Важным физиологическим свойством примитивной и фетальной форм гемоглобина является их высокое сродство к 02 и большая степень диссоциации оксигемоглобина. Наряду со значительным количеством эритроцитов это обеспечивает плоду
83


 достаточное снабжение тканей кислородом в условиях относительной гипоксии, связанной с тем, что оксигенация крови плода в плаценте ограничена по сравнению с оксигенацией крови после рождения (с началом легочного дыхания).
достаточное снабжение тканей кислородом в условиях относительной гипоксии, связанной с тем, что оксигенация крови плода в плаценте ограничена по сравнению с оксигенацией крови после рождения (с началом легочного дыхания).
Новорожденный. Сразу после рождейия в крови ребенка отмечается повышенное содержание гемоглобина (в среднем 210 г/л) и большое количество эритроцитов — _6Д): 1012/л. С конца 1-х — начала 2-х суток жизни происходит уменьшение содержания эритроцитов и гемоглобина, что объясняется усиленным разрушением эритроцитов. Максимальная скорость их разрушения приходится на 2—3-й день после рождения. В это время она в 4 —7 раз больше, чем у взрослых. Это ведет к повышению в крови билирубина, что на фоне недостаточности ферментативных систем печени приводит к физиологической желтухе (билирубин откладывается в коже и слизистых оболочках), которая появляется на 2 — 3-й день и исчезает к 7 —10-му дню после рождения.
Известно, чтентродукты разрушения эритроцитов являются стимуляторами гемопоэза. В связи с этим у новорожденных одновременно с массивным разрушением эритроцитов происходит интенсивное образование новых. Эритропоэз у новорожденных примерно в 5 раз выше, чем у детей старшего возраста и взрослых. При этом идет замена HbF на НЬА. К 3—5-му месяцу постнатального периода развития HbF в крови ребенка практически отсутствует.
У новорожденных отмечаются довольно резкие колебания размеров эритроцитов, что расценивается как физиологический ани-зоцитоз. Сравнительно много эритроцитов разной формы (физиологический пойкилоцитоз), воспринимающих как кислую, так и щелочную окраску (полихроматофилия). Среди эритроцитов много молодых, незрелых форм, что указывает на активно протекающие процессы эритропоэза. В течение первых 5 — 7 дней довольно много ретикулоцитов, встречаются ядросодержащие формы эритроцитов (нормоциты и эритобласты)- Осмотическая стойкость эритроцитов имеет характерные особенности: есть как более устойчивые, так и менее устойчивые к осмотическому гемолизу по сравнению с кровью взрослого. Эта особенность связана с наличием в крови новорожденных одновременно старых, разрушающихся эритроцитов и новых, молодых форм (более устойчивых), что также является отражением активного эритропоэза.
Эритроциты новорожденных обладают укороченным сроком жизни. Длительность жизни эритроцитов на 2—3-й день после рождения составляет около 12 дней, что примерно в 10 раз меньше длительности жизни эритроцитов взрослых. К 10-му дню этот показатель увеличивается почти в 3 раза.
Другие возрастные периоды. Кровь грудного ребенка по сравнению с кровью новорожденного, а также детей более старшего
84
возраста характеризуется относительно низким содержанием гемоглобина и эритроцитов. В возрасте 5—6 мес количество эритроцитов составляет в среднем 4,1 • 10|2/л, а гемоглобина — 120 г/л. Эти показатели остаются низкими до 1 года (физиологическая анемия). Воздействие на организм ребенка неблагоприятных факторов (ухудшение условий жизни или патологические процессы) может способствовать усилению этого состояния до степени истинной анемии (содержание гемоглобина ниже 100 г/л, эритроцитов — меньше 3 • 1012/л). У детей старше 1 года количество эритроцитов и гемоглобина постепенно увеличивается, а продолжительность жизни эритроцитов возрастает до 120 дней, как у взрослых.
В периоды от 1 года до 2 лет, в 5—7 лет и в 12—14 лет наблюдаются значительные индивидуальные вариации количества эритроцитов, что, по-видимому, связано с ускоренным ростом тела. Форменные элементы крови представлены на рис. IV.
|
|
| 85 |
В пубертатном возрасте можно установить у мальчиков и девочек разницу в количестве эритроцитов и гемоглобина. До 10-летнего возраста между мальчиками и девочками не наблюдается значительных расхождений в количестве эритроцитов. Начиная с 10 лет у мальчиков наблюдается значительное повышение числа эритроцитов (рис. 21). Повышение количества гемоглобина у мальчиков, как и увеличение массы крови, связано, по всей вероятности, с развитием мускулатуры (табл. 4).







 Таблица 4
Таблица 4
Дата добавления: 2018-11-24; просмотров: 354; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!

