Взаимопревращения аминокислот
Реакциями восстановительного аминирования a-кетокислот и трансаминированием синтезируются заменимые аминокислоты Ала, Асп, Асн, Глу, Глн, Сер.
Такие аминокислоты как пролин, тирозин, цистеин образуются в результате биохимических превращений других аминокислот, в которых принимают участие специфические ферментные системы.
Предшественником пролина (Про) является глутаминовая кислота. В первой стадии реакции Глу восстанавливается в g-полуальдегид, затем происходит образование пятичленного гетероцикла с его дальнейшим восстановлением:
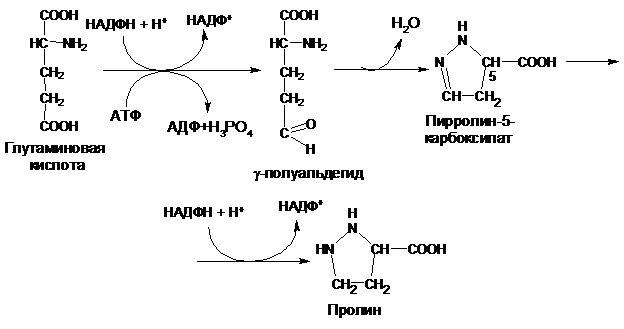
Предшественником тирозина (Тир) является незаменимая аминокислота фенилаланин. Он образуется путем гидроксилирования фенильной группы в положении 4. Эта реакция катализируется фенилаланин-4-монооксигеназой в присутствии НАДФН+Н+ и кислорода:
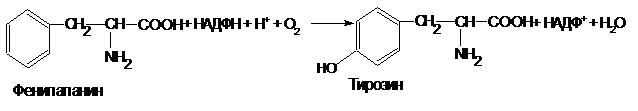
Таким образом, отсутствие в пище незаменимой кислоты фенилаланина ведет к отсутствию в организме и тирозина.
Предшественником глицина (Гли) является серин. Основной путь превращения заключается в переходе трехуглеродной молекулы серина в двухуглеродную молекулу глицина путем отщепления b-углеродного атома. Эта реакция катализируется ферментом серингидроксиметилтрансферазой, коферментом которой является тетрагидрофолат, представляющий собой активную форму фолиевой кислоты (вит.Вс). Он является переносчиком группы –СН2ОН от молекулы серина на какой-либо другой акцептор. Отщепляемый от серина b-углеродный атом образует метиленовый мостик между атомами азота тетрагидрофолата в положениях 5 и 10, в результате чего синтезируется N5-, N10-метилентетрагидрофолат:
|
|
|
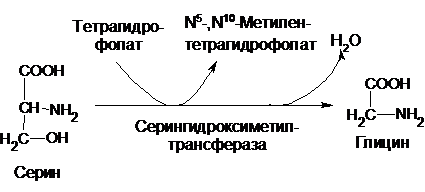
Важнейшим элементом в составе многих биологически активных соединений является сера. Она входит в состав двух аминокислот –цистеина и метионина.
Предшественником цистеина (Цис) является серин, а в качестве источника серы для синтеза цистеина используется неорганический сульфат SO42-.
В растениях и бактериях сульфатная группа восстанавливается в сульфит (SO32-), а затем в сульфид (S2-). Реакция катализируется двумя редуктазами, каждая из которых использует в качестве донора электронов НАДФН + Н+; всего необходимо 4 молекулы НАДФН + Н+ (8 электронов). Синтез цистеина из серина и сульфида идет через промежуточное производное о-ацетилсерин:
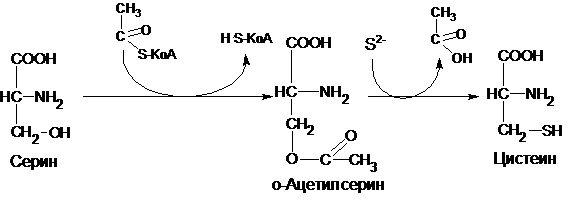
Прямое аминирование фумаровой кислоты
Одна из дикарбоновых аминокислот – аспарагиновая – может синтезироваться путем прямого присоединения аммиака к фумаровой кислоте.
Фермент аспартат-аммиак-лиаза, катализирующий эту реакцию, выделен из бактерий, представляет собой металлопротеин, активируемый Са2+. У высших растений активность фермента невысока, он обнаружен в клевере, горохе и других растениях.
|
|
|
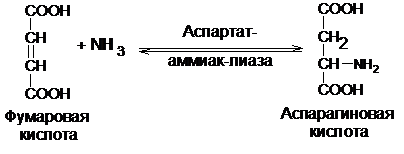
Дата добавления: 2018-05-02; просмотров: 593; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
