Растворимость. Произведение растворимости
Все вещества в той или иной степени способны растворяться и характеризуются растворимостью. Некоторые вещества неограниченно растворимы друг в друге (вода-ацетон, бензол-толуол, жидкие натрий-калий). Большинство соединений ограниченно растворимы (вода-бензол, вода-бутиловый спирт, вода-поваренная соль), а многие малорастворимы или практически нерастворимы (вода-BaSO4, вода-бензин).
Растворимостью вещества при данных условиях называют его концентрацию в насыщенном растворе. В таком растворе достигается равновесие между растворяемым веществом и раствором. В отсутствие равновесия раствор остается стабильным, если концентрация растворенного вещества меньше его растворимости (ненасыщенный раствор), или нестабильным, если в растворе содержится вещества больше его растворимости (пересыщенный раствор).
К равновесным системам следует отнести также и систему труднорастворимый электролит – его насыщенный раствор. В этом случае мы имеем дело с динамическим гетерогенным равновесием 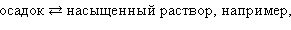
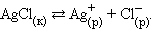
В этом растворе концентрация ионов очень мала и вследствие этого взаимодействие их друг с другом практически отсутствует.
Константу равновесия для гетерогенной системы можно записать так:

концентрацию твердой фазы AgClk можно считать постоянной, тогда
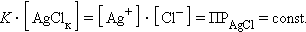
С другой стороны:
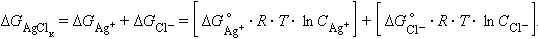
Так как 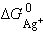 ,
, 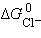 и
и 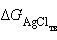 – постоянные величины, то:
– постоянные величины, то:
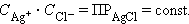
В общем виде для уравнения:

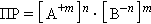
В насыщенном растворе труднорастворимого сильного электролита произведение концентрации его ионов в степенях стехиометрических коэффициентов при данной температуре есть величина постоянная, называемая произведением растворимости (ПР).
|
|
|
Произведение растворимости характеризует растворимость труднорастворимого электролита при данной температуре. Из двух однотипных солей большей растворимостью обладает та соль, у которой ПР больше.
Задача 1. Определите, какая соль обладает большей растворимостью: CaSO4или BaSO4.
Решение:ПР (CaSO4) = 2,5∙10–5; ПР (BaSO4) = 1,1∙10–10
Из двух однотипных солей большей растворимостью обладает та соль, у которой ПР больше.
Ответ: большей растворимостью будет обладать CaSO4.
Концентрация каждого иона в насыщенном растворе электролита может быть изменена, но при этом изменяется и концентрация другого иона так, что произведение концентраций сохраняет прежнюю величину. Поэтому, если в насыщенный раствор электролита ввести некоторое количество одного из ионов, входящих в состав электролита, то концентрация другого иона должна уменьшиться и часть растворенного электролита выпадет в осадок, то есть растворимость электролита понижается от введения в раствор одноименных ионов.
|
|
|
В общем виде растворимость L труднорастворимого электролита AnBm определяется соотношением:
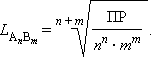
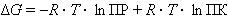
ПК – произведение концентраций ионов в степенях, соответствующих стехиометрическим коэффициентам для системы в неравновесном состоянии.
Зная ПК и сравнив его с ПР, можно установить, растворится или выпадет осадок при данной температуре:
1. Если ПК = ПР, ΔG = 0 – система находится в состоянии равновесия (раствор насыщенный).
2. Если ПК <ПР, ΔG < 0 – самопроизвольно протекает процесс растворения осадка.
3. Если ПК >ПР, ΔG > 0 – возможен только обратный процесс – выпадание осадка.
Дата добавления: 2018-04-15; просмотров: 286; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
