Диаграмма плавкости двухкомпонентных систем при
Неограниченной растворимости компонентов в жидком и твердом
Состоянии, компоненты не образуют химических соединений
Характерные кривые охлаждения (a) для данной системы и пример диаграммы (b) представлены на рис. 4.3. Кривые охлаждения для чистых компонентов имеют обычный вид, а на кривой охлаждения любого промежуточного состава при начале кристаллизации появляется перегиб вследствие замедления охлаждения за счет выделения теплоты кристаллизации, а после окончания кристаллизации вследствие прекращения тепловыделения на кривой охлаждения появляется второй излом (кривая охлаждения для состава М). То есть кристаллизация осуществляется в
интервале температур. Выше линии ликвидуса ТАLTBнаходится область, соответствующая
жидкофазному гомогенному состоянию системы. Ниже линии солидусаТАSTBрасположена область существования твердого раствора (f = 1). Между линиями солидуса и ликвидуса находится область равновесного сосуществования жидких и твердых растворов (f = 2). В этом случае при кристаллизации в системе не происходит образование эвтектической смеси.

Рис. 4.3. Диаграмма плавкости для систем при неограниченной растворимости
Компонентов в жидком и твердом состоянии
Рассмотрим процесс кристаллизации расплава, обозначенного на диаграмме точкой М. При охлаждении до температуры Т1система остается в жидком состоянии. При температуре T1из расплава состава m выпадают кристаллы твердого раствора, имеющего состав, характеризуемый точкой n(точка пересечения изотермы с линией солидуса). Состав образующихся кристаллов отличается от состава жидкой фазы, из которой они образуются. В твердый раствор в большей степени переходит более тугоплавкий компонент (в данном случае – это компонент В).
По мере понижения температуры от Т1до Т2состав расплава изменяется по линии ликвидуса от точки mдо точки k, а состав кристаллов твердого раствора, находящихся в равновесии с расплавом (жидкостью), будет изменяться по линии солидуса от точки nдо точки l. Последние капли жидкости будут при Т2иметь состав, характеризуемый точкой k. Дальнейшее понижение температуры системы, характеризуемой точкой М, не будет сопровождаться изменениями фазового состава. То обстоятельство, что во всем интервале температур ТА ÷ ТВсостав сосуществующих твердой и жидкой фаз отличаются друг от друга, позволяет осуществлять дробную кристаллизацию. Повторение такой кристаллизации, то есть операций расплавления и последующего отделения кристаллизующихся растворов позволяет выделять один из компонентов в более чистом состоянии.
Диаграмма плавкости двухкомпонентных систем с устойчивым хи-
Мическим соединением при неограниченной растворимости компонентов
В жидком состоянии и отсутствии растворимости в твердом состоянии
Если компоненты Аи Вмогут образовать устойчивое твердое химическое соединение AxBy, которое способно плавиться без разложения, то такие соединения называются конгруэнтно плавящимися. В этом случае на диаграмме плавкости такой системы (рис. 4.4) на кривой ликвидуса появляется максимум, который называется сингулярной точкой (точка С рис. 4.4). Соответствующий ей состав характеризует состав химического соединения АxBy. Для этой точки состав расплава совпадает с составом кристаллов, выделяющихся при охлаждении системы. Чем выше положение максимума на диаграмме, тем устойчивее образующееся химическое соединение. По обе стороны максимума находятся две эвтектики. Диаграмму плавкости в данном случае можно рассматривать как состоящую из двух самостоятельных диаграмм для следующих систем: компонент А– химическое соединение AxByи компонент В– химическое соединение AxBy. В каждой системе имеется своя эвтектика с соответствующей температурой ее кристаллизации, что отражено на диаграмме.
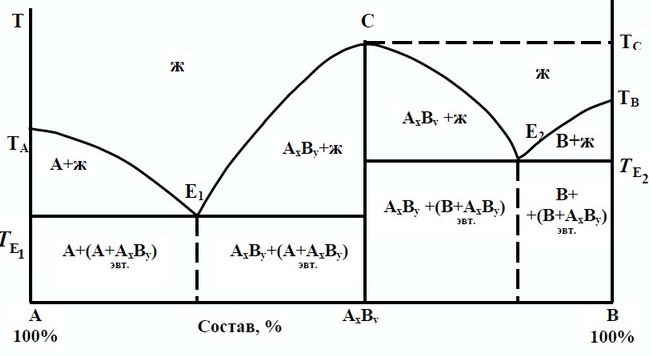
Рис. 4.4. Диаграмма плавкости с конгруэнтно плавящимсяхимическим соединением
На областях диаграммы, представленной на рис. 4.4, указаны фазы, которые находятся в равновесии при соответствующих составах систем и температурах.
Конгруэнтное плавление (лат. congruentis — совпадающий) — термин физической химии, обозначающий процесс, в котором состав жидкости совпадает с составом твердой фазы — химического соединения, из которого эта жидкость образовалась.
Дата добавления: 2018-02-28; просмотров: 1803; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
