Правило произведения растворимости
В аналитической химии используются, помимо гомогенных систем, гетерогенные (неоднородные) системы, состоящие из двух и более фаз.
Это касается прежде всего реакций осаждения, где существует равновесие между осадком, образующимся при осаждении, и раствором, соприкасающимся с осадком соответствующего вещества.
Раствор, находящийся в динамическом равновесии с соответствующей твердой фазой, называется насыщенным раствором. В насыщенном растворе скорость растворения осадка, т. е. перехода ионов с поверхности твердой фазы в раствор, равна скорости противоположного процесса – осаждения растворенных ионов на поверхности. Равновесие малорастворимого соединения MenAnm с его насыщенным раствором, в котором он диссоциирует нацело,
MenAnm(т)= nMe + mAn (8.1)
количественно может быть охарактеризовано константой равновесия
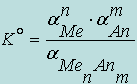 (8.2)
(8.2)
Активность твердого соединения αMenAnm постоянна, поэтому она может быть включена в константу:
 (8.3)
(8.3)
Полученная таким образом константа равновесия называется термодинамическим произведением растворимости, или произведением активности.
В насыщенном растворе малорастворимого соединения произведение активностей ионов малорастворимого соединения в его насыщенном растворе в степенях, равных его стехиометрическим коэффициентам, есть величина постоянная при данной температуре и называется произведением активности. Например:

Для весьма малорастворимых соединений (K°S < 10-7) концентрации ионов в его насыщенном растворе очень малы и межионные силы практически не играют роли. Поэтому коэффициенты активности можно принять равными единице. В данном случае вместо активностей можно использовать равновесные концентрации ионов малорастворимого соединения в его насыщенном растворе, а вместо произведения активностей (K°S) – произведение растворимости KS, или концентрационное произведение растворимости.
|
|
|
KS(MenAnm)=[Me]n [An]m (8.4)
Например:
KS(Ag2CrO4)=[Ag+]2[CrO2-4]
Значения K°S важнейших малорастворимых соединений приведены в справочниках (см. Приложение. 4). Для проведения приближенных расчетов нередко приравниваются KS = K°S и в расчетах используют табличные значения K°S. Правило произведения растворимости позволяет глубже понять процессы в насыщенном, ненасыщенном и пересыщенном растворах электролита. Раствор того или иного малорастворимого электролита становится насыщенным при данной температуре, когда произведение концентраций его ионов (ионное произведение) достигает величины KS. Например, в насыщенном растворе сульфата бария ионное произведение равно произведению растворимости:
[Ba2+][SO2-4]=K°S(BaSO4)
Концентрация растворенного вещества в ненасыщенном растворе ниже, чем в насыщенном, а ионное произведение меньше произведения растворимости:
|
|
|
[Ba2+][SO2-4] < K°S(BaSO4)
Наоборот, если ионное произведение превысит KS малорастворимого электролита, то процесс осаждения будет преобладать над процессом растворения и часть вещества выделится из раствора в твердую фазу. Для пересыщенного раствора BaSO4
[Ba2+][SO2-4] > K°S(BaSO4)
Пользуясь правилом произведения растворимости, можно теоретически обосновать условия осаждения осадков, их растворимость и условия протекания других реакций в растворе.
Можно предвидеть, произойдет ли выпадение осадка при смешении растворов заданной концентрации.
Пример.
Выпадет ли осадок BaSO4 при смешении равных объемов 0,02 М BaCl2 и 0,02 М Na2SO4?
Решение.
После смешения концентрация каждого иона за счет разбавления (объем увеличится в два раза) уменьшится в два раза и будет составлять [Ba2+]= [SO2-4]=0,01 моль/л.
Произведение их концентраций [Ba2+] [SO2-4]=0,01*0,01=1*10-4. Это число намного превышает табличное значение K°S(BaSO4)=1,1 *10-10 ; поэтому при смешении 0,02 М растворов BaCl2 и 0,02 М Na2SO4 осадок BaSO4 образуется.
Таким образом, осадок малорастворимого электролита образуется только тогда, когда произведение концентраций ионов в степенях, равных стехиометрическим коэффициентам, превысит его произведение растворимости.
|
|
|
Малорастворимый электролит будет осаждаться до тех пор, пока ионное произведение, постепенно уменьшаясь, не станет равным произведению растворимости осадка. Затем снова устанавливается равновесие между осадком и раствором, и осаждение прекращается.
Известно, что не существует веществ, абсолютно не растворимых в воде. Поэтому при осаждении в растворе всегда остается какое-то количество ионов, отвечающих величине произведения растворимости. Если оно не очень велико (< 10 - 6 моль/л) и выполнению последующих аналитических реакций не мешает, то говорят, что достигнуто практически полное осаждение.
Дата добавления: 2016-01-04; просмотров: 85; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
