Влияние сильных электролитов на растворимость
Растворимость малорастворимого соединения существенным образом зависит от присутствия в растворе сильных электролитов, не имеющих общего иона с осадком и имеющего общий ион.
Присутствие сильного электролита, не имеющего с осадком одноименного иона, увеличивает растворимость за счет снижения активности ионов в растворе. Это явление получило название солевого эффекта.
Пример.
Вычислить растворимость AgCl в воде и в присутствии 0,05 М NH4NO3.
Решение.
Растворимость AgCl в воде равна
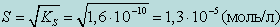
В присутствии сильного электролита NH4NO3, (не имеющего общего иона с осадком), необходимо учитывать влияние на растворимость ионной силы раствора, создаваемую сильным электролитом 0,05 М NH4NO3. Концентрация [NH4+] = [NO3-]=0,05 моль/л:


γ Ag+ Cl- = 0,8
Из произведения активности для AgCl можно найти значение S:
KºS(AgCl) = αAg+ · αCl- =[Ag+] [Cl-] · γ Ag+ · γ Cl- = S2 · γ2

Из приведенных расчетов видно, что, действительно, растворимость AgCl в присутствии 0,05 M NH4NO3 возросла.
Влияние сильного электролита, имеющего общий ион с малорастворимым соединением, на его растворимость
В присутствии сильного электролита, имеющего общий ион с осадком, растворимость осадка уменьшается вследствие увеличения концентрации одного из ионов малорастворимого соединения в растворе. В результате происходит дополнительное выпадение осадка, пока не наступит равновесие. Солевой эффект в данном случае также имеет место, однако вклад эффекта подавления растворимости является доминирующим.
|
|
|
Пример.
Вычислить растворимость AgCl в присутствии 0,05 М NH4Cl.
Решение.
При расчете растворимости надо учитывать тот факт, что концентрация Cl- – иона в растворе будет равна сумме концентрации (S + 0,05) за счет растворимости малорастворимого соединения ([Cl-]= S) и за счет диссоциации сильного электролита 0,05 М NH4Cl ([Cl - ] = 0,05 моль/л):
NH4Cl  NH4+ + Cl-
NH4+ + Cl-
0,05 0,05 0,05
AgCl  Ag+ + Cl-
Ag+ + Cl-
S S+0,05
Произведение растворимости для AgCl

т. к. S << 0,05,
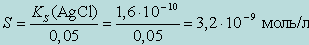
Таким образом, приведенные расчеты показывают, что растворимость AgCl в присутствии NH4Cl существенным образом понижается по сравнению с растворимостью в воде (SAgCl = 1,3 · 10 -5 моль/л.
Дата добавления: 2016-01-04; просмотров: 107; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
