Влияние температуры на скорость и степень превращения при протекании обратимых реакций.
В отличие от обратимых реакций влияние температуры на скорость обратимых реакций имеет более сложный характер, так как скорость прямой и скорость обратной реакций обладают разными энергиями активации, а значит и разной «чувствительностью» к изменению температуры Т. Для обратимой экзотермической реакции E 2 > E 1, для эндотермической – энергия активации ( E 1) выше, чем обратной ( E 2).
Для простых обратимых реакций типа А  В
В 
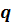 скорость реакции можнозаписать в виде: U = k 1· СА - k 2· СВ , (19)
скорость реакции можнозаписать в виде: U = k 1· СА - k 2· СВ , (19)
где: k 1 - константа скорости прямой реакции;
k 2 - константа скорости обратной реакции;
С учетом соотношений
СА= СА,О · (1- ХА ), СВ = СА,О · ХА, k = k 0·exp[- E /( RT ) ] , Кс = 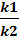
уравнение (18) преобразуется:
U = k 0· exp [- E1 /( RT ) ]· СА,0 · [1 - ХА·(1+  ) ]. (20)
) ]. (20)
Влияние температуры на скорость проявляется через изменение константы скорости и константы равновесия Кс , Если представить уравнение (8) :
m = 1 -  = k · C 1 – порядок
= k · C 1 – порядок
m = 2 -  = k · C 2 2 – порядок
= k · C 2 2 – порядок
в виде U = k ·Δ С, то можно сказать, что при изменении температуры изменяется и константа скорости реакции k и движущая сила процесса:
Δ С = СА,0 · [1 - ХА·(1+  ) ] (21)
) ] (21)
В случае экзотермической реакции влияние температуры на кинетический фактор (константа скорости) и термодинамический фактор (константа равновесия) противоречиво: с ростом Т увеличивается k и уменьшается Кс
Рис . Влияние температуры на значения константы скорости k и константы Кс

Из графика видно, что это приводит к экстремальной зависимости изменения скорости процесса от температуры.
Если в уравнение (20) подставить соответствующие значения
k 0,1, E1, СА,0 , то можно построить график зависимости U от Т для определенного значения ХА.
Рис. Характерные зависимости скорости обратимой экзотермической реакции от температуры.

Если таким же образом построить графики для других значений
ХА(Х1, Х2, Х3, Х4), то можно показать, что с увеличением степени превращения скорость реакции снижается, а температуры, соответствующие максимальным скоростям, Топт,1 , Топт,2 … (оптимальные температуры) уменьшаются, что отражено на графике.
Рис. Характерные зависимости скорости обратимой экзотермической реакции от температуры и степени превращения ( Х1 <Х2< Х3< Х4)

На графике линию MN, соединяющую максимальные значения скоростей, называют линией оптимальных температур. Она показывает, как надо изменять температуру по мере увеличения степени превращения, чтобы процесс шел с максимальной скоростью.
Значения ХА при некотором постоянном  с ростом Т вначале увеличиваются, достигают максимума, а затем снижаются, так как процесс ограничен равновесной степенью превращения Х*А.
с ростом Т вначале увеличиваются, достигают максимума, а затем снижаются, так как процесс ограничен равновесной степенью превращения Х*А.
Рис. Характерные зависимости степени превращения от температуры.

При проведении процессов с обратимой эндотермической реакцией с ростом Т увеличивается константа скорости k константа движущей силы Кс. С помощью уравнения(20) можно получить графическую зависимость скорости реакции от температуры для разных степеней превращения.
Рис. Изменение скорости обратимой эндотермической реакции в зависимости от температуры и степени превращения ( Х1<Х2< Х3< Х4).

Общая закономерность влияния температуры на скорость обратимых реакций заключается в том, что при малых степенях превращения и низких температурах преобладает фактор повышения константы скорости прямой реакции, а при высоких температурах сказываются термодинамические ограничения, затормаживающие рост эндотермических процессов и уменьшающие значения степеней превращения в экзотермических процессах.
Дата добавления: 2019-11-25; просмотров: 2309; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
