Література для оформлення роботи і підготовки
теоретичного матеріалу
Опрацювати підрозділи 9.1, 9.3-9.5 підручника [6] та підрозділи 3.2.1, 3.2.2 посібника [3].
Лабораторна робота 5 Приготування розчинів
Теоретична частина
Від концентрації залежить багато властивостей розчинів. У найбільш загальному вигляді концентрація може бути виражена через число частинок в одиниці об`єму або як відношення числа частинок даного виду до загального числа частинок у розчині. Вміст розчиненої речовини і розчинника може вимірюватися в одиницях маси, об`єму або в молях.
Склад розчину виражають за допомогою таких величин: безрозмірних – масової і молярної частки та розмірних – молярної концентрації, молярної концентрації еквівалента, моляльності тощо.
Масова частка 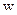 показує, яку частину від даної маси розчину
показує, яку частину від даної маси розчину  становить маса розчиненої речовини
становить маса розчиненої речовини  . Ця безрозмірна величина виражається в частках одиниці або у відсотках. Якщо позначити масову частку через
. Ця безрозмірна величина виражається в частках одиниці або у відсотках. Якщо позначити масову частку через  , формули для її розрахунку можна подати у такому вигляді:
, формули для її розрахунку можна подати у такому вигляді:
 або
або  .
.
Моляльність  показує кількість розчиненої речовини
показує кількість розчиненої речовини 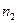 , яка припадає на 1000 г розчинника (моль/кг):
, яка припадає на 1000 г розчинника (моль/кг):
 ,
,
де  – маса розчинника в даній порції розчину;
– маса розчинника в даній порції розчину;  – маса розчиненої речовини;
– маса розчиненої речовини; 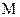 – молярна маса розчиненої речовини.
– молярна маса розчиненої речовини.
Молярна концентрація  показує кількість розчиненої речовини
показує кількість розчиненої речовини  , яка міститься в 1 л розчину (моль/л):
, яка міститься в 1 л розчину (моль/л):
 ,
,
де V – об’єм розчину, л.
|
|
|
Молярна концентрація еквівалента  показує кількість еквівалентів речовини, яка міститься в 1 л розчину, моль/л:
показує кількість еквівалентів речовини, яка міститься в 1 л розчину, моль/л:
 ,
,
де 
 - кількість еквівалента речовини;
- кількість еквівалента речовини; 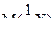 – молярна маса еквівалента речовини X.
– молярна маса еквівалента речовини X.
За законом еквівалентів об`єми реагуючих розчинів обернено пропорційні їх молярним концентраціям:
 .
.
У лабораторній практиці часто виникає необхідність приготування розчинів різних речовин заданого складу – певної молярної концентрації або масової частки розчиненої речовини. Для цього як вихідні беруть тверді речовини або їх концентровані розчини і розчинник (найчастіше – воду).
Необхідну масу твердої речовини зважують на технохімічних (за необхідності – на аналітичних) терезах, а об’єми води чи іншого розчинника або розчину відміряють за допомогою чистого мірного посуду.
Контрольні запитання і вправи
1 Якими способами можна виразити концентрацію розчиненої речовини в розчині?
2 Яку масу (г) 15% розчину кальцій хлориду можна приготувати, маючи 170 мл води?
3 Якийоб`єм (мл) 94 % розчину сульфатної кислоти (ρ=1,857г/мл) потрібно взяти для приготування 1 л 20% розчину (ρ=1,143г/мл)?
Практична частина
Мета роботи –сформувати навички приготування розчинів заданої концентрації.
|
|
|
Обладнання і реактиви: шпатель,хімічний стакан, скляна паличка з гумовим наконечником, шпатель, мірний циліндр, технохімічні терези, набір важків, промивалка з дистильованою водою, набір ареометрів, калій дихромат.
Перед виконанням роботи повторіть правила зважування на технохімічних терезах.
ДОСЛІД 3.5.1 Приготування розчину заданої концентрації
Отримати у викладача індивідуальне завдання на приготування 50 г розчину калій дихромату з певною масовою часткою солі.
Зробити необхідні для приготування розчину розрахунки: розрахувати масу солі та об’єм води. Зважити сіль на технохімічних терезах і відміряти об’єм води у мірному циліндрі. Пересипати в хімічний стакан сіль і додати воду. Розмішувати сіль скляною паличкою до повного її розчинення.
За значеннями, наведеними у таблиці 3.1, встановити теоретичне значення густини отриманого розчину і вибрати відповідний ареометр.
Таблиця 3.1 – Густина водних розчинів 
| Концентрація розчину, % | Густина, г/см3 | Концентрація розчину, % | Густина, г/см3 |
| 1 | 1,0052 | 6 | 1,0408 |
| 2 | 1,0122 | 7 | 1,0481 |
| 3 | 1,0193 | 8 | 1,0554 |
| 4 | 1,0264 | 9 | 1,0628 |
| 5 | 1,0336 | 10 | 1,0703 |
|
|
|
Промити невеликою кількістю приготованого розчину циліндр. Заповнити циліндр приготованим розчином і за допомогою ареометра виміряти густину розчину (ареометр - прилад, що складається зі скляної трубки, нижня частина якої має більший діаметр і закінчується шариком, заповненим дрібним дробом. Верхня тонка трубка має поділки з позначеннями густини рідини, г/см3. Ареометр поміщується в циліндр із рідиною тим глибше, чим менша її густина).
Порівняти отримане значення густини розчину з теоретичним. Розрахувати відносну похибку густини приготованого розчину.
Використавши отримані значення маси та густини розчину, розрахувати молярну концентрацію розчину, молярну концентрацію еквівалента, моляльну концентрацію.
Дата добавления: 2019-02-13; просмотров: 139; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
