Опыт 1. Зависимость скорости химической реакции от концентрации реагирующих веществ
Для исследования предлагается реакция:
Na2S2O3 + H2SO4 = Na2SO4 + SO2↑ + S↓ + H2O
Реакция в ионно-молекулярном виде:
S2O32- + 2Н+ = SO2↑ + S↓ + Н2О.
Рассмотрите применимость закона действующих масс для данной реакции в ионно-молекулярном виде. Изобразите графически вид зависимости скорости реакции при увеличении концентрации тиосульфата натрия, условно обозначив ее как 1С, 2С, ЗС (при СН+ = const). Обсудите также вид зависимости скорости реакции от концентрации серной кислоты и изобразите графически вид зависимости скорости реакции от концентрации серной кислоты, если 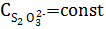 .
.
Методика выполнения опыта
Приготовьте три раствора тиосульфата натрия различной концентрации. Для этого в три пробирки налейте: в первую – 1 мл раствора Na2S2O3 и 2мл Н2О; во вторую – 2 мл Na2S2O3 и 1 мл Н2О; в третью – 3 мл того же раствора Na2S2O3. Затем в каждую пробирку добавьте по 1 мл раствора H2SO4 и измерьте время в секундах от момента добавления кислоты до появления первых признаков появления голубого окрашивания (помутнения) раствора вследствие образования микрокристаллов серы. Результаты опытов занесите в таблицу 3.2 и постройте график зависимости скорости реакции от концентрации тиосульфата натрия.
Опыт 2. Зависимость скорости реакции от температуры
Исследуется полуэмпирическое правило Вант-Гоффа и уравнение Аррениуса, графическое решение которого позволяет определить величину энергии активации реакции.
|
|
|
Методика выполнения опыта
В три пробирки налейте по 1 мл раствора Na2S2O3 и в каждую добавьте по 2 мл воды. В другие три пробирки налейте по 1 мл раствора H2SO4. В большой стакан налейте горячую воду (водяная баня), поставьте в водяную баню одну пробирку с раствором Na2S2O3 и одну пробирку с раствором H2SO4. Дайте растворам в пробирках прогреться в течение 1,5 мин, измерьте точно температуру водяной бани, запишите ее в таблицу 3.3. Далее, не вынимая пробирку с раствором Na2S2O3 из бани, вливаете прогретую кислоту в пробирку с раствором Na2S2O3. При сливании растворов включите секундомер и замерьте время появления голубоватого окрашивания (помутнения) раствора. Затем, разбавляя горячую воду в водяной бане холодной водой, понижайте температуру на 10 градусов. Поместите в баню следующую пару пробирок (с раствором Na2S2O3 и с раствором H2SO4), прогрейте и проведите те же действия, что и в первом случае. Третью пару пробирок поместите в водяную баню после понижения температуры (разбавлением холодной водой) еще на 10 градусов, прогрейте и проведите те же действия. Результаты опытов внесите в таблицу 3.3 и постройте график, откладывая по оси абсцисс – температуру, а по оси ординат относительную скорость (величину, обратную времени).
|
|
|
Рассчитайте средний температурный коэффициент реакции, используя правило Вант-Гоффа в заданном интервале температур. Расчет температурного коэффициента (коэффициента Вант-Гоффа - γ):
γ1 = ύ3/ ύ2, γ2 = ύ2/ ύ1, γсред = (γ1 + γ2)/2.
Для графического расчета энергии активации постройте зависимость
 и по тангенсу угла наклона прямой определите энергию активации данной реакции.
и по тангенсу угла наклона прямой определите энергию активации данной реакции.
Пример экспериментального определения энергии активации
1) во всех системах исследовался раствор тиосульфата натрия с концентрацией равной 1С и в каждую систему добавлялся раствор серной кислоты объемом 1 мл;
2) по соответствующей методике проводился эксперимент, данные которого приведены в таблице 3.1, интервал температуры между измерениями составлял 100C;
Таблица 7.4.1
Экспериментальные данные υ = f (Т) или ln (ύ) = f (1/Т)
| № системы | Температур | ( 1 / T )∙103 | Время (τ) появления голубого окрашивания, с | Относительная скорость ύ = 1/τ , с-1 | − ln (ύ) | |
| t,0C | T, K | |||||
| 1 | 70 | 343 | 2,91 | 3 | 0,333 | 1,11 |
| 2 | 60 | 333 | 3,00 | 6 | 0,166 | 1,78 |
| 3 | 50 | 323 | 3,10 | 12 | 10,11 | 2,45 |
3) на основании экспериментальных данных строится графическая зависимость ln(ύ) = f (1/Т) (рис. 1);
|
|
|
| 2,9 3,0 3,1 3,2 |
| (1/T)∙103 |
| 2,5 2,0 1,5 1,0 |
| 2,000 |
| 1,5 |
| 1,0 |
| α |
| а |
| b |
| −ln(ύ) |
| Рис. 1. Экспериментальная графическая зависимость ln(ύ) = f (1/Т) |
R – газовая постоянная равна 8,31∙10-3 кДж/моль.
Тангенс α рассчитываем, как отношение противолежащего катета к прилежащему в выделенном на графической зависимости прямоугольном треугольнике: tg α = а/ b, где а и b определяются по графику. В данном примере:
а = −( ln(ύ)max − ln(ύ)min)
а = −(2,45−1,11) = − 1,34.
b = [(1/Т) max − (1/Т) min] = [3,1 – 2,91]∙10-3 = 0,19∙10-3,
tgα = − 1,34/0,19∙10-3 = −7,05∙103, − ЕА/R = − 1,34/0,19∙10-3.
Энергия активации будет равна: ЕА =7,05∙103∙8,31∙10-3=58,58 кДж/моль.
Дата добавления: 2018-11-24; просмотров: 262; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
