Хімічні реактиви, прилади та посуд
Реактиви:
· сірка - 50 г;
· гідроксид натрію NaOH - 20 г;
· вата гігроскопічна -10г;
· оксид магнію -10 г;
· діхлоретан -10г;
· соляна кислота - 20 мл;
· бензол - 20 мл;
· вуглець чотирихлористий - 20 мл;
· сірчана кислота - 20 мл;
· ацетон - 20 мл;
· оцтова кислота -20 мл.
Прилади та посуд:
· тришийкова колба;
· зворотний холодильник;
· мішалка;
· реостат;
· електричний мотор;
· водяна баня;
· електроплита;
· штатив - 1 шт.;
· фарфорова чашка - 3 шт.;
· краплинна лійка - 1 шт.;
· лійка з коротким носиком - 2 шт.;
· колби V = 100 мл - 10 шт.;
· термометр - 2 шт.;
· ваги технічні.
Опис лабораторної установки
На рисунку 11.1 зображено лабораторну установку, яка складається з круглодонної колби 1, водяної бані 2, мотора з мішалкою 3, краплинної лійки 4, зворотного холодильника 5, термометра 6.
Розчин тетрасульфіду заливають у колбу 1, маса підігрівається на водяній бані 2 до температури 70°С. При діючій мішалці з краплинної лійки 4 доливають діхлоретан у присутності диспергатора - оксиду магнію. Одержується тіокол.
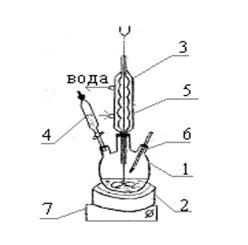
1– круглодонна тришийкова колба; 2-водяна баня ; 3- мішалка;
4 - краплинна лійка; 5 - зворотний холодильник; 6 – термометр; 7 - електрична плита
Рисунок 11.1 - Лабораторна установка
Послідовність виконання роботи
Перший етап роботи полягає в приготуванні розчину тетрасульфіду натрію Na2S4. Він утворюється при нагріванні сірки з концентрованим розчином їдкого натру
|
|
|
6 NaOH + 10 S  2 Na2S4 + З Н2О + Na2S2O3 (11.5)
2 Na2S4 + З Н2О + Na2S2O3 (11.5)
Для цього приблизно 48-52 см заздалегідь підігрітої води швидко доводять до кипіння в фарфоровій чашці і потім обережно додають 15,5 г їдкого натру. В одержаний розчин порціями додають раніше розраховану кількість сірки, помішуючи вміст чашки до повного розчинення. Утворений прозорий розчин бурого кольору після охолодження до 30-40°С фільтрують через гігроскопічну вату, поміщену в лійку з коротким носиком. Профільтрований розчин заливають в тришийкову крутлодонну колбу 1 і на водяній бані нагрівають до 70°С.
Після досягнення вказаної температури в колбу через один з отворів вводять як диспергатор оксид магнію (2% від усієї реагуючої маси, їдкий натр + сірка) і далі при ретельному перемішуванні мішалкою 3 додають
10 см3 дихлоретан ( температура його кипіння - 82-84°С). Подачу здійснюють з швидкістю 8-10 крапель на хвилину при температурі близько 70°С (якщо потрібно, в водяну баню додають холодну воду, але потім, в кінці реакції, її знову підігрівають).
Після закінчення процесу весь вміст колби виливають у чисту фарфорову чашку, промивають теплою водою (температура 40-50°С), 2-3% розчином соляної кислоти об'ємом 20 см3 (до нейтральної реакції за лакмусом) і потім знову (3-4 рази) теплою водою. Тіокол висушують при температурі 18-20°С і за зваженою масою визначають його вихід.
|
|
|
Далі одержаний тіокол випробовують на стійкість різними розчинниками.
Для цього під тягою до пробірки з 1-2 cmj розчинника вносять 0,2 г тіоколу і спостерігають його стійкість,відмічаючи через 15-20 хв. в таблиці "++" - якщо розчиняється, "+" - якщо набухає, "-" - якщо не змінюється. Для досліду беруть такі розчинники:
1) чотирихлористий вуглець;
2) ацетон;
3) оцтову кислоту;
4) розчин сірчаної кислоти 5, 10, 20%;
5) розчин соляної кислоти 5,10, 20%;
6) розчин їдкого натру 5%.
Одержані дані заносять в таблицю.
Опрацювання результатів
1. В результаті проведеної роботи при взаємодії тетрасульфіту натрію та дихлоретану одержують полісульфідний каучук - тіокол.
2. Складають матеріальний баланс процесу.
3. У таблицю заносять отримані дані про дослідження тіоколу на стійкість в різних розчинниках.
| маса тіоколу | Час спостереження | назва розчинників | |||||
| m,г |  ,с ,с
| 1 | 2 | 3 | 4 | 5 | 6 |
|
|
|
6. Вимоги до звіту
1. У звіті коротко викладають теоретичні основи реакції поліконденсації і утворення полісульфідних каучуків.
2. Наводять схему і опис лабораторної установки, послідовність виконання роботи.
3. Слід зробити всі необхідні виміри, одержані результати опрацювати і занести в таблицю.
4. Скласти матеріальний баланс процесу.
5. В кінці звіту необхідно зробити висновок про виконану роботу.
7. Техніка безпеки
1. Необхідно додержуватися обережності при роботі з кислотами та лугами.
2. Роботу вести при ввімкненій витяжній вентиляції.
3. Додержуватися техніки безпеки при роботі з розчинниками.
4. Обережно поводитися з електричними приладами та нагрівальною банею.
5. Після виконання роботи здати лаборанту робоче місце в чистоті.
8. Контрольні питання
1. Синтез каучуків, реакція поліконденсації.
2. Дві групи каучуків, їх властивості.
3. Тіоколові каучуки.
4. Процес одержання тіоколових каучуків.
5. Властивості тіоколів.
9. Література
1. Мухленов И.П. Практикум по общей химической технологии. - М. Высшая школа, 1979. - 421 с.
2. Мухленов И.П. Общая химическая технология. - М: Вьісшая школа, 1984.- 256 с.
|
|
|
3. Загальна хімічна технологія: Підручник / В.Т. Яворський, Т.В. Перекупко, З.О. Знак, Л.В. Савчук. – Львів: Видавництво Національного університету „Львівська політехніка”, 2005. – 552 с.
ЛАБОРАТОРНА РОБОТА №12
Дата добавления: 2018-08-06; просмотров: 182; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
