Гемолитическая болезнь – смотри в 1 вопросе
Рант-болезнь развивается у новорожденных животных после трансплантации им во время эмбрионального развития или в период новорожденности гомологичных кроветворных тканей от взрослых организмов
Механизм развития патологического процесса обусловлен несколькими моментами: иммунологической незрелостью эмбрионов и новорожденных организмов, в силу которой чужеродный трансплантат не может быть отторгнут; способностью пересаживаемых клеток к приживлению и размножению; наличием в пересаживаемой ткани иммунологически активных лимфоидных клеток. Колонизация донорскими клетками организма иммунологически инертного новорожденного заканчивается иммунологической реакцией пересаженных клеток против тканей реципиента (реакция «трансплантат против хозяина»). Синдром рант-болезни складывается из нескольких типичных проявлений: 1) отставание в росте и развитии, резкое истощение, диарея; 2) дерматиты с поражением кожных придатков; 3) резкие нарушения в кроветворной системе: пролиферация, а затем атрофия лимфоидной ткани, анемия, фокальные некротические изменения, выраженная спленомегалия.
32 Механизм образования белого тромба
Белый тромб называется также серым, агглютинационным, поскольку в нем преобладают агглютинированные тромбоциты, а также фибрин и лейкоциты. Микроскопически нем различают в преимущественно тромбоциты, образующие многоэтажные балки, напоминающие ветвления кораллов и волокнистые , сетчатые, грубозернистые массы, положительно окрашивающиеся на фибрин. Макроскопически белый тромб имеет белую или серую окраску, спаен со стенкой сосуда, поверхность его гофрированная, консистенция сухая, крошащаяся. Локализуется в артериях и полостях сердца — между трабекулярными мышцами, на створках клапанов. Образуется медленно при быстром токе крови.
|
|
|
Стадии образования:
1. Повреждение эндотелия и первичный спазм сосудов. Спазм: секреция эндотелиоцитами эндотелинов Высвобождение Са++ Торможение синтеза NO (стимуляция гемостаза) (сужение сосудов) • Повреждение эндотелия сопровождается обнажение субэндотелиальных тканевых структур, в частности, коллагена.
2. Адгезия тромбоцитов к участку деэндотелизации.
• Под действием коллагена и содержащегося в субэндотелии фактора Виллебранда происходит быстрая активация тромбоцитов, которые, изменяя свою форму, набухая и образуя шиповидные отростки, адгезируют к волокнам соединительной ткани по краям раны.
• Фактор Виллебранда образует своеобразные мостики между коллагеном субэндотелия сосудов и рецепторами (Iв) тромбоцитов. Адгезия тромбоцитов связана с взаимодействием трех компонентов:
|
|
|
• 1) специфических рецепторов мембран тромбоцитов (гликопротеина Ib, IIIа);
• 2) коллагена;
• 3) фактора Виллебранда и некоторых других белков (тромбоспондин, фибронектин).
3. Активация тромбоцитов и вторичный спазм сосудов. Тромбоциты активируются: • коллагеном (играет главную роль), • тромбином (активирует фосфолипазу С ИТФ Са++) норадреналином Активируются ферменты: гликозилтрансфераза, фосфолипаза А 2, которая запускает реакции высвобождения арахидоновой кислоты и образование из нее простагландинов PGG 2 и PGH 2, из которых в тромбоцитах образуется тромбоксан А 2, обладающий мощным агрегирующим и сосудосуживающим эффектом(вторичный спазм сосудов).
4. Агрегация тромбоцитов. (обратимая фаза – 2 мин, необратимая → выход серотонина, адреналина, тромбоксана А 2) Под влиянием аденозиндифосфата (АДФ), Тх. А 2, катехоламинов и серотонина, выделяющихся из поврежденных клеток, а также коллагена повышается способность тромбоцитов к агрегации.
5. Ретракция – образование белого тромба. Образуется в результате агрегации тромбоцитов. Участвует тромбостенин – сократительный белок тромбоцитов, который обеспечивает сближение тромбоцитов и уплотнение тромба.
|
|
|
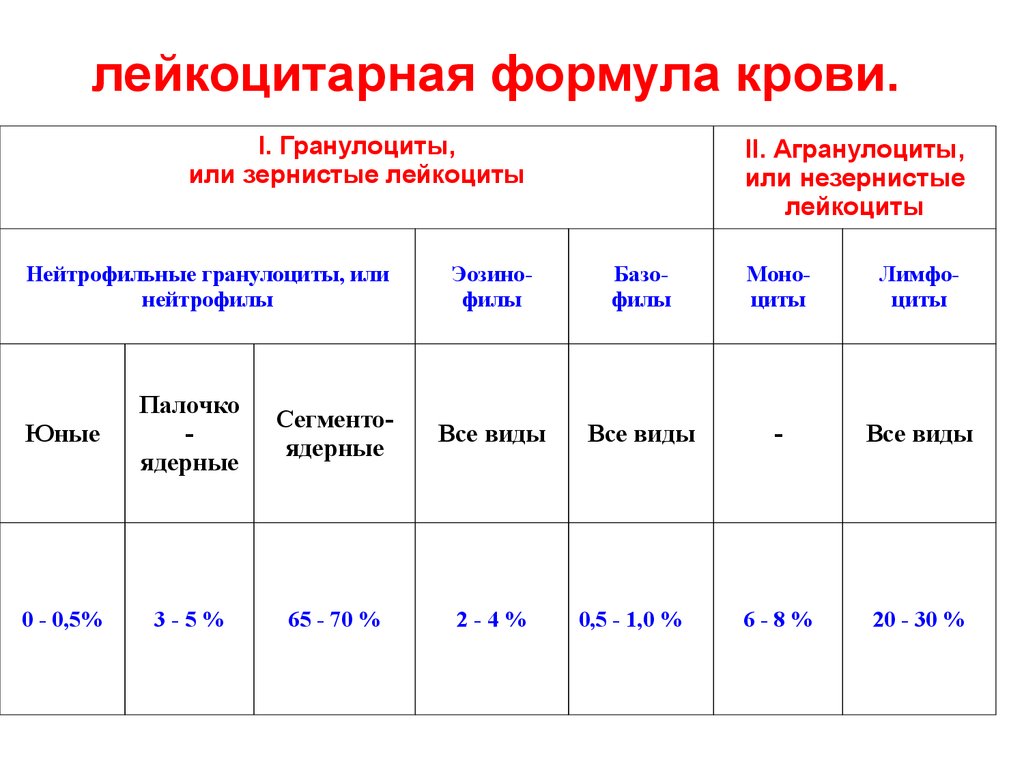
33 Виды лейкоцитов, формула крови
34 Почему развивается тромбогеморагический синдром?-смотри 5 вопрос
35 Картина крови при железодефицитной анемии
Картина крови. ЖДА -анемия с эритробластным типом кроветворения. гипохромная (ЦП составляет 0,6 и менее, до 0,4). Количество гемоглобина снижено в большей степени, чем количество эритроцитов, которое может быть в пределах нормы в начальной стадии развития ЖДА . Для мазка крови характерны гипохромия, ''тени'' эритроцитов, наличие анулоцитов, микроцитоз, пойкилоuитоз. Количество ретикулоцитов зависит от регенераторной способности эритроцитарного ростка, но чаще это гипорегенераторная анемия.
36 Механизм возникновения красного тромба
32 вопрос + красный тромб, помимо тромбоцитов и фибрина, содержит большое число эритроцитов, образуется быстро при медленном токе крови (обычно в венах)
37 Жировая эмболия эндогенного происхождения
Жировая эмболия наблюдается при попадании в кровь капель жира, преимущественно эндогенной этиологии (вследствие раздробления трубчатых костей, повреждения подкожной или тазовой клетчатки, жирового перерождения печени). С возрастом в результате замещения красного костного мозга трубчатых костей желтым и увеличения содержания в нем жиров с низкой температурой плавления опасность возникновения жировой эмболии возрастает. Поскольку источник эмболии локализуется преимущественно в бассейне вен большого круга кровообращения, жировая эмболия развивается, прежде всего, в сосудах малого круга кровообращения. Лишь со временем возможно проникновение капель жира через легочные капилляры (или артериовенозные анастомозы малого круга кровообращения) в левую половину сердца и артерии большого круга кровообращения. Количество жира, которое может вызвать смертельную жировую эмболию, у различных видов животных составляет от 0,9 до 3 мл/кг.
|
|
|
38 Картина крови при хроническом миелолейкозе
Картина крови: Хронический миелолейкоз характеризуется увеличением количества нейтрофильных rранулоцитов (метамиелоцитов, палочкоядерных, сегментоядерных) с ядерным сдвигом лейкоцитарной формулы влево до миелоцитов, промиелоцитов и единичных миелобластов. Может увеличиваться количество эозинофильных и базофильных rранулоцитов (эозино-базофильная ассоциация). Наблюдаются дегенеративные изменения клеток. В терминальной стадии наступает бластный криз, при котором в крови резко возрастает количество бластных клеток миелобластов и недифференцированных бластов.
39 Пути движения эмболов
Пути движения эмболов:
1) ортоградная эмболия - эмбол движется по току крови.
2) ретроградная эмболия-против тока крови из-за его тяжести.
3) парадоксальная эмболия - эмбол проходит из вен большого круга кровообращения в артерии большого круга кровообращения через дефекты в перегородках сердца, исключая малый круг кровообращения
40 Факторы тромбообразования
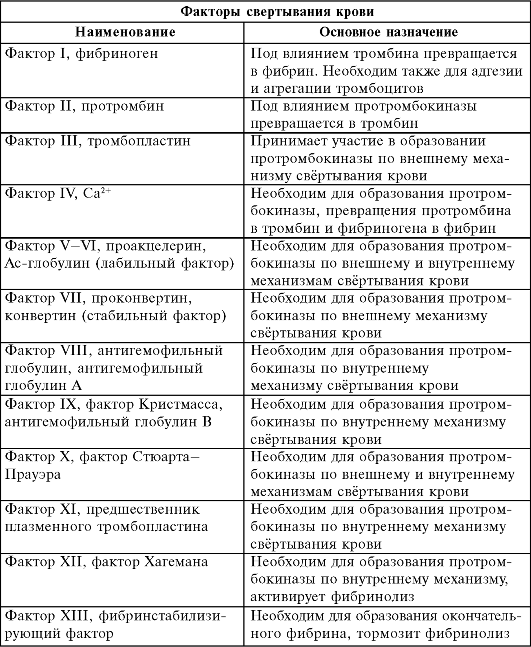
МОЖНО СКАЗАТЬ СЛЕДУЮЩЕЕ:
МЕСТНЫЕ. 1Изменения сосудистой стенк. При выработке эндотелием противосвертывающих факторов тромбоза не происходит. Особым противосвертывающим фактором является простациклин. Он препятствует склеиванию тромбоцитов. Повреждение эндотелия ведет к тромбообразованию. 2Замедление тока крови и 3 Нарушение тока крови способствуют тромбообразованию. Обычно эти факторы сопровождают такие патологические процессы, как-то: аневризмы сосудов и сердца, варикозные расширения вен, чаще на ногах, ослабление сердечной деятельности.
ОБЩИЕ. 1 Нарушение регуляции гемостаза. Это изменение соотношения между свертывающей и противосвертывающей системами. Причины:1)инфекции, аутоаллергия, интоксикация, неправильное лечение при использовании коагулянтов и антикоагулянтов. 2 Изменения качества крови. Это: увеличение грубодисперстный фракций белка, увеличение количества тромбоцитов, увеличение вязкости крови. Причины: лейкозы, атеросклероз, ревматические болезни, лекарства, стероиды, контрацептивы.
Сердечно-сосудистая система
1 Виды сердечной недостаточности
Различают три патофизиологических варианта сердечной недостаточности.
1. Сердечная недостаточность от перегрузки, развивающейся при: болезнях, которые обусловливают усиленный приток крови к сердцу или определенному его отделу (например, порок сердца или чрезмерная физическая нагрузка, артериовенозные фистулы); повышение сопротивления сердечному выбросу при гипертензии в сосудах большого или малого круга кровообращения или стенозирующих пороках сердца.
2. Сердечная недостаточность вследствие повреждения миокарда, вызванная инфекцией, интоксикацией, гипоксией, авитаминозом, нарушением венечного кровообращения, физическим и психическим перенапряжением, некоторыми наследственными дефектами обмена. В таких случаях недостаточность развивается даже при нормальной или уменьшенной нагрузке на сердце.
3. Смешанная форма сердечной недостаточности, возникающая при сочетании повреждения миокарда и его перегрузки (например, при ревматизме, который характеризуется комбинацией воспалительного повреждения миокарда и нарушением клапанного аппарата сердца). Такой вариант сердечной недостаточности наблюдается и в тех случаях, когда вследствие дистрофических изменений или гибели части мышечных волокон сердца на остальные приходится повышенная нагрузка.
2 Особенности инфаркта миокарда на ЭКГ
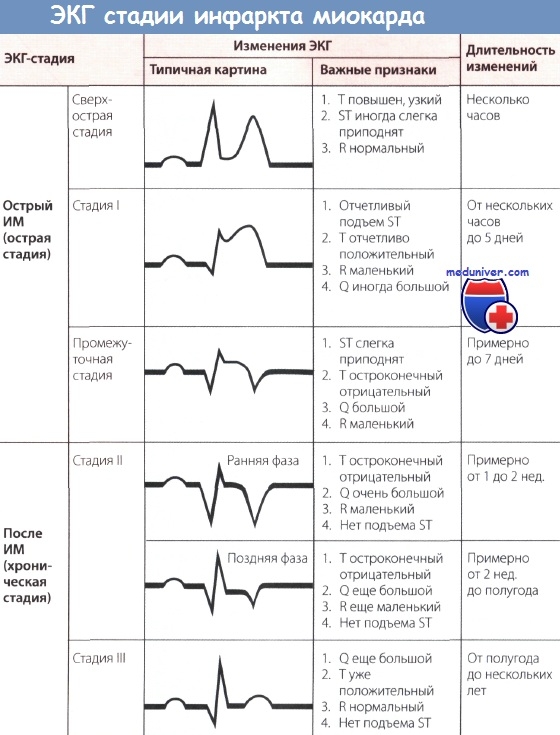
3 Некоронарные механизмы развития ИБС
Некоронароrенные повреждения сердца. Если повреждение миокарда непосредственно не связано с нарушением его кровоснабжения по коронарным сосудам, то такое повреждение называется некоронарогенным. Сушествует множество клинических причин, перечисленных выше, и несколько экспериментальных модели некроза сердечной мышцы, развитие которого не связано с патологией сосудов сердца.
Так, гипоксический некроз миокарда может быть воспроизведен с помощью различных видов гипоксии экзогенной, гемической, тканевой. Возникновению некроза при гипоксии способствует дополнительная физическая нагрузка ил11 эмоциональное возбуждение с активацией симпато-адреналовой системы (например, стрессовая ситуация у человека или фиксация животных в неудобной позе).
Электролитно-стероидная кардиопатия с некрозом. Согласно наблюдениям Селье, при введении крысам большого количества солей натрия в сочетании с некоторыми анионами (сульфатами, фосфатами) в сердце образуются очаги повреждения дегенеративно-некротического характера, которые часто сопровождаются гиалинозом сосудов других органов. Эти повреждения распространяются или возникают после использования меньшего количества солей, если одновременно вводятся некоторые стероидные гормоны надпочечников. На таком фоне легче развиваются повреждения сердца, обусловленные другими причинами, а также наблюдается более тяжелое их течение. Например, даже невысокие дозы норадреналина, производных кальциферола, гипоксия, мышечное напряжение или, наоборот, значительное ограничение подвижности приводят к распространению некроза миокарда. Соли калия и магния при этом оказывают защитное действие.
Иммунные повреждения сердцавозможны после введения в организм экспериментальных животных гетерогенной сыворотки, содержащей антитела к белкам сердечной мышцы животных данного вида (кардиоцитотоксины). Доказано также.что в организме могут образовываться антитела и сенсибилизированные лимфоциты, повреждающее действие которых направлено против тканей собственного сердца. Этому способствует проникновение в кровь денатурированных компонентов некротизированных сердечных миоцитов. Повреждение сердца могут обусловливать и циркулирующие иммунные комплексы антиген антитело комплемент.
Активация пероксидного окисления липидов кардиомиоцитов может быть следствием избытка прооксидантных Fe2+ Mn2+ Cu2+ Cd2+ Со2+ Ni2+ РЪ2+ или недо- ' ' ' ' ' ' статка антиоксидантных Zn2+ и Se2+ (см. главу XII ''Патологическая физиология обмена микроэлементов'') и/или дефицита витаминов С, Р, Е и группы В (с?-1. главу XIII ''Патологическая физиология обмена витаминов'').
4 Патогенез первичной гипертензии
В зависимости от того, увеличение какого из двух параметров (Q или R) способствует повышению артериального давления, различают следующие гемодинамические типы первичной артериальной гипертензии: 1) гиперкинетический увеличенный Q, не измененный или несколько сниженный R; 2) эукинетический - увеличение как Q, так и R; 3) гипокинетический значение Q не изменено или несколько уменьшено, R резко повышено. Вторичная артериальная гипертензия также может иметь различные гемодинамические типы. Например, гипертиреоз вследствие усиления работы сердца под влиянием тиреоидных гормонов и, соответственно, увеличения Q соответствует гиперкинетическому типу. Гипотиреоз, наоборот, сопровождается отложением мукополисахаридов в стенке артериол, их сужением, повышением R, ослаблением сердечной деятельности и уменьшением Q, что соответствует гипокинетическому типу. Следует отметить, что на начальном этапе первичной артериальной гипертензии в молодом и среднем возрасте основным ее признаком является повышение артериального давления, обусловленное не увеличением сосудистого тонуса, а усиленнои сократительнои деятельностью миокарда, что соответствует гиперкинетическому типу артериальной гипертензии. При дальнейшем развитии заболевания гиперкинетический тип переходит в эукинетический и гипокинетический. На вопрос, касается ли это так называемой изолированной систолической артериальной гипертензии, возникающей у лиц пожилого возраста (после 65 лет) на фоне сниженной эластичности сосудов, в настоящее время утвердительно ответить невозможно. Наследственная, стрессорная или центрально-ишемическая гиперактивация симпатической нервной системы непосредственно и в результате стимуляции секреции мозговым веществом надпочечников норадреналина и адреналина посредством воздействия на 131 -адренорецепторы миокарда повышает частоту v и силу сердечных сокращении, а с помощью влияния на а-адренорецепторы вызывает спазм неисчерченных мышц артерий, что повышает периферическое сопротивление в некоторых органах. Благодаря одновременному сосудорасширяющему действию адреналина на 132 -адренорецепторы сосудов скелетных мышц, которые представляют большую часть сосудов тела, активация симпатоадреналовой системы приводит к увеличению мое при практически неизмененной величине ОПС. Кроме того, симпатоадреналовая система через а-адренорецепторы стимулирует вазоконстрикцию вен, увеличивая приток венозной крови к сердцу. Благодаря влиянию на 131 -адренорецепторы гранулярных клеток юкстагломерулярного аппарата почек гиперактивация симпатического отдела нервной системы стимулирует секрецию ренина, который активирует РААС и, соответственно, почечную реабсорбцию натрия и воды. Посредством активации а1 -адренорецепторов симпатоадреналовая система стимулирует Nа+,Н+-противопереносчики на апикальной мембране нефроцитов, что непосредственно усиливает реабсорбцию натрия в проксимальных канальцах нефрона. Все это вызывает гиперволемию иувеличивает приток крови к сердцу. Однако сильнее всего ОЦК увеличивается при наследственной или приобретенной стимуляции РААС. Наиболее значимую роль в кардиоваскулярной патологии играет ангиотензин II . Он может быть как циркулирующим гормоном компонентом РААС, так и местным медиатором, который продуцируется многими тканями, в том числе сердцем и сосудами, в ответ на их повреждение. Ангиотензин II посредством АТ1 -рецепторов повышает вазомоторный тонус вследствие прямой стимуляции сокращений гладких мышц сосудов, угнетения высвобождения эндотелием NO и простациклина, а также инициации выработки эндотелиоцитами мощного вазоконстриктора эндотелина. Ангиотензин II непосредственно стимулирует реабсорбцию натрия в проксимальных канальцах и посредством активации секреции альдостерона клубочковой зоной коркового вещества надпочечников увеличивает реабсорбцию натрия в собирательных трубках. Усиленный приток крови в правое предсердие приводит к повышению чес и без предварительной активации симпатической нервной системы. Часть данного эффекта обусловлена прямым растяжением и раздражением атипичных клеток синусно-предсердного узла, однако бульшая роль в ускорении сердечных сокращений прина,цлежит развитию рефлекса Бейнбриджа: предсердные рецепторы растяжения посьmают импульсы по афферентным волокнам блуждающего нерва в продолговатый мозг, а эфферентные сигналы передаются по симпатическим нервам к сердцу, что повышает частоту и силу сердечных сокращений. Кроме того, чрезмерное наполнение левого желудочка и его растяжение по закону Франка Старлинга (гетерометрический механизм компенсации) дополнительно увеличивает силу сердечных сокращений и УОС. Все это повышает МОС и артериальное давление по гиперкинетическому типу. У здорового человека (при отсутствии нарушений нейроэндокринной регуляции и функции почек) непрерывно осуществляется контроль системного артери - ального давления. Так, внезапное повышение тонуса симпатического отдела нервной системы и артериального давления при психической или физической нагрузке вызывает раздражение синокаротидных и аортальных барорецепторов, импульсы от которых по афферентным волокнам языкоглоточного и блуждающего нервов поступают в продолговатый мозг, где обусловливают торможение тонической активности симпатических сосудосуживающих нервов и возбуждают парасимпатические центры блуждающих нервов. В результате этого происходит расширение артериол и вен в периферических отделах большого круга кровообращения, u уменьшение частоты и силы сердечных сокращении, что снижает артериальное давление. Если же фактор повышения артериального давления продолжает действовать более 1 2 сут. , барорецепторы привыкают к повышенному давлению, перестраиваются и начинают воспринимать высокое давление как нормальное . Длительный контроль артериального давления невозможен без нормального функционирования почек и их адекватной нейрогормональной регуляции, поскольку постоянство давления зависит от поддержания постоянного объема крови, который в свою очередь определяется способностью почек обеспечить нормальный уровень натрия и воды в организме с помощью вышеописанных механизмов (см. главу XI ''Нарушение водно-элек1ролитного обмена''). Если же из-за наличия наследственных или приобретенных нарушений защитные рефлекторные механизмы не способны быстро восстановить нормальный уровень артериального давления, то в этом случае артериальная гипертензия приобретает хроническое течение. На втором этапе патогенеза первичной гипертензии хроническое повышение артериального давления приводит к вазоконстрикции, повреждению сосудистой стенки с ее дальнейшим перманентным утолщением (ремоделированием), сужением просвета артериол и повьп11ением периферического сопротивления (см. схему 20). Это соответствует закону Лапласа: Т = Р · r, который гласит, что напряжение сосудистой стенки (Т) прямо пропорционально давлению (Р) в сосуде и его радиусу (r). Согласно данному закону, если в кровеносных сосудах повышается артериальное давление, то для сохранения целостности сосудистой стенки и обеспечения нормального обмена веществ, который прямо зависит от постоянства Т, необходимо уменьшить r. Эти теоретические соображения подтверждаются законом Остроумова Бейлиса, сформулированным на основании клинических наблюдений, который гласит, что повышение артериального давления приводит к генерализованному спазму артериол и росту ОПС. Это обеспечивает постоянство кровотока в периферических органах и тканях и предотвращает разрыв мелких сосудов. Сужение артериол происходит поэтапно благодаря следующим механизмам. Увеличение сердечного выброса и резкое повышение артериального давления, v сопровождающиеся ускорением кровотока, согласно миогеннои теории ауторегуляции кровотока приводят к растяжению гладкомышечных клеток стенки артерий и артериол, что по закону Франка Старлинга вызывает их дальнейшее спазмирование, уменьшение радиуса сосудов, повышение ОПС и уменьшение скорости кровотока до нормального уровня. Механизм усиленного сокращения после предшествующего растяжения как неисчерченных мышц, так и кардиомиоцитов, по современным представлениям, связан с быстрым поступлением кальция из внеклеточной жидкости в саркоплазму вследствие активации механозависимых кальциевых каналов сарколеммы. Пролонгированное и значительное повышение артериального давления вызывает повреждение сосудистой стенки, тем самым стимулируя местное образование и секрецию ангиотензина 11 и эндотелина- 1 мощных вазоконстрикторов. Кроме того, как стало известно в последнее время, они являются факторами роста, которые стимулируют миграцию, гипертрофию и гиперплазию гладкомышечных клеток и фибробластов сосудистой стенки, синтез ими коллагена, эластина, протеогликанов, что приводит к утолщению медии и интимы. Ангиотензин ll также обусловливает возникновение гипертрофии и фиброза миокарда после ишемического его повреждения или в ответ на постоянное повышение артериального давления. Пролиферативное утолщение артериол значительно усиливается при наличии инсулинорезистентности, поскольку гипергликемия дополнительно повреждает эндотелий, а избыток инсулина является фактором роста. Гипертен - зивное и гипергликемическое повреждение эндотелия также вызывает прилипание к сосудистой стенке тромбоцитов и моноцитов с развитием воспалительного процесса, сопровождающегося отеком и пролиферацией фибробластов интимы сосудов. Пролиферативное утолщение медии и интимы оставляет артериолы перманентно суженными, независимо от наличия или отсутствия стимулов, обусловливающих вазоконстрикцию. С этого момента ОПС постоянно повышено, а артериальная гипертензия приобретает признаки эукинетического, а после гипертрофии миокарда, кардиосклероза и истощения сердца гипокинетического типа.
5 Первичная гипотензия
В происхождении нейроциркуляторной (первичной) артериальной гипотензии ведущим этиологическим и патогенетическим фактором служит перенапряжение основных процессов коры головного мозга (возбуждение и торможение). Тем не менее, в отличие от первичной артериальной гипертензии, преобладают процессы торможения с распространением на подкорковые вегетативные структуры, в частности сосудодвигательный центр.
Ослабление в результате этого эффективных сосудосуживающих влияний на фоне свойственного астеническому типу конституции преобладания холинергических процессов над адренергическими является непосредственнои причинои снижения тонуса резистивных сосудов, периферического сопротивления и артериального давления. Определенную роль в развитии первичной артериальной гипотензии играют приобретенные и наследственные нарушения продукции и рецепции физиологически активных веществ вазоконстрикторного действия (катехоламинов, вазопрессина, ангиотензина 11, эндотелинов, ПГF2", тромбоксана А,_ и др.), с одной стороны, и гиперпродукция NO и простациклина с другой. Кроме того, повышенное количество NO в эндотелии усиливает эффекты эндотелийзависимых вазодилататоров (ацетилхолин, брадикинин и т. д.).
6 Стадии гипертрофии миокарда
Дата добавления: 2018-08-06; просмотров: 624; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
