СПОСОБЫ ПОЛУЧЕНИЯ ПОДСЛАЩИВАЮЩИХ ВЕЩЕСТВ
Производство одного из первых синтетических подслащивающих веществ — сахарина — было организовано еще в 1884 г. Натриевая соль сахарина обладает сладким вкусом, превосходящим сахарозу в 500 раз; она хорошо растворима в воде и в спирте. Сахарин прошел проверку на токсичность и разрешен ФАО для применения во всех странах как синтетическое подслащивающее вещество в количестве 15мг/кг при производстве кондитерских изделий, диетических сыров, напитков для больных диабетом или соответственно 2,5 мг на 1 кг массы взрослого человека в сутки.
В настоящее время сахарин вытесняется новыми низкокалорийными сахарозаменителями: пептидами, получившими название (по одной формирующей их аминокислоте) аспартамов:
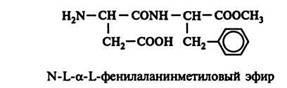
Сладкие дипептиды — аспартамы индифферентны к микроорганизмам и могут быть использованы как пищевые добавки. Они безопасны при потреблении диабетиками, не вызывают развитие кариеса зубов, нетоксичны, неканцерогенны и разрешены к использованию в пищу.
Аспартамы выпускают в гранулированном и порошкообразном виде и применяют для изготовления газированных и негазированных напитков, кондитерских изделий, жевательной резинки, джемов, повидла, конфитюров.
В пищеварительном тракте происходит гидролиз аспартама на две аминокислоты. Аспартам устойчив при комнатной температуре, в таких условиях не теряет стабильности в течение 5 лет. При нагревании выше 150 °С он распадается, поэтому аспартам возможно использовать при подслащивании продуктов, не требующих термической обработки, например мороженого и крема. Аспартам (торговое название Нутрисвит) широко используют при производстве диетических напитков.
Триптофан — незаменимая аминокислота, в 25—50 раз слаще сахарозы. Его производные также обладают сладким вкусом, в том числе D-6-трифторметилтриптофан, D-6-хлортриптофан (в 1300 раз слаще сахарозы) и др.
За рубежом широко используют различные синтетические сахарозаменители с высоким коэффициентом сладости (ацесульфам-К, цикламаты, перилартин, отизон, неотам и др.).
Таким образом, число подслащивающих веществ, используемых в производстве продуктов питания, достаточно велико. Природные подслащивающие вещества в основном безопасны для здоровья человека, использование же синтетических требует тщательной дозировки и ограниченного применения.
Биотехнологическими методами получен ряд весьма эффективных продуктов, заменителей сахарозы. Так, из растения Thaumatococcus damelli, произрастающего в Судане, в клетки Е. coli был трансплантирован ген, детерминирующий синтез сверхсладкого белка тауматина. Рекомбинантная бактерия стала продуцентом сладкого белка, который производят на нескольких биотехнологических заводах и применяют в пищевой промышленности в качестве искусственного подсластителя. Из южноамериканского растения Stevia rebaudiana в клетку Е. coli трансплантирован ген сладкого белка стевиозида. С помощью генной инженерии или путем совмещения микробного синтеза с химической трансформацией микробных метаболитов получен ряд эффективных подсластителей.
Рассмотренный ранее дипептид аспартам образован молекулами фенилаланина и аспарагиновой кислоты; обе молекулы можно синтезировать микробиологическим путем, а аспартам из этих мономеров — с помощью ферментов.
На основе фруктозы создается новый класс подсластителей — заменителей сахарозы, фруктозилолигосахаридов, в состав которых входят от 2 до 5 остатков фруктозила. Они не разрушаются в организме человека, имеют сладкий вкус и безвредны. Продуцируют их микроорганизмы, содержащие фруктозилтрансферазу (представители родов Aspergillus, Fusarium, Aureobasidium). Создан полунепрерывный биотехнологический процесс на основе иммобилизованных в геле альгината кальция (2%-го) клеток Aureobasidium pullulans. Клетки продуцента осуществляют конверсию сахарозы в течение 60 сут при температуре 50 °С, рН 5,5 и скорости протока 0,05 ч-1. Выход фруктозилолигосахаридов составляет 55 %.
Перспективным направлением является использование гидролизатов крахмала (мальтин, мальтодекстрин, мальтозная патока) в качестве сахарозаменителей в продуктах питания, особенно функционального назначения.
В технологиях этих продуктов, разработанных во ВНИИ крахмалопродуктов, используют картофельный и кукурузный крахмал.
Катализаторами процесса гидролиза крахмала являются амилолитические ферментные препараты как отечественного, так и зарубежного производства. На стадии разжижения крахмала применяют водный экстракт сухого ячменного солода, обладающий а-амилазной, β-амилазной и глюкоамилазной активностями. В качестве бактериальной ос-амилазы используют отечественный ферментный препарат Амилосубтилин Г10Х, обладающий также небольшой протеолитической, β-глюканазной и глюкоамилазной активностями. На стадии ферментативного осахаривания разжиженного крахмала применяют водный экстракт ячменного солода, а также ферментный препарат Spezyme BBA.
При применении экстракта ячменного солода получают мальтозную патоку с низким содержанием глюкозы и высоким содержанием мальтозы. Однако при этом цветность гидролизатов возрастает в связи с увеличением в гидролизате массовой доли белка до 0,45 %. При применении ферментного препарата Spezyme BBA снижается продолжительность осахаривания, в гидролизате содержится значительно меньше глюкозы — соответственно ее массовой доле в разжиженном крахмале.
Согласно разработанным техническим условиям на мальтозную патоку возможно получение трех видов этого продукта, отличающихся углеводным составом, %:

Мальтозная патока с низким содержанием глюкозы (марки А) менее гигроскопична, чем карамельная патока, что обусловливает ее применение в кондитерском производстве для получения твердой карамели.
Мальтозную патоку марки Б используют как патоку специального олигосахаридного состава при производстве детского питания на молочной основе. Этот компонент играет двоякую роль: как подсластитель (заменитель свекловичного сахара) и как хорошая питательная среда для бифидобактерий.
Мальтозная патока усваивается организмом с меньшей скоростью, чем глюкоза, благодаря чему достигается более равномерная гликемическая нагрузка на организм, т. е. поддерживается постоянный уровень глюкозы в крови.
В последние годы возрос интерес к изучению инулинсодержащих растений и созданию научных основ их переработки в связи с созданием диетических и лечебно-профилактических пищевых продуктов. Одним из нетрадиционных видов инулинсодержащего сельскохозяйственного сырья является якон. Это пищевая и кормовая культура горных районов Анд. Начало интродукции якона в России было положено в 1995 г. Корнеплоды якона содержат углеводы в форме полифруктозида — инулина и свободных моносахаридов — глюкозы и фруктозы.
Специфический фермент инулиназа катализирует расщепление гликозидных связей в инулине с образованием главным образом D-фруктозы. В связи с этим был исследован ферментативный гидролиз инулина, содержащегося в яконе, с помощью высокоактивного продуцента инулиназы штамма дрожжей Kluyveromyces marxianus Y-303, обладающего также высокой инвертазной активностью.
При оптимальных условиях (рН 4,5 и температуре 40 °С) фермент из дрожжей К. marxianus способен гидролизовать 95 % инулина до фруктозы. Полученные гидролизаты из якона могут быть применены для получения глюкозно-фруктозных сиропов, пюре, в качестве добавок и заменителя сахара при производстве хлебобулочных и кондитерских изделий.
БИОЛОГИЧЕСКИЕ КОНСЕРВАНТЫ
Особую группу пищевых добавок, замедляющих порчу пищевых продуктов, представляют антибиотики и другие продукты метаболизма микроорганизмов. Применение антибиотиков позволяет продлить срок хранения пищевого сырья и некоторых видов пищевых продуктов в 2—3 раза. Обычно антибиотики применяют для обработки свежих растительных продуктов путем их погружения в раствор антибиотика на короткий срок или орошения поверхности пищевого продукта раствором различной концентрации.
Однако использование антибиотиков человеком вместе с пищей может привести к нежелательным последствиям, в том числе к нарушению нормального баланса микроорганизмов желудочно-кишечного тракта.
Низин Q43H230O37S7 — один из немногих антибиотиков, разрешенный в небольших дозах для использования в пищевой промышленности. Он быстро разрушается ферментами пищевого тракта до аминокислот.
Использование низина позволяет получать пищевые продукты высокого качества с длительным сроком хранения. Обработка их сведена к минимуму, однако они не подвержены быстрой порче и не представляют опасности для здоровья человека. Минздравсоцразвития РФ разрешено применение низина в пищевой промышленности при изготовлении плавленых сыров, овощных продуктов, соков, грибов и консервированных супов, а также в хлебопечении.
Низин — антибиотик полипептидного типа с молекулярной массой около 7000. В его состав входят аминокислоты: лизин, гистидин, аспарагиновая кислота, лантионин, β-метиллантионин, пролин, глицин, аланин, валин, метионин, изолейцин, лейцин, дегидроаланин и β-метилдегидроаланин. Характерная особенность низина — наличие в его составе двух серосодержащих аминокислот: лантионина и β-метиллантионина, редко встречающихся в природе. В каждой молекуле низина содержится два остатка лантионина и восемь — β-метиллантионина.
По химической структуре низин представляет собой два спаренных кольца, каждое из которых состоит из 13 атомов, в том числе одного атома серы:
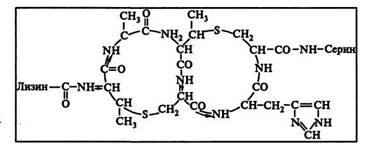
Антибактериальное действие низина обусловлено особенностями его химического состава и структуры. Отечественная промышленность выпускает препараты низина в виде сухого мелкого порошка. В таком виде при температуре 18...22 °С низин сохраняет активность в течение нескольких лет.
Низин продуцируется штаммами Lactococcus lactis, которые широко распространены в природе. По сравнению с другими антибиотиками он не обладает широким спектром действия на микроорганизмы. Подавляет развитие стафилококков, стрептококков, сарцин, бацилл и клостридий, прорастание спор. Механизм действия низина на микроорганизмы до конца не выяснен.
Наиболее благоприятная среда для биосинтеза низина — обезжиренное молоко. При использовании сыворотки вместо молока выход низина в 2 раза меньше. Добавление к сыворотке 25 % пепсинового гидролизата молочнокислых бактерий, картофельной патоки или глюкозы (2,5—5 %) способствует повышению выхода низина до 90 %.
Основные стадии технологического процесса получения низина представлены на рисунке 17.1.
Производственный посевной материал готовят в три стадии. Культуру выращивают сначала в обезжиренном молоке (300 см3) с содержанием сухих веществ до 8 % в течение 24 ч, на второй стадии — в 4000 см3 обезжиренного молока 22—24 ч, на третьей — в инокуляторе с 80 дм3 обезжиренного молока (рН 6,8—6,9) в течение 18—20ч.
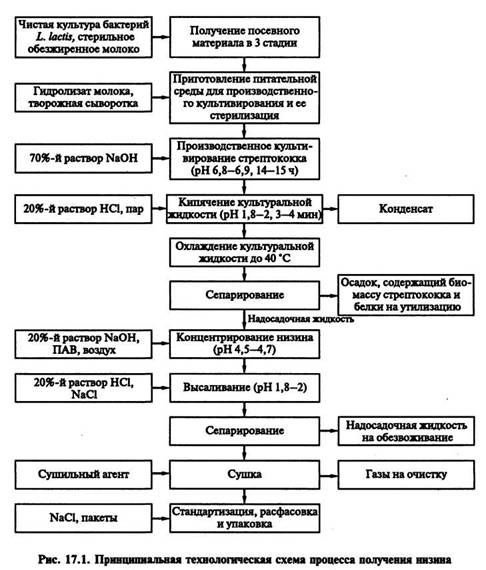
Готовый посевной материал представляет собой густую взвесь дипло- и стрептококков в свернувшемся обезжиренном молоке с рН 4,5—4,7, активность не ниже 50—60мкг/см3.
Производственное культивирование ведут на смеси гидролизата молока с творожной или сырной сывороткой в соотношении 1:2. Гидролизат получают в результате обработки 6%-го обезжиренного молока протеолитическим ферментом панкреатином при температуре 45 °С и рН смеси 8,1 в течение 24 ч.
В ферментере на питательной среде происходят рост и развитие низинобразующего молочнокислого стрептококка. При этом образуется молочная кислота, которая, закисляя среду, тормозит развитие микроорганизма и биосинтез низина. В связи с этим основным условием при выращивании культуры — продуцента низина — является поддержание рН питательной среды в пределах 6,8—6,9. Обычно выращивание культуры заканчивают за 14—15 ч. При этом активность должна быть не ниже 100 мкг/см3.
Культуральную жидкость подкисляют соляной кислотой до рН 1,8—2 и кипятят 3—4 мин. После охлаждения до 40 °С на сепараторе отделяют микробную массу и нерастворимые белки. Низин, содержащийся в нативном растворе, концентрируют флотационным методом. Для этого нативный раствор подщелачивают 20%-мраствором NaOH до рН 4,5—4,7, добавляют поверхностно-активное вещество типа Твин-80 и пропускают через раствор воздух в течение 2—2,5 ч при температуре 20...25 °С. Большая часть низина (от 50 до 100 %) выходит в пену. Собранную пену разбивают, в образующейся жидкости доводят рН до 1,8—2. Антибиотик высаливают сухой поваренной солью (25% объема жидкости) или осаждают ацетоном (5% объема жидкости).
Высоленный низин отделяют в виде пасты сепарированием или центрифугированием и высушивают в сублимационной сушилке до остаточной влажности 3,5—4 %. Пасту можно сушить в распылительной сушилке, если приготовить раствор с 4,5—5%-м содержанием сухих веществ. Потери активности при сушке незначительны.
После сублимационной сушки препарат измельчают до состояния пудры и стандартизируют NaCl до активности 0,6 • 106 ед/г. Препарат слабо растворяется в воде и хорошо растворяется в 0,02 н. НС1 при подогреве до 80 °С.
В присутствии низина терморезистентность спор микроорганизмов уменьшается, следовательно, можно понижать температуру или продолжительность стерилизации продукта, что положительно сказывается на его качестве.
Возможно консервирование растительных, мясных (говядина, свинина, конина, баранина) и рыбных продуктов путем использования в качестве консервантов неспорообразующих грамположительных бактерий рода Lactobacillus, например, L. plantarum, L. sake, L. curvatus и преимущественно L. casei, штамм LMGP-21007, вводимых в продукты при 2О...44°С в атмосфере воздуха или его смеси с СО2 и N2; при этом подавляются рост и развитие патогенной микрофлоры, например Enterococcus, Pseudomonas, Staphy-lococcus и др., и сохраняются внешний вид, цвет, вкус и другие органолептические характеристики продуктов [бактерии вводят в концентрациях (1—4)109ед/см3 в присутствии стабилизирующих веществ, %: декстрина — 5, пептона — 10, экстракта дрожжей - 0,2].
Известен способ предупреждения порчи пищевых продуктов (молока, йогурта, сыра, плодовых и овощных соков, приправ к салатам и т. д.) дрожжами, предусматривающий введение в продукт метаболитов, образуемых культурой Propionibacterium. Обезжиренное молоко пастеризуют при 87,8 °С в течение 45 мин и охлаждают до температуры 30 °С, после чего его подкисляют 85%-й молочной кислотой до рН 5,3 и инокулируют 0,5 % культуры Propionibacterium shermanii. Инокулируемое молоко термостатируют в течение 48 ч при слабом перемешивании и нейтрализуют NaOH до рН 7,0. Затем продукт пастеризуют при температуре 62,8 °С в течение 20 мин, охлаждают до 23 °С, фасуют в стерильную полимерную тару и замораживают. Эффективное предупреждение размножения дрожжей обеспечивается не пропионовой кислотой, а другими метаболитами Propionibacterium.
Глава 18 ПОДКИСЛИТЕЛИ
Подкислителями считаются пищевые кислоты, используемые как вкусовые добавки для придания продуктам «острого» вкуса и для сохранения пищи.
Главными пищевыми кислотами считаются четыре органические кислоты: лимонная, молочная, уксусная и винная (иногда к ним причисляют яблочную).
Несмотря на значительный прогресс в области органического синтеза, многие пищевые кислоты получают в настоящее время микробиологическим синтезом (табл. 18.1).

Продукты естественного брожения для пищевой промышленности более предпочтительны, чем синтетические кислоты, так как они безвредны для организма человека.
Для получения пищевых кислот используют как традиционные технологии, так и новейшие достижения биотехнологии.
ЛИМОННАЯ КИСЛОТА
Лимонная кислота (СН2СООН—СОНСООН—СН2СООН) — трехосновная оксикислота, кристаллизующаяся из водных растворов с одной молекулой воды в виде бесцветных, прозрачных кристаллов ромбической формы. Из всех пищевых кислот она обладает наиболее мягким вкусом и не оказывает раздражающего действия на слизистые оболочки желудочно-кишечного тракта. Регуляторами рН пищевых систем являются соли лимонной кислоты — цитраты натрия, калия, кальция, магния и аммония.
В природных условиях лимонная кислота встречается главным образом в незрелых плодах цитрусовых, ананасов, груш, инжира, брусники, клюквы и др. Первые заводы по производству кристаллической лимонной кислоты из природных источников — апельсинов и лимонов — были созданы в Италии в середине XIX в.
В настоящее время по объему производства лимонная кислота является одним их главных продуктов микробного синтеза. Ее общий выпуск в различных странах достигает 800 тыс. т в год.
Годовой прирост производства лимонной кислоты составляет 5 % существующего уровня. Около 70 % производимой лимонной кислоты используют в пищевой промышленности, 18—20 % — в виде ее соли, цитрата натрия, для изготовления экологически чистых моющих средств.
Многие органические вещества могут быть трансформированы микромицетами в лимонную кислоту, но ее максимальный выход достигается при биосинтезе из сахарозы или фруктозы.
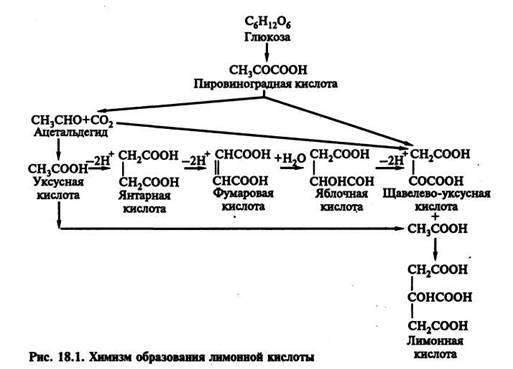
Химизм образования лимонной кислоты. Синтез лимонной кислоты связан с циклом дикарбоновых кислот и происходит в результате конденсации щавелево-уксусной кислоты, содержащей четыре атома углерода и две карбоксильные группы, с уксусной кислотой, имеющей два атома углерода и одну карбоксильную группу (рис. 18.1).
Промышленным способом лимонную кислоту получают из мелассы микробиологическим синтезом, применяя главным образом мутантные штаммы микроскопического гриба Aspergillus niger. Заводы малой и средней мощности производят лимонную кислоту поверхностным методом культивирования. Глубинный метод экономически выгоден, если мощность завода превышает 2500 т лимонной кислоты в год.
Меласса считается пригодной для производства лимонной кислоты поверхностным способом, если съем лимонной кислоты при контрольном сбраживании составляет не менее 1,25 кг/м2 в сутки, глубинным способом —10—12 кг/м3.
Хорошо сбраживаемые мелассы обычно содержат, %: инвертного сахара — не более 1, СаО — 1, SO2 — 0,06 при общем содержании сухих веществ не менее 75 и сахара более 46.
Производство лимонной кислоты включает следующие основные технологические стадии:
• получение посевного материала;
• подготовка мелассы к сбраживанию;
• сбраживание растворов мелассы в лимонную кислоту;
• отделение мицелия;
• выделение из сброженных растворов лимонной кислоты;
• получение ее в кристаллическом виде и высушивание. Тщательно проверенную на микробиологическую чистоту и биохимическую активность музейную культуру используют для приготовления посевного материала. Посевной материал размножают в пробирках с агаризованной средой (сусло-агар), а затем в колбах и кюветах — на твердой питательной среде. Длительность каждой стадии 2—7сут, оптимальная температура выращивания 32 °С.
В зависимости от способа сбраживания мелассу разбавляют и готовят растворы с различной концентрацией сахара: для поверхностного выращивания A. nigerjxo 13—15 %, для глубинного культивирования — 3—4 и 25—28 %. рН приготовленных растворов доводят H2SO4 до 6,8—7,5. Для выращивания продуцентов лимонной кислоты возможно использование крахмалосодержащего сырья. Предварительно осуществляют гидролиз крахмальной суспензии, содержащей 26—30% СВ, ферментным препаратом бактериальной а-амилазы, взятым в количестве 1,5—2,0 ед. амилолитической активности (АС) на 1 г СВ крахмала, при повышенной температуре и избыточном давлении. К гидролизату добавляют минеральные соли в виде сульфатов цинка, железа (II), меди в количестве (2,0—7,0)10-3 г/дм3 гидролизата крахмала.
Поверхностный способ. При этом способе выращивания A. niger подготовленную мелассу подают в варочный аппарат, где разбавляют кипящей водой в соотношении 1:1, рН раствора доводят до 6,8—7,2. При кипячении вводят раствор желтой кровяной соли для осаждения железа и солей тяжелых металлов с таким расчетом, чтобы избыток свободного ферроцианида, угнетающего развитие микроорганизма, не превышал 10мг%.
Для активного биосинтеза лимонной кислоты в питательной среде кроме сахара должно содержаться 0,07 % азота, 0,02 % Р2О5, а также цинк, магний, калий и другие микроэлементы, которые вводят в среду в виде солей. Готовая среда с температурой 45...50 °С поступает в бродильные камеры. Культивирование гриба осуществляют в кюветах из нержавеющей стали или алюминия, установленных на стеллажах. После предварительной стерилизации камер парами формалина, дегазации газообразным аммиаком и охлаждения до 30... 40 °С воздухом производят заполнение кювет питательной средой (толщина слоя от 8 до 18 см). В камере предусмотрена система вентиляции для подачи нагретого (до 30...32 °С) стерильного кондиционированного воздуха из расчета 3—18 м3/ч на 1 м2 поверхности кювет. В питательную среду через воздуховоды с помощью специального устройства для распыления вносят посевной материал из расчета 50—75 мг конидий на 1 м2 площади кюветы.
Наиболее эффективный режим культивирования — так называемый бессменный способ с доливом. Суть его заключается в том, что раствор мелассы в количестве 30—35% начального объема вводят под пленку гриба. Долив питательной среды производят один или несколько раз, начиная с четвертых-пятых суток роста, через каждые 36—48 ч. Добавляемый раствор мелассы содержит 8,5—11,0 % сахара и не имеет в своем составе питательных солей и антисептиков. Такой режим обеспечивает увеличение съема лимонной кислоты с 1 м2 бродильной поверхности на 15—20% и снижает удельный расход мелассы на 10—45% по сравнению с другими методами.
Брожение прекращают, когда в растворе остается 1—2 % сахара и общая титруемая кислотность в сброженном растворе достигает 12—20 %. Сброженный раствор сливают в сборник. Для промывки мицелия под грибную пленку подливают горячую воду. После слива промывных вод мицелий по вакуум-линии транспортируют в запарник для отмывания от кислоты горячей водой. Кислые растворы (концентрация 2,5—6,0%), собранные из-под ложного днища запарника, подают на фильтр-пресс. Выгруженный из запарника с помощью шнека мицелий используют на корм скоту.
При поверхностном способе выращивания A. niger основные растворы содержат от 12 до 20 % органических кислот в пересчете на лимонную кислоту, 0,5—2,0 % несброженных сахаров и другие продукты метаболизма. Содержание лимонной кислоты в сброженных растворах составляет 94—98 %.
Глубинный способ. При глубинном способе выращивание A. niger ведут в ферментерах (рис. 18.2). Конидии проращивают в посевных аппаратах (инокуляторах).
Раствор мелассы, содержащий 3—4 % сахара, для посевных аппаратов готовят в варочном аппарате. Мелассу разбавляют кипящей водой, устанавливают рН 7,0—7,2, для удаления железа при кипячении добавляют желтую кровяную соль, растворы NH4CI и MgSO4 вводят в регламентированных количествах.
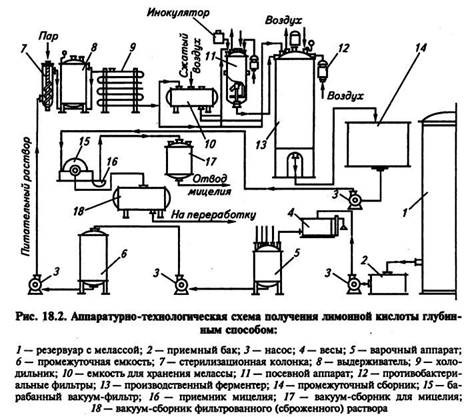
Подготовленный раствор стерилизуют при 128...130 °С в течение 12—15 мин. В раствор мелассы, охлажденный в посевном аппарате до 35...36 °С, добавляют стерильные растворы К2НРО4 и MgSO4. Для производственного ферментера раствор мелассы готовят в той же последовательности. Растворы питательных солей готовят отдельно и стерилизуют при температуре 123... 125 °С. Воду стерилизуют при 128...130ºС.
Подливной раствор должен иметь 25—28%-ю концентрацию по сахару и температуру 34...36 °С, как и основной сбраживаемый раствор. Подливной раствор направляют в сборник. Посевной аппарат засевают предварительно подготовленной суспензией конидий (3 г сухих конидий суспендируют в 2—3 дм3 стерильного раствора мелассы или питательной среды). Культуру выращивают при 34...35 °С при постоянном перемешивании, дробной аэрации и избыточном давлении в аппарате 10—20 кПа.
Процесс подращивания мицелия заканчивается через 30—36 ч. Общая титруемая кислотность культуральной жидкости составляет 1—2%. Подращенный мицелий передают для засева среды в производственном ферментере.
Процесс кислотообразования продолжается 5—-7сут при температуре 31...32 °С, непрерывном перемешивании и дробной аэрации от 1,0 до 1,5 м3/(м3-ч).
Начиная со 2-х суток после посева по мере снижения концентрации сахара в среде 2—3 раза проводят дробное введение подливного 25—28%-го раствора, обычно из расчета доведения конечной концентрации сахара в сбраживаемом растворе до 12—15 %. После окончания процесса сброженный раствор нагревают острым паром до 60...65 °С и сливают в сборник, откуда его подают на вакуум-фильтр для отделения мицелия и промывки его горячей водой. Отделенный и промытый мицелий направляется на корм скоту. Основной раствор лимонной кислоты вместе с промывными водами передается в химический цех для выделения лимонной кислоты.
При глубинном способе сбраживания основные растворы содержат от 5 до 12 % органических кислот, 0,2—1,5 % сахара, а лимонная кислота составляет 80—98% суммы всех кислот. Схема выделения лимонной кислоты из сброженных растворов представлена на рисунке 18.3.
Сброженные растворы представляют собой смесь лимонной, глюконовой и щавелевой кислот, несброженного сахара и минеральных примесей. Лимонную кислоту из раствора выделяют путем связывания ее катионами кальция с образованием слаборастворимой соли цитрата кальция.
Сброженный раствор нагревают в нейтрализаторе до кипения, после чего в него при непрерывном перемешивании вводят известковое молоко. Нейтрализация считается законченной при рН 6,8—7,5. При нейтрализации сброженного раствора образуются кальциевые соли лимонной, глюконовой и щавелевой кислот:
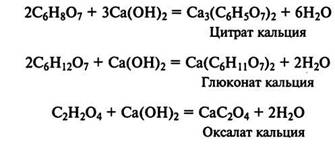
Кальциевые соли лимонной и щавелевой кислот выпадают при этом в осадок, а кальциевая соль глюконовой кислоты и основная часть органических и минеральных веществ мелассы остаются в растворе. После отделения маточного раствора осадок на вакуум-фильтре промывают горячей водой (температура около 95 °С).
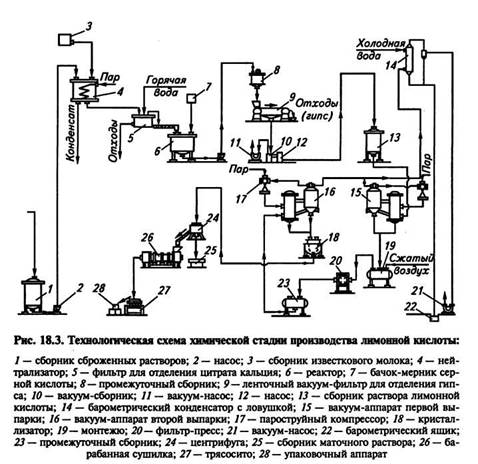
Перевод лимонной кислоты в свободное состояние и отделение ее от оксалата кальция достигается обработкой осадка H2SO4 с последующим фильтрованием. Разложение цитрата кальция осуществляют в реакторе, снабженном мешалкой и паровым барботером. В реактор подают воду из расчета 0,25—0,5 м3 на 1 т лимонной кислоты и при работающей мешалке загружают туда же цитрат кальция с таким расчетом, чтобы после его разложения концентрация лимонной кислоты в растворе была не ниже 25 %. В качестве осветлителя в реактор вводят активированный уголь (2 % массы лимонной кислоты), содержимое реактора нагревают до 60 °С и при перемешивании подают из мерника серную кислоту (плотность 1,8—1,84) из расчета 0,425 дм3 на 1 кг лимонной кислоты в цитрате. Смесь кипятят в течение 10—20 мин.
Разложение цитрата кальция серной кислотой протекает по уравнению
Са3(С6Н6О7)2 + 3H2SO4 = 2С6Н8О7 + 3CaSO4
После полного разложения цитрата кальция в реактор вводят гранулированный сернистый барий (из расчета 0,1—0,15 кг на 100 кг лимонной кислоты) для осаждения тяжелых металлов. Для отделения раствора лимонной кислоты от осадка, содержащего гипс, оксалат кальция, уголь, сернистые соединения, тяжелые металлы и берлинскую лазурь, горячую реакционную смесь направляют из реактора на вакуум-фильтр. Отфильтрованный раствор передают на дополнительное выпаривание, а осадок на фильтре промывают горячей водой (90 °С). Промывку осадка прекращают при содержании лимонной кислоты в промывной воде 0,1 %. Средняя концентрация раствора лимонной кислоты (вместе с промывными водами) должна быть не ниже 16 %.
Выпаривание осуществляют в вакуум-аппаратах и проводят в две стадии с промежуточным освобождением раствора от осадка гипса. В первом аппарате раствор выпаривают до плотности 1,24— 1,26 кг/дм3, осадок отделяют на фильтре-прессе. Во втором аппарате прозрачный раствор выпаривают до плотности 1,35—1,36 кг/дм3, что соответствует 80%-й концентрации лимонной кислоты, и передают на кристаллизацию (температура раствора 70 °С), затем раствор охлаждают до 35... 37 °С и вносят в него затравку — кристаллы лимонной кислоты. Кристаллизацию проводят при непрерывном перемешивании и медленном охлаждении до температуры 8...10 °С, при этой температуре раствор выдерживают не менее 30—45 мин. Кристаллы отделяют в центрифуге, промывают их небольшим количеством холодной воды и передают на сушку.
Сушку проводят в ленточных или барабанных пневматических сушилках при температуре воздуха не более 35 °С. В товарном продукте должно содержаться не менее 99,5 % лимонной кислоты (в пересчете на моногидрат), зольность не более 0,1 % для высшего сорта и 0,35 % для I сорта.
Лимонную кислоту широко используют в кулинарии и пищевой промышленности для приготовления хлебного кваса, безалкогольных напитков, мармелада, вафель, пастилы и др. Лимонная кислота включена в рецептуру некоторых сортов колбас и сыра, ее применяют в виноделии, для рафинирования растительных масел, для производства сгущенного молока. С ее помощью сохраняют естественный вкус и аромат мяса и рыбы при длительном хранении.
Пищевые добавки на базе солей лимонной кислоты, придающие целевые функциональные свойства пищевому сырью и продуктам питания, считаются наиболее безопасными.
Целесообразно применение цитрата кальция, малая растворимость которого сбалансирована со скоростью всасывания кальция в кишечном тракте.
О широком применении таких добавок в мировой практике (в основном за рубежом) свидетельствуют данные, приведенные в таблице 18.2.
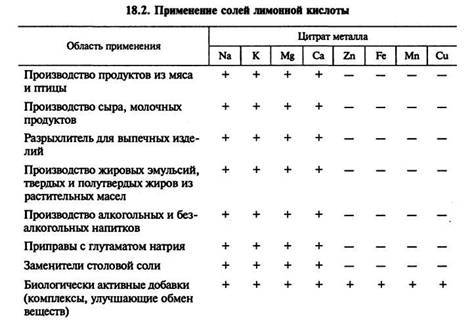
Применение цитратов при производстве различных напитков позволяет обогащать их важными минеральными добавками, а также модифицировать органолептические показатели (цвет, вкус). Цитраты кальция и магния используют в диетических составах, заменяющих столовую соль.
Замена поваренной соли цитратом калия позволяет выпекать лечебный ахлоридный хлеб для больных сердечно-сосудистыми заболеваниями.
Интерес к применению цитратов при производстве продуктов питания в последние годы увеличивается, однако по мере развития и углубления исследований возможного влияния добавок (микроэлементов, витаминов) меняются (в основном ужесточаются) допустимые нормы содержания отдельных добавок в пищевых продуктах, устанавливаются нормативы для отдельных групп населения, уточняются нормативы для диетического питания, напри мер верхний уровень допустимой дозы кальция для взрослых — 2500 мг/сут, магния — 350 мг/сут.
В ближайшем будущем лимонная кислота и ее соли найдут более широкое применение в нашей стране в составе продуктов нового поколения, что будет способствовать оздоровлению всего населения.
УКСУСНАЯ КИСЛОТА
Уксусная кислота (СН3СООН) — наиболее известная пищевая кислота, представляющая собой бесцветную жидкость с резким запахом. В результате перегонки перебродившего спиртового раствора получают 70—80%-й раствор уксусной кислоты, известный под названием уксусной эссенции. Из товарных форм уксусной кислоты известны чистая пищевая (70—80%), безводная или ледяная (98—99 %), выпадающая при охлаждении в осадок в виде кристаллов.
Уксусная кислота находит широкое применение в пищевой промышленности. Ежегодно в мире производят более 100 тыс. т уксусной кислоты, причем более половины — микробиологическим синтезом.
Уксуснокислое брожение основано на способности уксуснокислых бактерий рода Acetobacter окислять этанол в уксусную кислоту. В реакции образования уксусной кислоты участвует фермент алкогольоксидаза. Окисление этанола в уксусную кислоту может быть описано уравнением
СН3СН2ОН + О2 = СН3СООН + Н2О + 490 кДж
В промышленных условиях уксуснокислое брожение проводят непрерывным способом при глубинном проточном культивировании уксуснокислых бактерий в батарее последовательно соединенных аппаратов. Схема производства включает следующие основные технологические стадии:
• получение посевного материала;
• подготовка сырья;
• уксуснокислое брожение;
• розлив готового продукта.
Способностью превращать этанол в уксусную кислоту обладают различные виды уксуснокислых бактерий. В уксуснокислом брожении используют в основном два вида бактерий: Bacterium schutzenbachii и Bacterium curvum.
Для уксуснокислого брожения благоприятны температуры 28 °С для культуры В. schutzenbachii и 35 ºС для культуры В. curvum, a также кислая реакция среды.
Для получения посевной культуры уксуснокислые бактерии выращивают в колбах на жидкой питательной среде, а затем в лабораторном аппарате объемом 30 дм3.
Наилучшее сырье для уксуснокислого брожения — этанол, полученный из зернового и картофельного сырья. Для переработки используют как ректификат, так и спирт-сырец.
На жизнедеятельность уксуснокислых бактерий большое влияние оказывает реакция среды. Принято считать, что оптимальные значения рН для их развития находятся в пределах 3—3,2, однако избыток уксусной кислоты в сбраживаемой среде угнетает жизнедеятельность бактерий-продуцентов. Для сохранения естественной чистоты бактериальной популяции оптимальной считается концентрация кислоты около 10 %. Важным показателем является и предельная концентрация этанола в сбраживаемой среде. Для В. schutzenbachii она составляет 6—7 об. %, для В. curvum — 9—14.
В промышленности уксуснокислое брожение проводят в батарее, состоящей из пяти последовательно соединенных ферментеров. Первый аппарат батареи является генератором уксуснокислых бактерий и непрерывно снабжает все последующие аппараты активной культурой. В нем создаются условия, способствующие быстрому размножению уксуснокислых бактерий. Кроме того, в аппарате происходит интенсивное окисление этанола в уксусную кислоту. Для осуществления этих процессов в первый аппарат непрерывно подается среда, суммарная концентрация этанола и уксусной кислоты в которой составляет 6,4—6,7 %.
В процессе уксуснокислого брожения температура от ферментера к ферментеру снижается. Если в первом она равна 28 °С, то в последнем — 25 °С. Уменьшается также и аэрация с 0,35— 0,40 м3/(м3•мин) в первом ферментере до 0,1—0,15 м3/(м3•мин) в последнем. В каждом ферментере создаются условия, способствующие интенсивному окислению этанола в уксусную кислоту. Для поддержания заданной концентрации спирта во второй, третий и четвертый аппараты подают среду с 40%-м этанолом. Процесс ведут таким образом, чтобы из пятого аппарата выводилась культуральная жидкость с концентрацией уксусной кислоты не ниже 9—9,3 %. Из 100 дм3 безводного спирта получают 75—90 кг уксусной кислоты.
Перед розливом 9%-ю уксусную кислоту (столовый уксус) осветляют бентонитом с добавлением небольшого количества лимонной кислоты. Отфильтрованный на фильтре-прессе раствор поступает на розлив.
В производстве уксуса спиртовое брожение лучше всего осуществляют отселекционированные штаммы винных дрожжей (например, Saccharomyces ellipsoideus), которые помимо этанола синтезируют побочные продукты метаболизма, улучшающие вкус и аромат. Уксус, полученный микробиологическим путем (пищевая уксусная кислота, столовый уксус), как и вино, различается по сортам в зависимости от характера сбраживаемого субстрата. Известны яблочный, виноградный, грушевый и другие сорта уксуса. Уксус, полученный при брожении, имеет приятные аромат и вкус, которые обусловливают побочные продукты брожения: сложные эфиры, высшие спирты, органические кислоты.
Уксусная кислота стала первым микробиологическим продуктом, полученным с помощью иммобилизованных клеток. В течение длительного времени применяется адсорбирование уксуснокислых бактерий на древесной стружке, древесном угле, коксе и других субстратах. Пропуская раствор этанола через генераторы с иммобилизованными бактериями, получают 10—15%-й раствор уксусной кислоты.
Действие уксусной кислоты, основанное обычно на снижении рН консервируемого продукта, проявляется при концентрации выше 0,5 % и направлено главным образом против бактерий. Ее используют при изготовлении майонезов, соусов, при мариновании рыбной продукции, овощей, ягод и фруктов. Уксусную кислоту также широко применяют как вкусовую добавку.
Применение ацетата калия, натрия, кальция и аммония разрешено в производстве овощных консервов и маринованных продуктов.
МОЛОЧНАЯ КИСЛОТА
В настоящее время около половины мирового производства молочной кислоты (СН3СНОНСООН) осуществляется микробиологическим методом, основанным на сбраживании таких ценных углеводсодержащих субстратов, как сахар, рафинадная патока, меласса, сахарный сироп и др., что существенно увеличивает себестоимость конечного продукта. Относительно высокая стоимость молочной кислоты — основной фактор, ограничивающий ее широкое применение в качестве подкислителя, консерванта, регулятора рН, улучшителя вкуса, запаха и структуры пищевых продуктов.
Для получения молочной кислоты микробиологическим методом используют анаэробное превращение углеводов молочнокислыми бактериями. Гидроксильная группа этой кислоты может находиться в двух (α и β) положениях углеродной цепи. Промышленное значение имеет α-оксипропионовая кислота, продуцируемая в процессе молочнокислого брожения.
В промышленных условиях обычно применяют штаммы: Lacto-bacillus delbrueckii, L. leichmannii, L. bulgaricus, Streptococcus lactis.
Различают гомо- и гетероферментативное молочнокислое брожение. В первом случае образуется почти исключительно молочная кислота; во втором — и другие продукты брожения.
Образование молочной кислоты из глюкозы при сбраживании гомоферментативными молочнокислыми бактериями (Lactobacillus) происходит согласно уравнениям:
С6Н12О6 → СН2ОНСНОНСНО → 2СН3СОСНО + 2Н2О
Глицеральдегид Метилглиоксаль
 СН3СОСНО + Н2О Глиоксалаза СН3СНОНСООН
СН3СОСНО + Н2О Глиоксалаза СН3СНОНСООН
Метилглиоксаль Молочная кислота
Расщепление глюкозы происходит по ФДФ-пути, бактерии имеют для этого все необходимые ферменты, включая альдолазу.
Другой вариант схемы молочнокислого брожения включает распад глюкозы до пировиноградной кислоты и восстановление пировиноградной кислоты до молочной:
СН3СОСООН + 2Н+ → СН3СНОНСООН
Пировиноградная кислота Молочная кислота
Кристаллы молочной кислоты при атмосферном давлении быстро плавятся с образованием бесцветной сиропообразной жидкости без запаха с резко кислым вкусом.
В промышленных условиях молочную кислоту получают глубинным способом с помощью культуры L. delbrueckii (рис. 18.4). В качестве основного сырья используют мелассу, сахарозу, гидролизаты крахмала, кукурузный сироп. Концентрация сахара в среде составляет 5—20 %, рН 6,3—6,5. Во время ферментации рН среды поддерживают при помощи СаСО3, который добавляют 3—4 раза в сутки. Молочнокислое брожение проводят при строго постоянной температуре 50 °С. Снижение температуры до 46...48 °С вызывает резкое ослабление биохимической активности культуры и способствует развитию посторонней микрофлоры. Повышение температуры, например до 53...55°С, также вызывает инактивацию культуры и замедление брожения.
При нормальном брожении бактерии сбраживают за сутки 1—1,5 % сахара, и весь цикл брожения заканчивается за 7—11 сут. При этом количество несброженного сахара составляет 0,5—0,7 %, а концентрация лактата кальция — 10—15%. Для отделения СаСО3 и коллоидов сброженный раствор нагревают до 80...90 ºC, a затем обрабатывают гашеной известью до слабощелочной реакции и отстаивают в течение 3—5 ч.
Фильтрацию проводят при температуре раствора лактата кальция 70...80 °С. Полученный фильтрат упаривают до концентрации 27—30 %, затем охлаждают до температуры 25...30 °С и выдерживают 36—48 ч в кристаллизаторе. Кристаллизация считается законченной, если в маточном растворе остается не более 5—6% растворенного лактата кальция.
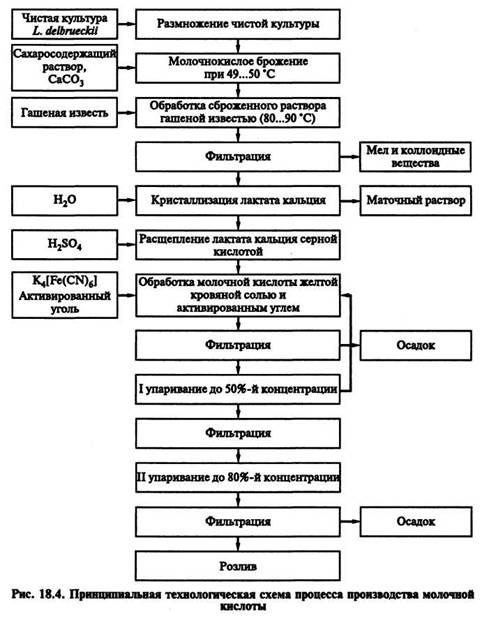
Промытый холодной водой лактат кальция отделяют на центрифуге и расплавляют. С целью предохранения лактата от обугливания расщепление лактата кальция серной кислотой с выделением свободной молочной кислоты проводят при 60...70 °С.
Для отделения ионов железа полученную сырую молочную кислоту при температуре 65 °С обрабатывают K4[Fe(CN)6] (желтой кровяной солью). В осадок выпадает берлинская лазурь. Тяжелые металлы и мышьяк осаждают Na2SO4 и Ba2S. Для освобождения молочной кислоты от красящих веществ используют активированный уголь. После обработки полученную смесь фильтруют, а осадок гипса промывают для извлечения оставшейся молочной кислоты.
После расщепления кристаллического лактата кальция и последующей обработки получают 18—20%-ю молочную кислоту, которую упаривают до 50%-й и осветляют активированным углем, затем обрабатывают желтой кровяной солью. Отфильтрованную 50%-ю молочную кислоту сливают в сборник готовой продукции, а из него подают на фасовку.
Для получения 80%-й кислоты 50%-ю молочную кислоту вторично упаривают при большом разрежении в вакуум-аппаратах. 80%-ю молочную кислоту фильтруют на фильтре-прессе и подают на розлив или на приготовление 80%-й пастообразной кислоты, которую получают внесением в нее небольших количеств мела (4 % массы кислоты).
Один из возможных путей создания высокоэффективных и ресурсосберегающих технологий производства молочной кислоты — расширение сырьевой базы для культивирования молочнокислых бактерий для замены дорогостоящих и дефицитных источников углеводов более дешевым и доступным сырьем, например разнообразными отходами перерабатывающей промышленности и сельского хозяйства.
В качестве основных углеводсодержащих субстратов для молочнокислого брожения возможно использование молочной сыворотки, а также яблочных выжимок и нестандартного, дефектного яблочного сырья.
Для ферментации молочной сыворотки оптимально использование культуры Lactobacillus acidophillus BKM 1660 (Т), для ферментации плодового сырья и отходов переработки сельскохозяйственного сырья — культуры Lactobacillus plantarum BKM 578, как обеспечивающих высокий выход молочной кислоты и высокую бродильную активность.
В качестве питательной среды для культивирования кислотообразующих бактерий могут быть использованы заводская нефильтрованная сыворотка и осветленная сыворотка (полученная при сепарировании и ультрафильтрации). Активнее процесс накопления молочной кислоты происходит на осветленной молочной сыворотке. В этом случае выход молочной кислоты в 1,5—1,7 раз выше, чем на неосветленных образцах сыворотки, и в 1,1—1,2 раза больше, чем на ультрафильтрате.
Ферментацию молочной сыворотки с применением культуры L. acidophillus BKM 1660 (Т) осуществляют анаэробно, при температуре 30 °С, рН 6—6,5. Посевной материал, выращенный в течение 48 ч и содержащий не менее 109 клеток/см3, вносят в ферментационную среду в дозировке 20 % общего объема. Начальная концентрация лактозы составляет 5—10 %.
При сбраживании молочной сыворотки без проведения подтитровки молочнокислые бактерии могут накапливать до 2,2 % молочной кислоты. Содержание в растворе более 2,5 % молочной кислоты подавляет развитие бактерий, поэтому образующуюся в процессе ферментации молочную кислоту периодически нейтрализуют СаСО3. Это позволяет добиться увеличения выхода молочной кислоты.
По отношению к различным титрантам (20%-й КОН, NaOH, NH4OH, CaCO3, MgCO3, CaO) молочнокислые бактерии ведут себя практически одинаково. Установлено, что подтитровку нужно проводить до содержания свободной кислоты в среде 0,2— 0,5 %, рН 5—5,5. При этом процесс накопления молочной кислоты продолжается до 6 сут.
Получаемая молочная кислота обогащена аминокислотами и микроэлементами, нетоксична, а осадок, получаемый при производстве молочной кислоты, можно использовать в качестве полноценной кормовой добавки.
На основе подробного химического анализа, а также микробиологической оценки установлено, что яблочное сырье (яблочные выжимки, смесь кожуры и семян, а также дефектное и нестандартное сырье) может служить полноценной питательной средой для молочнокислых бактерий.
Содержащиеся в яблочном сырье макро- и микроэлементы, витамины оказывают положительное влияние на биосинтез молочной кислоты.
Подготовка яблочного сырья к сбраживанию включает стадию измельчения и резки. Размеры частиц яблочной мезги должны составлять от 2 до 5 мм. Оптимальным является режим разваривания яблочного сырья при гидромодуле 2,5 в течение 30 мин при 120 °С.
Эффективное расщепление полисахаридов яблочного сырья возможно с помощью ферментных препаратов пекто- и целлюлолитического действия. После проведения ферментативной обработки и последующего брожения среда лучше подвергается фильтрации и дальнейшим конечным производственным операциям, что является положительным фактором при промышленном производстве.
Возможно использование ферментных препаратов в концентрациях: Пектофоетидина П10Х — 0,03%, Целлюлазы — 0,06% массы сырья. Режим обработки ферментами — 1 ч при температуре 32... 35 °С.
При ферментации полисахаридов яблочного сырья можно технологически совместить стадии ферментативной обработки сырья и культивирования бактериальной культуры.
Культура Lactobacillus plantarum BKM 578 обеспечивает на яблочном сырье достаточно продолжительный и стабильный синтез молочной кислоты при начальной концентрации углеводов 4,5—5%. Наилучшие показатели достигаются в случае дробной подачи сгущенного яблочного сока до содержания в среде СВ 15 %.
Раствор молочной кислоты, полученный на яблочном сырье, представляет собой коричневую или темно-коричневую жидкость.
Очистка получаемой молочной кислоты от примесей осуществляется активированным углем марки БАУ А, наилучший режим осветления: температура 50 °С, дозировка активированного угля 4 %, время экспозиции 30 мин.
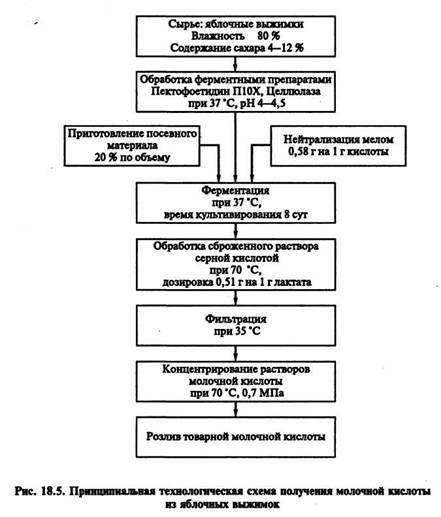
Принципиальная технологическая схема представлена на рисунке 18.5.
Возможно получение молочной кислоты из пшеничной муки II сорта (сырья с невысокой стоимостью) с использованием в качестве продуцента бактерий вида Streptococcus bovis.
Str. bovis обладает способностью гидролизовать сырой зерновой крахмал, поэтому для организации производства молочной кислоты не требуется сложного оборудования.
Осуществляют ферментацию сред с мукой II сорта, содержащих 5—20 % Сахаров, концентрация посевного материала составляла 5—20%.
Молочную кислоту выпускают в виде 40%-го раствора и концентрата, содержащего не менее 70 % кислоты. В пищевых продуктах разрешено использование ее солей: лактатов натрия, калия, кальция, аммония и магния, которые вводят в пищевую систему отдельно или в комбинации. Молочная кислота используется в производстве пива, кваса, безалкогольных напитков, карамельных масс, кисломолочных продуктов, ограниченно — в продуктах детского питания.
Дата добавления: 2018-05-12; просмотров: 1278; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
