Химические свойства кислородсодержащих органических соединений.
Цель:формировать умения проводить наблюдения и делать выводы, записывать уравнения соответствующих реакций в молекулярном и ионном видах.
Обеспеченность занятия
1. Сборник методических указаний для студентов по выполнению практических занятий и лабораторных работ по учебной дисциплине «Химия».
2. Раствор гидроксида натрия, карбонат натрия, карбонат кальция, оксид меди (II), уксусная кислота, лакмус синий, цинк; штатив с пробирками, водяная баня, прибор для нагревания, спички, держатель для пробирок.
Теоретический материал
Карбоновые кислоты - органические соединения, в молекулах которых содержатся одна или несколько карбоксильных групп, соединённых с углеводородным радикалом или атомом водорода.
Получение: В лаборатории карбоновые кислоты можно получить из их солей, действуя на них серной кислотой при нагревании, например:
2СН3– СООNa + H2SO4 ® 2СН3 – СООН + Na2SO4
В промышленности получают окислением углеводородов, спиртов и альдегидов.
Химические свойства:
1. Из-за смещения электронной плотности от гидроксильной группы O–H к сильно
поляризованной карбонильной группе C=O молекулы карбоновых кислот способны к
электролитической диссоциации: R–COOH → R–COO- + H+
2.Карбоновые кислоты обладают свойствами, характерными для минеральных кислот. Они реагируют с активными металлами, основными оксидами, основаниями, солями слабых кислот. 2СH3COOH + Mg → (CH3COO)2Mg + H2
2СH3COOH + СaO → (CH3COO)2Ca + H2O
H–COOH + NaOH → H–COONa + H2O
2СH3CH2COOH + Na2CO3 → 2CH3CH2COONa + H2O + CO2
СH3CH2COOH + NaHCO3 → CH3CH2COONa + H2O + CO2
Карбоновые кислоты слабее многих сильных минеральных кислот
СH3COONa + H2SO4(конц.) →CH3COOH + NaHSO4
3. Образование функциональных производных:
a) при взаимодействии со спиртами (в присутствии концентрированной H2SO4) образуются сложные эфиры.
Образование сложных эфиров при взаимодействии кислоты и спирта в присутствии минеральных кислот называется реакцией этерификации . CH3–  –OH + HO–CH3 D CH3–
–OH + HO–CH3 D CH3–  –OCH3 + H2O
–OCH3 + H2O
уксусная кислота метиловый метиловый эфир
спирт уксусной кислоты
Общая формула сложных эфиров R–  –OR’ где R и R' – углеводородные радикалы: в сложных эфирах муравьиной кислоты – формиатах –R=H.
–OR’ где R и R' – углеводородные радикалы: в сложных эфирах муравьиной кислоты – формиатах –R=H.
Обратной реакцией является гидролиз (омыление) сложного эфира:
CH3–  –OCH3 + HO–H DCH3–
–OCH3 + HO–H DCH3–  –OH + CH3OH.
–OH + CH3OH.
Глицери́н (1,2,3-тригидроксипропан; 1,2,3-пропантриол) (гликос — сладкий) химическое соединение с формулой HOCH2CH(OH)-CH2OH или C3H5(OH)3. Простейший представитель трёхатомных спиртов. Представляет собой вязкую прозрачную жидкость.
Глицерин — бесцветная, вязкая, гигроскопичная жидкость, неограниченно растворимая в воде. Сладкий на вкус(гликос — сладкий). Хорошо растворяет многие вещества.
Глицерин этерефицируется карбоновыми и минеральными кислотами.
Эфиры глицерина и высших карбоновых кислот — жиры.
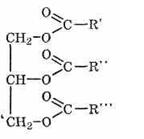 Жиры — это смеси сложных эфиров, образованных трехатомным спиртом глицерином и высшими жирными кислотами. Общая формула жиров, где R — радикалы высших жирных кислот:
Жиры — это смеси сложных эфиров, образованных трехатомным спиртом глицерином и высшими жирными кислотами. Общая формула жиров, где R — радикалы высших жирных кислот:
Чаще всего в состав жиров входят предельные кислоты: пальмитиновая С15Н31СООН и стеариновая С17Н35СООН, и непредельные кислоты: олеиновая С17Н33СООН и линолевая С17Н31СООН.
Общее название соединений карбоновых кислот с глицерином — триглицериды.

б) при воздействии водоотнимающих реагентов в результате межмолекулярной
дегидратации образуются ангидриды
CH3–  –OH + HO–
–OH + HO–  –CH3 →CH3–
–CH3 →CH3–  –O–
–O–  –CH3 + H2O
–CH3 + H2O
Галогенирование. При действии галогенов (в присутствии красного фосфора) образуются α-галогензамещённые кислоты:
|
| α |
| CH3–CH2–COOH + Br2→CH3– | CH–COOH + HBr │ Br α -бромпропионовая кислота(2-бромпропановая кислота) |
Применение:в пищевой и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров).
Вопросы для закрепления теоретического материала
1 Какие органические соединения относятся к карбоновым кислотам?
2 Почему среди карбоновых кислот нет газообразных веществ?
3 Чем обусловлены кислотные свойства карбоновых кислот?
4 Почему изменяется цвет индикаторов в растворе уксусной кислоты?
5 Какие химические свойства для глюкозы и глицерина являются общими, и чем эти вещества отличаются друг от друга? Напишите уравнения соответствующих реакций.
Задание
1. Повторить теоретический материал по теме практического занятия.
2. Ответить на вопросы для закрепления теоретического материала.
3. Исследовать свойства кислородсодержащих органических соединений.
4. Оформить отчет.
Инструкция по выполнению
1. Ознакомьтесь с правилами по технике безопасности при работе в химической лаборатории и распишитесь в журнале по ТБ.
2. Выполните опыты.
3. Результаты внесите в таблицу.
Опыт № 1 Испытание раствора уксусной кислоты лакмусом
Разбавьте полученную уксусную кислоту небольшим количеством воды и прибавьте несколько капель синего лакмуса или опустите в пробирку индикаторную бумажку.
Опыт №2 Взаимодействие уксусной кислоты с карбонатом кальция
В пробирку насыпьте немного мела (карбоната кальция) и прилейте раствор уксусной
кислоты.
Опыт № 3 Свойства глюкозы и сахарозы
а) В пробирку внесите 5 капель раствора глюкозы, каплю раствора соли меди (II) и при взбалтывании несколько капель раствора гидроксида натрия до образования светло - синего раствора. Такой опыт проделывали с глицерином.
б) Полученные растворы нагрейте. Что наблюдаете?
Опыт № 4 Качественная реакция на крахмал
К 5-6 каплям крахмального клейстера в пробирке прибавьте каплю спиртового раствора йода.
Образец отчёта
Лабораторная работа № 9 Химические свойства кислородсодержащих органических соединений.
Цель:формировать умения проводить наблюдения и делать выводы, записывать уравнения соответствующих реакций в молекулярном и ионном видах.
| Название опыта | Что делаете | Наблюдения и их объяснения | Уравнения реакций |
| опыт № 1 Испытание раствора уксусной кислоты лакмусом | |||
| опыт №2 Взаимодействие уксусной кислоты с карбонатом кальция | |||
| опыт № 3 Свойства глюкозы и сахарозы | |||
| опыт № 4 Качественная реакция на крахмал |
Вывод делать в соответствии с целью работы
Литература 0-2 с. 94-98
Лабораторная работа № 10
Дата добавления: 2018-04-15; просмотров: 1482; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
