Вопрос 1. Тромбоэмболия легочной артерии
Тромбоэмболия легочной артерии (ТЭЛА) — внезапная закупорка ветвей или ствола легочной артерии тромбом (эмболом), образовавшимся в правом желудочке или предсердии сердца, венозном русле большого круга кровообращения и принесенным с током крови. В результате ТЭЛА прекращается кровоснабжение легочной ткани. Развитие ТЭЛА происходит часто стремительно и может привести к гибели больного.
От ТЭЛА умирает 0,1% населения земного шара ежегодно. Около 90% больных, умерших от ТЭЛА, во время не был установлен правильный диагноз, и не было проведено необходимое лечение.
Среди причин смерти населения от сердечно-сосудистой заболеваний ТЭЛА стоит на третьем месте после ИБС и инсульта. ТЭЛА может приводить к летальному исходу при некардиологической патологии, возникая после операций, полученных травм, родов. При своевременном оптимальном лечении ТЭЛА наблюдается высокий показатель снижения уровня смертности до 2 – 8%.
Причины развития ТЭЛА
Наиболее частыми причинами развития ТЭЛА служат:
тромбоз глубоких вен (ТГВ) голени (в 70 – 90% случаев), часто сопровождающийся тромбофлебитом. Может иметь место тромбоз одновременно глубоких и поверхностных вен голени
тромбоз нижней полой вены и ее притоков
сердечно-сосудистые заболевания, предрасполагающие к появлению тромбов и эмболий в легочной артерии (ИБС, активная фаза ревматизма с наличием митрального стеноза и мерцательной аритмии, гипертоническая болезнь, инфекционный эндокардит, кардиомиопатиии неревматические миокардиты)
септический генерализованный процесс
онкологические заболевания (чаще рак поджелудочной железы, желудка, легких)
тромбофилия (повышенное внутрисосудистое тромбообразование при нарушении системы регуляции гемостаза)
антифосфолипидный синдром — образование антител к фосфолипидам тромбоцитов, клеток эндотелия и нервной ткани (аутоиммунные реакции); проявляется повышенной склонностью к тромбозам различных локализаций.
Факторы риска тромбозов вен и ТЭЛА - это:
длительное состояние обездвиженности (постельный режим, частые и продолжительные авиаперелеты, поездки, парез конечностей), хроническая сердечно-сосудистая и дыхательная недостаточность, сопровождаются замедлением тока крови и венозным застоем.
прием большого количества диуретиков (массовая потеря воды приводит к дегидратации, повышению гематокрита и вязкости крови);
злокачественные новообразования - некоторые виды гемобластозов, истинная полицитемия (большое содержание в крови эритроцитов и тромбоцитов приводит к их гиперагрегации и образованию тромбов);
длительный прием некоторых лекарственных препаратов (оральные контрацептивы, заместительная гормональная терапия) повышает свертываемость крови;
варикозная болезнь (при варикозном расширении вен нижних конечностей создаются условия для застоя венозной крови и образования тромбов);
нарушения обмена веществ, гемостаза (гиперлипидпротеинемия, ожирение, сахарный диабет, тромбофилия);
хирургические операции и внутрисосудистые инвазивные процедуры (например, центральный катетер в крупной вене);
артериальная гипертензия, застойная сердечная недостаточность, инсульты, инфаркты;
травмы спинного мозга, переломы крупных костей;
химиотерапия;
беременность, роды,послеродовый период;
курение, пожилой возраст и др.
Классификация ТЭЛА
В зависимости от локализации тромбоэмболического процесса различают следующие варианты ТЭЛА:
массивная (тромб локализуется в главном стволе или основных ветвях легочной артерии)
эмболия сегментарных или долевых ветвей легочной артерии
эмболия мелких ветвей легочной артерии (чаще двусторонняя)
В зависимости от объема отключенного артериального кровотока при ТЭЛА выделяют формы:
малую (поражены менее 25% легочных сосудов) - сопровождается одышкой, правый желудочек функционирует нормально
субмассивную (субмаксимальную - объем пораженных сосудов легких от 30 до 50%), при которой у пациента отмечается одышка, нормальное артериальное давление, правожелудочковая недостаточность мало выражена
массивную (объем отключенного легочного кровотока более 50%) - наблюдается потеря сознания, гипотония, тахикардия, кардиогенный шок, легочная гипертензия, острая правожелудочковая недостаточность
смертельную (объем отключенного кровотока в легких более 75%).
ТЭЛА может протекать в тяжелой, среднетяжелой или легкой форме.
Клиническое течение ТЭЛА может быть:
острейшим (молниеносным), когда наблюдается моментальная и полная закупорка тромбом главного ствола или обеих основных ветвей легочной артерии. Развивается острая дыхательная недостаточность, остановка дыхания, коллапс, фибрилляция желудочков. Летальный исход наступает за несколько минут, инфаркт легких не успевает развиться.
острым, при котором отмечается быстро нарастающая обтурация основных ветвей легочной артерии и части долевых или сегментарных. Начинается внезапно, бурно прогрессирует, развиваются симптомы дыхательной, сердечной и церебральной недостаточности. Продолжается максимально 3 – 5 дней, осложняется развитием инфаркта легких.
подострым (затяжным) с тромбозом крупных и средних ветвей легочной артерии и развитием множественных инфарктов легких. Продолжается несколько недель, медленно прогрессирует, сопровождаясь нарастанием дыхательной и правожелудочковой недостаточности. Могут возникать повторные тромбоэмболии с обострением симптомов, при которых нередко наступает смертельный исход.
хроническим (рецидивирующим), сопровождающимся рецидивирующими тромбозами долевых, сегментарных ветвей легочной артерии. Проявляется повторными инфарктами легких или повторными плевритами (чаще двусторонними), а также постепенно нарастающей гипертензией малого круга кровообращения и развитием правожелудочковой недостаточности. Часто развивается в послеоперационном периоде, на фоне уже имеющихся онкологических заболеваний, сердечно-сосудистых патологий.
Симптомы ТЭЛА
Симптоматика ТЭЛА зависит от количества и размера тромбированных легочных артерий, скорости развития тромбоэмболии, степени возникших нарушений кровоснабжения легочной ткани, исходного состояния пациента. При ТЭЛА наблюдается широкий диапазон клинических состояний: от практически бессимптомного течения до внезапной смерти.
Клинические проявления ТЭЛА неспецифические, они могут наблюдаться при других легочных и сердечно-сосудистых заболеваниях, их главным отличием служит резкое, внезапное начало при отсутствии других видимых причин данного состояния (сердечно-сосудистой недостаточности, инфаркта миокарда, пневмонии и др.). Для ТЭЛА в классическом варианте характерен ряд синдромов:
1. Сердечно – сосудистый:
острая сосудистая недостаточность. Отмечается падение артериального давления (коллапс, циркуляторный шок), тахикардия. Частота сердечных сокращений может достигать более 100 уд. в минуту.
острая коронарная недостаточность (у 15-25% больных). Проявляется внезапными сильными болями за грудиной различного характера, продолжительностью от нескольких минут до нескольких часов, мерцательной аритмией, экстрасистолией.
острое легочное сердце. Обусловлено массивной или субмассивной ТЭЛА; проявляется тахикардией, набуханием (пульсацией) шейных вен, положительным венным пульсом. Отеки при остром легочном сердце не развиваются.
острая цереброваскулярная недостаточность. Возникают общемозговые или очаговые нарушения, церебральная гипоксия, при тяжелой форме - отек мозга, мозговые кровоизлияния. Проявляется головокружением, шумом в ушах, глубоким обмороком с судорогами, рвотой, брадикардией или коматозным состоянием. Могут наблюдаться психомоторное возбуждение, гемипарезы, полиневриты, менингиальные симптомы.
2. Легочно-плевральный:
острая дыхательная недостаточность проявляется одышкой (от ощущения нехватки воздуха до очень выраженных проявлений). Число дыханий более 30-40 в минуту, отмечается цианоз, кожные покровы пепельно-серые, бледные.
умеренный бронхоспастический синдром сопровождается сухими свистящими хрипами.
инфаркт легкого, инфарктная пневмония развивается на 1 – 3 сутки после ТЭЛА. Появляются жалобы на одышку, кашель, боли в грудной клетке со стороны поражения, усиливающиеся при дыхании; кровохарканье, повышение температуры тела. Становятся слышны мелкопузырчатые влажные хрипы, шум трения плевры. У пациентов с тяжелой сердечной недостаточностью наблюдаются значительные выпоты в плевральную полость.
3. Лихорадочный синдром - субфебрильная, фебрильная температура тела. Связан с воспалительными процессами в легких и плевре. Длительность лихорадки составляет от 2 до 12 дней.
4. Абдоминальный синдром обусловлен острым, болезненным набуханием печени (в сочетании с парезом кишечника, раздражением брюшины, икотой). Проявляется острой болью в правом подреберье, отрыжкой, рвотой.
5. Иммунологический синдром (пульмонит, рецидивирующий плеврит, уртикароподобная сыпь на коже, эозинофилия, появление в крови циркулирующих иммунных комплексов) развивается на 2-3 неделе заболевания.
Осложнения ТЭЛА
Острая ТЭЛА может служить причиной остановки сердца и внезапной смерти. При срабатывании компенсаторных механизмов пациент сразу не погибает, но при отсутствии лечения очень быстро прогрессируют вторичные гемодинамические нарушения. Имеющиеся у пациента кардиоваскулярные заболевания значительно снижают компенсаторные возможности сердечно-сосудистой системы и ухудшают прогноз.
Диагностика ТЭЛА
В диагностике ТЭЛА главная задача – установить местонахождение тромбов в легочных сосудах, оценить степень поражения и выраженность нарушений гемодинамики, выявить источник тромбоэмболии для предупреждения рецидивов.
Сложность диагностики ТЭЛА диктует необходимость нахождения таких пациентов в специально оборудованных сосудистых отделениях, владеющих максимально широкими возможностями для проведения специальных исследований и лечения. Всем пациентам с подозрением на ТЭЛА проводят следующие обследования:
тщательный сбор анамнеза, оценку факторов риска ТГВ/ТЭЛА и клинической симптоматики
общий и биохимический анализы крови, мочи, исследование газового состава крови, коагулограмму и исследование Д-димера в плазме крови (метод диагностики венозных тромбов)
ЭКГ в динамике (для исключения инфаркта миокарда, перикардита, сердечной недостаточности)
рентгенографию грудной клетки (для исключения пневмоторакса, первичной пневмонии, опухолей, переломов ребер, плеврита)
эхокардиографию (для выявления повышенного давления в легочной артерии, перегрузок правых отделов сердца, тромбов в полостях сердца)
сцинтиграфию легких (нарушение перфузии крови через легочную ткань говорит об уменьшении или отсутствии кровотока вследствие ТЭЛА)
ангиопульмонографию (для точного определения локализации и размеров тромба)
УЗДГ периферических вен, контрастную флебографию (для выявления источника тромбоэмболии)
Лечение ТЭЛА
Пациентов с ТЭЛА помещают в реанимационное отделение.
В неотложном состоянии пациенту проводятся реанимационные мероприятия в полном объеме.
Дальнейшее лечение ТЭЛА направлено на нормализацию легочного кровообращения, профилактику хронической легочной гипертензии.
С целью предупреждения рецидивов ТЭЛА необходимо соблюдение строгого постельного режима. Для поддержания оксигенации проводится постоянная ингаляция кислорода.
Осуществляется массивная инфузионная терапия для снижения вязкости крови и поддержания АД.
В раннем периоде показано назначение тромболитической терапии с целью максимально быстрого растворения тромба и восстановления кровотока в легочной артерии. В дальнейшем для предупреждения рецидивов ТЭЛА проводится гепаринотерапия.
При явлениях инфаркт-пневмонии назначается антибактериальная терапия.
В случаях развития массивной ТЭЛА и неэффективности тромболизиса проводится хирургическая тромбоэмболэктомия (удаление тромба). Как альтернативу эмболэктомии используют катетерную фрагментацию тромбоэмбола. При рецидивирующих ТЭЛА
Прогноз и профилактика ТЭЛА практикуется постановка специального фильтра в ветви легочной артерии, нижнюю полую вену.
При раннем оказании полного объема помощи пациентам прогноз для жизни благоприятный. При выраженных сердечно-сосудистых и дыхательных нарушениях на фоне обширной ТЭЛА летальность превышает 30%.
Половина рецидивов ТЭЛА развивается у пациентов, не получавших антикоагулянты. Своевременная, правильно проведенная антикоагулянтная терапия вдвое снижает риск рецидивов ТЭЛА.
Для предупреждения тромбоэмболии необходимы ранняя диагностика и лечение тромбофлебита, назначение непрямых антикоагулянтов пациентам из групп риска.
Вопрос 2. Синдром приводящей петли (синдром желчной рвоты, дуоденобилиарный синдром) может развиваться после резекции желудка по способу Бильрот II, когда образуется выключенный с одной стороны слепой отдел кишечника (двенадцатиперстная кишка и сегмент тощей кишки до соединения с культей желудка) и нарушается его моторно-эвакуаторная функция. В основе патогенеза этого синдрома лежит нарушение эвакуации содержимого из приводящей петли и его рефлюкс в желудок вследствие изменения нормальных анатомо-функциональных взаимоотношений.
Чем проявляется синдром приводящий кишки?
Отмечаются жалобы на тяжесть или распирающие боли в эпигастральной области и правом подреберье, усиливающиеся после приема пищи. Эти ощущения постепенно нарастают и вскоре завершаются обильной желчной рвотой (иногда с примесью пищи), приносящей заметное облегчение. Частота желчной рвоты и ее обилие определяют степень тяжести синдрома.
Как выявляется синдром приводящей кишки?
Диагностика синдрома основывается на характерной клинической картине. При осмотре больного иногда можно отметить заметную асимметрию живота за счет выбухания в правом подреберье, легкую желтушность склер, падение массы тела. Лабораторные исследования могут указывать на нарушение функции печени, отмечается анемия. При рентгенологическом исследовании и фиброгастроскопии можно обнаружить органическую патологию в области анастомоза (рубцовая деформация, пептическая язва), а также массивный рефлюкс и длительный стаз в атоничной приводящей петле, гипермоторную дискинезию отводящей петли, признаки рефлюкс-гастрита.
Лечение больных с синдромом приводящей петли легкой степени консервативное: щадящая диета, противовоспалительные средства, повторные промывания желудка.
Выраженный синдром с частой и обильной рвотой является показанием к хирургическому лечению. Наиболее обоснованная операция — реконструкция гастроэнтероанастомоза. При сочетании синдрома с другими пострезекционными нарушениями метод оперативного вмешательства избирают с учетом их особенностей.
Консервативное лечение синдрома приводящей петли (СПП) малоэффективно, может применяться лишь при его легкой степени и сводится к щадящей диете, противовоспалительной терапии, повторным промываниям желудка. Устраняют гипопротеинемию и анемию. Назначают переливание крови и плазмы, спазмолитические средства и витамины.
Выраженный синдром с частой и обильной рвотой является показанием к хирургическому лечению.
Наиболее обоснованная операция - реконструкция гастроэнтероанастомоза. При сочетании синдрома с другими пострезекционными нарушениями метод оперативного вмешательства избирают с учетом их особенностей.
Все оперативные методы лечения СПП можно разделить на три группы:
- операции, устраняющие перегибы приводящей петли или укорачивающие ее;
- дренирующие операции;
- собственно реконструктивные вмешательства.
Операции первой группы, направленные на устранение перегибов, инвагинации приводящей петли, создание клапанного механизма в устье приводящей петли не являются радикальными и их выполняют только при тяжелом общем состоянии пациента.
Более эффективно наложение брауновского анастомоза между приводящей и отводящей кишками. Успешные результаты лечения отмечаются при применении операции Таннера-Ру: приводящую кишку пересекают, дистальный ее отрезок вшивают в бок отводящей петли, проксимальный, отходящий от двенадцатиперстной кишки, вшивают в бок тощей кишки на расстоянии 45-50 см от предыдущего анастомоза.
Вопрос 3. Доброкачественные опухоли печенивстречаются крайне редко и представлены в основном гепатоаденомами. Источником возникновения доброкачественных опухолей могут послужить эпителиальные и соединительнотканные элементы печени, желчных протоков, а также кровеносные и лимфатические сосуды (лимфангиома, гемангиоэндотелиома, холангиома и другие виды опухолей).
Аденомы печени
Аденомы печени представляют собой доброкачественные опухоли, возникающие из печеночных клеток или эпителиальных клеток желчных протоков.
В зависимости от их строения различают:
доброкачественную гепатому, исходящую из печеночных клеток;
доброкачественную холангиому, исходящую из эпителия желчных протоков;
доброкачественную аденому смешанного строения - гепатохолангиому.
Макроскопически аденомы печени имеют вид круглых сероватых или темно-красных образований различных размеров, располагающихся под капсулой или в толще печени, и могут быть одиночными или множественными.
Микроскопически холангиомы подразделяют на опухоли солидного типа, тубулярного типа и цистаденомы. Аденомы солидного и тубулярного типов обычно не достигают больших размеров, тогда как цистаденомы могут достигать значительной величины и склонны к злокачественному перерождению.
Гепатомы могут быть представлены в виде простой дизэмбриомы печени, инкапсулированной и с четким дольчатьм строением, либо в виде трабекулярной аденомы, где клеточные пластинки лишены долькового расположения и опухоль не имеет собственной капсулы. Последние потенциально активны и склонны к злокачественному перерождению.
В последнее время аденомы печени все чаще описываются у женщин после длительного применения пероральных стероидных контрацептивов.
Гемангиома печени
Гемангиома печени - самая частая из всех доброкачественных опухолей этого органа.
Гемангиомы относят к сосудистым опухолям. Они представляют собой доброкачественные пещеристые кровяные опухоли губчатого строения (ангиомы, кавернозные гемангиомы и каверномы), исходящие из венозных сосудов печени. Некоторые авторы считают гемангиомы не истинной опухолью, а пороком развития, васкулярной гамартомой.
В литературе имеются указания, что гемангиомы печени часто сочетаются с кистами или кистозным поражением других органов. Гемангиомы печени могут быть пограничными между доброкачественными и злокачественными опухолями.
По гистологическому строению различают кавернозную и скиррозную гемангиому. Отдельно выделяют гемангиоэндотелиому, при которой обнаруживают признаки безудержного инфильтративного роста, характерного для злокачественных опухолей. По расположению гемангиомы печени бывают поверхностными, глубокими и смешанными. Гемангиомы печени встречаются в виде небольших множественных образований или одиночных опухолей различной величины.
Узловатая гиперплазия
Узловатая гиперплазия печени представляет определенный онкологический интерес, так как по своим клиническим проявлениям она мало отличается от опухолей этого органа.
Узловатую гиперплазию даже во время операции трудно отличить от истинной опухоли - рака или аденомы.
В возникновении узловатой гиперплазии большое значение придают локальным циркуляторньм и билиарным нарушениям в отдельных участках печени.
Макроскопически узловатые гиперплазии имеют вид темно-красного, бурого или розового образования различной величины с гладкой или мелкобугристой поверхностью. По консистенции они плотнее, чем интактная печеночная ткань, и не имеют собственной капсулы.
Микроскопически при узловатой гиперплазии обнаруживают картину локального цирроза, иногда очень сходную с гистологическим строением гепатом.
Не исключено, что локальная гиперплазия печени является стадией единого процесса: локальный цирроз - аденома - злокачественная гепатома.
Непаразитарные кисты
Непаразитарные кисты печени не представляют большой редкости; причина их образования различна.
Непаразитарные кисты чаще бывают врожденными и возникают из зачатков желчных протоков и остатка зародышевой ткани. Травматические кисты печени образуются из гематомы после разрыва печени.
Кисты связок печени встречаются исключительно редко и могут быть как истинными, врожденными, так и ложными - травматическими и воспалительными.
Диагностика, клиника, лечение доброкачественных опухолей печени
Ранняя диагностика аденом представляет трудную задачу, поскольку эти опухоли не дают каких-либо патогномоничных симптомов и сходны по клиническому течению с другими доброкачественными очаговыми заболеваниями печени. Применение современных методов исследования при подозрении на опухоль печени дает возможность точной диагностики. Наибольшее диагностическое значение имеет сканирование печени, гепатоангиография и лапароскопия с прицельной биопсией.
При клинических признаках опухоли и подтверждении диагноза данными объективного исследования, больного необходимо оперировать, не дожидаясь осложнений. Методом выбора при хирургическом лечении аденомы печени является резекция органа в пределах здоровых тканей. Узловатая гиперплазия печени долгое время протекает бессимптомно и проявляется при достижении больших размеров или же обнаруживается случайно во время других операций.
Особенности клинического течения гемангиом во многом зависят от их размеров и распространения.
Бессимптомные гемангиомы печени клинически ничем не проявляются, их обнаруживают случайно во время лапароскопии или на аутопсии. По мере роста опухоли и увеличения ее размеров появляются различные клинические сиптомы - боли и тяжесть в эпигастральной области, тошнота, отрыжка воздухом.
Среди объективных симптомов первостепенное значение имеет наличие пальпируемой опухоли. В отличие от злокачественных опухолей, гемангиома печени характеризуется медленным ростом, длительньм течением и удовлетворительным состоянием больного.
Клиническое течение гемангиом может осложняться разрывом опухоли и внутрибрюшным кровотечением, гемобилией, перекручиванием ножки опухоли.
Бессимптомные формы непаразитарных кист печени клинически ничем не проявляются. По мере увеличения размеров кисты больные предъявляют жалобы на чувство тяжести, давления и боли в эпигастрии и правом подреберье.
С увеличением объема кисты значительно возрастает угроза осложнений - разрыв кисты, нагноение, кровоизлияние в полость кисты, механическая желтуха.
С целью диагностики доброкачественных опухолей печени используются: ультразвуковое и радиоизотопное исследование, компьютерная томография, ангиография, лапароскопия.
Лечение доброкачественных опухолей печени хирургическое. Объем резекции печени зависит от размеров и локализации доброкачествнных опухолей, начиная от сегментэктомии и кончая расширенной правосторонней гемигепатэктомией.
При кистах печени применяют вскрытие и дренирование полости кист, иссечение кисты, резекцию печени, цистодигестивные анастомозы и марсупиализацию кисты.
Киста печени– очаговое полостное образование печени, ограниченное соединительнотканной капсулой с жидкостью внутри. Киста печени проявляется болевым синдромом в правом подреберье, дискомфортом в эпигастрии, тошнотой, диспепсией, асимметрией живота. Диагностика кист печени основывается на данных ультразвукового и томографического сканирования. Лечение кисты печени может включать ее радикальное удаление (вылущивание, резекцию печени, иссечение стенок кисты) или паллиативные методы (опорожнение, марсупиализацию кисты, создание цистоэнтеро- или цистогастроанастомоза).
Киста печени представляет собой доброкачественное полостное образование, заполненное жидкостью, изнутри выстланное слоем цилиндрического или кубического эпителия. Чаще всего кисты заполнены прозрачной жидкостью, не имеющей запаха и цвета; реже кисты печени могут содержать желеподобную массу или жидкость коричневато-зеленого цвета, состоящую их холестерина, билирубина, муцина, фибрина, эпителиальных клеток. При кровоизлияниях в полость кисты печени содержимое становится геморрагическим; при инфицировании – сливкообразным, гнойным.
Кисты печени могут располагаться в различных сегментах, долях и даже связках печени, поверхностно или в глубине; иногда имеют тонкую перемычку (ножку кисты). Диаметр выявляемых кист печени варьирует от нескольких миллиметров до 25 и более сантиметров. В гепатологии и гастроэнтерологии кисты печени диагностируются приблизительно у 0,8 % населения. У женщин кисты печени выявляются в 3-5 раз чаще, чем у мужчин, как правило, в возрасте 40-50 лет. По клиническим наблюдениям, кисты печени могут сочетаться с желчнокаменной болезнью, циррозом печени, кистами желчных протоков, поликистозом яичников, поликистозом почек и поджелудочной железы.
Классификация кист печени
Понятие «кисты печени» объединяет различные по происхождению нозологические формы. Прежде всего, выделяют истинные и ложные кисты печени. Истинные кисты являются врожденными по происхождению и имеют внутреннюю эпителиальную выстилку. Среди солитарных истинных образований встречаются простые, ретенционные, дермоидные кисты печени, многокамерные цистаденомы.
Ложные кисты носят вторичный, приобретенный характер; чаще образуются после операций, травм, воспалений, в связи с чем стенками их полости служат фиброзно-измененные ткани печени.
По количеству полостей различают одиночные и множественные кисты печени. При выявлении кист в каждом сегменте печени говорят о поликистозе печени.
Кроме этого, выделяют непаразитарные и паразитарные кисты печени; последние, как правило, представлены эхинококковыми кистами (эхинококкоз печени).
Причины образования кист печени
В вопросе происхождения истинных непаразитарных кист печени нет единого мнения. Часть авторов придерживается взглядов, что кисты образуются в результате воспалительной гиперплазии желчных путей в период эмбриогенеза и их последующей обструкции. Рассматривается связь между возникновением кисты печени и приемом гормональных препаратов (эстрогенов, оральных контрацептивов).
Преобладающей в современной медицине является теория, объясняющая возникновение кист печени из аберрантных внутри- и междольковых желчных ходов, которые в процессе эмбрионального развития не включаются в систему желчных путей. Секреция эпителия этих замкнутых полостей приводит к накоплению жидкости и их превращению в кисту печени. Эта гипотеза подтверждается тем фактом, что секрет кисты не содержит желчи, а полость образования не сообщается с функционирующими желчными ходами.
Ложные кисты образуются вследствие некроза опухолей, травматического повреждения печени, паразитарного поражения печени эхонококком, амебного абсцесса.
Симптомы кисты печени
Небольшие одиночные кисты печени, как правило, не имеют клинических проявлений. Симптоматика чаще развивается при достижении кистой размера 7-8 см, а также при поражении множественными кистами не менее 20 % объема печеночной паренхимы.
В этом случае отмечается чувство распирания и тяжести в правом подреберье и эпигастрии, которые усиливаются после еды или нагрузки. На фоне увеличения кисты печени развиваются диспепсические явления: отрыжка, тошнота, рвота, метеоризм, понос. Среди прочих неспецифических симптомов сопровождающих развитие кисты печени, отмечают слабость, потерю аппетита, повышенную потливость, одышку, субфебрилитет.
Гигантские кисты печени вызывают асимметричное увеличение живота, гепатомегалию, похудание, желтуху. В ряде случаев киста пальпаторно определяется через переднюю брюшную стенку в виде тугоэластического флюктуирующего безболезненного образования в правом подреберье.
Осложненное течение кисты печени развивается при кровоизлиянии в ее стенку или полость, нагноении, перфорации, перекруте ножки кисты, злокачественном перерождении. При геморрагии, разрыве кисты или прорыве ее содержимого в прилежащие органы развивается острый приступ абдоминальных болей. В этих случаях высока вероятность кровотечения в брюшную полость, перитонита. При сдавлении расположенных рядом желчных протоков появляется желтуха, а при инфицировании – образуется абсцесс печени.
Эхинококковые кисты печени опасны распространением паразитов гематогенным путем с образованием отдаленных инфекционных очагов (например, эхинококковых кист легкого). При распространенном поликистозе печени со временем возможно развитие печеночной недостаточности.
Диагностика кисты печени
Большая часть кист печени обнаруживается случайно при проведении УЗИ брюшной полости. По данным эхографии киста печени определяется как ограниченная тонкой стенкой полость овальной или округлой формы с анэхогенным содержимым. При наличии в полости кисты крови или гноя, становятся различимы внутрипросветные эхосигналы.
В ряде случаев УЗИ печени используется для проведения чрескожной пункции кисты с последующим цитологическим и бактериологическим исследованием секрета.
С помощью КТ, МРТ, сцинтиграфии печени, ангиографии чревного ствола и брыжеечных артерий проводится дифференциальная диагностика кисты печени с гемангиомой, опухолями ретроперитонеального пространства, опухолями тонкого кишечника, поджелудочной железы, брыжейки, водянкой желчного пузыря, метастатическими поражениями печени. При сомнениях в диагнозе выполняется диагностическая лапароскопия.
Для исключения паразитарной этиологии кист печени проводятся специфические серологические исследования крови (ИФА, РНГА).
Лечение кисты печени
Пациенты с бессимптомными кистами печени, не превышающими 3-х см в диаметре, нуждаются в динамическом наблюдении гастроэнтеролога (гепатолога).
Показаниями к хирургическому лечению кист печени оперативным путем служат осложнения (кровотечение, разрыв, нагноение и др.); большие и гигантские размеры кисты (до 10 см и более); сдавление желчных путей с нарушением желчеоттока; компрессия системы воротной вены с развитием портальной гипертензии; выраженная клиническая симптоматика, ухудшающая качество жизни; рецидивы кисты печени после попытки ее пункционной аспирации. Лечение паразитарных кист печени проводится под наблюдением инфекциониста или паразитолога.
Все оперативные вмешательства, производимые по поводу кист печени, могут быть радикальными, условно-радикальными и паллиативными. К радикальным способам при солитарной кисте относят резекцию печени; при поликистозе – трансплантацию печени.
Условно-радикальные методы могут включать вылущивание (энуклеацию) кисты или иссечение стенок кисты. При выполнении данных вмешательств широко используется малоинвазивный лапароскопический доступ.
Паллиативные вмешательства при кистах печени не подразумевают удаления полостного образования и могут заключаться в прицельной пункционной аспирации содержимого кисты с последующей склерооблитерацией полости; вскрытии, опорожнении и дренировании остаточной полости кисты; марсупиализации кисты; фенестрации кисты; цистоэнтеростомии или цистогастростомии.
Стойкий эффект после чрескожной пункционной аспирации кисты и ее склерозирования достигается при относительно небольших размерах (до 5-6 см) полости. Проведение вскрытия и наружного дренирования показано при солитарных посттравматических кистах печени, осложненных разрывом стенки или нагноением. Марсупиализацию (опорожнение кисты с подшиванием ее стенок к краям операционной раны) проводят при центральной локализации кисты в воротах печени, сдавлении желчных путей, наличии портальной гипертензии. К фенестрации - вскрытию и иссечению свободных стенок кист, как правило, прибегают при множественных кистах или поликистозе печени в отсутствие признаков печеночно-почечной недостаточности. При гигантских кистах производится наложение цистогастроанастомоза или цистоэнтероанастомоза, т. е. создается сообщение полости кисты печени с полостью желудка или кишечника.
Прогноз при кисте печени
После радикального удаления солитарных кист печени прогноз в целом благоприятный. После паллиативных вмешательств в различные отдаленные сроки возможны рецидивы кисты печени, требующие проведения повторных лечебных мероприятий.
Прогрессирующее увеличение нелеченных кист печени может привести к целому ряду опасных осложнений. В случае распространенного поражения печени возможно наступление летального исхода вследствие печеночной недостаточности.
Билет № 3
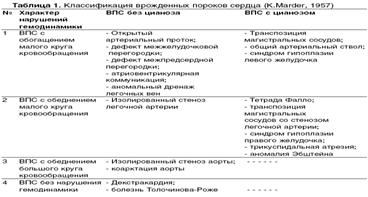
Вопрос 1. Врожденные пороки сердца. Классификация. Открытый артериальный проток. Коарктация аорты. Дефект межпредсердной перегородки. Тетрада Фалло. Клиника. Диагностика. Лечение.
Это групповое понятие объединяет аномалии положения и морфологической структуры сердца и крупных сосудов. Среди всех пороков сердца чаще всего встречаются дефекты межжелудочковой перегородки. Без оперативного лечения большинство детей с врожденными пороками сердца погибают в течение 1—2-го года жизни. Кл пороков. В настоящее время клинически значимые пороки сердца подразделяют по характеру гемодинамических нарушений в малом круге кровообращения на следующие группы:
1) пороки с переполнением (гиперволемией) малого круга кровообращения;
2) пороки с обеднением (гиповолемией) его;
3) пороки с малоизмененным или неизмененным кровотоком. В 1и2 группах выделяют пороки с цианозом и без цианоза кожных покровов.
1 группы., не сопровождающимся ранним цианозом, относятся открытый артериальный (боталлов) проток, дефект межпредсердной или межжелудочковой перегородки, коарктация аорты и др. К порокам, сопровождающимся цианозом, относятся атрезия трехстворчатого клапана с нормальным калибром легочного ствола и большим дефектом межжелудочковой перегородки, открытый артериальный проток со стоком крови из легочной артерии в аорту.
2 группы, не сопровождающимся цианозом, изолированный стеноз ствола легочной артерии.К порокам, сопровождающимся цианозом, относятся триада, тетрада, пентада Фалло (комбинация нескольких врожденных пороков), атрезия трехстворчатого клапана с сужением ствола легочной артерии или малым дефектом межжелудочковой перегородки и др.
3 группы с неизмененным кровотоком в сосудах легкого относятся аномалии дуги аорты и ее ветвей, отсутствие дуги аорты, стеноз и коарктация аорты, митральная атрезия, атрезия аортального клапана, недостаточность митрального клапана.
У б-х с пороками первой группы имеется внутрисердечное патологическое сообщение со сбросом крови из артер русла в венозное (из левого желудочка сердца и сосудов, т. е. слева направо), поэтому в периферическое артер русло поступает недостаточное количество артериальной крови. В связи с этим дети отстают в физ развитии, часто болеют пневмонией, кожные покровы у них бледные, иногда с подчеркнуто яркой окраской губ. Бледность усиливается после физической нагрузки. Для всех пороков этой группы характерно переполнение кровью (гиперволемия) правых отделов сердца и сосудов легкого. При R легких признаки гиперволемии в малом круге проявляются усилением легочного рисунка, расширением корней легких, выбуханием легочной артерии вследствие переполнения ее кровью. Перкуторно и R определяется расширение правых камер сердца. На ЭКГ четко выявляются гипертрофию правого жел. При узи(эхокардиография, цветное допплеровское сканирование) или зондировании сердца ангиокардиографии подтверждается дилатация правых отделов сердца, повышение давления и содержания кислорода в крови, взятой из них. Распознав синдром переполнения малого круга кровообращения, врач по клиническим признакам может выбрать из группы пороков с гиперволемией малого круга кровообращения тот, которому будут соответствовать аускультативные и другие симптомы. систолический шум во 2 межреберье у левого края грудины характерен для открытого артериального (боталлова) протока, а резкий дующий систолический шум в 4 межреберье слева от грудины — для дефекта межжелуд перегородки.
Ко 2группе относят пороки, при которых имеется обеднение малого круга кровью (гиповолемия) вследствие затруднения ее выброса правым желуд в систему легочной артерии, например при стенозе легочной арт. Ограниченное поступление крови в легкие наблюдается не только при стенозе путей оттока крови из правого желудочка,но и при сбросе крови из него в систему большого круга кровообращения (сброс справа налево). Это обычно наблюдается при тетраде, триаде, пентаде Фалло.
При значительном сужении легочной артерии они испытывают слабость, быструю утомляемость, боли в области сердца, одышку при физической нагрузке. Цвет кожных покровов у таких детей нормальный, часто наблюдается "сердечный горб". Ультразвуковое исследование (так же как и ангиокардиография) позволяет выявить сужение клапана легочной артерии
Артериальный проток(боталлов) соустье между аортой и легочным стволом, которое существует во время внутриутробного периода развития плода. Вскоре после рождения проток облитерируется, превращается в артериальную связку. Функционирование артериального протока в течение первого года жизни считается врожденным пороком. Эта аномалия развития встречается наиболее часто и составляет до 25 % от их общего числа.
Гемодчнамическая сущность порока состоит в постоянном сбросе артериальной крови в малый круг кровообращения, вследствие чего происходит перемешивание артериальной и венозной крови в легких и развивается гиперволемия малого круга, которая сопровождается необратимыми морфологическими изменениями в сосудах легких и последующим развитием легочной гипертензии. Прогрессирующее повышение сопротивления малого круга вызывает перегрузку правого желудочка сердца, обусловливая его гипертрофию и последующую дистрофию миокарда. Степень нарушения кровообращения зависит от диаметра протока и объема сбрасываемой через него крови.
Клиника и диагностика. Жалобы обычно появляются с развитием декомпенсации кровообращения и заключаются в повышенной утомляемости, одышке. Однако наиболее характерны для порока частые респираторные заболевания и пневмонии на первом и втором году жизни. При обследовании больного обнаруживается систоло-диастолический шум над сердцем с эпицентром над легочной артерией (анатомическое определение проекции). С развитием легочной гипертензии в этой же точке появляется акцент второго тона. Как правило, шум становится интенсивнее при выдохе или физической нагрузке. Электрокардиографические признаки нехарактерны. При рентгенологическом исследовании определяются признаки переполнения кровью малого круга кровообращения и умеренно выраженная митральная конфигурация сердца за счет выбухания дуги легочной артерии. В поздние сроки естественного течения порока становятся более выраженными рентгенологические признаки склерозирования сосудов легких и обеднение их рисунка. Катетеризация камер сердца необходима лишь в осложненных или неясных случаях. При введении контрастного вещества в восходящую аорту оно через проток попадает в легочные артерии. В целом диагностика этого порока больших трудностей не представляет.
Частым осложнением открытого артериального протока (особенно малого диаметра) является септический эндокардит.
Операцию выполняют из левостороннего бокового доступа. выделяют, перевязывают двумя лигатурами и прошивают третьей. При легочной гипертензии закрытие а протока может привести к повышению давления в легочной артерии, перегрузке правых отделов сердца и правожелудочковой недостаточности.
стали успешно применять торакоскопическое закрытие боталлова протока у новорожденных с высоком риском открытого оперативного вмешательства. По определенным показаниям с 1986 г. используют малоинвазивное транскатетерное закрытие протока специальными устройствами, позволяющими ввести их в просвет протока и обтурировать его. Эффективность и стоимость этой процедуры уступают открытому оперативному вмешательству. Оперативное вмешательство до 5-летнего возраста дает наилучшие результаты.
Лечение только оперативное. Операцию проводят в условиях искусственного кровообращения. Доступ к дефекту осуществляют, широко вскрывая правое предсердие. При незначительных размерах дефект ушивают. Если его диаметр превышает 1 см, то закрытие производят с помощью синтетической заплаты или лоскутом, выкроенным из перикарда. При впадении легочных вен в правое предсердие один из краев заплаты подшивают не к латеральному краю дефекта, а к стенке правого предсердия таким образом, чтобы кровь из легочных вен после реконструкции поступала в левое предсердие. Первичный дефект всегда устраняют с помощью заплаты. Перед его закрытием производят пластику расщепленной створки митрального клапана путем тщательного ушивания. Таким образом ликвидируют митральную недостаточность.
Коарктация аорты— врожденное сужение или полное закрытие ее просвета на ограниченном участке. Чаще всего (95 %) это сужение располагается в области перешейка аорты, под которым понимается отрезок от левой подключичной артерии до первой пары межреберных артерий. Возможны и другие локализации сужений — в восходящей, нисходящей грудной или брюшной аорте. Коарктация аорты составляет до 30 % всех врожденных пороков сердца.
Гемодинамическая сущность порока заключается в затруднении тока крови через суженный участок, в результате чего значительно возрастает артериальное давление в аорте и ее ветвях выше места сужения (до 200 мм рт. ст. и более) и понижается ниже него, т. е. развивается синдром артериальной гипертензии в сосудах головного мозга и верхней половины тела, что влечет за собой систолическую перегрузку левого желудочка, гипертрофию миокарда с последующей его дистрофией. Последняя усугубляется и присоединением со временем коронарной недостаточности. В итоге развивается тяжелая декомпенсация левого желудочка. Гипертония в системе сосудов мозга приводит к появлению ряда церебральных симптомов. В артериальной системе ниже места сужения артериальное давление значительно снижено, и кровоснабжение нижней части тела осуществляется преимущественно за счет коллатерального кровообращения, которое не всегда бывает достаточным.
Клиника и диагностика. Жалобы, как правило, отсутствуют. Лишь с достижением возраста половой зрелости могут появляться общая слабость, головокружение, головные боли, парестезии и повышенная зябкость ног. Диагностика заболевания весьма простая: знание этой патологии и внимательное обследование позволяют точно поставить диагноз в подавляющем большинстве случаев. Отсутствие пульсации на артериях ног при постоянном повышенном давлении в артериях верхних конечностей — почти патогномоничный признак коарктации аорты. При неполной окклюзии просвета аорты в области коарктации пульсация на артериях ног может сохраняться, но быть ослабленной, что подтверждается и сниженным артериальным давлением (у здорового человека артериальное давление на нижних конечностях на 20-40 мм рт. ст. выше, чем на верхних). При осмотре кроме соответствующей формы тела (нередко атлетический тип сложения у мужчин, пикнический — у женщин) можно заметить пульсацию расширенных межреберных артерий. Границы сердца, как правило, расширены влево за счет гипертрофии левого желудочка. При аускультации выслушивается систолический шум по всему левому краю грудины, а также со стороны спины над проекцией сужения аорты, а иногда и над расширенными, пульсирующими межреберными артериями. ЭКГ данные у детей могут выявить лишь признаки систолической перегрузки левого желудочка, у взрослых — его гипертрофию и коронарную недостаточность, нередко с диффузными мышечными изменениями.
На рентгенограммах определяется преимущественно аортальная конфигурация сердца за счет расширения левого желудочка. Характерным признаком коарктации аорты является наличие узур нижнего края 3-4 пар ребер. Узурация ребер развивается вследствие деформации кости в области нижней бороздки резко расширенными и извитыми межреберными артериями. Как пульсация межреберных артерий, так и узурация ребер могут быть выявлены при пальпации грудной клетки больного. На томограмме, как правило, хорошо видно место сужения аорты. Ангиокардиография показана в неясных случаях или при подозрении на сочетание коарктации аорты с другими пороками. Наиболее частый из них— открытый артериальный проток и стеноз устья аорты. В более поздние сроки может развиваться недостаточность аортального клапана вследствие дистрофических изменений в основании восходящей аорты.
Средняя продолжительность жизни неоперированных больных 25—30 лет. Наиболее часто причиной смерти больных являются внутричерепные кровоизлияния, разрывы аорты, инфаркт миокарда, острая сердечная недостаточность и септический эндокардит.
Дифференциальную диагностику коарктации аорты следует проводить с нейроциркуляторной дистонией, гипертонической болезнью, вазоренальной гипертонией, пороками сердца и заболеваниями почек, сопровождающимися артериальной гипертензией. Наибольшее число ошибок в распознавании этого порока связано с забвением основных клинических проявлений заболевания, недооценкой общеврачебных методов исследования, пренебрежением к пальпации артериального русла, а также измерению артериального давления на ногах и сравнительной оценкой полученных данных.
Лечение только оперативное. Идеальным видом операции, особенно у растущих детей, является резекция суженного участка аорты с ее анастомозом конец в конец. Однако такая операция нередко невыполнима при выраженной протяженности сужения и тяжелых склеротических изменениях стенки сосуда. В подобной ситуации проводится протезирование аорты синтетическим протезом. а также шунтирование места сужения левой подключичной артерией.
Результаты оперативного лечения определяются в значительной степени возрастом больного. Наилучшими они оказываются у детей, оперированных в возрасте до 3 лет, когда нет тяжелых изменений стенки аорты и межреберных артерий и имеются более благоприятные условия для радикальной коррекции порока, устранение которого обычно приводит к нормализации общего артериального давления. Операция у взрослых значительно сложнее в техническом отношении и, как правило, дает значительно менее выраженный гипотензивный эффект, так как в генезе артериальной гипертонии значительную роль играют изменения в центральной регуляции сосудистого тонуса и почечные механизмы формирования гипертонии. Однако после устранения коарктации артериальная гипертония становится более управляемой медикаментозными средствами, что позволяет предупредить развитие перечисленных выше тяжелых осложнений, так как через 1,5—3 года после коррекции порока артериальная гипертония становится менее выраженной. Таким образом, оперативное лечение коарктации аорты у взрослых в комплексе с антигипертензивной медикаментозной терапией в послеоперационном периоде позволяет значительно продлить и жизнь больных, и улучшить ее качество.
Дефект межпредсердной перегородки представляет собой патологическое соустье между правым и левым предсердием. Он составляет около 20 % от всех врожденных пороков сердца. Дефект может располагаться в различных отделах перегородки, иметь различную форму и размеры. Условно различают первичные (находящиеся на уровне фиброзного кольца атриовентрикулярных клапанов) и вторичные (высокие) дефекты межпредсердной перегородки. Нередко дефект сочетается с другими аномалиями развития внутрисердечных структур (расщеплением митрального или трикуспидального клапана, стенозом легочного ствола).
Гемодинамическая сущность порока заключается в сбросе артериальной крови из левого предсердия в правое и перемешиванием с венозной, вызывая гиперволемию малого круга кровообращения, сопровождаемую легочной гипертензией. Легочная гипертензия при дефекте межпредсердной перегородки носит весьма злокачественный характер, так как необратимые изменения в легких развиваются быстро и рано, приводя к тяжелой декомпенсации правого сердца. Частым осложнением такого порока является септический эндокардит.
Клиника и диагностика. Обычно жалобы связаны с декомпенсацией кровообращения. Тяжесть ее зависит от степени легочной гипертензии, которая в свою очередь определяется величиной объема крови, сбрасываемой в малый круг. Аускультативно дефект межпредсердной перегородки проявляется нежным систолическим шумом с эпицентром над легочной артерией. Шум обусловлен относительным стенозом основания легочного ствола, через который протекает избыточный объем крови. Второй тон над легочной артерией усилен и часто расщеплен. На ЭКГ имеются признаки перегрузки правых отделов сердца с гипертрофией правого желудочка и предсердия. Весьма часто обнаруживается неполная или полная блокада правой ножки пучка Гиса.
При рентгенологическом исследовании определяется увеличение сердца за счет правого предсердия, желудочка и ствола легочной артерии. Имеются также повышенная пульсация корней легких и усиление общего сосудистого рисунка легочной ткани.
При зондировании сердца обнаруживаются повышение давления в правом предсердии, правом желудочке и легочном стволе. Зонд свободно переходит из правого предсердия в левое. Контрастное вещество, введенное в левое предсердие, через дефект межпредсердной перегородки попадает в правое предсердие и далее в малый круг кровообращения. На основании рентгенологических данных можно рассчитать объем сброса крови, определить локализацию и размеры дефекта. Продолжительность жизни при дефекте межпредсердной перегородки в среднем составляет около 25 лет.
Лечение только оперативное. Преимущественно выполняют операции на открытом сердце в условиях искусственного кровообращения или гипотермии (общей или краниоцеребральной). Вторичные средней величины дефекты могут быть ушиты. Большие вторичные и все первичные дефекты, как правило, закрываются с использованием пластических материалов (ауто- или ксено-перикард, синтетические ткани). Хорошие результаты операции могут быть получены лишь при выполнении ее в раннем детском возрасте. Выполнение операции в более поздние сроки не позволяет добиться всесторонней реабилитации пациентов вследствие формирования вторичных морфологических изменений в легких, миокарде и печени.
Тетрада Фалло — наиболее часто встречающийся порок синего типа. Его анатомическая сущность заключается в сочетании сужения выходного отдела правого желудочка, высокого дефекта межжелудочковой перегородки, смещения устья аорты вправо (декстрапозиция) и гипертрофии миокарда правого желудочка.
Основные нарушения гемодинамики при тетраде Фалло обусловлены тем, что венозная кровь из правого желудочка во время его систолы с трудом и в недостаточном количестве попадает в легочный ствол, вследствие чего возникает гиповолемия малого круга кровообращения. Большая же часть венозной крови из правого желудочка через дефект межжелудочковой перегородки попадает в левый желудочек и аорту, смешиваясь с артериальной, что обусловливает цианоз кожных покровов.
Клиника и диагностика. Тетрада Фалло сопровождается одышкой даже в состоянии покоя. Обращает на себя внимание цианоз кожных покровов и слизистых оболочек различной интенсивности. Пальцы рук деформированы в виде «барабанных палочек». Дети обычно значительно отстают в физическом развитии, часто болеют различными респираторными заболеваниями, ангинами и т. п. Грудная клетка, как правило, деформирована. После физической нагрузки возникают одышечно-цианотические приступы. Эти приступы, являясь следствием хронической субпороговой ишемии мозга, выражаются одышкой, тахикардией, нередко с аритмией и усилением цианоза. Больные часто принимают положение на корточках, что облегчает их состояние, так как в этих условиях, по-видимому, увеличивается сопротивление в большом круге кровообращения, и благодаря этому возрастает легочный кровоток.
Аускультативно порок проявляется грубым пансистолическим шумом с максимумом звучания в четвертом межреберье слева от грудины. Второй тон над легочной артерией ослаблен. На ЭКГ отмечаются признаки значительной перегрузки и гипертрофии правого желудочка, а рентгенологически выявляется характерная конфигурация сердца — западание легочной артерии с высоко приподнятой и закругленной верхушкой сердца, легочный рисунок значительно обеднен. В боковых позициях определяется выраженное увеличение правого желудочка. При зондировании катетер не удается провести в легочную артерию и он легко проходит из правого желудочка в аорту. Контрастное вещество, введенное в правый желудочек, попадает и в легочную артерию, и в аорту, причем степень контрастирования этих сосудов зависит от величины транспозиции аорты.
Продолжительность жизни больных тетрадой Фалло определяется степенью кислородного голодания и в среднем составляет около 10—14 лет.
Лечение только оперативное. Во время одышечно-цианотического приступа больному следует придать коленно-локтевое положение, дать кислород, ввести промедол и препараты, снижающие сопротивление в малом круге кровообращения. Радикальная коррекция порока выполняется в условиях искусственного кровообращения и заключается в расширении выходного отдела правого желудочка (т. е. в ликвидации препятствия оттока крови в малый круг) и закрытии дефекта межжелудочковой перегородки с перемещением аорты в левый желудочек. Операция сопровождается довольно высокой летальностью в ближайшем послеоперационном периоде. Однако у выживших, как правило, отдаленные результаты вполне оправдывают риск вмешательства. Если тяжесть состояния больных или анатомические особенности порока не позволяют выполнить его радикальную коррекцию, применяют паллиативные операции. Смысл их заключается в обогащении кровью малого круга кровообращения (создается соустье между аортой и легочной артерией, т.е. открытый артериальный проток, или между полыми венами и легочной артерией). У ряда больных кроме сужения собственно выходного отдела правого желудочка имеется тяжелое сужение легочного ствола и его артерий вплоть до гипоплазии. Этим больным могут быть выполнены только паллиативные операции.
Дата добавления: 2018-04-04; просмотров: 888; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
