Провести химические испытания на подлинность, чистоту и количественное определение фенола
| Методика проведения | Наблюдения | Выводы | |||
| Свойства: бесцветные или бледно-желтоватые кристаллы или кристаллическая масса, которая расплывается при соприкосновении с воздухом. |
| ||||
| Растворимость: растворим в воде, очень легко растворим в спирте, глицерине, метиленхлориде. |
| ||||
| Приготовление раствора: 1,0 г субстанции растворяют в воде, доводят объем раствора до 15 мл тем же растворителем. Подлинность: 1. К 1 мл раствора, приготовленного как указано выше, прибавляют 10 мл воды и 0,1 мл раствора железа (III) хлорида – появляется фиолетовое окрашивание. |
| ||||
| Химизм: | |||||
| 2. К 1 мл раствора прибавляют 10 мл воды и 1 мл бромной воды; выпадает осадок бледно-желтого цвета. |
| ||||
| Химизм:
| |||||
| 3. Кислотность: К 2 мл раствора прибавляют 0,05 мл раствора метилового оранжевого. Полученный раствор должен быть жёлтым. |
| ||||
| Количественное определение: 0,5 г субстанции растворяют в воде и доводят объём раствора тем же растворителем до 250,0 мл. 25,0 мл полученного раствора помещают в колбу с притертой стеклянной пробкой, прибавляют 50,0 мл 0,0167 М и раствора калия бромата, 1 г калия бромида и 10 мл 50% раствора кислоты серной. Раствор в колбу тщательно перемешивают и оставляют на 15 минут. Затем к смеси добавляют 20 мл раствора калия йодида, сильно взбалтывают, оставляют на 10 минут в темном метсе, после чего, выделившийся йод оттитровывают 0,1 М раствором натрия тиосульфата (индикатор – крахмал). Параллельно проводят контрольный опыт.
1 мл 0,0167 М соответствует 0,001572 г фенола, которого в препарате должно быть 99-105%. | Формула расчета содержания действующего вещества (Х%, Хг) | Расчет теоретического объема титранта (мл) | |||
|
| |||||
| Химизм: | |||||

Задание № 6
Провести химические испытания на подлинность, чистоту и количественное определение резорцина.
| Методика проведения | Наблюдения | Выводы | |||
| Свойства: белый или со слабым желтоватым оттенком кристаллический порошок со слабым характерным запахом. Под влиянием света и воздуха постепенно окрашивается в розовый цвет. |
| ||||
| Растворимость: очень легко растворим в воде, 95% спирте, легко растворим в эфире, очень малорастворим в хлороформе, растворим в глицерине и жирном масле. |
| ||||
| Подлинность: 1. К 0,1 г субстанции приливают 2 мл воды, 3 капли раствора хлорида окисного железа появляется сине-фиолетовое окрашивание, переходящее от прибавления раствора аммиака в буровато-желтое. |
| ||||
| Химизм: | |||||
| 2. 0,1 г субстанции растворяют в 1 мл воды, прибавляют 1 мл раствора натрия гидроксида концентрированного и 0,1 мл хлороформа, нагревают и охлаждают; появляется интенсивное темно-красное окрашивание, которое при прибавлении небольшого избытка кислоты хлористоводородной переходит в бледно-жёлтое окрашивание. |
| ||||
| Химизм:
| |||||
| Примесь: 4. Пирокатехин К 0,1 г субстанции приливают 10 мл воды и 0,5 мл раствора ацетата свинца в течение 2-х минут не должно появляться ни осадка ни мути. |
| ||||
| Химизм:
| |||||
| 5. Фенол При нагревании 1 г субстанции с 2 мл воды на водяной бане (40-50°С) не должно ощущаться запаха фенола. |
| ||||
| Количественное определение: 0,2 г препарата помещают в мерную колбу на 100 мл, растворяют в 20 мл воды и доводят до метки. 20 мл этого раствора переносят в склянку для бромирования объемом 250мл добавляют 40 мл 0,0167 М бромата калия, 10 мл раствора бромида калия, 10 мл 50% серной кислоты, перемешивают, оставляют на 15 мин. Затем прибавляют 20 мл раствора калия йодида, взбалтывают и оставляют в темном месте на 10 минут, прибавляют 2-3 капли хлороформа и титруют выделившийся йод 0,1 М тиосульфатом натрия. 1мл 0,0167 М бромата калия соответствует 0,001837 С6Н6О2 которого должно быть 99,0%. | Формула расчета содержания действующего вещества (Х%, Хг)
| Расчет теоретического объема титранта (мл) | |||
|
| |||||
| Химизм: | |||||
Вывод по работе: __________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Лабораторная работа № 6
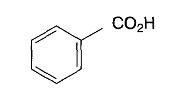
Тема:Лекарственные вещества – производные бензойной и салициловой кислот. Лекарственные вещества – производные ароматических аминокислот.
 Цель:определить подлинность, доброкачественность лекарственных веществ, провести их количественное определение.
Цель:определить подлинность, доброкачественность лекарственных веществ, провести их количественное определение.
Задание № 1
Дата добавления: 2018-02-28; просмотров: 615; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
