Завдання 1-15мають по чотири варіанти відповідей, із яких тільки одна відповідь правильна. Оберіть правильну, на Вашу думку відповідь
1. Еквівалент H2SO4 у реакціях
H2SO4+Mg → MgSO4+H2; H2SO4+2KOH → K2SO4+2H2O
становить: а) 1/2 моль; б) 1 моль; в) 0,5 моль; г) 2моль.
2. Молярна маса еквіваленту H2SO4 у реакціях:
H2SO4+Zn=ZnSO4 + H2; H2SO4+Ba(OH)2=BaSO4+2H2O
Дорівнює: а) 98г/моль; б) 49г/моль; в) 0,5г/моль; г) 1г/моль.
3. Еквівалент Al(OH)3 у реакціях
Al(OH)3+HCl → Al(OH)2Cl+H2O; Al(OH)3+HNO3 → Al(OH)2NO3+H2O
становить: а) 1/2 моль; б) 1/3 моль; в) 1 моль; г) 26 моль.
4. Молярна маса еквіваленту Al(OH)3 у реакціях.
Al(OH)3+2HNO3 → AlOH(NO3)2+2H2O;
Al(OH)3+H2SO4 → AlOHSO4+2H2O.
дорівнює: а) 39г/моль; б) 78г/моль; в) 26г/моль; г) 0,5 г/моль.
5. Fe(OH)3 взаємодіє з хлоридною кислотою з утворенням хлорид дигідроксоферума. Еквівалент Fe(OH)3 в цій реакції становить:
а) 1/2 моль; б) 1 моль; в) 1/3 моль; г) 0,5 моль.
6. Маса 1 еквіваленту елементу називається:
а) еквівалент; в) молярна маса;
б) еквівалентна маса; г) мольна маса.
7.Молярна маса еквіваленту виражається в:
а) моль; б) л/моль; в) г/моль; г) г/мл.
8.Кількість речовини, що сполучається з 1 моль атомів гідрогену або зміщує цю саму кількість атомів гідрогену у хімічних реакціях називається:
а) еквівалентний об’єм; в) закон еквівалентів;
б) еквівалентна маса; г) еквівалент.
9.Еквівалентний об’єм водню становить:
а) 22,4 л/моль; б) 5,6 л/моль; в) 11,2 л/моль; г) 7,4 л/моль.
|
|
|
10.Математичний вираз закону еквівалентів:
а)  ; б)
; б) 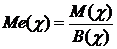 ;
;
в)  ; г)
; г) 
11. Число, що показує, яка частка реальної частинки речовини еквівалентна одному йону гідрогену в даній кислотно – основній реакції або одному електрону в реакції окиснення – відновлення називається:
а)еквівалент; в)фактор еквівалентності;
б)еквівалентна маса; г)еквівалентний об’єм.
12.Молярний об’єм будь-якого газу при н.у. дорівнює:
а) 11,2 л; б) 5,6 л; в) 1 л; г) 22,4 л.
13. Молярна маса еквіваленту для оксидів визначається за формулою:
а) 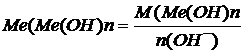 ; б)
; б)  ;
;
в)  ; г)
; г) 
14.Молярна маса еквіваленту чисельно дорівнює:
а)відносній масі еквівалента в г/моль; в)еквіваленту;
б)еквівалентному об’єму в л/моль; г)молярній масі в г/моль.
15.Молярна маса еквівалента сполуки дорівнює:
а)сумі молярних мас еквівалентів складових його частин;
б)добутку фактора еквівалентності на молярну масу речовини;
в)молярній масі;
г)еквівалентному об’єму.
При виконанні завдань 16-30 Ви повинні дати одну правильну відповідь у вигляді числа, знайти яке можна лише виконавши на чернетці правильно певні розрахунки.
|
|
|
16. При розчиненні у воді 0,045 г тривалентного металу виділилось 56 мл водню, виміряного за н.у. Молярна маса еквіваленту металу дорівнює:
а) 9 г/моль; б) 27 г/моль; в) 3 г/моль; г) 16 г/моль.
17. Молярна маса еквіваленту металу у 2 рази більша, ніж молярна маса еквіваленту оксигену. У скільки раз маса оксиду більша маси металу:
а) у 2 рази; б) у 2,5 рази; в) у 1,5 рази; г) у 3 рази.
18. Сульфур утворює хлориди S2Cl2 і SCl2, молярна маса еквіваленту сульфура в SCl2 дорівнює 16г/моль. Вибрати правильне значення молярної маси еквіваленту сульфура в S2Cl2:
а) 8 г/моль; б) 16 г/моль; в) 32 г/моль; г) 4 г/моль.
19. Молярна маса еквіваленту металу дорівнює 12г/моль. Чому дорівнює молярна маса еквіваленту його оксиду;
а) 24 г/моль; б) 20 г/моль; в) 32 г/моль; г) неможливо визначити.
20.На нейтралізацію 2,45 г кислоти потрібно 2,00 г натрій гідроксиду. Молярна еквіваленту кислоти становить:
а) 45г/моль; б) 24г/моль; в) 49г/моль; г) 40г/моль.
21. Маса натрій гідросульфата, що утворюється при нейтралізації сульфатної кислотою розчину, який містить 8 г NaOH, дорівнює:
а) 24 г; б) 40 г; в) 8 г; г) 120 г.
22. При згоранні 5,00 г металу утворюється 9,44 г оксиду металу. Молярна маса еквіваленту металу становить:
|
|
|
а) 9,01 г/моль; б) 9 г/моль; в) 12 г/моль; г) 24г/моль.
23.Метал масою 3,24 г утворює оксид масою 3,48 г і сульфід масою 3,72 г. Молярна маса еквіваленту металу і сульфуру становить відповідно:
а)102 г/моль і 16 г/моль; б) 108 г/моль і 16 г/моль;
в) 32 г/моль; і 100 г/моль г) 104 г/моль і 48 г/моль.
24. Деякий метал масою 1,00 г сполучається з 8,89 г брому і з 1,78 г сульфуру. Молярна маса еквіваленту сульфуру дорівнює 16,0 г/моль, а молярні маси еквівалентів брому і металу становлять:
а) 80 г/моль і 9,02 г/моль; б) 79 г/моль і 10 г/моль;
в) 79,9 г/моль і 9 г/моль; г) 82 г/моль і 18 г/моль.
25. Для розчинення 16,88 г металу потрібно 14,7 г сульфатної кислоти. Молярна маса еквіваленту металу і об’єм гідрогену, який виділився, дорівнюють відповідно:
а) 56 Г/моль і 3,36 л; в) 24 г/моль і 336 л;
б) 48 г/моль і 33,6 л; г) 12 г/моль і 3,36 л.
26. На відновлення 1,8 г оксиду металу витрачено 883 мл гідрогену ( при н.у.) Молярна маса еквіваленту оксиду і металу дорівнюють:
а) 22,4 г/моль і 16 г/моль; в) 44 г/моль і 24 г/моль
б) 24 г/моль і 18 г/моль г) 2402 г/моль і 16,2 г/моль.
|
|
|
27.Кальцій масою 1,60 г і цинк масою 2,16 г витісняють із кислоти однакові кількості гідрогену, молярна маса еквіваленту кальцію дорівнює 20 г/моль, тоді молярна маса еквіваленту цинку становить:
а) 32,6 г/моль; б) 64 г/моль; в) 16 г/моль; г) 24 г/моль.
28.Вибрати правильне значення еквівалентних об’ємів оксигену і гідрогену при нормальних умовах:
а) 11,2 л О2 і 22,4л Н2; в) 5,6 л О2 і 11,2 Н2;
б) 11,2 л О2 і 11,2 л Н2; г) 22,4 лО2 і 11,2 л Н2.
29. Деяка кількість металу, молярна маса еквіваленту якого дорівнює 28 г/моль, витісняє із кислоти 0,7 л гідрогену (н.у.) і маса металу дорівнює:
а) 1,75 г; б) 28 г; в) 3,50 г; г) 12 г.
30.Із нітрату металу масою 3,85 г одержали його гідроксид масою 1,60 г. Молярна маса еквіваленту металу дорівнює:
а) 62 г/моль; б) 15 г/моль; в) 17 г/моль; г) 31 г/моль
Практичне заняття
Дата добавления: 2018-02-28; просмотров: 874; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
