МІСЬКА ОЛІМПІАДА З ХІМІЇ. 2004 рік. М (AsxSy) = 428 Мr (AsxSy) = х∙Ar(As) + y∙Ar(S)
 5. Дано: Розв’язок:
5. Дано: Розв’язок:
М (AsxSy) = 428 Мr (AsxSy) = х∙Ar(As) + y∙Ar(S)
n (As) = n(S) згідно умови х = у
 428 = х∙75 + х∙32
428 = х∙75 + х∙32
Формула? 107х = 428
х =4
As4S4
Відповідь: As4S4, ні.
6. 1). t0C
2H2 + O2 → 2H2O x → O2
2). t0C
H2S + I2 → S + 2HI z → HI
3). t0C
2F2 + 2H2O → O2 + 4HF z → HF
|
4NH3 + 3O2 → 2N2 + 6H2O x → N2
б) М (N2) = 28г/моль
-
 Дано: Розв’язок:
Дано: Розв’язок:
ν (N2) = 2моль N = NА∙ν
 N(N2) = 6,02∙10231/моль ∙ 2моль = 12,04∙1023молекул
N(N2) = 6,02∙10231/моль ∙ 2моль = 12,04∙1023молекул
N (N2) – ? 1молекула N2 містить 2атоми N,
N (N) – ? тому N(N) = 2∙12,04∙1023 = 24,08∙1023атомів
Відповідь: 28г/моль; 12,04∙1023молекул N2; 24,08∙1023атомів N.
Й клас
 1. Дано: Розв’язок:
1. Дано: Розв’язок:
Na2SO3·xH2O М(Na2SO3)=126г/моль, якщо маса кристалогідрату після зневоднення
Після зневоднення зменшилась у 2 рази, тоді m(Н2О)=126г
m < у 2 рази М(Н2О)= 18г/моль, то х = 126г : 18г/моль = 7моль

Формула ? Формула: Na2SO3·7H2O
Відповідь: Na2SO3·7H2O
 2. Дано: Розв'язок:
2. Дано: Розв'язок:
|
|
|
Mg на повітрі Нехай маса Mg, до реакції 100 г, тоді 10% - це 10 г Оксигену, тому щ
окиснився що маса суміші збільшилась за рахунок окиснення.
m(Mg) > на 10% Отже маса суміші (MgO та Mg) після реакції – 110 г.
10г. х
 ν(Mg) до ν(MgO) За рівнянням: 2Mg + О2 = 2 MgO х = 10 · 80 : 32 = 25г (MgO)
ν(Mg) до ν(MgO) За рівнянням: 2Mg + О2 = 2 MgO х = 10 · 80 : 32 = 25г (MgO)
1 моль 2 моль
32г. 80г.
Тоді в 110 г суміші буде 25г. MgO і 110 – 25 = 85 г Mg
ν(Mg) = 85 : 24 = 3,4 моль; ν(MgO) = 25 : 40 = 0,625 моль
ν(Mg) : ν(MgO) = 3,4 : 0,625 = 17 : 5
Відповідь: 17 моль Mg до 5 моль MgO.
МІСЬКА ОЛІМПІАДА З ХІМІЇ. 2004 рік
 3. Дано: Розв'язок:
3. Дано: Розв'язок:
m(газу)= 0,02г 1. Знаходимо υ(СО2), який помістився в даній посудині.
m (СО2)= 0,44г υ = 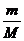 ; υ(СО2) =
; υ(СО2) =  = 0,01 моль
= 0,01 моль
|
|
|
 М(А) -? 2. М(А) =
М(А) -? 2. М(А) =  ; υ(А) = υ(СО2) – тому, що об’єм посудини однаковий.
; υ(А) = υ(СО2) – тому, що об’єм посудини однаковий.
V(посудини) - ? М(А) = 0,02г : 0,01 моль = 2 г/моль
m(повітря) - ? 3. V(посудини) = υ · Vm = 0,01 моль · 22,4 л/моль = 0,224 л.
4. m(повітря), яка може зайняти цей об’єм посудини рівна:
m(повітря) = υ · М(повітря) = 0,01 моль · 29 г/моль = 0,29 г.
Відповідь: 2 г/моль; 0,224 л.; 0,29 г.
4. Дано: Розв'язок:
ІІ ІІІ 6,5г z1
 m(Ме1 і Ме2)= 11,9г Ме′ + 2 НСl = Ме′Сl2 + H2 І
m(Ме1 і Ме2)= 11,9г Ме′ + 2 НСl = Ме′Сl2 + H2 І
НСl 2,41x 22,4л
V(газу) = 8,96л 5,4г z2
Ar(Me1) : Ar(Me2) = 2Ме″ + 6НСl = 2Ме″Сl3 + 3H2 ІІ
2,41 2x 67,2л
N(Me1) : N(Me2) = Нехай Ar(Me″) = х, тоді Ar(Me′) = 2,41х
|
|
|
1 : 2 Нехай в суміші m(Ме′) = у, тоді m(Ме″) = (11,9 – у) г.
 Me1 - ? Ме2 - ? N(Ме′) =
Me1 - ? Ме2 - ? N(Ме′) = 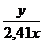 · NА ; N(Ме″) =
· NА ; N(Ме″) =  · NА
· NА
2 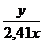 ·NА =
·NА =  ·NА / · 2,41х
·NА / · 2,41х
2у = 2,41(11,9 – у)
2у = 28,679 – 2,41у
у = 6,5 г - m(Ме′) в суміші, тоді m(Ме″) = 11,9 – 6,5 = 5,4г
Згідно І і ІІ рівнянням
z1 =  =
=  ; z2 =
; z2 =  =
= 
z1 + z2 = 8,96
 +
+  = 8,96 ; х = 27; Ar(Al) = 27 – Me″
= 8,96 ; х = 27; Ar(Al) = 27 – Me″
Ar(Me′) = 2,41x = 2,41 · 27 = 65; Ar(Zn) = 65 - Me′
Відповідь: Zn і Al
5. а) -2 +4 0 б) +5 -2 +4 0
2H2S + SO2 = 2S + 2H2O 4HNO3 → 4NO2 + O2 + 2H2O



 S-2 -2℮ → S0 2 – відновник N+5 + 1℮ → N+4 4 - окисник
S-2 -2℮ → S0 2 – відновник N+5 + 1℮ → N+4 4 - окисник
4 4
|
|
|
S+4 + 4℮ → S0 1 – окисник 2O-2 - 4℮ → O20 1 - відновник
в) -3 0 +5 -2 -2
2РН3 + 4О2 = Р2О5 + 3Н2О

 2Р-3 - 16℮ → 2Р+5 1 - відновник
2Р-3 - 16℮ → 2Р+5 1 - відновник
16
О20 + 4℮ → 2О-2 4 - окисник
 МІСЬКА ОЛІМПІАДА З ХІМІЇ. 2004 рік
МІСЬКА ОЛІМПІАДА З ХІМІЇ. 2004 рік
 6. Дано: Розв'язок:
6. Дано: Розв'язок:
N(Х2)= 2,35 · 1023 молекул υ(Х2) = N : NА ; υ(Х2) = 2,35 · 1023 : 6,02 · 10231/моль = 0,39 (моль)
Їх m(Х2) = 12,5г тоді М(Х2) =  ; М(Х2) = 12,5 г : 0,39 моль = 32 г/моль
; М(Х2) = 12,5 г : 0,39 моль = 32 г/моль
 М(О2) = 32 г/моль; зв’язок ковалентний неполярний.
М(О2) = 32 г/моль; зв’язок ковалентний неполярний.
Формула газу? Ізотопи: 16О 17О 18О
Тип зв’язку? Ізотопи? +8 +8 +8
Й клас
 1. Дано Розв’язок
1. Дано Розв’язок
m (МеНСО3) = 15 г 15г 3,36л
НCl МеНСО3+ НCl → МеCl + Н2О + СО2
V(газу) = 3,36 л. 1 моль 1моль
 х 22,4 л.
х 22,4 л.
Ме - ? х =  = 100г/моль (МеНСО3)
= 100г/моль (МеНСО3)
Гідроліз солі. Мr(МеНСО3) = Ar(Me) + Ar(H) + Ar(C) + 3Ar(O)
100 = х + 1 + 12 + 3· 16; х = 39
Ar(К) = 39; КНСО3.
КНСО3 + НCl = КCl + Н2О + СО2
Гідроліз: КНСО3 ↔ К+ + НСО3-
Н2О: НСО3- + НОН → Н2О + СО2 + ОН-
КНСО3 + НОН → КОН + Н2О + СО2
К+ + НСО3- + НОН → К+ + ОН- + Н2О + СО2
 2. Дано Розв’язок
2. Дано Розв’язок
V1(р-ну СаCl2) = 200мл 1. Знаходимо w(СаCl2) в СаCl2 · 6Н2О.
ρ(СаCl2) = 1,01г/мл М(СаCl2 · 6Н2О) = 40 + 71 + 6·18 = 219г/моль
w1(СаCl2) = 5% w(СаCl2) =  · 100% = 51% (в кристалогідраті)
· 100% = 51% (в кристалогідраті)
w2(СаCl2) = 0,2. 2.За правилом діагоналей:


 51% 15 в.ч. - кристалогідрата
51% 15 в.ч. - кристалогідрата
m(СаCl2 · 6Н2О) - ? 20%


 5% 31 в.ч. – розчину 5%
5% 31 в.ч. – розчину 5%
m1(р-ну) = 200мл · 1,01 г/мл = 202 г.
15 в.ч. (СаCl2 · 6Н2О) ― х г.
31 в.ч. (5% СаCl2) ― 202 г.
х =  = 97,74 г. (СаCl2 · 6Н2О)
= 97,74 г. (СаCl2 · 6Н2О)
Відповідь: 97,74 г. СаCl2 · 6Н2О.
 3. Дано Розв’язок
3. Дано Розв’язок
m (Аl, Mg, SiO2) = 5 г 1. x 1,12л
NaOH 2Al + 2NaOH = 2Na[Al(OH)4] +3H2
V(газу) = 1,12 л. 54г 67,2л
HCl SiO2 + 2NaOH = Na2SiO3 + Н2О
V(газу) = 2,24 л Mg + NaOH = не відбувається
 W(Al)- ? w(SiO2)-? х =
W(Al)- ? w(SiO2)-? х =  = 0,9 г. (Al)
= 0,9 г. (Al)
W(Mg)- ?
МІСЬКА ОЛІМПІАДА З ХІМІЇ. 2004 рік
2. 0,9г. х
2Al + 6HCl = 2AlCl3 + 3Н2
54г 67,2л
 х =
х =  = 1,12 л.(Н2)
= 1,12 л.(Н2)
V(Н2) = 2,24л – 1,12 л = 1,12 л.(Н2) - Mg
3. х 1,12л
Mg + 2HCl = MgCl2 + Н2
24г 22,4л
х =  = 1,2 г (Mg)
= 1,2 г (Mg)
4. SiO2 + HCl = не відбувається
m(SiO2) = 2,5г – 0,9г – 1,2г = 0,4г
Тоді в 5 г. суміші буде : 1,8г – Al; 2,4 г. – Mg; 0,8 г. - SiO2
5. w (SiO2) =  = 0,16 або 16%
= 0,16 або 16%
w (Mg) =  = 0,48 або 48%
= 0,48 або 48%
w (Al) = 100% - 16% - 48% = 36%
Відповідь:SiO2 - 16%; Mg - 48%; Al - 36%.
 4. Дано: Розв’язок
4. Дано: Розв’язок
ІІ 1. Знаходимо формулу нітроген оксиду
m ( Mе ) = 1,28 г N : О =  :
:  = 2,17 : 4,43 = 1 : 2 ; NО2
= 2,17 : 4,43 = 1 : 2 ; NО2
НNO3 (конц.) М(NхОу) = 23 · 2 г/моль = 46 г/моль
V(газу) = 896мл. М(NО2) = 46 г/моль- таким чином при взаємодії Ме з кислотою
W(N) = 30,43% утворюється NО2 .
W(О) = 69,57% 1,28г 0,896л
Dводнем = 23 Ме + 4НNO3 (конц.) = Ме(NO3)2 + 2NО2 + 2Н2О
 Ме -? хг 44,8л
Ме -? хг 44,8л
х =  = 64г
= 64г
Ar (Cu) = 64.
Відповідь:Мідь.
5. а) -3 +3 0 б) +7 -2 +4 0
NH4NO2 → N2 + 2H2O 4HClO4 → 4ClO2 + 3O2 + 2H2O
Дата добавления: 2018-02-18; просмотров: 985; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
