МІСЬКА ОЛІМПІАДА З ХІМІЇ. 2003 рік. ТЕКСТИ ЗАДАЧ МІСЬКОЇ ОЛІМПІАДИ З ХІМІЇ
ХІМІЯ
ТЕКСТИ ЗАДАЧ МІСЬКОЇ ОЛІМПІАДИ З ХІМІЇ
Й клас
1. До розчину, який містить калій бромід масою 1,60 г, добавили бром-сирець масою 6 г, що має домішку хлору. Суміш випарили і залишок висушили. Маса залишку 1,36 г. Обчисліть масову частку хлору в бромі-сирці. (4 бали)
2. Обчисліть об'єм газу, що виділився при дії надлишку хлоридної кислоти на магній силіцид. Силіцій для реакції добування магній силіциду було отримано в результаті повного відновлення 30 г силіцій (IV) оксиду вуглецем. (4 бали) 3.Над 10 г розжарених залізних ошурок пропустили водяну пару. Ошурки прореагували повністю. Об'єм одного з продуктів реакції - водню - при н. у. склав 5.3 л. Визначте формулу другого продукту реакції. (5 балів)
4.Допишіть рівняння реакцій, підберіть коефіцієнти методом електронного балансу:
а) НNO2 → НNO3 ... + ? + ?
б) Н2S + J2 →
в) Zn + SО2 → (5,5 балів)
|
|
|
5. Порцію фосфор (V) оксиду масою 14,2 г додали до розчину ортофосфатної кислоти масою 135,8 г (масова частка Н3РО4 - 49%). Яка масова частка кислоти в отриманому розчині? (4,5 балів)
6. Для розчинення одновалентного металу масою 5,4 г витратили розчин сульфатної кислоти об'ємом 3,55 мл (р = 1,73 г/мл) з масовою часткою Н2SО4 80 %. Визначте, який метал був розчинений. (6 балів)
Й клас
1. Сполука А – легкокипляча рідина із приємним запахом. При гідролізі А утворюється дві сполуки з однаковим числом атомів Карбону. Густина парів однієї з цих сполукВ лише трохи перевищує густину повітря. Речовина В може бути окиснена СuO у речовину С, що використовується для зберігання біопрепаратів. Наведіть можливі формули А, В і С про які йде мова в задачі.
2. Ступінь дисоціації бензойної і ортонітробензойної кислот у розчині концентрацією 0,1 моль/л дорівнює відповідно 2,5% і 22,9%. Обчисліть концентрацію Гідроген-іонів у кожному з розчинів. Знайдіть відношення констант дисоціації цих кислот.
|
|
|
3. Нікелеву пластинку 18,9 г опустили в 455 г розчину ферум ( ІІІ ) хлориду з масовою часткою солі 0,1. Після деякого витримування пластинки в розчині, її вийняли , при цьому виявилось, що масова частка ферум ( ІІІ ) хлориду дорівнювала масовій частці утвореної солі. Визначте масу пластинки після того, як її вийняли з розчину.
4. До 300 г 19,1 % розчину купрум ( ІІ ) сульфату додали 300 г 28,3 % розчину калій хлориду і отриманий розчин піддали електролізу з інертними електродами. Після електролізу масова частка сульфат - іонів дорівнювала 6 %. Розрахуйте маси продуктів, які виділилися на електродах, та кількість електрики, що пропущено через розчин.
5. Розташуйте в порядку зростання кислотності наступні речовини: сульфідна кислота, 2-пропанол, фенол, йодидна кислота. Наведіть рівняння хімічних реакцій, що підтверджують правильність обраної послідовності.
6. До 48,35 мл 7,3% хлоридної кислоти (  = 1,035 г/мл ) додали 91,75 мл 11,2 % розчину натрій гідроксиду (
= 1,035 г/мл ) додали 91,75 мл 11,2 % розчину натрій гідроксиду (  = 1,09 г/мл). Скільки молекул води міститься у одержаному розчині?
= 1,09 г/мл). Скільки молекул води міститься у одержаному розчині?
МІСЬКА ОЛІМПІАДА З ХІМІЇ. 2003 рік
РОЗВ'ЯЗКИ ЗАДАЧ МІСЬКОЇ ОЛІМПІАДИ З ХІМІЇ
Й клас
1.  Дано: Розв'язок:
Дано: Розв'язок:
|
|
|
V (газу) = 8 л. 1.Знаходимо молярну масу газу.
m (газу) = 5,72 г. М =  ;
; 
 М (газу)- ?
М (газу)- ?  8 л : 22,4 л/моль = 0,357 моль
8 л : 22,4 л/моль = 0,357 моль
m(1 молекули)- ? М(газу)= 5,72 г : 0,357 моль = 16 г/моль
2.Знаходимо масу однієї молекули.
6,02·1023молекул газу ─ 16 г
1 молекула ─ х г
х = 16 г : 6,02 · 1023 = 2,66 · 10-23 г
Відповідь: 16 г/моль; 2,66 · 10-23г.
2.  Дано : Розв'язок :
Дано : Розв'язок :
 С : Н = 3 : 1 1.Складаємо атомний фактор.
С : Н = 3 : 1 1.Складаємо атомний фактор.
СхНу - ? С : Н =  = 0,25 : 1 = 1 : 4
= 0,25 : 1 = 1 : 4
W ( С ) - ? Формула : СН4
 W ( Н ) - ?
W ( Н ) - ?  2. Знаходимо масову частку Карбону.
2. Знаходимо масову частку Карбону.
W=  ; W ( C ) = 12 : 16 = 0,75 або 75 %
; W ( C ) = 12 : 16 = 0,75 або 75 %
3. Знаходимо масову частку Гідрогену.
W=  ; W ( Н ) = 4 · 1 : 16 = 0,25 або 25 %
; W ( Н ) = 4 · 1 : 16 = 0,25 або 25 %
Відповідь : СН4 ; W ( С ) = 75 % ; W ( Н ) = 25 %.
-
 Дано : Розв’язок :
Дано : Розв’язок :
ХУО3 1. Знаходимо молярну масу речовини.
|
|
|
W ( О ) = 47,5 % W=  ; Мr =
; Мr = 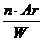 ;
;
Ar ( X ) = Ar (У) – 25 Мr= 3 · 16 : 0,475 = 101
 Формула - ? М (ХУО3) = 101 г/моль
Формула - ? М (ХУО3) = 101 г/моль
Х - ? 2.Нехай Аr ( Х ) = а, тоді Аr ( У ) = а-25.
У - ? Мr(ХУО3) = Аr ( Х ) + Аr ( У ) + 3 · Аr ( О )
101 = а + (а – 25) + 3 · 16
101 = 2а +23
2а = 78
а = 39, Аr (К)=39, це Калій
Аr ( У ) = 39 – 25 = 14, Аr ( N ) = 14, це Нітроген
Формула : КNO3
Відповідь : КNO3
-
 Дано : Розв’язок :
Дано : Розв’язок :
m (Р) = 1 г. 1. Знаходимо масу фосфора, що прореагував.
m (Р)залишок=0,783 г. m(Р)що прореагував=1 – 0,783 = 0,217 г.
2. Записуємо рівняння реакції горіння фосфору.
 V(повітря) - ?
V(повітря) - ?
Дата добавления: 2018-02-18; просмотров: 1494; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
