Внутриклеточные и внеклеточные буферные системы
Поддержание КОС обеспечивается буферными (физико-химическими) и физиологическими системами.
Буферная система крови и любой биологической среды представляет собой сочетание слабой кислоты и соли, образованной этой кислотой и сильным основанием. В этой системе слабая кислота называется буферной кислотой, а ее соль – буферным основанием. При включении буферных систем происходит замена сильной кислоты (или основания) на слабую, количество свободных ионов водорода уменьшается.
Буфером называются группы веществ, которые могут поглощать кислую или щелочную валентность, химически связывать и, тем самым, препятствовать изменениям рН.
рК угольной кислоты при температуре 38 градусов равна 6,1. Концентрация Н2СО3 равна 1,2. Концентрация [НСО3ˉ] составляет 24 ммоль/л.
Подставляя в формулу числа, получаем: рН=7,4. Эта формула лежит в основе определения показателей КОС.
Буферная емкость крови и тканей обеспечивается буферными системами. В организме имеется ряд буферных систем, поддерживающих КОС.
Основные буферные системы, предохраняющие рН жидкостей организма от значительных колебаний – это белковая и бикарбонатная буферные системы. Эти буферные системы можно назвать системами быстрого реагирования, поскольку в случае необходимости они могут немедленно вступить во взаимодействие с избытком кислот или оснований и предотвратить существенные изменения рН в течение периода, необходимого для развертывания действия респираторных и почечных механизмов. Костная ткань также является важным звеном, обеспечивающим буферизацию кислот и оснований. Хотя это трудно измеримо, было установлено, что при острых нарушениях кислотно-основного состояния 40% буферирования происходит в костной ткани. При хронических нарушениях кислотно-основного баланса роль костных буферов возрастает. Следствием костной буферизации является высвобождение кальция и повышенная экскреция его с мочой. Кроме того, постоянное задействование костных буферов в регуляции нарушений кислотно-основного состояния является причиной деминерализации костей и предрасполагающим фактором образования камней в почках.
|
|
|

Рис.3. Роль внутриклеточных и внутриклеточных буферных систем, легочного и почечного механизмов в поддержании нормального уровня рН крови (по Rhoades R. A., Tanner G.A., 1996).

Бикарбонатная буферная система
Бикарбонатная буферная система состоит из слабой кислоты и соли сильного основания, соотношение Н2СО3 /NаНСО3 составляет 1/20.
Емкость бикарбонатной буферной системы составляет 53% всей буферной емкости крови. При этом на бикарбонат плазмы приходится 35% и на бикарбонат эритроцитов 18% буферной емкости.
|
|
|
Иногда вместе с натрием в состав соли может входить любой одновалентный катион (например, калий). Его можно обозначить символом В, и тогда в общем виде бикарбонатная система будет представлена как: Н2СО3/ ВНСО3.
Соль, входящая в состав буферной системы, обладает свойствами основания, то есть анион |НСО3ˉ|, согласно теории Бронстеда, может быть акцептором водорода.
Угольная кислота – нестойкое соединение, которое разлагается с образованием воды и углекислого газа. Последний через дыхательную систему удаляется в атмосферу. Учитывая эту особенность, бикарбонатную буферную систему называют летучим буфером, а его действие в организме описывается уравнением:

Поскольку в крови константа диссоциации (К) и коэффициент растворимости углекислого газа (s) в физиологических условиях величины постоянные, то влияние бикарбонатного буфера на рН крови можно описать простой зависимостью:

Из этого следует, что основными параметрами, определяющими вклад бикарбонатной буферной системы в регуляцию КОС служат парциальное давление углекислого газа крови и концентрация бикарбоната крови.
|
|
|
Определение компонентов бикарбонатного буфера крови используется для оценки КОС.
Фосфатная буферная система.
Фосфатная буферная система обеспечивает 5% буферной емкости крови, и представлена одноосновным (NаН2РО4) и двуосновным (Nа2НРО4) фосфатом в соотношении 1:4. Этот буфер имеет ведущее значение в почечной и тканевой регуляции КОС.
В крови его роль сводится к поддержанию постоянства и воспроизводства бикарбонатного буфера (регенерации бикарбоната почками):

Этот процесс происходит в клетках почечного эпителия при непосредственном участии ферментов – карбоангидразы и глутаминазы. Карбоангидраза трансформирует продукты аэробного окисления (Н2О и СО2) в Н2СО3, а глутаминаза поставляет NН3 в ходе дезаминирования аминокислот. В результате значительная часть канальцевого натрия ассоциируется с ионом бикарбоната и в виде NаНСО3 возвращается в сосудистое русло. При этом в просвете канальца увеличивается содержание NаН2РО4. Ион хлора, ассоциируясь с NН3, выводится в виде NН4Cl. Анионы сильных кислот выводятся с ионом аммония, который образуется в почках из NН3 и Н+. Этот процесс направлен на удаление избытка протонов.
Белковая буферная система.
|
|
|
Белковая буферная система обеспечивает 7% буферной емкости крови. Система функционирует в зависимости от рН среды, поскольку белки являются амфотерными электролитами.
В щелочной среде:

В кислой среде:
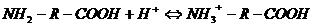
Белки содержат много ионизируемых групп, которые могут высвобождать или связывать Н+. Большое количество протеиновых буферов локализовано в клетках, ионы Н+ и СО2 диффундируют через клеточные мембраны для буферирования внутриклеточными белками. Альбумин и глобулины плазмы являются основными протеиновыми буферами в сосудистом секторе.
Буферные свойства белков плазмы (альбумина и др.) и гемоглобина эритроцитов связаны с тем, что входящие в их состав аминокислоты содержат как кислые (–СООН), так и основные (–NН2) группы и могут диссоциировать с образованием как водородных, так и гидроксильных ионов в зависимости от реакции среды. Большая часть буферной емкости белковой системы приходится на долю гемоглобина.
Дата добавления: 2018-02-15; просмотров: 3064; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
