Понятие, классификация и виды травм.
Травма (trauma) или повреждение - комплекс морфо-функциональных и физико-химических нарушений, возникающих в тканях и органах в результате воздействия на эти ткани и органы различных травмирующих факторов. При этом:- нарушается целостность структуры на клеточном, тканевом и органном уровнях; - нарушается энергообмен; -нарушается обмен веществ. При действии сильных кратковременно травмирующих (повреждающих) факторов возникает острая травма, а при слабых, но длительных или многократных воздействий - хроническая травма.
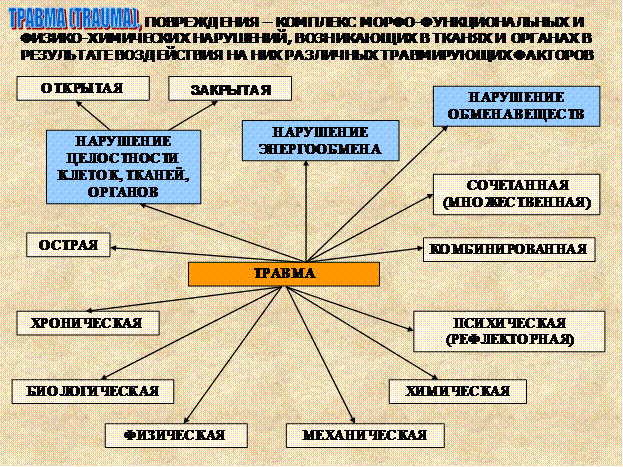
Рис.2. Содержание травмы.
Под влиянием травмирующих факторов нарушается целостность и функция тканевых структур, кровеносных, лимфатических сосудов и нервных образований. Организм на это отвечает соответствующей общей и местной защитно-приспособительной реакцией. В зависимости от характера поражения различают пять основных травмирующих факторов: механические, физические, химические, биологические и психические или стрессовые. Под воздействием этих факторов на организм возникают: механические, физические, химические, биологические и психические травмы или повреждения. Далее выделяют комбинированные травмы-повреждения, обусловленные одновременным или последовательным воздействием разных травмирующих факторов (электрический ток и механическая сила), а также сочетанные травмы, возникающие при воздействии данного травмирующего фактора на различные области организма (механическая сила- перелом и разрыв внутренних органов). В таких случаях в организме возникают более тяжелые повреждения, нередко заканчивающиеся смертью пострадавшего.
|
|
|
Исходы травм, вызванных воздействием факторов одинаковой силы и продолжительности, зависят от анатомических и физиологических особенностей повреждаемых тканей и органов, наличия в них предшествующих патологических изменений, а также от функционального состояния нервной системы в момент нанесения травм и видовой реактивности травмированных животных.
Механическая травма является следствием воздействия механической силы на животный организм, в результате которой возникают различной степени повреждения тканей и органов. Способствуют механическим повреждениям: алиментарная витаминно-минеральная недостаточность, нарушение обмена веществ, недостаточный моцион и изнуряющие движения. Следует также иметь в виду, что у молодняка и старых животных кожа, мягкие ткани, сухожильно-связочный аппарат и кости менее устойчивы к механическим и другим травмам. Сопротивляемость к ним одних и тех же тканей и органов неодинакова у разных видов животных. Так, сухожильно-связочный аппарат у лошадей и собак обладает большей эластичностью и прочностью на разрыв, а кожа у них более эластична и подвижна, чем у крупного рогатого скота и, особенно, свиней. Кости у лошадей и собак прочнее и менее хрупкие в сравнении с костями коров, овец и свиней.
|
|
|
Механическая сила, повреждающая ткани организма, может действовать в виде сжатия, растяжения, скручивания, сгибания, размозжения, удара. Степень повреждения тканей организма при этом зависит от направления и угла силы действия, скорости движения, величины и плотности травмирующего предмета, а также в зависимости от анатомического строения и функционального состояния травмируемых тканей и органов. Так, напряжение мышц и некоторые положения суставов усугубляют травму и способствуют возникновению переломов, вывихов и разрывов. Переполненный желудок, кишечник и мочевой пузырь при пулевом ранении разрываются вследствие возникающих гидродинамических сил, обусловливающих боковые удары (см. ниже), но повреждение будет минимальным, если они пустые в момент ранения. В ряде случаев при беременности наблюдаются множественные переломы костей вследствие развившейся остеомаляции и разрывы мышц в результате истончения и перерастяжения их.
|
|
|
Механические травмы подразделяются на: операционные, случайные, родовые и военного времени. Они могут быть закрытыми и открытыми. Те и другие бывают прямыми и непрямыми, множественными и одиночными.
Прямые механические повреждения возникают на месте приложения травмирующей механической силы. Непрямые повреждения появляются на некотором расстоянии от места приложения травмирующего воздействии.
Паренхиматозные органы, а также все отделы мозга легко повреждаются при воздействии на них механических травм относительно небольшой силы и нередко заканчиваются смертью животного, Наибольшей стойкостью к механической и другим травмам обладают кости.
Закрытые механические повреждения характеризуются сохранением анатомической целости кожи и слизистых оболочек. К ним относятся ушибы пли контузии, растяжения, разрывы мягких тканей и паренхиматозных органов, вывихи суставов, нарушения целости костей и др. Вследствие особенностей анатомо-гистологического строения кожи она обладает большой эластичностью и прочностью. Поэтому ее анатомическая непрерывность может сохраняться даже при тяжелых травмах, когда ткани и органы, лежащие под нею, оказываются в состоянии растяжения, разрыва, раздавливания, размозжения, перелома и даже раздробления.
|
|
|
Открытые механические повреждения, или раны, характеризуются разъединением кожи, слизистых оболочек и лежащих под ними мягких тканей, внутренних органов и даже костей. Они больше, чем закрытые повреждения, подвержены повторному травмирующему воздействию внешней среды, а также загрязнениям, обсеменению различными микроорганизмами. К открытым, повреждениям относятся различного вида и характера раны, открытые переломы и вывихи.
Физические травмы вызываются термическими, электрическими и лучевыми травмирующими факторами.
-Термическая травма встречается реже механической. Она связана с воздействием на кожу животных высоких (ожоги) или низких (отморожение) температур.
-Электрическая травма сопряжена с прохождением через организм технического электротока или молнии.
-Лучевая травма обусловлена более или менее длительным воздействием на организм лучистой энергии и ионизирующей радиации (альфа и бета частицы, гамма- излучение). Эта травма в отличие от предыдущих в большинстве случаев не вызывает у животных моментальной защитной реакции и не распознается непосредственно после ее нанесения, за исключением воздействия на организм мощных доз.
Химическая травма. Является следствием воздействия на ткани чаще всего кислот, щелочей, солей тяжелых металлов, боевых отравляющих веществ (БОВ), сильнодействующих ядовитых веществ (СДЯВ), а также некоторых химических средств (серный ангидрид, применяемый для обработки животных, пораженных макропаразитами и кровососущими насекомыми). Одни из химических веществ вызывают преимущественно местные повреждеиия; другие, такие, как фосфор и БОВ, всасываясь через кожу и слизистые оболочки, действуют токсически на весь организм.
Биологическая травма. Повреждающими факторами при этой травме являются вирусы, микробы, грибки, макропаразиты, токсины и другие продукты их жизнедеятельности, а также яды и аллергены животного и растительного происхождения.
Укусы ядовитыми змеями. В нашей стране обитает 11 видов ядовитых змей. Их околоушные железы продуцируют яд. Выводные каналы желез проходят через два самых крупных зуба и открываются наружу через специальные отверстия. При вонзании зубов в тело животного происходит сдавливание желез, из которых выпрыскивается в рану яд.
Смерть от укуса змеи наступает от паралича дыхательного центра. Змеиный яд, помимо местного действия (обширные отеки, болезненность, покраснение), по мере всасывания вызывает нарушение постоянства крови, паралич вазомоторов, повышение проницаемости гематоэнцефалического и других гистогематических барьеров и гемастатических механизмов. Кроме того, змеиный яд действует на клетки и ткани цитолитически, чем и обусловливает развитие местной реакции. В большинстве случаев змеи наносят укусы животным в области конечностей, вымени, мошонки и лицевой части головы. Лошади гибнут через 12 ч или через несколько суток, овцы и ягнята — в течение нескольких минут. Крупный рогатый скот и свиньи наиболее устойчивы к змеиному яду.
Лечение. При укусе конечности ее следует немедленно туго перетянуть вблизи и выше укуса, затем иссечь либо прижечь зону укуса раскаленным железом; вокруг места укуса инъецируют: 0,25—1%-ный свежеприготовленный раствор калия перманганата или 2%-ный раствор хлорной извести. Наиболее эффективна противозмеиная сыворотка: мелким животным при тяжелом отравлении инъецируют под кожу 60—90 мл, при среднем — 40—70 мл, при легком—15—30 мл; крупным животным—соответственно 500—800 мл, 300—400 и 150—200 мл.
Профилактика. Укусы змей чаще наблюдаются ранней весной и в начале лета; в эти времена года не следует использовать пастбища, где водятся змеи. Для уничтожения их пастбища выжигают либо перепахивают с последующим боронованием и укатыванием почвы, кроме того, проводят лугомелиоративные работы.
Укусы ядовитыми пауками. В СНГ обитают два вида ядовитых пауков: кара-курт («черная смерть») и фаланга, которая редко нападает на животных. Особенно опасен первый вид. Он встречается на Украине, в Молдавии, в зоне Нижней Волги, на Кавказе и в Средней Азии. Яд каракурта вырабатывается в железах челюстей (хелицерах), он довольно стойкий, относится к токсальбуминам. Особенно чувствительны к яду каракурта верблюды и лошади, меньше — другие животные; совсем нечувствительны овцы. Общие признаки отравления после укуса чаще проявляются через 6—7 ч. Смерть наступает при сильном слезотечении, судорогах и удушье.
Лечение такое же, как и при укусах змей. В вену медленно вводят 1%-ный раствор калия перманганата (лошади—200—300 мл) и подкожно—5%-ный раствор эфедрина (лошадям и крупному рогатому скоту по 0,05—0,4 мл).
Профилактика: выжигают пастбища, либо уничтожают каракуртов путем выпаса свиней и овец, которые поедают их, или обрабатывают территорию ядохимикатами.
Психическая травма возникает под влиянием стрессовых факторов, воздействующих как поток раздражителей преимущественно через зрительный и слуховой анализаторы на нервные центры и через них на эндокринную систему. В результате этого в организме животных возникает адаптационная напряженность, приводящая к нарушению механизмов генетической адаптации, декомпенсации, развитию патологических реакций, дистрофических изменений в клеточных и тканевых структурах, что обусловливает развитие заболеваний. Психическая травма, протекающая без морфологического полома, чаще наблюдается у животных с повышенной возбудимостью и преобладанием возбудительных процессов над тормозными в условиях шумовых и других факторов, обусловленных механизацией, высокой концентрацией животных на ограниченных площадях при условии гипо- и адинамии, экранировании от естественно-природных факторов. Установлено, что у животных, содержащихся в таких условиях, перегруппировка, погрузка и транспортировка, а также проведение массовых профилактических, противоэпизоотических и других обработок усиливают стрессовое напряжение и приводят к резкому снижению адаптационных возможностей, шоковому состоянию и даже гибели наиболее ослабленных животных, особенно телят и свиней.
2.2 Влияние травм на организм.
При оценке вида и степени повреждения необходимо учитывать:
1.-характер травмирующего фактора и механизм его действия (характер повреждающего действия зависит от физических качеств травмирующего фактора:- обьем и вес травмирующей силы; -форма травм. предмета; -консистенция травм. предмета; -физическое состояние травм. Предмета (пар, жидкость,лед); -загрязнения микроорганизмами и от механизма повреждения: продолжительность действия (особое значение при физических и хим.травмах); -вида действия (сжатие или растяжение, пример ударная волна с изб.давлением и зоной ваукума);
2.-анатомо-физиологические особенности тканей и органов (анатомическое строение и физиологическое состояние тканей –кость или мышца, напряжена или расслаблена);
3.-условия и обстоятельства при, которых происходит травмирование (заполненный желудок или мочевой пузырь или пустые, состояние покоя или движения).
Непосредственно после нанесения тяжелых механических, термических, электрических и некоторых химических травм, а иногда в момент их нанесения, возникает опасность развития коллапса, шока, парезов, параличей, выхода из строя отдельных тканей, органов, частей тела; возможна внезапная смерть. Механические травмы, особенно открытые (раны), сопровождаются кровотечением, нередко угрожающим жизни животного. Повреждения покровов способствуют проникновению инфекта в ткани внутренней среды организма, что создает опасность развития местной или общей инфекции, исходы которой могут оказаться неблагоприятными. При обширных, особенно закрытых, повреждениях нередко развивается травматический токсикоз, обусловленный всасыванием продуктов ферментативного распада мертвых тканей.
Повреждающее действие механической травмы. Наиболее часто у животных наблюдаются механические травмы, поэтому ветеринарный врач должен особенно хорошо знать не только этиологию, но и механизм действия на ткани таких травмирующих факторов. В зависимости от силы сжатия в тканях появляются различной степени повреждения, начиная от нарушения крово- и лимфообращения, раздавливания мышц, разрыва фасций, связок и внутренних органов до раздробления костей. Чем интенсивнее и продолжительнее сжатие, тем тяжелее последствие этого вида травмы. При скручивании той или иной части тела вначале возникает растяжение, затем разрыв связок, мышц, фасций, при продолжающемся скручивании происходит вывихивание костей в суставах с разрывом лимфатических, кровеносных сосудов и нервов. Обладая исключительными эластическими возможностями, кожа при этом истончается в зоне скручивания, но может сохранить свою непрерывность. При такого рода повреждениях кровотечения почти никогда не наблюдаются, даже при разрыве кровеносных сосудов значительного диаметра. Это обусловлено тем, что при перекручивании сосуда первой разрывается интима и завертывается внутрь просвета, затем, штопорообразно скручиваясь, медиа и адвентиция вытягиваются в конус и разрываются. Все это обеспечивает очень прочное закрытие просвета сосуда.
Наиболее детально изучен механизм огнестрельной травмы, характеризующейся огромной ударной кинетической энергией, способной пронизать тело животного в тысячные доли секунды (0,0001—0,001 с) и одновременно вызвать тяжелые разрушения на всем пути продвижения в организме. Другие травмы, возникшие в результате ударного воздействия в несколько раз меньшей кинетической энергии, по своему механизму действия на ткани организма более или менее приближаются к ударному механизму огнестрельной травмы.
Сущность механизма ударной травмы может быть представлена следующим образом. При воздействии ударной волны или предмета на поверхность тела мгновенно возникает давление большой силы. Это сопровождается моментальным вдавливанием (камень, палка и др.) или проникновением травмирующего предмета (пуля, осколок) в ткани при одновременной передаче им кинетической энергии. Возникшее таким образом значительной силы давление передается в виде ударной волны частицам тканей с поверхности вглубь (сила прямого удара) и в стороны (сила бокового удара), вызывая волнообразное колебание, которое распространяется с большой силой и скоростью по оси травмирующего предмета и с меньшей — в стороны. Воздействуя на ткани, предмет, непрерывно теряя кинетическую энергию, продолжает сообщать частицам тканей волнообразное движение. Последнее оказывается тем сильнее, чем больше теряется энергии ранящим предметом в единицу времени. Пришедшие в колебательное движение частицы тканей образуют конус, основание которого обращено в противоположную сторону от действия травмирующего предмета. В пределах этого конуса ткани смещаются и частично размозжаются.
При огнестрельном ранении скорость распространения ударной волны в тканях примерно равна скорости распространения звука (1440 м в секунду). Вследствие этого ударная волна, опережая скорость движения пули или осколка снаряда, распространяется впереди них. Проникая в толщу тканей, ранящий предмет, например пуля, встречает сопротивление частиц тканей, расталкивает их в стороны от оси своего полета. В результате этого позади нее образуется временная коническая пульсирующая полость. Частицы тканей, составляющие стенки раневого канала, ритмично колеблются, чем и обусловливается то увеличение, то уменьшение полости данного канала. Ткани, составляющие пульсирующую полость, повреждаются различно, в зависимости от их плотности и эластичности.
Принято считать, что сопротивление тканей животных (кроме костей и хрящей) приближается к сопротивлению воды, так как она количественно составляет главную часть клеток тканей. Именно поэтому ударное воздействие на них до известной степени подчиняется закону гидродинамики Паскаля, согласно которому давление на жидкость, заключенную в герметически замкнутом сосуде, передается во все стороны с одинаковой силой. Но так как ткани обладают несколько большим сопротивлением, то давление, оказываемое на них при травме, хотя и передается во все стороны, однако его сила (кинетическая энергия) уменьшается по мере удаления от места ее приложения. Экспериментально было установлено, что в тканях энергия ранящего предмета обратно пропорциональна квадрату плотности тканей, а скорость движения частиц тканей прямо пропорциональна их плотности. Иначе говоря, при ударной травме более плотные ткани приобретают большую скорость движения и, «настигая» менее плотные, внедряются в них. Степень сопротивления тканей к ударной травме определяется рядом их свойств, причем первое место по сопротивляемости занимает плотность, затем вязкость, эластичность, насыщенность водой, анатомическая и гистологическая структура. Перечисленные свойства обеспечивают тканям амортизационные качества. Максимальное сопротивление ударной кинетической энергии оказывают плотные, практически несжимаемые ткани, полостные органы с плотной оболочкой и полужидким содержимым (головной мозг, защищенный черепными костями).
По мере снижения плотности и повышения эластичности тканей сопротивление их уменьшается, минимальным оно оказывается в рыхлой соединительной клетчатке и легких. Сопротивление воздуха примерно в 800 раз меньше, чем жидкости, поэтому, находясь в альвеолах, он значительно снижает сопротивление легких к травме.
В настоящее время известно, что энергия разрушения при огнестрельном ранении зависит от: 1) массы ранящего предмета; 2) скорости его полета при ударе и 3) быстроты амортизации живой силы, т.е. от физического состояния тканей.
Чем больше масса и скорость ранящего предмета, тем значительнее его живая сила и тем сильнее удар и разрушение тканей.
При этом следует иметь в виду, что наибольшее значение для интенсивности огнестрельного ранения имеет не масса, а скорость полета снаряда (пули, осколка) при ударном воздействии на ткани. Для обычной (не огнестрельной) ударной кинетической энергии, для которой характерна сравнительно небольшая скорость ранящего предмета, наибольшее значение имеет масса последнего. Наряду с этим тяжесть разрушения при ранении зависит и от степени амортизации, т.е. истощения за единицу времени кинетической энергии снаряда или другого ранящего предмета, проникающего в ткани. Доказано, что быстрота истощения энергии ранящего предмета обратно пропорциональна интенсивности разрушения. Так, если начальная скорость снаряда при вхождении в ткани равна 1000 м/с, а при вылете из раневого канала она снизится до 500 м/с, то разрушение будет меньше, чем при ранении таким же снарядом с начальной скоростью, равной 800 м/с, но полностью теряющий свою скорость при прохождении через ткани, что может привести даже к взрывному эффекту. Необходимо иметь в виду, что полная амортизация живой силы снаряда и другого предмета (камень и пр.), действующего как ударная травма, приводит к слепому ранению. При этом у слепого конца раневого канала будет максимальное разрушение.
Морфологические изменения, возникающие в организме под влиянием ударной травмы, обусловлены действием прямого и бокового ударов. При огнестрельной травме, кроме того, повреждающее действие на ткани связано с противоударом или отраженным ударом. Сущность механизма противоудара сводится к действию отраженной о плотные ткани ударной волны, а также более или менее многократным ударам органа о его плотную оболочку или плотный соседний орган. Экспериментально установлено, что чем больше пробивная способность у пули, тем слабее рассеивание кинетической энергии, и наоборот. Поэтому кинетическая энергия прямого и бокового ударов находится в обратном отношении друг к другу. Сила бокового удара увеличивается, когда возрастает плотность и вязкость пронизываемых тканей. В этих условиях травмирующий предмет теряет кинетическую энергию, целиком передает ее тканям, которые приходят в ритмично-колебательное движение (молекулярное сотрясение по Борсту), возникшее вследствие боковой и отраженной ударных волн.
Боковой удар наиболее выражен в жидких несжимаемых тканях, меньше—в малоэластических и самый минимальный—в эластических. В тканях организма он проявляется в виде взрывного эффекта или коммоции. Взрывной эффект наблюдается только при огнестрельном ранении и является следствием максимального проявления бокового и отраженного ударов, когда вся пробивная способность травмирующего предмета сводится к нулю, т.е. вся его живая сила превращается в энергию ударной волны. Эта энергия исчисляется многими сотнями килограммометров, мгновенно действующих на ткани. Частицы тканей в зоне ударной волны получают огромное ускорение, а так как амортизация силового воздействия на несжимаемые ткани, богатые водой, оказывается невозможной, то возникает разрушение органа. Наиболее часто взрывной эффект наблюдается в полостных органах, до предела наполненных жидким содержимым. В мышцах взрывной эффект возникает при резком их напряжении. Часто его можно наблюдать при огнестрельных ранениях коротких костей, разрывающихся на мелкие кусочки.
Под коммоцией понимают смещение тканей при образовании временной пульсирующей раневой полости и действии энергии ударной волны за пределами этой полости. Коммоция бывает выражена сильнее в головном, спинном и костном мозге, слабее — в мышцах, паренхиматозных органах и минимально — в органах, которые легко амортизируют силу ударной волны (кожа, легкие). Коммоционные повреждения распространяются вокруг зоны прямого воздействия ударной травмы. Однако нередко они наблюдаются и в соседних органах.
Прямой удар в зависимости от величины кинетической энергии травмирующего предмета может привести к разъединению, расщеплению, размозжению и раздроблению тканей, находящихся на пути травмирующего предмета. Возникшая при этом рана всегда имеет следы большей или меньшей степени ушиба. Такие эластичные структуры, как кожа и сосуды, при ударной травме растягиваются и впячиваются по направлению действующей силы. Если последняя превышает физическую и физиологическую сопротивляемость их, то они расщепляются и разрываются. Паренхима органов в зоне прямого удара разрушается, а волокнистые структуры (фасции, апоневрозы, соединительнотканные прослойки) разрываются или раздвигаются. В зависимости от состояния тканей и органов их повреждение может быть различным. Так, малоэластичные напряженные тканевые структуры, например растянутые коллагеновые волокна, нервы, сокращенные мышцы и клетки паренхимы, разрываются и размозжаются. В отличие от этого напряженные эластические структуры (сосуды, эластические волокна) выдерживают значительное растяжение и обычно не разрываются.
То же самое можно сказать и об относительно ненапряженных волокнистых образованиях, таких, как покоящаяся мышца и расслабленные коллагеновые волокна. Под влиянием ударной волны возникают значительной степени расслоения межфасциальных пространств и прослоек рыхлой клетчатки.
Механическое воздействие острыми предметами характеризуется разъединением кожи, слизистых и лежащих под ними мягких тканей и органов. При этом зона непосредственного повреждения обычно меньше, чем при воздействии тупыми предметами, а зона молекулярного сотрясения, как правило, отсутствует.
Хирургия боли.
История борьбы человека с болью уходит своими корнями в глубь веков, к эпоху героических сказаний прошлого, к древним мифам и полузабытым преданиям. По пути ошибок, неудач, случайных наблюдений, мистических и религиозных предрассудков и величайших открытий шло сражение человека с болью. И лишь в XIX веке, когда учение о хирургическом обезболивании с триумфом распространилось по всему земному шару, сметая противодействие, фанатизм, невежество, косность, традиции и привычки, наметились контуры полной победы над болью и медицина подошла к решению самой трудной задачи проблемы обезболивания – к регулированию болевого восприятия.
С незапамятных времен люди смотрят на боль как на сурового и неизбежного спутника. Не всегда человек понимает, что она верный страж, бдительный часовой организма, постоянный союзник и деятельный помощник врача. Именно боль учит и человека, и животное осторожности, заставляет беречь свое тело, предупреждая о грозящей опасности и сигнализируя о болезни. Во многих случаях боль позволяет оценить степень и характер нарушения целости организма.
«Боль – это сторожевой пес здоровья», – говорили в Древней Греции. И в самом деле, несмотря на то что боль почти всегда мучительна и угнетает, снижает работоспособность, лишает сна, она необходима и до известных пределов полезна. Чувство боли предохраняет живой организм от обморожения и ожогов, предупреждает о грозящей опасности. При сильном морозе, когда коченеет тело, боль нередко спасает от гибели. Боль не позволяет животному положить конечность в огонь или схватить раскаленный кусок железа. Боль защищает от обжигающих лучей солнца и ледяного дыхания ветра. Животное, лишенное чувства боли, превратилось бы в игрушку стихий, в жалкую жертву каждой случайности. Оно узнавало бы о ранах и язвах на своем теле, только увидев или нащупав их. Кровотечение, ожог, злокачественная опухоль не привлекали бы его внимания. Зачастую животное может погибнуть еще до того, как оно разглядит смертельную рану.
Советский физиолог П. К. Анохин утверждает, что боль – это своеобразное психическое состояние, определяющееся совокупностью физиологических процессов в центральной нервной системе, вызванных каким-либо сверхсильным или разрушительным раздражением. «Боль, – говорит французский невролог Бодуэн, – это не что иное, как деятельность нервных центров, возбужденных возникшим на периферии раздражением».
Венгерский ученый Хораньи расценивает боль, как сигнал об угрожающем воздействии на организм. Боль сосредоточивает и организует силы организма, направленные на устранение вредного воздействия и восстановление нормальной деятельности органов и физиологических систем.
Боль играет положительную роль в жизни живых существ до тех пор, пока она предохраняет организм от грозящей опасности. Она приносит пользу, подобно огню, когда он согревает, а не сжигает, подобно воде, когда она орошает, а не затопляет.
До тех пор, пока боль предупреждает о грозящей опасности, о болезни, о нарушении целостности организма, она нужна и полезна. Как только информация учтена и боль превращается в страдание, ее необходимо выключить. Однако боль далеко не всегда прекращается после того, как ее защитная функция выполнена. Животное не в состоянии по собственному желанию прекратить боль в тот час, когда она становится не только излишней, но из друга превращается во врага.
Если боль длится долго, если болевые раздражения продолжают бомбардировать нервную систему, если животное не в состоянии преодолеть боль, она постепенно покоряет его сознание.
«Боль, – писал в одной из своих книг видный советский патолог И.В. Давыдовский, – формально патологическое явление, снижающее трудоспособность, часто симптом серьезной болезни. Но боль – это болевой импульс, служащий спасению организма», Давыдовского дополняет американский ученый Норберт Винер, основоположник современной кибернетики: «Нет более ужасной судьбы индивидуума, страдающего от отсутствия ощущения боли».
Вопреки широко распространенному мнению обезболивание – это вовсе не уничтожение одной из важнейших анатомических и физиологических систем в организме. От чувства боли нельзя безнаказанно освободиться, так же как нельзя без ущерба для здоровья лишиться зрения, слуха, обоняния, осязания, вкуса. Нормальная жизнедеятельность человека и животных требует сохранности всех чувств. Какова же в таком случае конечная цель обезболивания, т. е. искусственного устранения боли, если она из сигнала опасности превратилась в жестокого, изнуряющего врага, способного довести человека не только до болезни, но и до смерти? Цель эта научиться регулировать болевые ощущения, получить возможность управлять ими, смягчать или снимать боли, если их сигнальное значение потеряло свой биологический смысл. Цель эта стоит перед хирургом не только в ту минуту, когда он рассекает живые ткани или, закончив операцию, отправляет животное в стационар, а потом обследует его, перевязывает, снимает швы. Она стоит перед ним, когда больное животное корчится от почечной или печеночной колики, страдает или стонет от мышечных судорог, язвенных или раковых болей, приступов стенокардии.
Обезболивание часто смешивают с анестезией, т. е. общей потерей чувствительности. При определенных воздействиях на организм можно потерять чувствительность к прикосновению, теплу, холоду, но сохранить ее по отношению к боли. Правильнее говорить об аналгезии, то есть о потере болевой чувствительности. К решению этой задачи ведут многие пути. Современная фармакология дает возможность выключить нервные окончания и сделать их нечувствительными к сверхсильным раздражениям. Можно заблокировать нервные стволы, по которым передается информация в центральную нервную систему. Известны методы, позволяющие прервать поток импульсов в спинном и продолговатом мозгу. Удается задержать формирование болевого ощущения в ретикулярной формации, лимбической системе, зрительных буграх. Наконец, существует много способов погасить сознание и тем самым приостановить превращение болевого раздражения в чувство боли.
Болеутоляющие средства
В борьбе с болью важную роль сыграло развитие новой области медицинских знаний – психофармакологии. Неоценимую помощь оказало науке обезболивания применение химических соединений, которые влияют определенным образом на высшую нервную деятельность животного, блокируют передачу импульсов в центральных и периферических нейронах, успокаивают, снимают состояние тревоги, повышенной возбудимости и т. д. К числу этих веществ относятся сложные препараты с различными свойствами и особенностями. Одни из них успокаивают (транквилизаторы), другие регулируют деятельность нервных структур (невролептики), третьи снимают депрессию или возбуждение (психотропные вещества) и т. д.
Число новых препаратов, облегчающих или снимающих боль, растет из года в год. Новым является стремление исследователей воздействовать на биохимические процессы, протекающие в различных отделах центральной и периферической нервных систем. В первую очередь объектом воздействия служат адренергические, холинергические и серотонинергические структуры головного мозга.
Чаще всего применяются четыре вида противоболевых веществ:
1) морфин и морфиноподобные вещества, к которым относятся петидин (лидол), декстроморамид, промедол, изопромедол;
2) противоболевые средства группы салициловой кислоты, прозалона и анилина (антипирин, пирамидон, анальгин, бутадион, аспирин, фенацетин и др.);
3) различные невролептические и психотропные препараты, способные регулировать процессы возбуждения и торможения в центральных и периферических отделах нервной системы, а также в вегетативно-эндокринном аппарате. Эти искусственно синтезированные химические соединения оказывают во многих случаях отчетливое противоболевое действие, снимая эмоциональное напряжение, страх, раздражительность, бессонницу. Таких препаратов известно очень много. Наибольшей популярностью пользуется либриум (элениум), дуксен (валиум), мепробомат (андаксин), резерпин, аминазин (хлорпромазин) и особенно имипрамин (тофранил). О действии последнего следует сказать особо.
Имипрамин относится к группе дибензазепинов. Его аналитические свойства проверены в эксперименте и используются в клинической практике, хотя он совершенно неэффективен при острых болях (головных, зубных). Но при тяжелых болях (например, вызванных раковой опухолью) применение имипрамина дает хорошие результаты. Видимо, имипрамин оказывает определенное влияние не на ощущение боли, а на аффективную сторону болевого синдрома;
4) некоторые противосудорожные препараты – бромистый натрий, барбитураты, гидантоины. К этой группе относится и тегретол (карбамазепин). По своему строению он, как и имипрамин, относится к дибензазепинам и применяется при лечении эпилепсии. Однако выяснилось, что тегретол специфически снимает болевой синдром при невралгиях тройничного нерва. Механизм его действия в этих случаях неясен. Однако эффективность несомненна. Можно высказать предположение, что, проникая через гематоэнцефалический барьер непосредственно в ядра тройничного нерва, тегретол прерывает в них синаптические связи. К тегретолу близок иминостильбен, также снимающий тригеминальные боли, хотя и в более слабой степени.
Заменителем морфина может служить лидол (петидин, долантин, димедрол). Он действует слабее, чем морфин, но менее токсичен и не вызывает такого быстрого привыкания. Лидол снимает боли, вызванные спазмом гладкой мускулатуры, например при почечных и печеночных коликах.
В середине 50-х годов советский химик И. Н. Назаров синтезировал новый болеутоляющий препарат – промедол. Благодаря своим противоболевым и противоспазматическим свойствам промедол получил широкое распространение в медицинской практике. С успехом применяются также изопромедол, анадол и другие препараты этого ряда. Применение промедола при висцеральных болях, обезболивании родов, в послеоперационном периоде показало, что советская медицина обогатилась новым эффективным болеутоляющим средством.
Выраженными аналгетическими свойствами обладает также пальфий (аналог зарубежного, даурана или тросилана). Применяется он при болях, вызванных травмами и злокачественными новообразованиями. Однако пальфий в некоторых отношениях подобен морфину и может вызвать болезненное пристрастие со всеми пагубными последствиями. Фенодон, введенный в практику несколько лет назад, действует сильнее, чем морфин и лидол. Однако этот препарат снимает не все виды болей. Так, он мало активен при обезболивании родов, при некоторых хирургических осложнениях. Длительное употребление фенодона может привести к отравлению. С успехом применяется также декстроморамид, мощный противоболевой препарат, значительно более активный, чем морфин. Его аналгетическое действие проявляется через 10 минут после введения в организм и длится примерно столько же, сколько действие морфина или лидола.
При болях, вызванных накоплением в крови и тканях гистамина, облегчение больному животному приносят антигистаминные препараты. Боли сосудистого происхождения, возникающие при накоплении адреналина и норадреналина, снимаются препаратами, блокирующими их действие, например эрготамином, дибенамином, аминазином.
В настоящее время противоболевых препаратов так много и среди них такое обилие патентованных, выпускаемых конкурирующими между собой фирмами, что разобраться в них подчас трудно не только больному, но и специалисту. Здесь необходимы как осторожность, так и умение расшифровать механизмы возникновения болевого синдрома в каждом отдельном случае.
Более тонкий физиологический анализ показывает, что действие различных болеутоляющих средств на отдельные компоненты болевого синдрома неодинаково. Используя методику регистрации отдельных проявлений боли, французские ученые показали, что морфин, петидин (лидол) и декстроморамид слабо влияют на реакцию прыжка и бегства у крыс, но отчетливо подавляют крик и конечную поведенческую реакцию – кусание электродов.
Аспирин действует иначе. Он почти не влияет на реакцию лая и кусания электродов, но подавляет прыжок и бегство. Психотропное вещество имипрамин (тофранил) также ослабляет общую болевую реакцию у крыс; оно подавляет все четыре ее компонента (прыжок, бегство, лай, кусание электродов).
Понятие и виды травматизма.
Травматизм — совокупность травмирующих факторов, вызывающих повреждения у животных, находящихся в одинаковых условиях существования либо содержания и эксплуатации.
Различают следующие виды травматизма животных: 1) сельскохозяйственный; 2) эксплуатационный; 3) спортивный; 4) транспортный; 5) случайный; 6) военный, 7) кормовой травматизм и 8) пушных зверей.
Сельскохозяйственный травматизм возникает при некачественном устройстве животноводческих помещений и их оборудования, при плохой механизации и автоматизации; при нарушении техники безопасности, зоогигиенических условий содержания и эксплуатации животных; некачественном и несбалансированном кормлении, а также при недостатках технологических процессов.
Эксплуатационный травматизм наблюдается при неправильной и чрезмерной эксплуатации животных, например при нарушении правил перевозки тяжестей, машинной дойки, взятия спермы, стрижке овец и пр.
Спортивный травматизм, являясь разновидностью эксплуатационного, наблюдается преимущественно у спортивных лошадей. Чаще всего он возникает при участии их в спортивных состязаниях, а также неправильном тренинге.
Транспортный травматизм возникает у животных при перевозке их железнодорожным, автомобильным, водным и воздушным транспортом.
Характеризуется он относительной массовостью и своеобразием поражения статодинамического аппарата животных (растяжения сухожильно-связочного аппарата, миозиты, миопатозы, артриты, переломы, пододерматиты и др.).
Кормовой травматизм связан с кормопроизводством, приготовлением и качеством кормов, приемом корма, состоянием пастбищных угодий (засоренность металлическими и другими предметами, ядовитыми травами и пр.). Кормовой травматизм чаще возникает при заглатывании крупных, особенно мороженых, корнеплодов, костей, металлических и других предметов, колючек, жестких стеблей растений; поедании перезрелого ковыльного сена и заглатывании химических веществ; поедании ядовитых трав, что приводит к отравлению.
Случайный травматизм нередко связан с метеорологическими и стихийными бедствиями. Его труднее предусмотреть и профилактировать, чем другие виды травматизма.
Военный травматизм — совокупность различных повреждений, причиняемых животным во время военных действий.
2.4.1. Общие принципы профилактики травматизма.По официальным данным, из общего количества незаразно больных животных на долю хирургических заболеваний, обусловленных травматизмом, хирургической инфекцией и нарушением обмена веществ, приходится 25—30%. В этот процент не входят болезни органов дыхания, пищеварения и другие, при которых необходимо хирургическое лечение (трахеотомия, торакоцентез, руменоцентез, руменотомия, операции на сычуге и кишечнике с целью удаления конкрементов, пило- и фитобезоаров, кесарево сечение и пр.). Кроме того, хирургическое лечение является основным при ряде инфекционных и инвазионных заболеваний, например при некробактериозе, актиномикозе, столбняке, ценурозе, онхоцеркозе, инфекционном и инвазионном конъюнктивокератите и пр. Таким образом, если учесть все изложенное, то окажется, что около 50% общего числа больных животных нуждается в применении хирургических приемов, начиная с внутривенных вливаний, новокаиновых блокад и кончая полостными операциями.
По Абишеву, травматизм у взрослого крупного рогатого скота достигает 37,8% ; у молодняка трехлетнего возраста—26,5% ;
у овец в пастбищный период составляет 44,6% , в зимний—7,3% ;
у свиней травматизм встречается в 28,4% , а у лошадей—26,4% . По данным М. В. Плахотина и С. Т. Шитова, травматизм бычков в откормочном комплексе достигает от 12 до 30%.
Учитывая большой процент хирургической патологии, обусловленной преимущественно травматизмом, нарушением условий кормления, содержания и эксплуатации животных, необходимо принимать плановые научно обоснованные профилактические меры. При этом необходимо иметь в виду следующие биологические закономерности. У сельскохозяйственных животных жизнь протекает по следующей схеме: «организм+естественно-природная среда+условия среды, созданной человеком,®организм». Создавая искусственные условия жизни для сельскохозяйственных животных, человек способствует повышению продуктивности их в результате более лучшего использования энергии и питательных веществ корма, но при этом организм в значительной мере утрачивает разнообразие адаптационных возможностей и приспосабливается к искусственным условиям. Поэтому, чем выше продуктивность сельскохозяйственного животного, тем больше оно нуждается в создании для него наиболее благоприятных условий жизни и выработки у него искусственно и генетически созданной устойчивости к новым условиям существования.
В профилактике травматизма хирургических и других болезней в условиях животноводческих комплексов ведущее значение имеют инженерно-строительные, зоогигиенические и ветеринарно-санитарные параметры животноводческих комплексов; инженерно-технологическое решение механизации и автоматизации, содержания, кормления, доения с учетом биологических потребностей и физиологических возможностей животных различного вида и направления. При этом недопустима механическая «подгонка» биологических систем с их филогенетически выработанным консерватизмом к создаваемым инженерно-техническим системам. Это возможно лишь при выведении животных, приспособленных к новым условиям жизни, когда технологические приемы ухода, кормления и эксплуатации не станут чрезвычайными, приводящими к заболеваниям. Эти теоретические положения необходимо иметь в виду при разработке общей и частной профилактики травматизма, хирургической инфекции и другой патологии.
Для своевременного проведения профилактических мероприятий очень важно уметь определять ранние первичные клинические признаки заболевания, такие, как ухудшение аппетита (прием корма), снижение молочной и другой продуктивности, работоспособности, отсутствие жвачки, уменьшение количества движений рубца, сухое носогубное зеркальце, необычные позы, нарушение координации движения, частое мочеиспускание, жидкий кал и др.
Организационные основы профилактики травматизма. Современная профилактика травматизма предусматривает большой круг вопросов, на которые нужно обращать внимание при организации мероприятий по предупреждению заболеваний животных. Одни из них могут быть решены в течение продолжительного времени. Эти вопросы должны включаться в перспективные планы развития животноводства данного хозяйства, района, области, республики. К ним относятся вопросы общей профилактики: 1. Санация (оздоровление) естественной и создаваемой человеком среды (недопущение загрязнений атмосферы, водоемов, почвы вредными агентами). 2. Строгое соблюдение научно обоснованных зоогигиенических нормативов и ветеринарно-санитарных требований к строительству животноводческих помещений, оборудованию, технологическим процессам, которые должны соответствовать биологическим потребностям продуктивных животных. В связи с этим предусматривается ветеринарно-санитарный контроль при проектировании, строительстве и приеме в эксплуатацию животноводческих помещений, выгульных площадок, пастбищно-лагерных помещений, ветеринарно-санитарных блоков, пунктов искусственного осеменения, других животноводческих построек, ветеринарных лечебниц и станций по борьбе с болезнями животных. 3. Физиологически обоснованное полноценное кормление, содержание и режим эксплуатации животных. 4. Выведение новых, высокопродуктивных пород, устойчивых к условиям внешней среды.
Другие вопросы оздоровления животных связаны с выполнением частной или специальной профилактики. Они должны осуществляться в повседневной животноводческой и ветеринарной практике с целью недопущения и ликвидации того или иного вида травматизма, хирургической и другой патологии животных. Для этого проводят: 1) регулярные ветеринарно-санитарные обходы-осмотры животноводческих помещений, кормовых и доильных цехов, выгульных двориков, пастбищ, мест хранения кормов и пр.; 2) систематические осмотры животных (текущая диспансеризация) и 3) диспансерные обследования животных.
Сущность текущей диспансеризации сводится к клиническому осмотру каждого животного. При этом обращается внимание на общий габитус, кожный покров, органы зрения, жвачку, поедаемость корма, состояние наружных половых органов, вымени, копыт, конечностей и т.д. Одновременно ветеринарный специалист проводит опрос обслуживающего персонала, касающийся продуктивности, упитанности и состояния животного. Результаты осмотра и указания кратко заносят в специальный журнал текущей диспансеризации, который хранят в данном животноводческом помещении. При следующем обходе-осмотре контролируют выполнение указаний.
Животные с низкой упитанностью, снизившие удои или приросты, не должны считаться здоровыми даже при нормальных показателях температуры, пульса, дыхания, руминации и пр., их необходимо подвергнуть детальному клиническому, а при необходимости и лабораторному исследованию и выяснить причины, вызвавшие снижение упитанности, продуктивности и другие первичные признаки физиологических и морфологических нарушений. При этом обращают внимание на режим кормления с последующим анализом питательной ценности рациона и качества корма; организацию труда и отношение людей к исполнению своих обязанностей; на обеспечение моциона и другие условия ухода, содержания и эксплуатации животных, а также на факторы, способствующие возникновению механического, эксплуатационного, кормового и прочих видов травматизма. Выявленные недостатки необходимо устранить, а животных с признаками заболевания подвергнуть изоляции и лечению.
Диспансерное обследование животных проводят 2 раза в год, весной и осенью (высокоудойных коров ежеквартально), с более детальным клиническим и лабораторным исследованием животных. Результаты заносят в диспансерные карточки, больных животных лечат и проводят необходимые профилактические мероприятия в отношении подобных и других возможных заболеваний.
Профилактика травматизма у свиней. В условиях хозяйств промышленного типа травматизм и хирургические заболевания находятся в определенной связи с технологическими процессами, конструкцией станков, щелевых полов, комплектованием возрастных групп, выгрузкой, погрузкой и транспортировкой свинопоголовья, а также каннибализмом и другими причинами. Профилактика травматизма прежде всего сводится к совершенствованию конструкций, технологических процессов, устранению выявляемых причин, способствующих травмированию свинопоголовья в соответствующих цехах; обеспечению полноценным сбалансированным кормлением; четкому выполнению и соблюдению зоогигиенических и ветеринарно-санитарных правил. При этом нужно учитывать, что в репродукторном цехе часто наблюдается травмирование и задушение поросят свиноматками, особенно при отсутствии или неисправности площадок обогрева. Вследствие этого поросята, чтобы согреться, ложатся к свиноматке, которая и травмирует их. Создание оптимальной температуры в свинарнике и функционирование площадок обогрева резко сокращают травматизм. Скусывание клыков у поросят острыми инструментами не у основания, а ниже верхушки на 1—1,5 мм предупреждает трещины, переломы зубов, развитие пульпита и других осложнений и травмирование сосков при сосании. Полноценное сбалансированное кормление свиноматок и своевременно примененное лечение поносов и запоров профилактирует образование пупочных, пахово-мошоночных грыж и выпадений прямой кишки у поросят.
В цехе доращивания при чрезмерной загрузке станков поросята травмируют друг друга ногами и зубами, а при широких просветах решеток жижесточных плит повреждаются копытца и дистальная часть конечностей, нередко возникают переломы. В цехе откорма также распространено травмирование зубами друг друга, повреждение копытец и пальцев вследствие некачественного и неисправного пола и решеток жижесточников. Содержание в условиях гиподинамии на цементных или бетонных полах,особенно без подогрева, способствует массовому ревматоидному поражению и параличам таза.
Устранение отмеченных конструктивных недостатков и строительного материала, недопущение перегрузки станков, изоляция агрессивных животных и каннибаллов, обеспечение свиноматок и хряков-производителей ежедневным моционом, расчистка и обрезка рога копытец у них значительно профилактируют травматизм свинопоголовья комплекса.
Профилактика травматизма овец. Травматизм кожи наблюдается редко, так как она защищена мощным шерстным покровом, но он довольно часто отмечается при стрижке шерсти. При рационе, бедном витаминными и минеральными веществами, у овец развивается извращение аппетита (лизуха), они обгрызают шерсть и отгрызают хвосты друг у друга, что способствует формированию у них пилобезоаров.
Для предупреждения этого следует кормить овец разнообразными, полноценными кормами и обеспечивать солью (лизунцом), ветками хвои, минеральными кормами и микроэлементами, особенно в стойловый период. Тепляки и кошары надлежит содержать в чистоте, соблюдая ветеринарно-санитарные требования. Продолжительное содержание овец в тесных влажных, занавоженных кошарах, без моциона приводит к деформации копытец, наминам, заломам, копытной гнили либо развитию некробактериоза. Травматизм копытец овец иногда охватывает 30—70% отары. Поэтому для предупреждения травматизма копытной гнили и некробактериоза необходимо содержать овец в просторных кошарах, при достаточном количестве сухой подстилки. Избегают выпас овец на пастбищах с высокой влажностью почвы, среди колючих кустарников, по стерне, не используют для водопоя крутые и илистые берега водоема. Не реже двух-трех раз в год необходимо производить обрезку копыт, особенно перед выгоном на пастбище.
2.5. ОБЩАЯ И МЕСТНАЯ РЕАКЦИЯ ОРГАНИЗМА
2.5.1. ОБЩАЯ РЕАКЦИЯ ОРГАНИЗМА НА ТРАВМЫ.
Нейрогуморальная реакция при травмах. Невозможно правильно понять патогенез травматических и других заболеваний животных без уяснения основных положений нейрогуморальной регуляции защитно-приспособительных реакций в норме и при патологии. Следует учитывать, что организм высокоорганизованных животных, как сложная биологическая саморегулирующаяся система, управляется по принципу прямых и обратных связей.
При этом нервная система, выполняя защитно-приспособительную роль, в ходе развития заболевания может оказывать противоположное влияние на организм и играть роль существенного, иногда важнейшего патогенетического фактора. Установлено, что морфофункциональная целостность и реактивность отдельных клеток и всей системы организма находятся под влиянием условий внешней среды и в зависимости от исходного в данный момент функционального состояния нервной системы, а также функциональной полноценности эндокринной системы, взаимодействующих друг с другом. Ухудшение координирующей адаптационной функции нервно-эндокринной системы способствует снижению физиологических функций и сопротивляемости клеток периферии. В результате этого внешние факторы, обычно не вызывающие повреждения клеток, оказываются для них «травмирующими».
Таким образом, физиологическое состояние, жизненность клеток любой части тела находятся в прямой зависимости от функционального состояния всего организма, его нейрогуморальной регуляции.
В процессе эволюционного развития высших животных и формирования центральной нервной системы с ее периферическими приборами клетки тканей сохранили некоторую способность непосредственно реагировать на прямые раздражения (ранение, ожог, инфекция и др.). Поэтому они могут самостоятельно отвечать на раздражения и повреждения определенной, присущей им, защитной реакцией. При этом изменяется реактивность не только в поврежденных, но и в соседних клетках.
Возникшие в зоне повреждения сильные раздражения идут как импульсы сигнализации по обычным афферентным путям (периферическим нервам), симпатической цепочки, сосудисто-нервным сплетениям и достигают ретикулярной формации и подкорковых центров, где под их влиянием возникает возбуждение. Отсюда оно передается но внутрицентральным эфферентным путям к коре полушарии большого мозга, где также возникает очаг возбуждения. Последний направляет к возбужденной подкорке ответные импульсы, интегрируя и координируя ее функции. Возбужденная подкорка по эфферентным путям посылает ко всем органам и особенно к зоне повреждения трофические и другие импульсы, управляющие защитно-приспособительными и иными реакциями целостного организма. Одновременно с этим из очага возбуждения коры головного мозга импульсы поступают на эфферентные проводящие пути и по ним достигают зоны повреждения. От последней кора вновь получает сигналы, но уже с теми изменениями, которые возникли в зоне повреждения под влиянием импульсов, идущих из очага возбуждения коры и подкорковых центров.
Импульсы раздражения, возникшие в зоне повреждения, могут замыкаться в периферических нервных приборах, параганглиях или симпатических ганглиях, в спинном мозге, не затрагивая при этом подкорковых центров и коры полушарий большого мозга. Однако чем сильнее повреждение, тем более высокие этажи нервной системы включаются в регуляцию защитно-приспособительной реакции. Адаптационный ответ со стороны головного мозга возникает, по-видимому, в тех случаях, когда функциональные возможности ниже лежащих этажей нервной системы оказываются недостаточными, чтобы восстановить нарушенное равновесие. При нормальном функциональном состоянии коры и подкорки возникшее в них возбуждение организует под влиянием травмы в зоне повреждения нормергическую защитно-приспособительную реакцию, направленную на восстановление возникших нарушений. В результате же длительного воздействия сильных, чрезвычайных раздражителей, идущих из зоны повреждения или функционально нарушенных внутренних органов, в коре головного мозга постепенно нарастает перераздражение и истощение ее клеток. Вследствие этого очаг возбуждения превращается в очаг торможения. По мере дальнейшего поступления с периферии сильных раздражений очаг торможения коры головного мозга все больше и больше распространяется по коре, и в ней возникает разлитое запредельное торможение. Эти явления развиваются быстрее, если сильные или сверхсильные раздражения обусловлены тяжелыми механическими, термическими и химическими травмами, либо инфекцией, или интоксикацией, сопровождающейся нарушением гематоэнцефалического и других барьеров.
Под влиянием запредельного торможения снижается интегрирующая и координирующая функции коры головного мозга. В связи с этим в подкорковых центрах, освобожденных от влияний коры, возникает положительная индукция. Она проявляется возбуждением и хаотической деятельностью подкорки, что прежде всего сказывается на функциональном состоянии таламогипоталамической области, в которой возникает «застойный» очаг возбуждения (длительное неколеблющееся возбуждение нервных клеток). Под влиянием такого «застойного» очага в подкорковом центре и на периферии возникают и развиваются нервнодистрофические явления. Они наблюдаются и при «застойном» неколеблющемся возбуждении, возникающем в каком-либо периферическом нерве. При этом нарушается трофическая регуляция со стороны нервных центров, в результате чего ухудшается внутриклеточный обмен веществ и снижается жизненность клеток, целых органов и всего организма.
Вместе с этим необходимо учитывать, что возникшие в результате повреждения патологические изменения, будучи локализованы анатомически, оказываются генерализованными в функциональном отношении преимущественно нервной системой. С другой стороны, нервная система, управляя защитно-приспособительными механизмами, организует локализацию патологического процесса в зоне первичного его возникновения и таким образом как бы ограждает организм от генерализации возникшего местного патологического процесса (см. «Воспаление»).
Роль желез внутренней секреции в защитно-приспособительном процессе очень большая. Нарушение функции их, обусловленное травмами, инфекцией и другими причинами, может также неблагоприятно сказываться на обмене веществ и функциональном состоянии органов, что дополнительно ухудшает защитно-адаптационные реакции всего организма. Нормальное же их функционирование способствует выздоровлению. В связи с этим теоретическое и практическое значение приобретает теория Г. Селье, согласно которой гипоталамус, гипофиз и надпочечники, управляя адаптационными процессами, обеспечивают гомеостаз — постоянство внутренней среды целостного организма. Доказано, что задние ядра гипоталамуса осуществляют интеграцию симпатических, а передние — парасимпатических функций. Эти ядра выполняют координационную функцию гипоталамуса, которая протекает под контролирующим и интегрирующим влиянием коры и структуры висцерального мозга, в состав которого гипоталамус входит.
Далее установлено, что гипоталамус является центром единой системы многозвеньевых механизмов прямых и обратных связей желез внутренней секреции. В нем образуются первые гормональные вещества, называемые рилизинг-факторами (их около 10). Известно, что нарушение любого звена гормональной системы вызывает нарушение обмена в каком-либо органе или во всем организме, что приводит к развитию болезни, обусловленной эндогенным фактором. Недостаток, например, кортикостероидов приводит к Адиссоновой болезни, а избыток их способствует развитию болезни Иценко — Кушинга (ожирение, гипертония, хрупкость костей и пр.). Доказано, что синтез ферментов определяется генами-носителями наследственной информации, сосредоточенной в хромосомах клеточного ядра. Гормоны же, не изменяя наследственной программы, управляют ею. Под влиянием гормонов гены могут переходить из неактивного состояния в активное и наоборот. Это значит, что влияние гормонов на гены, а последних на ферменты, под влиянием которых в организме протекают все биохимические процессы, происходит, как утверждает Н. Юдаев, по формуле «гормон — ген — фермент». Следовательно, направленно изменяя гормональ-ную функцию, можно управлять через систему генов ферментативными системами, обменом веществ, а следовательно, и адаптационными реакциями, которые, как известно, могут нарушаться под влиянием травмирующих и других факторов внешней и внутренней среды организма. Сущность управления защитно-приспособительными процессами, по Г. Селье, представляется в следующем виде. В гипоталамусе возникает возбуждение, адекватное степени и продолжительности воздействия на него обычных и чрезвычайных раздражений, идущих с периферии, внутренних органов и внутренней среды (рис. 1). В возбужденном гипоталамусе, как нейроэндокринной железе, соответственно степени раздражения вырабатывается нейрогормон, который, проникнув в капилляры, переносится по портальной артерии в гипофиз. Под влиянием нейрогормона и рефлекторного воздействия со стороны коры головного мозга и центров подкорки гипофиз вырабатывает адренокортикотропный (АКТГ) и соматотропный (СТГ) гормоны, поступающие в кровь. Циркулируя в крови, они воздействуют на клетки организма и кору надпочечников. Возбужденные адренокортикотропным гормоном клетки коры надпочечников вырабатывают гормон кортизон, который так же, как и АКТГ, ослабляет защитно-адаптационные реакции на травму и другие раздражения. Оба этигормона отнесены автором к противовоспалительным. Под влиянием же соматотропного гормона кора надпочечника выделяет дезоксикортикостерон (ДОКС). Этот гормон, наоборот, усиливая адаптационные реакции, является воспалительным. Так, сомато-тропный гормон, являясь одним из гормонов, устанавливающих связь между головным мозгом и железами внутренней секреции, контролирует синтез гормона роста. Известно, что применение соматотропина или молекулы, аналогичной ему, предупреждает излишнее выделение гормона роста и развитие акромегалии. Возможно, что соматотропный гормон оказывает определенное влияние и на опухолевый рост. Установлено его участие в регулировании уровня сахара в крови. Доказано, что соматотропин поддерживает адаптационное равновесие между гормонами инсулином (снижающим содержание сахара в крови) и глюкагоном (повышающим его содержание), ответственными за физиологический уровень сахара в крови. Таким образом, регулируя систему «инсулин—глюкагон», можно управлять этой системой в целях профилактики и лечения.
Из всего изложенного следует, что ответная защитно- приспо-собительная реакция организма на травмирующие и другие чрезвычайные воздействия регулируется нервной системой и гуморальными факторами через посредство простагландинов.
Приведенные теоретические положения и практический опыт указывают на возможность управления ответной реакцией организма на травмы и другие чрезвычайные факторы путем воздействия на нервную и эндокринную системы средствами и методами патогенетической терапии (новокаиновые блокады, медикаментозный сон, физиотерапия, иглоукалывание, инъекции гормонов гипофиза—АКТГ, СТГ, коры надпочечников—кортизон, ДОКС и др.).
Клинически общая реакция высокоорганизованных животных на сильную травму может проявляться в виде обморока, коллапса, шока или проявляться коматозным состоянием.
Обморок- внезапное и кратковременное проявление малокровия мозга, которое выражается в расстройстве чувствительности и нарушении рефлекторной деятельности. В результате действия сильного раздражителя (испуг, боль, тепловой перегрев) на сосудодвигательный центр происходит рефлекторное сокращение периферических кровеносных сосудов, в том числе сосудов центральной нервной системы. Часто наступает вследствие испуга, страха и клинически проявляется в головокружении (нарушении координации), холодной потливости и потере сознания (рефлекторной деятельности). Отмечается сужение зрачков, пульс слабый, дыхание поверхностное.
Лечение- покой, горизонтальное положение, освобождение от ошейника, намордника и тесемок, использование спирта нашатырного, сердечных средств.
Коллапс—временная, внезапно возникшая слабость сердечной деятельности и падение сосудистого тонуса, сопровождающиеся резким снижением артериального давления и всех жизненных функций.
Причинами возникновения его являются травмы с обильным кровотечением и сильными болевыми раздражениями. Иногда коллапс возникает как следствие острой интоксикации продуктами тканевого распада или в результате испуга и мышечного переутомления.
Клинические признаки—внезапная общая слабость, животные ложатся, пульс частый, слабый, нитевидный, дыхание редкое, поверхностное, видимые слизистые оболочки и конъюнктива бледные с цианотичным оттенком, общая температура и реакция на внешние раздражения понижены, конечности холодные, мускулатура расслаблена.
Лечение сводится к устранению причины, вызвавшей ослабление сердечной деятельности, и нормализации ее функции. При наличии кровотечения принимают меры к его остановке (накладывают жгут, делают тампонаду, лигируют сосуды, внутривенно вводят кальция хлорид). Для пополнения крови, повышения кровяного давления и улучшения сердечной деятельности рекомендуется ввести в вену физиологический раствор поваренной соли с глюкозой и аскорбиновой кислотой. Лучшие результаты достигаются при переливании совместимой крови или после вливания специальных кровезаменяющих жидкостей (полиглюкин, реополиглюкин, гемодез, гидпролизат Л-103, гидролизат казеина ЦР-ЛИПК, аминопентид и др.).
В случаях интоксикации внутривенно вводят 40%-ный раствор гексаметилентетрамина с дозой кофеина. Для стимуляции сердечной деятельности и улучшения периферического кровообращения целесообразно подкожно инъецировать кофеин, камфорное масло или внутривенно ввести камфорную сыворотку (мелким животным 25—30 г; крупным 250—300 г 2 раза в день). Одновременно с использованием указанных средств необходимо растереть животное соломенными жгутами, согреть его грелками, рефлекторами и другими приборами, создающими тепло, после чего укутать или укрыть.
Шок—тяжелое общее состояние животного, характеризующееся кратковременным резким возбуждением, переходящим в глубокое угнетение нервной системы и всех функций организма. Это тяжелое состояние животного, наиболее близкое к терминальному. В быту мы часто пользуемся этим термином, подразумевая прежде всего нервное, душевное потрясение. Пожалуй, нет в медицине и ветеринарии ни одного синдрома, с которым бы так давно не было знакомо человечество. Клиническую картину шока описал еще Амбруаз Паре.
Понятие «шок» (англ. shock — удар, потрясение) ввел в начале XVIII в. французский врач Ле-Дран – консультант армии Людовика XV, он же предложил тогда простейшие методы лечения шока: согревание, покой, алкоголь и опий, а также описавший его основные симптомы. Н. И. Пирогов первый в мире достаточно правильно представил патогенез шока, описал его и наметил способы профилактики и лечения. Затем было предложено значительное количество теорий, однако все они неполно раскрывают патогенез шока.
В ветеринарной медицине - это действительно удар по организму больного животного в целом, приводящий не толькок каким-то конкретным нарушениям в функциях отдельных органов, а сопровождающийся общими расстройствами вне зависимости от приложения повреждающего фактора. Шок нужно отличать от обморока и коллапса.
Классификация шока. Существуют две основные классификации шока-
1.В зависимости от этиологии шока - этиологическая.
2. В зависимости от патогенеза шока- патогенетическая.
1. В зависимости от причин, вызвавших шок, различают: травматический — возникающий после случайных травм; операционный—во время и после хирургических или гинекологических операций, проводимых при недостаточном обезболивании или без него; гемотрансфузионный — вследствие белковой несовместимости, гемолиза или коагуляции при переливании несовместимой крови; анафилактический шок—на фоне предварительной сенсибилизации животных чужеродным белком или бактерийными токсинами.
Наиболее часто наблюдается травматический шок. По времени проявления различают: первичный шок, возникающий в момент нанесения травмы или непосредственно после нее и продолжающийся от нескольких минут до нескольких часов; вторичный шок, проявляющийся через несколько часов или дней после травмы, хирургической операции или оказания акушерской помощи, вследствие интоксикации, либо дополнительной травмы, или усиления боли после прекращения действия обезболивающих средств.
Первичный шок нередко протекает трехфазно. Его первая фаза характеризуется резким возбуждением и называется эректильной, вторая — торпидная проявляется глубоким торможением и третья — паралитическая приводит к летальному исходу.
Травматический шок встречается у свиней, кошек, лошадей и собак, реже у крупного рогатого скота. При неуравновешенной, легко возбудимой нервной системе он возникает значительно чаще. Такие животные нуждаются в обязательном применении перед операцией местного или общего обезболивания.
Этиология. Шок возникает при обширных повреждениях мягких тканей, сочетающихся с переломами костей; ущемлениях нервных стволов; сильном натяжении брыжейки при оперативных вмешательствах на органах брюшной полости; ранениях грудной полости, особенно при вхождении в нее воздуха (пневмоторакс); грубо проводимом родовспоможении; ожогах 2, 3, 4 и 5-й степеней; сильном и длительном сдавливании нервов эластическим, жгутом, накладываемым на конечности, отрыве органа и т.п.
Развитию шока способствуют стрессовый фон (см. «Психическая травма»), предварительное перевозбуждение центральной нервной системы; длительные нагноения, сопровождающиеся гнойно-резорбтивными явлениями; предшествующее травме тяжелое заболевание, охлаждение, перегревание, длительное кормовое и водное голодание, дополнительные травмы, отсутствие или недостаточная иммобилизация переломленных костей; грубое проведение лечебных процедур (вправление переломов, вывихов, ревизия ран и пр.); большие кровопотери; гипо- и авитаминозы А и В1 а также страх, сопутствующий травме. Новорожденные животные более чувствительны к шоку. Сочетание первичных причин, вызвавших шок, с последующими болевыми или токсическими воздействиями способствует усилению нервнорефлекторных нарушений и утяжеляет шок. Суммация же первичных и последующих раздражений нервных центров приводит к развитию вторичного шока. Тяжелые формы первичного и вторичного шока могут закончиться смертью.
Патогенез шока пока полностью не выяснен. Более правильно его характеризует нервнорефлекторная теория Э. А. Асратяна. Заслуживает также внимания теория Г. Шушкова.
Нервнорефлекторная теория порочного круга, по Э. А. Асратяну, сводится к следующему. Под влиянием сильных болевых воздействий возникает эректильная фаза шока как следствие возбуждения подкорковых центров и коры головного мозга. По мере его усиления эректильная фаза переходит в торпидную. При этом в коре головного мозга развивается охранительно-целебное торможение как своеобразная защита нервных центров от истощения, приводящего к глубокому запредельному парабиотическому их состоянию, легко переходящему в паралитическую стадию. В эректильной фазе вследствие функциональных изменений, возникших в центральной нервной системе, наступают нарушения в гемодинамике, что, в свою очередь, приводит к изменению химизма крови и тканей. Это способствует углублению первичных нарушений в центральной нервной системе и гемодинамике, отрицательно влияя на химизм крови и функциональное состояние всех органов и систем. Возникшие изменения в нервной системе, гемодинамике и химизме крови углубляют и отяжеляют шоковое состояние; в нервной системе постепенно нарастает истощение, приводящее к астении. Еще более ухудшается гемодинамика, падает кровяное давление, этому способствует выраженная атония и повышенная проницаемость капилляров, выход же плазмы крови в ткани сопровождается сгущением и уменьшением объема циркулирующей крови. Почти одновременно с указанными явлениями в крови и тканях возникают гиперкалиэмия, ацидоз, аноксемия, аноксия, фосфотемия. К данным изменениям присоединяются гистолитическая, метаболическая и бактериальная токсемии, которые усиливают и углубляют шок. Токсемические шокогенные влияния на органы и нервную систему начинают включаться примерно через 20—30 мин, чаще через 2—3 ч после травмы.
Клинические признаки. Эректильная фаза шока развивается в момент нанесения травмы и продолжается от нескольких секунд до нескольких минут. Клинически она проявляется резким, буйным возбуждением: животное издает сильные звуки (визг, ржание и пр.), бьется, стремится освободиться от фиксации; глаза широко открыты, зрачки и ноздри расширены, дыхание учащено; пульс частый, сильного наполнения, кровяное давление повышено. Может наблюдаться усиленное потоотделение. При легкой форме эректильного шока и прекращении сильных болевых раздражений животное выходит из шокового состояния. В случаях средней и особенно тяжелой формы эректильная фаза переходит в торпидную фазу шока. Последняя характеризуется резким угнетением, понижением рефлексов при сохранении «сознания»; отсутствием реакции на вновь наносимую боль; снижением всех функций организма, в результате чего мускулатура становится вялой, животное ложится или падает, лежит неподвижно, слабо реагируя на слуховые раздражители; дыхание становится поверхностным, неправильным и редким, слизистые оболочки бледные; пульс слабый, частый, едва различимый, кровяное давление прогрессивно падает; наблюдается стеклянный блеск роговицы, зрачки расширены, вяло реагируют на свет; температура тела снижается на 1—2°; наблюдается непроизвольное отделение кала и мочи. Кровь постепенно сгущается; уменьшается количество плазмы, вследствие чего число эритроцитов в объеме крови оказывается увеличенным; ухудшается гемодинамика, ослабевает сердечная деятельность; нарушается обмен веществ; снижается функция почек, возникает олигурия и даже анурия; изменяется функциональное состояние других органов и систем.
При благоприятном течении и своевременном лечении торпидная фаза шока заканчивается выздоровлением, в других случаях — переходит в паралитическую фазу вследствие истощения нервных центров и возникновения центральных параличей. При этой фазе снижается температура тела на 2° и даже 3°, кровяное давление становится очень низким, пульс — едва уловимым, рефлексы и другие реакции на внешние раздражители отсутствуют.
Лечение шока должно быть комплексным, направленным на: 1) устранение источника болевого раздражения и нормализацию функции нервной системы; 2) восстановление гемодинамики; 3) борьбу с токсемией и нарушением обмена веществ.
При эректильной фазе шока необходимо устранить причину возбуждения (травма, операция и т.п.), улучшить сердечную деятельность введением кофеина. Одновременно с этим нужно предупредить развитие генерализованного возбуждения в центральной нервной системе путем временного прекращения операции и тщательного местного обезболивания зоны травмы. В случаях пневмоторакса плевропульмональный шок снимают новокаиновой блокадой вагосимпатического ствола по А. В. Вишневскому. При выпадении кишечника после ранения его следует вправить в брюшную полость (после тщательно проведенной антисептической обработки), ввести в брюшную полость 0,25% -ный раствор новокаина с канамицином и сделать трубчатый дренаж, затем наложить швы на рану. В данном случае и с целью профилактики шока перед абдоминальными операциями следует сделать эпиплевральную новокаиновую блокаду по В. В. Мосину. Для предупреждения и снятия шока при переломах в зону перелома инъецируют 2— 3%-ый новокаин на 30%-ном этиловом спирте, высвобождают ущемленный отломками нервный ствол и иммоби-лизируют отломки.
При торпидной фазе шока, по Э. А. Асратяну, следует устранить запредельное торможение нервных центров новокаиновой блокадой симпатических ганглиев или симпатического ствола; по Г. Шушкову, прежде всего необходимо снять парабиотическое состояние периферических нервных приборов и проводящих путей соматического и вегетативного отделов нервной системы, используя внутрикожную, короткую, циркулярную и другие подобные виды новокаиновых блокад.
В целях восстановления гемодинамики, объема циркулирующей крови, поднятия артериального давления, уменьшения проницаемости капилляров, борьбы с плазмореей и сгущением крови необходимо внутривенно вводить вышеприведенный состав 0,125%-ного раствора новокаина по В. Сологубу, М. Долгиной и В. Лаврову; целесообразна трансфузия одногруппной крови: мелким животным 50—100 мл, крупным—1500—2000 мл. При отсутствии крови вводят внутривенно капельным способом полиглюкин или реополиглюкин (80—90 кап. в 1 мин). Если при введении раствора в течение первых 2—3 мин не возникает беспокойства, капельное введение продолжают. В случае беспокойства делают временный перерыв до успокоения животного. Для снятия спазма сосудов, возникающего при шоке, применяют внутривенно адреноблокатор—фентоламин: мелким животным 0,001, крупным—0,03; растворяют его непосредственно перед введением в 1 мл стерильной дистиллированной воды. При кровотечении из артериол во время операционного шока под кожу инъецируют 5%-ный эфедрин: мелким животным 0,1—0,2, крупным—5—8 мл.
Наряду с изложенным заслуживают применения противошоковые жидкости: 1. Жидкость Э. А. Асратяна состоит из двух растворов. Первый содержит: натрия хлорида 16 г, натрия бромида 1,5 г и натрия бикарбоната 1,2 г, воды до 100 мл; второй—уретана 2,4 г, веронала 0,3 г, кальция хлорида 3 г, глюкозы 32 г, этилового спирта 30 г, воды до 100 мл. Перед введением растворы смешивают: на 10 частей первого раствора берут 1 часть второго и вводят животному внутривенно из расчета 5 мл на 1 кг его массы.
2. Жидкость Попова содержит: натрия хлорида 15 г, кальция хлорида 0,2 г, калия хлорида 0,2 г, натрия бикарбоната 4 г, глюкозы 150 г, этилового спирта 100 г, воды дистиллированной 100 г. Мелким животным вводят внутривенно 200—300 мл; жеребятам и телятам в возрасте до года — 500—800 мл; крупным животным — 2000—3000 мл. Лечебный эффект возрастает при добавлении аскорбиновой кислоты и витамина B1 (мелким животным соответственно 0,1—0,3 и 0,01 г, крупным животным 1—1,5 и 0,1 г).
3. «Камфорная сыворотка» по прописи М. В. Плахотина обеспечивает высокий терапевтический эффект. Она включает: камфоры 3 г, этилового спирта 200 г, гексаметилентетрамина 10 г, глюкозы 100 г, кальция хлорида 20 г, физиологического раствора натрия хлорида 2000 мл. Ее вводят внутривенно крупным животным в дозе 1500—2000 мл, мелким— 150—200 мл.
При вторичном шоке, возникшем вследствие интоксикации и инфекции, целесообразнее использовать «камфорную сыворотку» или 40%-ный раствор гексаметилентетрамина с кальция хлоридом и кофеином. Оба средства обеспечивают дезинтоксикацию, выведение токсинов из организма, снижают проницаемость капилляров и клеточных мембран. Кроме того, необходимо полное или частичное иссечение мертвых тканей и тщательное дренирование (см. ниже).
Профилактика шока сводится: к недопущению механических и других видов травм, сенсибилизации организма; к применению местного и общего обезболивания перед операциями и при тяжелых случаях травм. Не меньшее значение в профилактике шока имеют: ранняя остановка кровотечения; хирургическое удаление ранящих предметов, мертвых тканей, костных осколков, давящих на нерв; иммобилизация костных отломков; тщательное закрытие ран грудной полости; устранение интоксикаций травматического и другого происхождения.
2. Наиболее целесообразным представляется деление шока на виды с учетом патогенеза происходящих в организме изменений (рис. 5 ). С этой точки зрения выделяют гиповолемический, кардиогенный, септический и анафилактический шок. При каждом из этих видов шока происходят специфические изменения.
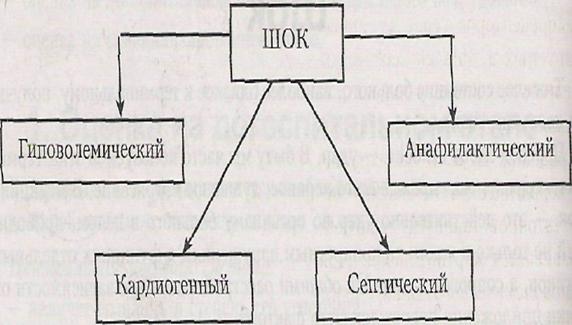
Рис. 5 Деление шока с учетом патогенеза.
Гиповолемический шок
Циркуляторная система организма состоит из трех основных частей: сердце, сосуды, кровь. Изменения параметров деятельности сердца, тонуса, сосудов и объема циркулирующей (ОЦК) определяют развитие симптомов, характерных для шока. Гиповолемический шок вызывается острой потерей крови, плазмы или жидкостиркулирующей крови(ей организма. Гиповолемия (снижение ОЦК) приводил к уменьшению венозного возврата и снижению давления наполнения сердца (ДНС). Это, в свою очередь, ведет к снижению ударного объема сердца (УОС) и падению артериального давления (АД). Вследствие стимуляции симпато-адреналовой системы возрастает частота сердечных сокращений (ЧСС) и возникает вазоконстрикция (рост общего периферического сопротивления — ОПС), что поддерживает центральную гемодинамику и вызывает централизацию кровообращения. При этом существенное значение в централизации кровотока (наилучшее снабжение кровью сердца, мозга и легких) имеет преобладание а-адренорецепторов в сосудах, иннервируемых n. splanchicus, а также в сосудах почек, мышц и кожи. Такая реакция организма вполне оправдана, но, если гиповолемия корригируется, то вследствие недостаточной тканевой перфузии развивается картина шока. Для гиповолемического шока, таким образом, характерны снижение ОЦК, снижение давления наполнения сердца и сердечного выброса, снижение артериального давления и возрастание периферического сопротивления.
Кардиогенный ШОК
Наиболее частой причиной кардиогенного шока является острый инфаркт миокарда, реже миокардит и токсическое поражение миокарда. При нарушении насосной функции сердца, аритмии и других острых причинах падения эффективности сердечных сокращений происходит снижение УОС. Вследствие этого возникает снижение АД, в то же время возрастает ДНС из-за неэффективности работы сердца (рис. 7). В результате стимулируется симпато-адреналовая система, возрастает ЧСС и ОПС. Изменения в принципе сходны с таковыми при гиповолемическом шоке. Это — гиподинамичесвие формы шока. Патогенетическое различие заключается лишь в значении ДНС: при гиповолемическом шоке оно снижено, а при кардиогенном — повышено.
Септический шок
При септическом шоке первичные расстройства касаются периферии кровообращения. Под влиянием бактериальных токсинов открываются короткие артерио-венозные шунты, через которые кровь устремляется, обходя капиллярную сеть, из артериального русла в венозное (рис. 8). При уменьшении поступления крови в капиллярное русло ток на периферии высок и ОПС снижено. Соответственно снижается АД, компенсаторно увеличивается УОС и ЧСС. Это так называемая гипердинамическая реакция циркуляции при септическом шоке. Снижение АД и ОПС происходит при нормальном или увеличенном УОС. При дальнеишем развитии гипердинамическая форма переходит в гиподинамическую.
Анафилактический шок
Анафилактическая реакция является выражением особой повышенной чувствительности организма к инородным субстанциям. В основе развития анафилактического шока — резкое снижение сосудистого тонуса под воздействием гистамина и других медиаторных субстанций (рис. 9 ). Вследствие расширения емкостной части сосудистого русла (вены) развивается относительное снижение ОЦК: возникает несоответствие между объемом сосудистого русла и ОЦК. Гиповолемия приводит к уменьшению обратного кровотока к сердцу и снижениюДНС. Это ведет к уменьшению УОС и АД. Снижению производительности сердца способствует и прямое нарушение сократительной способности миокарда. Характерным для анафилактического шока является отсутствие выраженной реакции симпато-адреналовой системы, этим во многом объясняется прогрессивное клиническое развитие анафилактического шока.
Следует отметить, что в лечении шока, как, пожалуй, ни при каких других ситуациях, нужна четкая программа действий, а также хорошее знание патогенеза происходящих в организме изменений.
2.5.2. Местная реакция организма на травму (воспаление).
Воспаление — ответная защитно-приспособительная реакция организма высокоорганизованных животных на разнообразные повреждения, возникающие под влиянием механических, физических, химических и биологических травмирующих факторов.
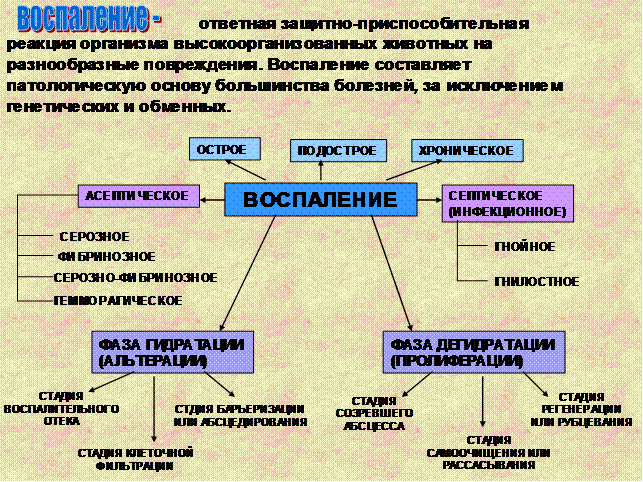
Рис. Содержание местной реакции организма на травму.
Воспаление составляет патогенетическую основу многих болезней, за исключением генетических и болезней обмена. Поэтому рассмотрение с клинических позиций биологии воспаления, фазности и стадий ее развития позволит яснее освоить и понять патогенетическую основу хирургической и другой патологии.
Различают асептическое и инфекционное воспаления. Асептическое воспаление возникает под влиянием механических, физических и химических повреждающих воздействий. По течению оно может быть острым и хроническим, а по характеру экссудата — серозным, серозно-фибринозным и фибринозным. В тех случаях, когда в серозном экссудате содержится значительное количество эритроцитов, его называют геморрагическим. Под воздействием инъекций скипидара и некоторых других химических веществ развивается асептическое гнойное воспаление.
Инфекционное воспаление возникает при внедрении в ткани живых возбудителей болезни и протекает преимущественно остро и тяжелее асептического. При некоторых видах инфекции и микотических поражениях оно приобретает подострое и хроническое течение. Для аэробной инфекции, вызываемой стрептококками, синегнойной палочкой и некоторыми другими микроорганизмами, характерно гнойное воспаление. Под воздействием факультативных анаэробов развивается гнилостное воспаление.
Местные симптомы воспаления.
Местная реакция при острой гнойной инфекции проявляется симптомами, характеризующими развитие воспалительной реакции:
rubor (краснота)
calor (местный жар)
tumor (припухлость)
dolor (боль)
function laesa (нарушение функции).
Краснота легко определяется при осмотре. Вначале отмечается расширение сосудов (артериол, венул, капилляров), затем наступает замедление кровотока вплоть до почти полной его остановки – стаза. Такие изменения называются «гиперемия» и связаны с воздействием на сосуды гистамина и ацидозными изменениями в зоне воспаления.
Местный жар связан с усилением катаболических реакций и высвобождением получаемой энергии в виде тепла.
Припухлость тканей обусловлена изменением проницаемости стенки сосудов для плазмы и форменных элементов крови, а также резким повышением гидростатического давления в капиллярах. Плазму легко связывают тканевые коллоиды.
Боль обусловлена сдавливанием или нарушением целостности нервных окончаний.
Воспаление, как единый двуфазный защитно-приспособительный процесс, включает два основных взаимосвязанных компонента: разрушительный (альтеративный), регенеративно-восстановительный (пролифиративный). Оно может протекать с преобладанием нейродистрофических - разрушительных или компенсаторных -восстановительных явлений. На основании интенсивности проявления этих процессов различают: 1) нормергическое; 2) гиперергическое и 3) гипоэргическое воспаление.
Нормергическое воспаление характеризуется адекватной ответной реакцией организма на механическое, физическое, химическое или биологическое (микробное, вирусное) повреждающее воздействие. Исходом такой воспалительной реакции является выздоровление, так как под влиянием ее происходят нейтрализация, подавление или полное уничтожение вредоносных агентов, выведение, рассасывание или изоляция (инкапсуляция) инородных предметов, попавших в ткани организма. В клиническом плане важно знать, что при нормергическом воспалении преобладают регенеративные явления, а разрушительные направлены на подавление инфекционного начала и ферментативное разжижение мертвых тканей, возникших под воздействием повреждающего агента (травма, микробный фактор). При этом формируется биологически совершенный клеточный и грануляционный барьеры, а реактивный ферментолиз ограничивается преимущественно зоной травмированных тканей. Нормергическое гнойное воспаление свидетельствует о подавлении инфекта и формировании добро-качественного абсцесса. При таком воспалении, как правило, не требуется применения сложных лечебных процедур.
Гиперергическое воспаление возникает при нарушении адаптационно-трофической функции нервной системы, аллергическом состоянии организма, при большом количестве мертвых тканей; оно отмечается и при инфекционных формах воспаления,протекает сверхостро, не адекватно вредоносности агента, вызывающего повреждение. При нем разрушительные явления (процессы гистолиза и некроза) преобладают над регенеративными. Таким образом, гиперергическое воспаление наряду с активным воздействием на вредоносный агент сопровождается дополнительными обширными реактивными некрозами тканей и в связи с этим задержкой формирования клеточного и грануляционного барьеров, неполноценных в биологическом отношении. Вследствие этого в кровь и лимфу всасывается большое количество токсических продуктов тканевого распада, токсинов и микроорганизмов, что приводит к тяжелой интоксикации и даже генерализации инфекта. Это сопровождается сильной болью и отеками, развитием местного ацидоза. Сверхсильные раздражения, исходящие из такого очага воспаления, вызывают перераздражения нервных центров, что, ухудшая трофику и защитную роль воспаления, способствует развитию нервнодистрофических явлений, в результате чего усиливаются и прогрессируют дегенеративные и некротические процессы в неповрежденных тканях.
Снятие сильных раздражений, удаление мертвых тканей, обеспечение свободного стока для экссудата и подавление инфекта способствуют нормализации трофики, устранению нервнодистрофических явлений и нормализации воспаления.
Гипоэргическое воспаление характеризуется несоответственно слабой реакцией на вредоносное воздействие повреждающего агента. Такая воспалительная реакция может быть обусловлена истощением защитных сил огранизма предшествующими заболеваниями, физическим переутомлением, голоданием или слабым типом высшей нервной деятельности. Недостаточность и неполноценность воспалительной реакции способствует развитию прогрессирующей, нередко быстро генерализующейся тяжелой инфекции. Такой тип воспаления обычно наблюдается при анаэробной инфекции и совсем подавляется при ионизирующих радиационных поражениях. Учитывая защитительную недостаточность такого воспаления, следует нормализовать воспалительную реакцию путем повышения общей сопротивляемости организма и одновременно принимать меры к подавлению и ликвидации повреждающих агентов.
Фазы развития воспаления. Как уже отмечалось, воспаление характеризуется двухфазным течением. Каждой фазе присущи определенные местные био-физико-химические, морфологические и клинические изменения.
Первая фаза протекает на фоне гидратации и характеризуется разрушительными явлениями (альтерация), которые наиболее ярко выражены при остром инфекционном (гнойном, гнилостном) воспалении. Чем больше нарушена трофическая регуляция со стороны нервных центров, тем сильнее проявляются разрушительные нервнодистрофические процессы в зоне воспаления. Это сопровождается расстройством крово- и лимфообращения, снижением сосудистого тонуса, повышенной экссудацией, клеточковой инфильтрацией, фагоцитозом, гистолизом тканей и более или менее резко выраженными био-физико-химическими нарушениями. Все это при нормергически протекающем воспалении направлено на локализацию, нейтрализацию, подавление и ликвидацию инфекта, других вредоносных агентов, ферментативное расплавление нежизнеспособных тканей и формирование полноценного грануляционного барьера. При гиперергическом воспалении вышеописанные явления приобретают резко обостренный характер, неблагоприятно влияют на трофику пограничных здоровых тканей, вследствие чего в них ухудшается кровообращение, понижается активность фагоцитарной реакции, замедляется либо подавляется формирование клеточного барьера, что способствует генерализации инфекта и расширению зоны первичного некроза, вызванного травмирующим фактором.
При асептических формах воспаления первая фаза характеризуется менее выраженными расстройствами трофики, крово- и лимфообращения, наличием компенсированного ацидоза, умеренно выраженными ферментативными, гистолитическими процессами и преобладанием восстановительно-пролиферативных явлений над альтеративными (разрушительными). Этот вид воспаления в отличие от инфекционного довольно скоро переходит во вторую фазу.
Видовые особенности первой фазы воспаления. У лошадей и собак преобладает серозная, а при инфекционном воспалении серозно-гнойная экссудация с ярко выраженным протеолизом (расплавление мертвых тканей).
У крупного рогатого скота, овец и свиней чаще отмечается серозно-фибринозная, а при инфекционном воспалении — фибринозно-гнойная экссудация с пролиферацией и менее выраженным протеолизом мертвых тканей. Последние задерживаются в очаге гнойного воспаления более продолжительное время, так как у этих животных преобладают гнойно-демаркационные явления, способствующие секвестрации мертвых тканей, и менее выражены гнойно-ферментативные процессы. В результате этого мертвые ткани могут прорастать соединительной тканью и инкапсулироваться.
У грызунов и птиц резко преобладает фибринозная экссудация с превращением сгустков фибрина в фибрино-тканевую массу с последующим превращением ее в струп (при открытых повреждениях), который секвестрируется на фоне демаркационной воспалительной реакции и формирования в зоне секвестрации грануляционного барьера.
Описанные видовые особенности первой фазы воспалительной реакции необходимо учитывать при выборе лекарственных форм и проведении лечебных процедур при гнойных процессах.
Вторая фаза воспаления характеризуется регенеративными явлениями, протекающими на фоне дегидратации зоны воспаления. В данной фазе завершается барьеризация и наступает полное отграничение зоны повреждения либо инфекционного очага. Параллельно происходит
рассасывание или выведение из организма продуктов тканевого распада и инородных частиц, после чего полностью развертываются процессы регенерации. Все это протекает на фоне снижения клинических признаков воспаления, нормализации био-физико-химическнх и функциональных нарушений, возникающих в первой фазе воспаления.
Постепенно нормализуются трофика и обмен веществ, улучшается крово- и лимфообращение, уменьшается количество недоокисленных продуктов, снижается ацидоз, начинает преобладать макрофагальная реакция. В очаг воспаления пролиферируют в большом количестве гистиоцитарные клетки и соединительнотканные элементы, вследствие чего в зоне воспаления возникают более или менее выраженные пролифераты (см. ниже).
Стадии воспаления. Установлено, что каждая фаза воспаления включает взаимосвязанные и взаимообусловленные стадии. Деление единого воспалительного процесса на фазы и стадии до известной степени условно. Однако оно обосновано практической необходимостью, а также клиническими и патогенетическими особенностями, характерными для каждой из них, с учетом которых и должно проводиться лечение, так как больные обычно поступают на разных стадиях воспалительного процесса.
Первая фаза острого асептического воспаления включает две стадии: 1) воспалительного отека; 2) клеточной инфильтрации и фагоцитоза, последняя нередко бывает выражена слабо. При острогнойном воспалении к этим двум хорошо выраженным стадиям присоединяется третья — стадия барьеризации и абсцедирония.
Вторая фаза асептического воспаления также представлена двумя стадиями: 1) биологического очищения (рассасывания) и 2) регенерации и рубцевания. Вторая фаза острогнойного воспаления включает три стадии: созревшего абсцесса и две указанные выше. Перечисленные стадии наиболее ярко выражены при остро-гнойном воспалении. Ниже дается их описание.
2.5.3. Клиническое проявление асептического воспаления.
Серозное воспаление характеризуется экссудацией, слабо выраженными признаками альтерации, незначительным лейкоцитозом и преобладанием регенеративно-компенсаторных процессов. Оно возникает после нанесения умеренной механической травмы, обморожений, химической травмы и других причин. На фоне активной гиперемии, сопровождающейся замедленным током крови, расширением и повышением проницаемости капилляров, происходит выпот (экссудация) жидкой части крови в поврежденные ткани или анатомические полости. Накапливаясь в мягких тканях, серозный экссудат вызывает воспалительный тестоватый отек, а скапливаясь в анатомических полостях, способствует переполнению их. Надавливая попеременно пальцами обеих рук (бимануальное исследование) на такие переполненные серозным экссудатом полости, получают ощущение перемещения жидкости от пальцев одной руки к пальцам другой. Боль и местная температура при этой форме воспаления повышены незначительно, функция воспалительного органа нарушается умеренно; общая температура и другие физиологические показатели остаются почти неизмененными, за исключением незначительного учащения пульса и дыхания.
Покой и соответствующее лечение способствуют рассасыванию экссудата и восстановлению морфологических и функциональных нарушений. Повторные воздействия травмирующих факторов удлиняют воспалительный процесс или он переходит в хроническую форму.
Хроническое серозное воспаление характеризуется экссудативными и пролиферативными явлениями при слабой альтерации. Пролиферативные явления, развивающиеся при затянувшемся серозном воспалении, способствуют образованию соединительной ткани, которая в последующем превращается в рубцовую ткань. Это сопровождается сдавливанием кровеносных и лимфатических сосудов и нарушением оттока крови и лимфы, что приводит к застойным явлениям. Ткани отекают, а в анатомических полостях накапливается серозный экссудат, который по своему составу, приближаясь к транссудату, переполняет их, что дотаточно легко устанавливается осмотром и пальпацией. Вследствие отека и пролиферата уменьшается подвижность кожи в зоне воспаления, а в глублежащих тканях, например мышце, пальпацией определяется умеренное диффузное или узловатое утолщение. Болевая реакция при хроническом серозном воспалении выражена слабо или отсутствует; степень нарушения функции зависит от анатомических и физиологических особенностей вовлеченных в хронический процесс тканей и органов.
В связи с довольно стойким и нередко значительным разростом соединительной ткани в зоне воспаления не всегда можно достичь лечебными мерами полного морфологического и функционального восстановления поврежденного органа.
Серозно-фибринозное воспаление возникает при относительно интенсивном воздействии травмирующих факторов, вызывающих повышенную проницаемость сосудов и выход фибриногена, превращающегося в тканях и анатомических полостях в хлопья фибрина, которые в полостях при покое оседают на дно. Вследствие этого при пальпации верхней части соответствующей полости устанавливается флюктуация, а в нижней — тестоватость и умеренно выраженная крепитация. После активных или пассивных движений тестоватость и крепитация в суставах и сухожильных влагалищах исчезают, но возникает флюктуация. Предоставление покоя способствует восстановлению прежних признаков. Выпавшие хлопья фибрина медленно рассасываются или организуются, превращаясь в коллагеновые частицы.
Клинические признаки при остром серозно-фибринозном воспалении выражены сильнее, чем при серозном воспалении.
Предоставление покоя и своевременное лечение обычно способствуют выздоровлению. В запущенных случаях процесс переходит в хроническую форму.
Хроническое серозно-фибринозное воспаление по клиническим признакам и патогенетическим изменениям мало отличается от хронического серозного воспаления. Из особенностей следует отметить более интенсивное узловатое склеротическое уплотнение мягких тканей и наличие в полостях организовавшегося фибрина, превращенного в плотные коллагеновые частицы (рисовые зерна), которые иногда подвергаются кальцификации и остаются на всю жизнь в полостях суставов. Попадая между хрящами суставных поверхностей, они вызывают сильную боль и повреждение суставных хрящей, что проявляется перемежающейся хромотой и приводит к обострению воспалительной реакции, принимающей затяжной характер.
Фибринозное воспаление возникает в результате механических, чаще химических, термических и даже инфекционных поражений слизистых оболочек, капсул суставов, стенок сухожильных влагалищ, бурз, а также серозных покровов. В зависимости от причинного фактора оно может быть асептическим и инфекционным. В последнем случае все изменения протекают тяжелее.
Характерной особенностью фибринозного воспаления является высокая проницаемость капилляров, поэтому экссудат содержит значительно большее количество форменных элементов крови, чем при описанных выше формах воспаления, кроме того, в нем много мелко- и крупномолекулярных белков и фибриногена.
Сущность патогенетических изменений, возникающих при этом воспалении, сводится к следующему. Под воздействием тромбокиназы и других ферментов фибриноген, вышедший в ткани в полости, превращается в хлопья и фибринозную сеть. Она густо покрывает поверхность оболочек, а также в большом количестве накапливается в тканях, особенно вблизи капилляров и мелких сосудов. Вскоре вокруг них образуется плотная фибринозная муфта, которая охватывает капилляры и мелкие сосуды и как бы замуровывает их. Это затрудняет выход жидкой части крови из сосудов. Одновременно с этим фибрин, накапливаясь в большом количестве на стенках анатомических полостей и слизистых оболочек, может образовывать пленки, что препятствует нормальному выделению ими в полости соответствующих жидкостей. Таким образом, вскоре после начала фибринозного воспаления в суставах, сухожильных влагалищах, плевральной и брюшной полостях количество обычного жидкого их содержимого и серозного экссудата начинает уменьшаться. Именно поэтому, заболевание, сопровождающееся фибринозным воспалением, нередко называют сухой плеврит, сухой артрит и т.п. Фибринозная сеть и пленки, покрывающие стенки полостей, подвергаются затем организации и превращаются в соединительнотканные тяжи, нити, «ворсинки», «шнуры». В результате такого процесса плевра и брюшина, например, прочно срастаются с внутренними органами, синовиальная оболочка суставов — с суставными концами костей, а сухожильные влагалища — с сухожилиями.
Клинические признаки фибринозного воспаления выражены хорошо. Местная температура и болевая реакция повышены, наблюдается значительное нарушение функции пораженного органа, например при фибринозном синовите сустава отмечается значительная хромота даже при движении шагом. В отличие от серозного и серозно-фибринозного воспалений припухлость при нем проявляется слабо, изменений контуров суставов и сухожильных влагалищ не наблюдается, активные и пассивные движения сопровождаются хорошо выраженной крепитацией (хрустом) в воспаленных суставах и сухожильных влагалищах; крепитация и шумы трения наблюдаются при плевритах.
При инфекционном фибринозном воспалении к изложенным клиническим признакам присоединяются высокая общая температура, иногда гнойный экссудат (фибринозно-гнойное воспаление) или образование дифтеритических пленок, покрывающих слизистые и конъюнктиву.
Исходя из сказанного, при остром асептическом фибринозном воспалении необходимо предупреждать организацию фибрина и способствовать его рассасыванию, усиливая фибринолитические процессы. С этой целью после стихания острых воспалительных явлений наряду с лечебными процедурами (инъекции в полости гепарина, протеолитических ферментов) рекомендуется применять вначале пассивные, а затем активные движения. При инфекционном фибринозном воспалении необходимо специфическое противомикробное лечение.
Хроническое фибринозное воспаление характеризуется образованием спаек между брюшиной, плеврой и органами, заключенными в брюшной и грудной полостях; при поражении суставов и сухожильных влагалищ возникает тугоподвижность, заканчивающаяся внутрисуставным анкилозом или тендогенной контрактурой (см. ниже). Предсказание при такого рода изменениях в пораженных суставах и сухожильных влагалищах сомнительное или неблагоприятное в смысле восстановления функции.
Принципы лечения при воспалительных процессах сводятся к устранению причин, вызвавших повреждение, к нормализации воспалительной реакции или снятию ее. Для этого необходимо: 1) исключить влияние на организм этиологического фактора; 2) обеспечить покой поврежденному органу и предупредить перераздражение нервной системы или снять уже возникшее перераздражение; 3) создать больному животному наиболее благоприятные условия ухода и содержания и 4) обеспечить его сбалансированным диетическим рационом, насыщенным комплексом витаминов.
Управление и нормализация воспалительного процесса и его снятие могут быть достигнуты сочетанием местного и общего воздействия на организм больного животного средствами и методами этиологической и патогенетической терапии. Лучшие результаты достигаются при сочетанном их применении.
Этиологическая терапия направлена на снижение или полное устранение травмирующих, в том числе микробных, факторов путем воздействия на них физическими, химическими и биологическими средствами и методами. Однако этот вид терапии не во всех случаях позволяет вывести организм из патологического состояния и обеспечить выздоровление. В таких случаях его следует осуществлять на фоне патогенетической терапии (см. хирургическую инфекцию).
Патогенетическая терапия предусматривает нормализацию нарушенных функций организма, стимуляцию механизмов защиты, адаптации и регенерации. Это прежде всего достигается новокаиновыми блокадами, которые ослабляют сильные и сверхсильные раздражения нервных центров и вегетативной нервной системы. Вследствие этого уравновешиваются возбудительные и тормозные процессы коры головного мозга; улучшается ее координирующее и интегрирующее влияние на подкорковые центры и железы внутренней секреции; улучшаются и нормализуются адаптационные реакции, трофическое влияние нервных центров на периферию, кровообращение; активируются физиологическая система соединительной ткани, иммуногенез, фагоцитоз, компенсаторные процессы; в очаге воспаления снижается интенсивность разрушительных процессов и возрастают регенеративно-восстановительные явления, нормализуются жизненно важные функции организма.
В патогенезе болезни начинают преобладать регенеративно-восстановительные процессы, подавляться патогенные факторы и наступает выздоровление животного.
Принципы лечения при остром и хроническом асептическом воспалении сводятся: к устранению травмирующего фактора; прекращению крово- и лимфоизлияний, излишней экссудации в ткани и анатомические полости; предоставлению покоя поврежденному органу или части тела; применению средств и способов, обеспечивающих рассасывание крово- и лимфоизлияний, мертвых клеток и экссудата, а также средств, улучшающих регенерацию и восстановление нарушенных функций.
При остром воспалении периодически в течение первых 12—24 ч после травмирования применяют местную гипотермию в сочетании с умеренно давящей повязкой (охлаждающе-вяжущие примочки, орошение хлорэтилом и другие средства гипотермии). Это предупреждает обильный выход крови, экссудата в ткани, способствует уменьшению боли и нормализации воспалительной реакции. Вместо гипотермии в первые часы после нанесения травмы и в последующее время целесообразна короткая новокаиновая блокада с гидрокортизоном, которые можно вводить в ткани с помощью ионофореза.
Со вторых суток следует применять тепловые процедуры. (спиртовысыхающие повязки, согревающие компрессы, лампа Минина, красный свет). На третий-четвертый день, когда уменьшится болевая реакция, тепловые процедуры (аппликации парафина, озокерита и пр.) желательно сочетать с массажами, выполняемыми по ходу лимфатических сосудов, от периферии к центру. Тепловые процедуры и массаж улучшают кровообращение и способствуют рассасыванию кровоизлияний, экссудата и продуктов ферментативного лизирования поврежденных тканей.
При подостром и хроническом асептическом воспалении лечебные мероприятия должны быть направлены на снижение фибрино-пластических и пролиферативных явлений, склерозирования тканей и предупреждение обширного рубцевания. Это достигается путем применения средств и способов, обостряющих воспаление, улучшающих крово- и лимфообращение, способствующих протеолизу, рассасыванию пролиферата и разрыхлению рубцовой соединительной ткани. С этой целью применяют: массажи, втирания острых резорбирующих мазей, линиментов в сочетании с тепловыми процедурами (лампа соллюкс, парафиновые и озокеритовые аппликации), подсадки консервированных семенников, хрусталиков, рубцовой и селезеночной тканей; заслуживают применения подкожные инъекции пирогенала, скипидара пополам с персиковым или прованским маслом, метила салицилата и других раздражающих средств. Хорошие результаты дает правильно осуществленное точечное или полосчатое прижигание в сочетании с последующим втиранием в зону прижигания лошадям красной ртутной мази, рогатому скоту мази двухромовокислого калия с наложением теплого укутывания. Более эффективно ультразвуковое воздействие на зону пролиферата или рубца, особенно в сочетании с фонофорезом (М. В. Плахотин, М. С. Борисов).
Принципы лечения при острогнойном воспалении должны осуществляться с учетом стадии развития его и сводиться к нормализации воспалительной реакции средствами этиологической и патогенетической терапии; локализации и подавлению инфекционного начала; формированию полноценного клеточного и грануляционного барьеров; предупреждению обширных некрозов и нагноений; нейтрализации и выведению из организма продуктов тканевого распада и токсинов микробов; своевременному и возможно полному выведению экссудата из гнойно-некротического очага во внешнюю среду; созданию благоприятных условий для регенерации и предупреждению формирования обширных рубцов в зоне бывшего гнойно-некротического очага (подробно см. лечение абсцессов, флегмон, сепсиса).
Патогенетическая терапия — комплекс методов и средств воздействия через нейроэндокринную систему в целях нормализации нарушенных функций и направленного управления адаптационными реакциями, механизмами защиты и регенеративно-восстановительными процессами организма. Замена сильных раздражителей, воздействующих на макроорганизм слабыми либо противоположно действующими раздражителями, является основой патогенетической терапии. Она включает прежде всего новокаиновые блокады, внутрисосудистые введения растворов новокаина; применение нейролептиков, гормонов, рефлексотераиии (иглоукалывание, прижигание, электро- и лазеропунктура); медикаментозный сон; тканевую терапию; физиотерапевтические процедуры (массаж, гипо- и гипертермию, световые и электропроцедуры, токи Бернара, магнитное поле, ультразвук, другие физические факторы); пирогенотерапию, эндокринотерапию и прочие неспецифические средства воздействия на больной организм.
Таким образом, в основе патогенетической терапии лежит антипатогенетический эффект, возникающий в результате воздействия на высокоорганизованный организм слабыми физическими, химическими или биологическими факторами в сочетании с полноценным сбалансированным рационом, соответствующим содержанием и физиологически допустимой эксплуатацией животных.
Отеки.
Непосредственно после механических и термических воздействий в организме возникают более или менее значительные повреждения тканей, капилляров, рецепторного аппарата, нервных, артериальных, венозных и лимфатических стволов, на этом фоне проявляется травматический отек. Затем к нему присоединяется воспалительный отек, а по мере развития первой фазы воспалительной реакции формируются клеточковые инфильтраты, отличающиеся друг от друга по клеточному составу и клиническим признакам. Во второй фазе воспаления клинически выявляются пролифераты. Каждый из перечисленных клинических признаков воспалительной реакции имеет важное диагностическое и прогностическое значение.
Травматический отек — транссудативное пропитывание тканей с последующим набуханием коллоидов преимущественно поврежденных тканей, в которых вначале возрастает проницаемость резко расширенных капилляров, гидрофильность коллоидов и гидролиз мертвых тканей под влиянием выхода в ткани и активации внутриклеточных гидролитических ферментов. Это способствует повышению онкотического и осмотического давления, обильному выходу жидкой части крови в ткани, которая сдавливает всю капиллярную сеть, и развитию ишемии. На ее фоне развивается травматический отек, который начинает выявляться клинически через 10—15минпосле травмирования и может достигать значительных размеров. У лошадей и собак травматический отек формируется быстрее и более заметен, чем у рогатого скота. При этом он оказывается сильнее выражен в тех местах, где больше рыхлой клетчатки. Чем сильнее повреждены ткани, тем значительнее отек. По мере его развития он распространяется и на неповрежденные ткани.
По своему составу отечная жидкость напоминает транссудат. Она не свертывается, обладает щелочной реакцией, содержит не более 3% белка, при соотношении альбуминов к глобулинам 2,5 : 2 плотность ее колеблется от 1,007 до 1,013.
Клинические признаки. Травматический отек характеризуется разлитой тестоватой припухлостью, переходящей без резких границ в здоровые участки. При давлении пальцем в нем легко образуется ямка, которая затем выравнивается в течение 2—3 мин. Температура кожи в зоне отека несколько ниже температуры соседних здоровых участков, общая температура не повышена или увеличена незначительно. Кожа непигментированных участков бледно-синюшного оттенка. При внедрении в зону отека инфекта, как правило, возникает местный гнойный процесс.
Лечение. Зону травматического отека смазывают 5%-ным спиртовым раствором йода, целесообразно сделать короткую новокаиновую блокаду с гидрокортизоном и антибиотиком и наложить умеренно давящую охлаждающую антисептическую повязку с буровской жидкостью или 2%-ной свинцовой водой. Этими жидкостями орошают повязку через каждые 11/2—2 ч в течение первых 12—24 ч. Затем применяют тепловые процедуры: согревающие компрессы, лучше спиртовые; парафиновые, озокеритовые аппликации; мешки с горячим песком и др. В дальнейшем, при отсутствии признаков инфекции, применяют массаж с резорбирующими мазями и линиментами.
Невропатический отек чаще возникает в результате паралича конечностей, иногда после проведенной невректомии. По клинической картине он, будучи сходен с травматическим отеком, носит стойкий характер. По мере восстановления нервной проводимости отек постепенно рассасывается. Лечение его сводится к восстановлению нарушенной нервной проводимости (см. лечение параличей и парезов нервов).
Холодный, или застойный, отек является следствием затрудненного оттока крови и лимфы, чаще всего при сердечно-сосудистой недостаточности, заболеваниях почек, во второй половине беременности, недостаточном моционе, нарушении белково-минерального обмена, сдавливании вен и лимфатических путей рубцовой тканью, тромбофлебитах яремной и других крупных вен. Застойные отеки тестоватые, холодные и безболезненные. Чаще они наблюдаются в дистальных частях конечностей, в области подгрудка, живота и половых органов. Необходимо иметь в виду, что при хроническом течении застойных и других отеков развиваются пролифераты с последующей гиперплазией соединительнотканных элементов и превращением рыхлой соединительной ткани в рубцовую, что может привести к слоновости (см. ниже).
Воспалительный отек — экссудативно-серозное пропитывание тканей, развивающееся на фоне активной гиперемии и характеризующееся преобладанием набухания эластических, коллагеновых волокон и клеток поврежденных тканей. Воспалительныйотек, как правило, наслаивается на травматический. Различают асептические и инфекционные воспалительные отеки. При первых экссудат преимущественно серозный, прозрачный, желтоватого цвета, кислой реакции, содержит от 3 до 6% белков, до 3% альбуминов, иногда содержит небольшое количество лейкоцитов и отдельные эритроциты, хлопья фибрина; плотность его более 1,018 (в среднем 1,022); при хроническом отеке преобладают лимфоциты. В экссудате инфекционных отеков, кроме лейкоцитов и эритроцитов, обнаруживаются микробы. Асептические воспалительные отеки чаще бывают ограниченными, а инфекционные — диффузными.
Клинические признаки. При асептических отеках отмечается болезненность, более или менее тестоватая припухлость, повышена местная, а при инфекционных и общая температура. Припухлость инфекционных отеков резко болезненная, горячая, более напряженная, ямка от давления образуется при большем усилии и медленнее выравнивается в сравнении с асептическим воспалительным и тем более травматическим отеками.
Лечение. См. лечение при воспалительных процессах.
Коллатеральные отеки развиваются вблизи инфекционного очага, локализованного в плотных тканях или глубоких слоях той или иной части тела. Напряжение тканей при коллатеральных отеках выражено умеренно, местная температура в норме или незначительно повышена, зато всегда высокая температура тела. При пальпации они умеренно болезненные, боль усиливается при «глубокой» пальпации вследствие передачи давления на инфекционный очаг. В экссудате таких отеков микробы обычно отсутствуют.
Опускающиеся отеки чаще локализуются на конечностях, реже в других частях тела. От коллатеральных отеков они отличаются малой болезненностью, большей тестоватостью и распространением книзу от основного, нередко инфекционного очага.
Инфильтраты. Воспалительные инфильтраты—скопление клеток вазогенного и гистиоцитарного происхождения на фоне воспалительного отека, в зоне локализации микро- и макроорганизмов и инородных тел, а также после воздействия химическими веществами. Различают: сегментоядерный, лимфоцитарный, эозинофильный и гистиоцитарный инфильтраты. Все они характеризуются уплотнением центральной зоны воспалительного отека. Большинство из них при надавливании болезненны; ямка от давления на месте инфильтрата образуется при большем усилии, чем при отеке, и выравнивается медленнее, так как при надавливании вытесняются не только экссудат, но и клетки инфильтрата, которые затем медленно перемещаются в прежнее положение.
Сегментоядерный инфильтрат возникает при наличии мертвых тканей, развитии гноеродной инфекции и внедрении инородных тел. Он связан с активной борьбой организма с инфектом, процессом секвестрации мертвых тканей и внедрением в ткани инородных предметов. Сегментоядерный инфильтрат характеризует вторую стадию острого гнойного воспаления. Представлен этот инфильтрат преимущественно сегментоядерньми нейтрофилами. Формируется он довольно быстро и сопровождается сильной болью, повышенной местной и общей температурой тела. На месте возникшего инфильтрата затем могут сформироваться: остиофолликулит, фурункул, абсцесс или флегмона. При подавлении инфекта, удалении мертвых тканей, инородного тела и других раздражителей инфильтрат рассасывается.
Лимфоцитарный инфильтрат представлен мелкими клетками лимфоидного типа. Этот инфильтрат в сочетании с сегментоядерным инфильтратом встречается у рогатого скота и свиней при остром, подостром и хроническом воспалениях; у лошадей и собак — только при хронических воспалительных процессах. Болезненность, местная и общая температура тела при нем менее выражены, а уплотнение сильнее, чем при сегментоядерном инфильтрате.
Эозинофильный инфильтрат наблюдается при внедрении в ткани макропаразитов и при аллергическом состоянии организма. При наличии в тканях макропаразитов инфильтрат состоит преимущественно из эозинофилов. При пальпации зона инфильтрата плотная и малоболезненная. В случаях гиперэргической воспалительной реакции эозинофильный инфильтрат сочетается с сегментоядерным. Такой инфильтрат по клиническим признакам сходен с сегментоядерным инфильтратом.
Гистиоцитарный инфильтрат отмечается в стадии регенерации раневого или острогнойного инфекционного процесса, а также при рассасывании инородных предметов, попавших в ткани (шовный, аллопластический, синтетический и другие материалы). Он представлен большим количеством гистиоцитов, макрофагов и полибластов гистиоцитарного и в меньшей степени вазогенного происхождения. Данный вид инфильтрата определяется лабораторно при микроскопии отпечатков, полученных из ран или очистившегося гранулирующего гнойно-некротического очага (см. ниже).
Лечение при инфильтратах должно быть направлено на устранение причин, способствующих их развитию. Целесообразно применение спиртовысыхающих повязок, тепловых процедур, новокаин-антибиотиковых блокад, внутривенных введений 0,25%-ного раствора новокаина и др. (см. ниже). Недопустимо применять массажи при лейкоцитарном инфильтрате, так как это может способствовать генерализации инфекции.
Воспалительный пролиферат—скопление в основной ткани большого количества фибробластических клеточных элементов физиологической системы соединительной ткани (лимфоцитов, гистиоцитов, фибробластов) с последующим продуцированном соединительной ткани. Развитию воспалительного пролиферата способствуют: длительное воздействие на ткани механических и других воздействий (давление, трение, растяжение и пр.); наличие в тканях инородных предметов (куски дерева, металлические и другие предметы, погружные, особенно капроновые, швы); хроническое течение гнойной и грибковой инфекции (ботриомикоз, актиномикоз); длительно протекающие некрозы и нагноения, внедрение в ткани некоторых гельминтов (онхоцерки); нарушение лимфо- и кровообращения и ряд других причин, поддерживающих хроническое течение воспаления.
Воспалительный пролиферат обычно развивается на фоне отека. Вначале между клетками основной ткани накапливаются (пролиферируют) фибробластические элементы физиологической системы соединительной ткани, которые затем продуцируют соединительнотканные волокна, пронизывающие основную ткань. В дальнейшем на месте пролиферата формируется рубцовая ткань. Пролиферативные явления наиболее выражены у рогатого скота и свиней.
Клинически пролифераты характеризуются ограниченной плотной припухлостью. При надавливании на нее ощущается упругое сопротивление ткани, ямка от давления не образуется; болевая реакция и местная температура, как правило, в пределах нормы, кожа над зоной пролиферата почти неподвижна вследствие рубцового перерождения подкожной клетчатки. Обширные пролифераты задерживают регенерацию и эпидермизацию ран; в области суставов, мышц и сухожилий пролифераты нарушают свободу движения; в паренхиматозных и железистых органах они значительно снижают или полностью выключают их функцию. Пролифераты трудно поддаются обратному развитию и рассасыванию, особенно в случаях развития рубцовой ткани.
Лечение должно сводиться к применению резорбирующих мазей, тепловых процедур в виде парафиновых аппликаций, прижигании, тканевой, пирогено- или ультразвуковой терапии (см. ниже).
Дата добавления: 2018-02-15; просмотров: 2711; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
