И чреспищеводной эхокардиографии 7 страница
105
обе стороны от изолинии. На слух
образуется громкий, «щелкающий»
звуковой сигнал.
Материальные эмболы, акустиче-
ское сопротивление которых близ-
ко к сопротивлению частиц крови,
представлены на СДСЧ в виде сиг-
налов меньшей интенсивности, чем
воздушные эмболы, но большей —
по сравнению с общим фоном
спектра. Сигналы от материальных
эмболов расположены по одну сто-
рону от изолинии, соответственно
регистрируемому потоку крови.
Появление эмболов сочетается с
мягким звуковым сигналом щелка-
ющего характера на слух. Таким об-
разом, качественный анализ спект-
ра допплеровского сдвига частот
позволяет диагностировать наличие
эмболических сигналов на спектре
допплеровского сдвига частот в ис-
следуемом сосуде, высказать пред-
положение о характере эмболиче-
ских частиц. Однако на сегодняш-
ний день в клинической практике
не представляется возможным диа-
гностировать точный состав и раз-
мер регистрируемых эмболов.
В настоящее время в клиниче-
ской практике применяют ультра-
звуковые системы, оснащенные
программным обеспечением авто-
матической регистрации эмболов.
Идентификацию микроэмболиче-
ских сигналов осуществляют мето-
дом автоматической детекции сиг-
налов специальным программным
обеспечением, методом визуально-
го определения по цветовой шкале
градаций и в соответствии с крите-
риями, определенными Spencer и
уточненными согласительным ко-
митетом 9-го Международного сим-
позиума по церебральной гемоди-
намике и межцентровыми соглаше-
ниями (1995).
|
|
|
Для отличия высокоинтенсивных
сигналов от прочих артефактов
было взято за основу, что они име-
ют длительность менее 150 мс в си-
столу и менее 300 мс в диастолу и
энергию, по меньшей мере на 6 дБ
выше фонового спектра скорости
крови, являются однонаправленны-
ми, расположенными внутри огиба-
ющей спектра допплеровского
сдвига частот, в сочетании со зву-
ковым сигналом, описываемым в
литературе как «щелчок». За период
мониторирования подсчитывают
количество микроэмболических
сигналов, измеряют их длитель-
ность, максимальную и среднюю
интенсивность, а также скорость.
2.2.4.5. Методика исследования
глубоких вен мозга и синусов
твердой мозговой оболочки
Исследование глубокой венозной
системы проводят через транстем-
поральное ультразвуковое окно, ис-
пользуя аксиальный срез через про-
межуточный мозг. Этот скан позво-
ляет визуализировать дорсальные
части таламуса и затылочные доли
конечного мозга. Параллельно
средней мозговой артерии распола-
гается глубокая средняя мозговая
вена. Прямой синус представляет
собой окрашенную в синий цвет
точечную структуру, расположен-
ную в дорсальной части серединной
линии, в ряде случаев возможно
визуализировать впадение его в си-
нусный сток. Синусный сток опре-
деляется каудальнее прямого сину-
са и проецируется несколько асим-
метрично на контралатеральную за-
тылочную кость. Кпереди от пря-
мого синуса, в среднедорсальной
части промежуточного мозга, опре-
деляется окрашенная синим цветом
тубулярная структура — большая
вена мозга, или вена Галлена, в ко-
торую впадают внутренние вены
мозга и базальные вены.
|
|
|
Через затылочное ультразвуковое
окно, располагающееся над транс-
форменным окном, используя сере-
динный сагиттальный сканирую-
щий план, визуализируют прямой
синус; также возможно получение
изображения верхнего и нижнего
сагиттальных синусов. В норме
106
спектр допплеровского сдвига час-
тот в венах мозга имеет слабовыра-
женную фазность.
При обследовании здоровых лиц
в возрасте от 25 до 35 лет, согласно
нашим данным, частота визуализа-
ции внутренних вен мозга состави-
ла 100 %, большая вена мозга диа-
гностирована в 71 % наблюдений,
глубокая средняя мозговая вена — в
85,7 %, прямой синус — в 57 %, си-
нусный сток — в 42,8 % случаев.
Количественная оценка кровотока
представлена в табл. 2.10.
Таблица 2.10. Показатели скорости
кровотока по глубоким венам мозга и
синусам в норме
|
|
|

В норме показатели кровотока,
зарегистрированные по данным
ТКД в горизонтальном положении
пациента, отличаются от показате-
лей, полученных при выполнении
ортостатических [изменение поло-
жения тела от ортоположения
(+75°)] и антиортостатических
(—45°) нагрузок. В горизонтальном
положении ЛСК в прямом синусе
(локация через затылочное окно)
находится в диапазоне от 14 до
30 см/с, в ортоположении снижает-
ся — от 13 до 25 см/с, а в антиорто-
положении — увеличивается от 19
до 41 см/с [Шахнович В.А., Галуш-
кина А.А., 1998]. Кроме абсолют-
ных значений скорости кровотока,
авторы предлагают использовать
орто- и антиортостатические ин-
дексы, которые рассчитываются
как процент изменения кровотока
при нагрузке по отношению к го-
ризонтальному положению пациен-
та. В группе здоровых лиц ортоста-
тический индекс составляет 18,8 %
(от 7 до 33 %), антиортостатиче-
ский - 24,9 % (от 11 до 33 %).
2.2.5. Ранние атеросклеретические
изменения в магистральных
артериях
Для диагностики ранних атероскле-
ротических поражений P.Pignoli и
др. впервые в 1986 г. предприняли
попытку количественного изучения
величины комплекса интима — ме-
диа (ВКИМ) в сонных артериях с
помощью ультразвукового исследо-
вания в В-режиме.
|
|
|
ВКИМ в дистальном отделе об-
щей сонной артерии более 1 мм
и/или в бульбусе сонной артерии
более 1,1 мм свидетельствует о на-
личии ранних атеросклеротических
изменений.
Связь между факторами риска
развития атеросклероза и ВКИМ
сонных артерий была убедительно
доказана многими эксперименталь-
ными и клиническими исследова-
ниями. Согласно результатам на-
ших работ, при обследовании лиц
мужского пола в возрасте от 40 до
59 лет с наличием таких факторов
риска развития атеросклероза, как
курение, артериальная гипертензия
в сочетании с начальными проявле-
ниями недостаточности мозгового
кровообращения, выявлены ранние
атеросклеротические изменения в
дистальном участке общих сонных
артерий. Средние значения величи-
ны комплекса интима — медиа со-
ставили 1,26+0,05 мм.
Сопоставление данных липидно-
го состава крови и результатов ис-
следования в В-режиме ОСА у 90
лиц с факторами риска развития
атеросклероза показало, что при
107
ВКИМ 1,1 — 1,2 мм гиперхолестери-
немия и гипертриглицеридемия
встречаются в 20 % наблюдений,
при КИМ 1,3—1,4 или 1,5 мм и бо-
лее высокий уровень липидов кро-
ви отмечался в 45,5 и 61,5 % на-
блюдений соответственно [Шути-
хина И.В., 1998].
Средние различия между ВКИМ
сонной артерии у лиц с наличием и
отсутствием отдельных факторов
риска развития атеросклероза, вы-
явленные C.Bonithon-Kopp (1996),
представлены в табл. 2.11.
Таблица 2.11. Средние различия меж-
ду ВКИМ сонной артерии у лиц с нали-
чием и отсутствием факторов риска
развития атеросклероза

Результаты наших исследований
ВКИМ у 95 больных с клиниче-
ским проявлением ИБС и отсутст-
вием окклюзирующих поражений в
магистральных артериях шеи и
нижних конечностей показали, что
ранние атеросклеротические изме-
нения только в общих сонных арте-
риях выявлены в 16 % наблюдений,
только в общей бедренной арте-
рии — в 23 % случаев, сочетанные
поражения ОСА+ОБА — у 43 % бо-
льных, и все это на фоне отсутст-
вия клинических проявлений ише-
мии нижних конечностей и нали-
чия дисциркуляторной энцефало-
патии у 11 % больных и ишемиче-
ского инсульта в 20 % наблюдений
[Кунцевич Г.И. и др., 2000]. При
этом по мере нарастания тяжести
клинических проявлений ИБС про-
грессировал ранний атеросклерети-
ческий процесс в общих сонных и
бедренных артериях. Так, у боль-
ных I ФК стенокардии средняя ве-
личина комплекса интима — медиа
в ОСА составляла 1,15+0,05 мм, в
ОБА - 1,19+0,05 мм. У лиц, пе-
ренесших инфаркт миокарда, —
1,25+0,05 и 1,44+0,05 мм соответст-
венно.
Основными признаками пораже-
ния коронарных артерий у больных
с приобретенными пороками серд-
ца следует считать изменение сосу-
дистой стенки при величине инти-
ма — медиа более 2,5 мм в общей
сонной и бедренной артериях и на-
личии мультифокальных пораже-
ний по данным дуплексного скани-
рования [Агаджанова Л.П. и др.,
1998]. Начаты исследования эласти-
котонических свойств артериаль-
ной стенки сонных и бедренных ар-
терий с использованием показателя
модуля Юнга. Модуль Юнга опре-
деляется как отношение стресса к
растяжению и рассчитывается по
формуле:

где R — радиус артерии; WT — ве-
личина комплекса интима — ме-
диа; РР — пульсаторное давление;
CAS — изменение диаметра арте-
рии за один сердечный цикл.
В норме величина модуля Юнга
составляет в ОСА 535+22 н/м2, в
ОБА — 682+20 н/м2. Природа более
высоких значений модуля Юнга в
бедренной артерии объясняется
биохимическими свойствами ее со-
судистой стенки, а именно преоб-
ладанием в ней коллагеновых воло-
кон и, следовательно, увеличением
упругости.
Согласно нашим данным, при
обследовании 95 больных ИБС при
отсутствии окклюзирующих пора-
жений в магистральных артериях
шеи и нижних конечностей по мере
нарастания клинических проявле-
ний ИБС регистрируется увеличе-
ние модуля Юнга в общей сонной и
бедренной артериях, где он дости-
гает значений 780+25 и 870+21 н/м2
108
соответственно [Кунцевич Г.И. и
др., 2000].
Следует подчеркнуть, что модуль
Юнга является более информатив-
ным показателем в диагностике ате-
росклеротического процесса на ран-
них этапах, чем ВКИМ. Так, при
нормальных значениях ВКИМ уве-
личение модуля Юнга выявлено в
ОСА в 23 % наблюдений, в ОБА — в
16 %, сочетанные изменения — в
20 % случаев. Чувствительность уль-
тразвукового исследования в В-ре-
жиме в диагностике атеросклерети-
ческого процесса на ранних этапах с
использованием модуля Юнга со-
ставляет 98 %, специфичность —
88% [Жукова Е.А., 2001].
По данным Э.Ч.Шанцило (2000),
для здоровых лиц характерны низ-
кие значения коэффициента упру-
гости, умеренные его изменения
при проведении проб со статиче-
ской и физической нагрузкой и ни-
федипином. У больных атероскле-
розом отмечаются высокие значе-
ния коэффициента упругости в по-
кое, значительное его возрастание
при пробе со статической нагруз-
кой и практически отсутствие реак-
ции на прием нифедипина. Коэф-
фициент упругости артерий боль-
ных гипертонической болезнью,
повышенный в покое, резко возра-
стает при пробе со статической на-
грузкой и резко снижается при про-
бе с нифедипином.
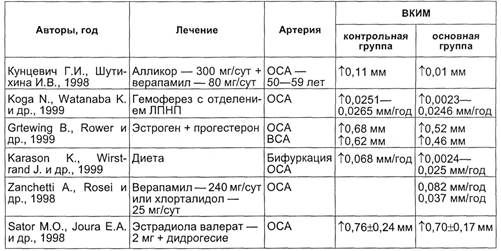
Метод УЗ-сканирования исполь-
зуется для оценки терапии, прово-
димой у лиц с ранними атероскле-
ротическими изменениями сонных
артерий (табл. 2.12).
Для оценки функционального
состояния эндотелия используют
тесты с анализом изменения плече-
вой артерии под влиянием эндоте-
лийзависимых и эндотелийнезави-
симых стимулов. В В-режиме фик-
сируют изменения в диаметре пле-
чевой артерии и линейной скорости
кровотока в ней в ответ на увеличи-
вающийся поток крови при прове-
дении пробы с реактивной гипере-
мией (эндотелийзависимая реак-
ция) и в ответ на сублингваль-
ный прием 500 мкг нитроглицерина
(эндотелийнезависимая реакция).
Промежуток времени между проба-
ми с реактивной гиперемией и при-
емом нитроглицерина составляет
10 мин. В ходе исследования диа-
метр плечевой артерии измеряют
|
|
| 109 |
Таблица 2.12. Оценка эффективности лечения ранних атеросклеротических из-
менений в сонных артериях по данным исследования в В-режиме
10 раз: в покое, через 4,5 мин после
наложения манжеты на область
плеча при пробе с реактивной гипе-
ремией, через 30 и 60 с после сня-
тия манжеты (декомпрессия), снова
в покое и через 1, 2, 3, 4, 5 мин по-
сле приема нитроглицерина. Ско-
рость кровотока оценивают в покое
и сразу после снятия манжеты. Из-
мерение диаметра плечевой арте-
рии проводят линейным методом,
предложенным D.S.Celermajer и со-
авт. (1992), который заключается в
непосредственном измерении диа-
метра артерии с использованием
двух точек: одной — на границе ад-
вентиция — медиа передней стенки
артерии, другой — на границе ме-
диа — адвентиция задней стенки
[Балахонова Т.В. и др., 1998].
Выявлено улучшение эндотелий-
зависимой реакции у больных ИБС
в ответ на пробу с реактивной гипе-
ремией на фоне приема L-аргинина
от 5 % перед началом лечения до
7,8 % после него. Потокзависимая
дилатация плечевой артерии у па-
циентов с распространенным ате-
росклерозом увеличивалась после
2 мес приема флувастатина с 4,7 до
7 % при значимом снижении уров-
ня общего холестерина и холесте-
рина ЛПНП в сыворотке крови
[Балахонова Т.В. и др., 1999].
Оценивая возможности метода
УЗ-исследования в В-режиме в диа-
гностике ранних атеросклеротиче-
ских поражений магистральных ар-
терий, следует подчеркнуть, что в
клинической практике целесооб-
разно использовать этот неинвазив-
ный и информативный способ диа-
гностики ранних морфологических
изменений магистральных артерий
у лиц с факторами риска развития
атеросклероза.
2.2.6. Окклюзионные поражения
внутренних сонных артерий
Дуплексное сканирование сонных
артерий обеспечивает получение
точной диагностической информа-
ции о состоянии стенки и просвета
сосуда, что позволяет применить
данную методику для оценки:
• локализации и степени пораже-
ния артерий;
• структуры атеросклеротической
бляшки.
Исследование больных с окклю-
зионными поражениями внутрен-
них сонных артерий целесообразно
начинать с исследования общих
сонных артерий с учетом количест-
венных показателей величины ком-
плекса интима — медиа в дисталь-
ном отделе общих сонных артерий
и определения локализации и сте-
пени стенозирующих поражений.
Согласно нашим данным, у паци-
ентов со стенозом ВСА менее 60 %
значения величины комплекса ин-
тима — медиа находились в диапа-
зоне 0,9—1,6 мм (среднее значение
1,1+0,2 мм); при стенозе более
60 % — 1,0—1,8 мм (среднее значе-
ние 1,3±0,2 мм).
2.2.6.1. УЗ-критерии диагностики
степени окклюзионных поражений
Степень поражения артерий оцени-
вают на основании суммарных дан-
ных, получаемых при расчете про-
цента стеноза по результатам реги-
страции УЗ-изображения и опреде-
ления степени локальных наруше-
ний кровотока по данным анализа
спектра допплеровского сдвига час-
тот. Первый подход основан на ин-
терпретации данных УЗ-изображе-
ния в В-режиме и режимов цвето-
вого допплеровского картирования
и/или ЭОДС. Как бы четко ни
были определены границы контура
бляшки в В-режиме, необходимо
подтверждать полученную инфор-
мацию в режиме ЦДК и/или
ЭОДС. Практически процент сте-
ноза может быть определен двумя
способами: на основании расчета
площади поперечного сечения (Sa)
и по диаметру сосуда (Sd). Все дуп-
лексные системы последнего поко-
ления позволяют производить эти
110
расчеты автоматически, с помощью
компьютерной программы. Вычис-
ление степени стеноза осуществля-
ют по формулам:

где D1 — истинный диаметр сосуда;
D2 — проходимый диаметр стено-
зированного сосуда; A1 — истинная
площадь поперечного сечения сосу-
да; А2 — проходимая площадь по-
перечного сечения стенозированно-
го сосуда.
Процент стеноза, определяемый
по площади, является более инфор-
мативным, поскольку учитывает
геометрию бляшки, формирующей
стеноз. Как правило, процент сте-
ноза, рассчитанный по площади
поперечного сечения, превышает
процент стеноза по диаметру на
10-20 %.
Гемодинамические характеристи-
ки кровотока в исследуемых арте-
риях включают качественную и ко-
личественную оценку спектра доп-
плеровского сдвига частот и изуче-
ние величины объемной скорости
кровотока.
Анализируют данные СДСЧ в
зоне атеросклеротической бляшки,
для чего контрольный объем поме-
щают в просвет сосуда и плавно пе-
ремещают его в позицию до, над и
непосредственно за бляшкой, а так-
же дистальнее нее, одновременно
регистрируя и оценивая СДСЧ и
звуковой сигнал на слух.
При стенозе почти в 40 % случа-
ев визуализируется выступающая в
просвет сосуда бляшка, более чет-
кая форма которой определяется
при исследовании в режиме ЦДК
или ЭОДС. Спектральный анализ
допплеровского сдвига частот не
выявляет отклонений от нормы.
При стенозе от 40 до 60 % векто-
ры эритроцитов становятся разно-
направленными, и вследствие не-
упорядоченного движения послед-
них возникает локальная потеря
устойчивости кровотока, проявляю-
щаяся расширением СДСЧ с одно-
временным уменьшением или ис-
чезновением площади окна под сис-
толическим пиком. Непосредствен-
но за бляшкой линейная скорость
кровотока может оставаться в пре-
делах нормы или возрастать, однако
кровоток не теряет своего пульсиру-
ющего характера, поэтому форма
контура спектра не меняется.
По мере нарастания стенозирую-
щего процесса регистрируют турбу-
лентный характер кровотока. При
стенозе 60—75 % увеличивается
скорость кровотока, обусловленная
уменьшением просвета сосуда, и
соответственно увеличивается сис-
толическая скорость кровотока, из-
меняется звуковой сигнал на слух.
Поскольку кровоток теряет свой
пульсирующий характер, изменяет-
ся форма контура спектра в виде
сглаживания катакротического
пика, увеличивается угол наклона
восходящей систолической части и
расстояние между восходящей и
нисходящей частями спектра. От-
мечаются значительное расширение
спектра и заполнение окна под сис-
толическим пиком.
Для стеноза 75—90 % присущи
все признаки, характерные для по-
ражения 60—75 %. Кроме этого,
как правило, регистрируют отрица-
тельные значения допплеровского
сдвига частот, обусловленные бес-
порядочным движением эритроци-
тов с направлением как к датчику,
так и от него.
Дата добавления: 2021-03-18; просмотров: 68; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!