ЗАДАНИЯ ДЛЯ КОНТРОЛЯ САМОПОДГОТОВКИ К ЗАНЯТИЮ.
1. Подготовить теоретический материал по вопросам для самоподготовки к занятиям.
2. Решить задачи 1, 5-8, 13-14, условие задач представлено на страницах 19-22 данного лабораторного практикума.
Примерный вариант заключительного контроля:
1. Приведите электронное строение сопряженной системы в органическом соединении. Укажите пиррольное и пиридиновое состояние гетероатомов:
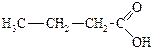
2. Докажите ароматичность соединений:
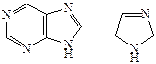
3. Укажите вид и знак электронных эффектов заместителей в соединении. Определите электронодонорные и электроноакцепторные заместители:
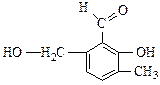
Задачи для самостоятельного решения
1. Выделите сопряженные и ароматические фрагменты в составе норадреналина. Приведите их электронное строение, укажите p,p и p,p-сопряженные системы. Докажите ароматичность соответствующих структурных фрагментов.
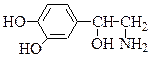
2. Выделите сопряженные и ароматические фрагменты в составе предшественника катехоламинов ДОФА. Приведите их электронное строение, укажите p,p и p,p-сопряженные системы. Докажите ароматичность соответствующих структурных фрагментов.
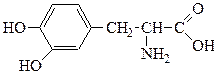
3. Выделите сопряженные и ароматические фрагменты в составе природной аминокислоты триптофана. Приведите их электронное строение, укажите p,p и p,p-сопряженные системы. Докажите ароматичность соответствующих структурных фрагментов.
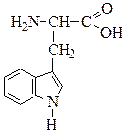
4. Выделите сопряженные и ароматические фрагменты в составе витамина В1. Приведите их электронное строение, укажите p,p и p,p-сопряженные системы. Докажите ароматичность соответствующих структурных фрагментов.
|
|
|
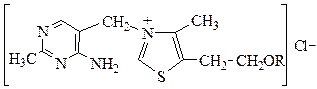
5. В состав нуклеиновых кислот входят гетероциклические соединения пиримидин и пурин. Объясните их принадлежность к ароматическим соединениям.

6. Объясните, с чем связана термодинамическая устойчивость порфина, входящего в состав гема.
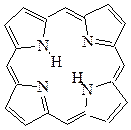
7. Выберите среди приведенных соединений ароматические структуры, используя для доказательства критерии ароматичности:
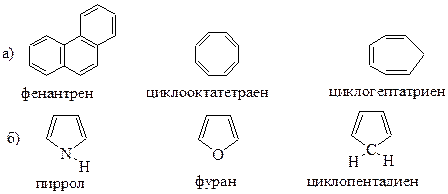
8. Покажите графически распределение электронной плотности, укажите вид и знак электронных эффектов функциональных групп и гетероатома в составе пиридоксаля (группа витаминов В6). Укажите электронодонорные и электроноакцепторные заместители.
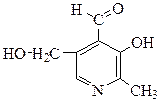
9. Покажите графически распределение электронной плотности, укажите вид и знак электронных эффектов функциональных групп в составе пангамовой кислоты (витамин В15). Укажите электронодонорные и электроноакцепторные заместители.
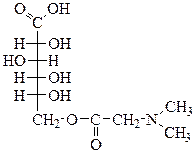
10. Покажите графически распределение электронной плотности, укажите вид и знак электронных эффектов функциональных групп и гетероатомов в составе природной аминокислоты гистидина. Укажите электронодонорные и электроноакцепторные заместители.
|
|
|
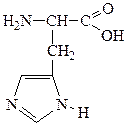
11. Покажите графически распределение электронной плотности, укажите вид и знак электронных эффектов функциональных групп и гетероатомов в составе сульфодиметоксина (сульфаниламидный препарат). Укажите электронодонорные и электроноакцепторные заместители.
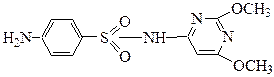
12. В качестве реагента для идентификации аминокислот применяют 2,4-динитро-1-нафтол-7-сульфокислоту. Определите вид и знак электронных эффектов, электронодонорные и электроноакцепторные заместители в ее составе:
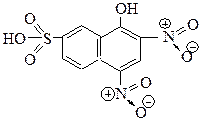
13. В качестве местноанестезирующего средства применяется новокаин. Определите электронодонорные и электроноакцепторные заместители в его составе:
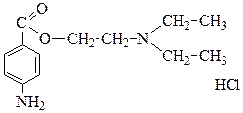
14. Расположите соединения в ряд по увеличению плотности в бензольном кольце, учитывая электронодонорный и электроноакцепторный характер заместителей.
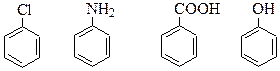
ЗАНЯТИЕ 3.
ПРОСТРАНСТВЕННОЕ СТРОЕНИЕ И СТЕРЕОИЗОМЕРИЯ.
ЦЕЛЬ: Сформировать знания:
– стереохимических понятий «конформация», «конфигурация», «хиральность», «энантиомерия», «диастереомерия»;
– единства электронного, структурного и пространственного строения органических молекул;
– конформационной изомерий алканов и циклоалканов;
|
|
|
– конфигурационной изомерии;
– понятий о взаимосвязи пространственного строения и биологической активности.
Сформировать умения:
– изображать конформации биологически важных соединений в виде проекций Ньюмена;
– проводить конформационный анализ циклогексана и его производных;
– изображать конфигурацию органических соединений в клиновидной записи и в виде проекций Фишера;
– определять хиральность органических соединений;
– изображать энантиомеры и s-диастереомеры хиральных молекул;
– писать p-диастереомеры для непредельных органических соединений.
Дата добавления: 2019-09-13; просмотров: 469; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
