Кислоты, их классификация и свойства на основе представлений об электролитической диссоциации.
Кислоты – это электролиты, при диссоциации водных растворов которых в качестве катионов отщепляются только ионы водорода.
HCl → H+ + Cl-
H2SO4 → 2H+ + SO42-
Отрицательные ионы, которые отщепляются от молекулы кислоты называются кислотными остатками.
Кислоты классифицируют по нескольким признакам.
По составу:
Бескислородные HCl, HNO3
Кислородосодержащие H2SO4, H2CO3
По основности:
Одноосновные HCl, HNO3
Двухосновные H2SO4, H2CO3
Трехосновные H3PO4
По силе:
Сильные HCl, HNO3, H2SO4
Слабые H2S, H2CO3
Общие химические свойства кислот обусловлены наличием иона водорода. Для кислот характерны следующие химические свойства:
1. Взаимодействие с активными металлами.
Zn + HCl = ZnCl2 + H2↑
2. Взаимодействие с основными оксидами.
CuO + H2SO4 = CuSO4 + H2O
3. Взаимодействие с основаниями.
HCl + NaOH = NaCl + H2O
H+ + Cl- + Na+ + OH- = Na+ + Cl- + H2O
H+ + OH- = H2O
4. Взаимодействие с солями – такая реакция протекает только в том случае, е6сли образуется осадок, летучее вещество или слабый электролит.
HCl + AgNO3 = AgCl↓ + HNO3
H+ + Cl- + Ag+ + NO3- = AgCl↓ + H+ + NO3-
Cl- + Ag+ = AgCl↓
Глицерин – многоатомный спирт; состав молекулы, физические и химические свойства, применение.
Глицери́н - химическое соединение с формулой HOCH2CH(OH)-CH2OH или C3H5(OH)3. Простейший представитель трёхатомных спиртов. Представляет собой вязкую прозрачную жидкость.
Глицерин — бесцветная, вязкая, гигроскопичная жидкость, неограниченно растворимая в воде. Сладкий на вкус, отчего и получил своё название (гликос — сладкий). Хорошо растворяет многие вещества.
Взаимодействие глицерином с натрием:
2СН2ОН – СНОН-СН2ОН + 6Nа = 2СН2ОNа –СНОNa- СН2ОNа +3 Н2 глицерат натрия.
ВОПРОС №40
Основания, их классификация и свойства на основе представлений об электролитической диссоциации.
Основания -- вещества, диссоциирующие в водном растворе с образованием катионов металла и гидроксид-анионов ОН−.
Основание -- NaOH:
NaOH ↔ Na+ + OH-
Существует также основание, в котором гидрокси-группа присоединена не к металлу, а к иону NH4+ (катиону аммония). Это основание называется гидроксидом аммония и имеет формулу NH4OH. Гидроксид аммония образуется в рекции присоединения воды к аммиаку, когда аммиак растворяют в воде:
NH3 + H2O = NH4OH (гидроксид аммония).
Основания бывают растворимыми и нерастворимыми. Растворимые основания называются щелочами. Растворы щелочей скользкие на ощупь ("мыльные") и довольно едкие. Они разъедают кожу, ткани, бумагу, очень опасны (как и кислоты) при попадании в глаза. Поэтому при работе со щелочами и кислотами необходимо пользоваться защитными очками.
Лишь небольшую часть всех оснований называют щелочами. Это, например, KOH – гидроксид калия (едкое кали), NaOH – гидроксид натрия (едкий натр), LiOH – гидроксид лития, Ca(OH)2 – гидроксид кальция (его раствор называется известковой водой), Ba(OH)2 – гидроксид бария. Большинство других оснований в воде нерастворимы и щелочами их не называют.
Щелочами называются растворимые в воде сильные основания.
Свойства, характерные для всех оснований, проявляются благодаря присутствию в их растворах гидроксид- ионов OH-..
1. Наиболее важное химическое свойство всех оснований – взаимодействие с кислотами – реакция нейтрализации.
NaOH + HCl = NaCl + H2O
Na+ + OH- + H+ + Cl- = Na+ + Cl- + H2O
H+ + OH- = H2O
2. Взаимодействие щелочей с кислотными оксидами.
NaOH + CO2 = Na2CO3
3. Взаимодействие щелочей с солями, если в результате реакции одно из веществ выпадает в осадок.
3NaOH + FeCl3 = Fe(OH)3↓ + 3NaCl
3Na+ + 3OH- + Fe3+ + 3Cl- = Fe(OH)3↓ + 3Na+ + 3Cl-
3OH- + Fe3+ = Fe(OH)3↓
Основания — электролиты, при диссоциации которых образуется только один вид анионов — гидроксид-ионы.
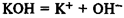
Классификация оснований
1. Растворимые в воде (щелочи) — гидроксиды металлов главных подгрупп I и II групп.
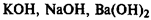
2. Нерастворимые в воде — гидроксиды остальных металлов.
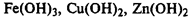
Химические свойства. Щелочи изменяют окраску индикаторов (лакмус становится синим, фенолфталеин – малиновым).
Взаимодействие с кислотами:
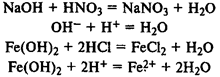
Взаимодействие с кислотными оксидами:
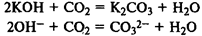
Растворы щелочей вступают в реакции ионного обмена с растворами солей, если образующийся при этом гидроксид нерастворим в воде:
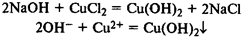
При нагревании слабые основания разлагаются на оксиды металлов и воду:

Получение оснований. Щелочи получают электролизом растворов солей.
Электролиз раствора хлорида натрия. Процессы на катоде и аноде:
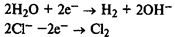
Уравнение реакции:
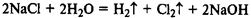
Нерастворимые в воде основания получают реакцией обмена со щелочами:
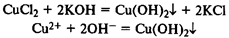
ВОПРОС №41
Дата добавления: 2019-07-15; просмотров: 675; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
